Volume 43 Number 4
Examining the association of immunosuppressants and wound healing: a narrative review
Aria Appoo, Brandon L Christensen, Ranjani Somayaji
Keywords wound healing, Calcineurin inhibitors, glucocorticoids, immunosuppressants, monoclonal antibodies, mTOR inhibitors
For referencing Appoo A, Christensen BL and Somayaji R . Examining the association of immunosuppressants and wound healing: a narrative review. WCET® Journal 2023;43(4):32-39.
DOI
10.33235/wcet.43.4.32-39
Submitted 1 February 2023
Accepted 23 May 2023
Abstract
Objective A review of recent literature to provide clinicians with an understanding of how different classes of immunosuppressants affect wound healing.
Data sources A literature search was conducted in PubMed, Google Scholar, and the University of Calgary Health Sciences Library.
Study Selection Studies chosen for inclusion were screened initially based on title using key words including “immunosuppressive medication, wound healing, and immunosuppression.” If the title and/or abstract contained these key words and addressed wound healing related to immunosuppressant medications and had been published after 2000, they were included in the review. When human data was not available for an immunosuppressant (class), animal studies were included.
Data Extraction Selected papers underwent full text review and summarisation.
Data Synthesis Data were synthesised in a descriptive manner. Corticosteroids and mechanistic target of rapamycin (mTOR) inhibitors most consistently demonstrate detrimental effects on wound healing. For other classes of immunosuppressants, evidence is limited with varying effects on wound healing described.
Conclusions Larger high-quality studies are required to better understand the effects of immunosuppressants particularly with development of new classes of these drugs on wound healing in order to identify those at highest risk of impairing wound healing.
Introduction
Immunosuppressants are medications with a variety of indications including in solid organ and hematopoietic transplants along with autoimmune diseases. They function by suppressing the activity of various components of the adaptive immune system thus diminishing the cascade of inflammatory response to normal host tissue or modulating the natural rejection response to transplanted materials.1 The main classes of immunosuppressants are corticosteroids/glucocorticoids,2,3 calcineurin inhibitors,2,4,5 mechanistic target of rapamycin (mTOR) inhibitors,2,4 polyclonal antibodies,2,4 monoclonal antibodies,2,4 and antiproliferative agents.2 For the purpose of this review, wounds are defined as an opening in the skin as a result of surgery, trauma, or disease that is susceptible to infection.
The immune system plays an important role in the prevention of infection but also the healing process of wounds, with the inflammatory effects leading to cellular proliferation and secretion of important intra and extracellular components.6 With immunosuppressants, the immune system is modulated, thus potentially affecting a wound’s healing time and susceptibility to infection.7 With a growing number of patients on immunosuppressing medications, particularly post-surgical transplant patients, the effect of immunosuppressants on wound healing is an important issue to be considered. This review article aims to provide clinicians with an understanding of how different classes of immunosuppressants affect wound healing.
Materials/methods
A literature search between 2000 through 2021 was conducted using the generic names of a number of commonly used immunosuppressants (glucocorticoids/corticosteroids, mTOR inhibitors, methotrexate, monoclonal antibodies, polyclonal antibodies, calcineurin inhibitors, mycophenolate, azathioprine) as well as the terms “wound healing” and “immunosuppression”. The primary database searched was PubMed. This was supplemented by Google Scholar and the University of Calgary Health Science Library database. When possible, the search was in the following format “immunosuppressant name [MeSH Terms] AND “wound healing [MeSH Terms].” If the immunosuppressant name was not available as a MeSH term, then the term was searched with no restriction applied. Article titles were then screened for relevance to the review based on whether wound healing was described in relation to the immunosuppressive medication/class. The abstract was screened similarly and included in the review accordingly. If the article compared various immunosuppressants, discussed their effects on wound healing, measured wound healing or deleterious effects on wounds it was considered relevant. If search terms did not identify human subject studies, then studies that used animals to evaluate immunosuppressive effects on wound healing were included. When no data was available from 2000 onwards, a historic search was conducted for the relevant immunosuppressive medications.
All included studies were summarised descriptively including immunosuppressive mechanism of action, study subjects, and evidence of effects on wound healing.
Results
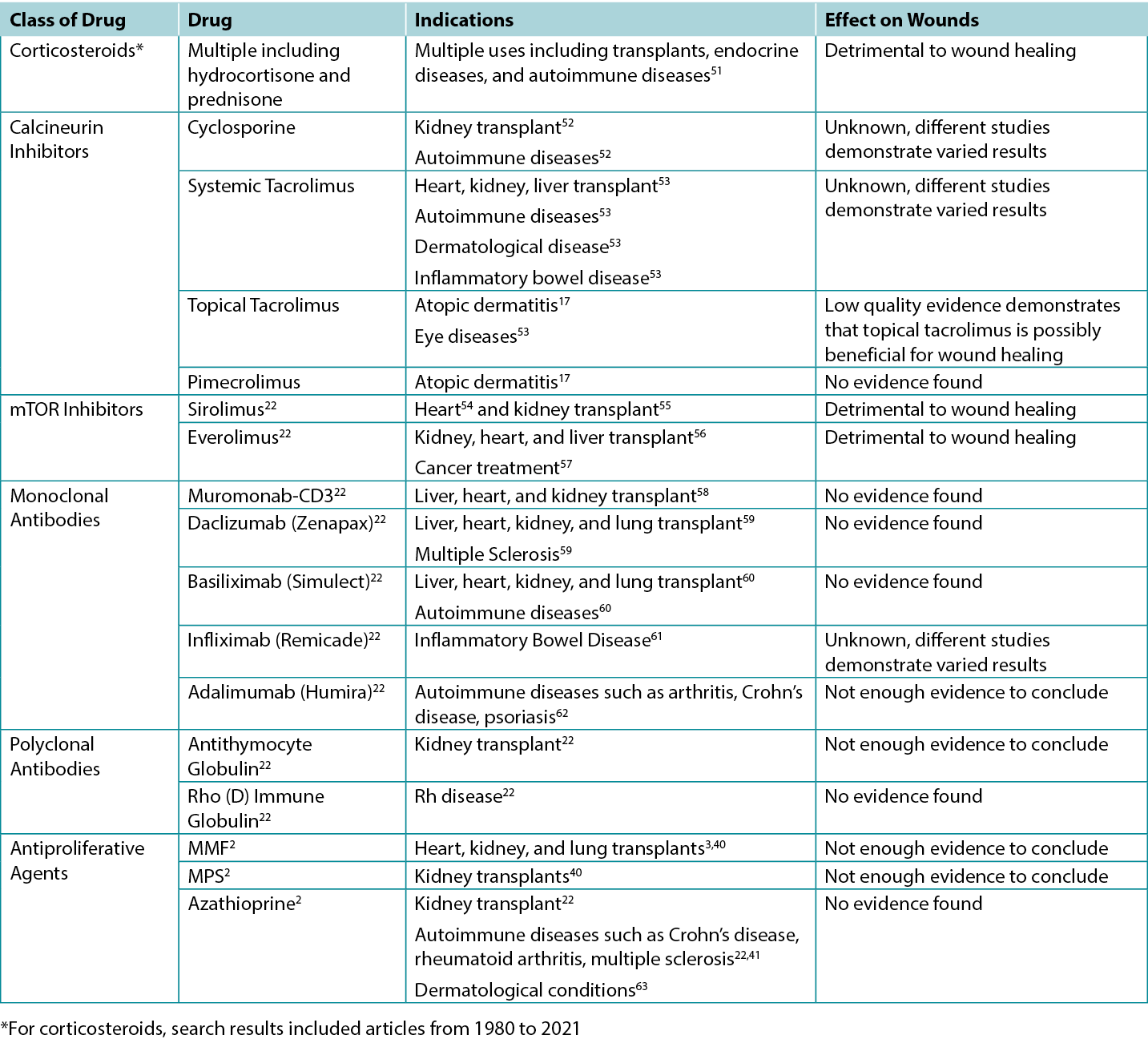
The studies screened relevant to this review were used to inform the various categories outlined below. A total of 200 article titles and abstracts were initially screened and 61 articles were included for review. Summary tables highlighting the results of clinical and animal studies are summarised in Table 1. The specific indications for various immunosuppressants including their possible impacts on wounds are outlined in Table 2.
Table 1. Studies Comparing the Effects of Different Immunosuppressants on Wounds
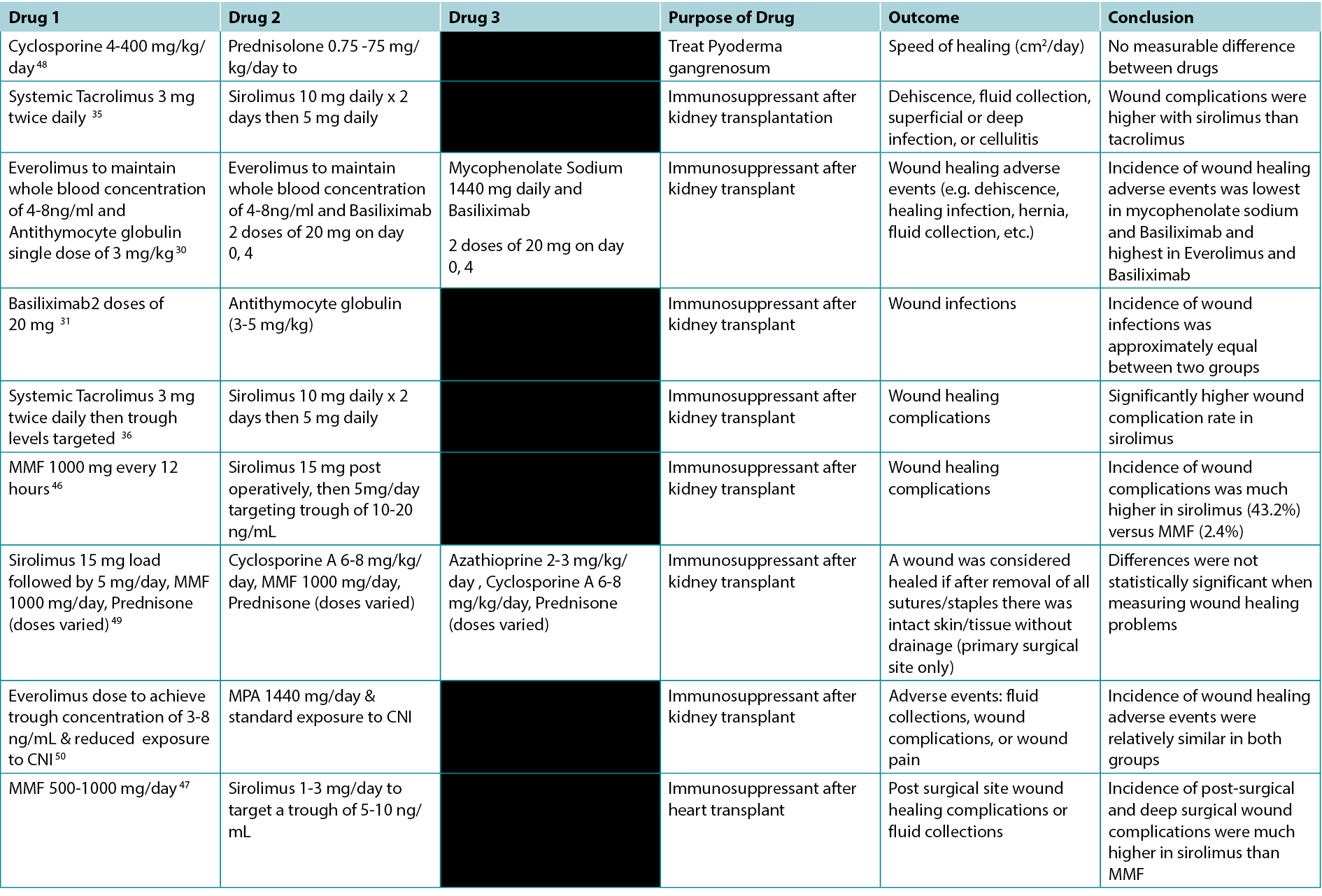
Table 2. Overview of Indications and Wound Effects of Various Immunosuppressants
Calcineurin Inhibitors
Calcineurin inhibitors (CNI) are used as immunosuppressants for a variety of different autoimmune diseases, organ transplants, dermatological conditions, and in chronic wounds.8 There are three main types of CNI’s: cyclosporine (systemic), tacrolimus (systemic and topical), pimecrolimus (topical).9 CNI’s work by binding to part of the calcineurin molecule found in human cells, thus stopping the release of certain cytokines that are responsible for activating T cells.8 Therefore, CNI’s disable one of the main arms of the body’s adaptive immune response.
Systemic
There are a lack of studies directly focusing on the effects of CNI’s on wound healing in humans; however, many basic science studies on animals have been performed. Two such studies using rats compared the effect of various doses of systemic tacrolimus versus a control, testing the breaking strengths of the wounds created through surgery. One of the rat studies concluded that tacrolimus does not affect wound healing10 while the other study concluded that tacrolimus is detrimental to wound healing.11 At the same time, case reports using systemic tacrolimus as a treatment for ulcers in a person with lichen planus and pyoderma gangrenosum demonstrated treatment success with this therapy.12
No recent human studies were found regarding the effect of cyclosporine and wound healing. Two other studies using rats also yielded contradictory results. These rat studies focused on the effects of cyclosporine on different markers in the body that signify effective wound healing. One study comparing cyclosporine to methylprednisone demonstrated that cyclosporine had no suppressive effect on the various inflammatory and biochemical markers compared to the glucocorticoid therapy13 whereas the other study showed that cyclosporine had a negative effect on the markers.14 In a different study, after receiving a lung transplant, dogs were assigned to a specific immunosuppressant drug or no immunosuppressant drug and, similar to control, Cyclosporine A was shown to have no significant effect on the healing of the surgical wound as measured by breaking strength in comparison to glucocorticoid and azathioprine immunosuppression.15 Overall, the literature on systemic calcineurin inhibitors and wound healing is dated with a heterogeneity of comparators and mixed results on wound healing.
Topical
Calcineurin inhibitors (tacrolimus and pimecrolimus) are used as topical ointments most commonly for dermatological conditions such as atopic dermatitis but also for chronic dermatologic conditions such as pyoderma gangrenosum.16–18 Some case studies have shown tacrolimus effective at healing complex leg ulcers in the context of venous insufficiency or necrobiosis lipoidica, when regular treatment strategies have been ineffective.19,20 Furthermore, a rat-based study with acute cutaneous injury demonstrated that wounds treated with topical tacrolimus healed equally as quickly as the control (petrolatum).21
Monoclonal Antibodies:
A variety of different monoclonal antibodies (mAb) therapies exist with indications in transplants and autoimmune disorders such as rheumatoid arthritis and psoriasis.22 In general, mAb work by binding to different receptors and antigens to inhibit the effect of cytokines and other signal pathways that activate the immune system.22 A small prospective cohort study among patients with rheumatoid arthritis undergoing orthopedic surgery demonstrated that there was no increased risk of surgical wound infections or healing complications in patients on infliximab compared to conventional therapy.23 Furthermore, a case report claims that topical infliximab was helpful in healing leg ulcers that were resistant to standard treatment suggesting that inhibiting tumor necrosis factor alpha is helpful to wound healing.24 Similar findings were concluded in a case report for treatment of pyoderma gangrenosum with infliximab resulting in improvement of the ulcer.25 Inhibiting tumor necrosis factor alpha was shown to be further associated with wound healing in venous leg ulcers through the use of Adalimumab systemically.26 However, another study used infliximab on rat abdominal wounds and demonstrated that the tensile strength was significantly lower in the wounds of rats who had been given infliximab compared to those who were the control.27 Overall, the limited literature on the subject to date suggests clinical outcomes thus far are favorable in terms of wound healing.
Polyclonal Antibodies
Polyclonal antibodies (pAb’s) are very similar to mAb’s in function, with slightly varied mechanism of action.28,29 Unlike mAb’s, a group of polyclonal antibodies are created from many different lines of B cells and within the group different pAb’s bind to different epitopes of an antigen. In contrast, mAb’s come from a single line of B cells and can bind to only one antigen.28,29 There are two main pAb’s: Antithymocyte Globulin and Rho (D) Immune Globulin.22 Antithymocyte Globulin also known as Antihuman Thymocyte Globulin is most commonly used as an immunosuppressant after kidney transplantation and works by binding to a variety of lymphocytes and depleting the number of T cells in the body.22 Rho (D) Immune Globulin is used in pregnancies where the mother is Rh- and the fetus is Rh+ and essentially stops the formation of anti Rh+ antibodies in the mother.22
Few studies looking at the effects of pAb’s on wound healing were found. Two studies outlined the effects of antithymocyte globulin and Basiliximab. The first study in patients with renal transplants, where both drugs were combined with everolimus, showed higher rates of adverse effects of wound healing in Basiliximab. 30 The second study demonstrating that the incidence of wound infections was equal in patients taking Basiliximab versus antithymocyte globulin post renal transplant.31 Since white blood cells play a key role in wound healing through secreting necessary cytokines and preventing infection,32 it would be reasonable to hypothesise that antithymocyte globulin will affect wound healing since it reduces the number of white blood cells as well as their regulatory mechanisms.
mTOR Inhibitors
Mechanistic target of rapamycin (mTOR) inhibitors are immunosuppressive drugs that works by interacting with proteins in complex signalling pathways to prevent cells moving into the S phase of the cell cycle and therefore suppressing proliferation.3,22 mTOR predominantly targets T cells, but can also affect B cells.3 Interestingly, mTOR can cause an increase of production of certain inflammatory cytokines such as interleukin-6 and decrease production of interleukin-10, an anti-inflammatory cytokine.3 There are two main mTOR inhibitors: sirolimus and everolimus.3,22 In general, mTOR inhibitors have a variety of applications including cancer therapy.3,22 As an immunosuppressant, they are used after transplants.3,22 Everolimus has been shown to inhibit the proliferation of fibroblast in in vitro models33 suggesting that everolimus could have negative consequences for wound healing since fibroblasts are essential for creating an extracellular matrix and creating a frame for other cells.34 In a study comparing sirolimus and systemic tacrolimus, sirolimus had a wound complication rate of 47% compared to tacrolimus with only 8%.35 This is consistent with another study by Larson et al demonstrating higher wound complications with sirolimus compared to tacrolimus.36 Interestingly, obese patients on sirolimus had very high rates of wound complications leading to the study excluding all patients with obesity.36 In line with previous findings, a study on rats showed that increased sirolimus doses decreases wound strength, which the authors hypothesising this effect may be due to lower levels of VEGF and nitric oxide in rats receiving higher doses of sirolimus.37 In one review authors concluded that mTOR inhibitors are harmful to wound healing in high doses, but seem to have a neutral effect in low does.38 Given early concerns with mTOR inhibitors and wound healing, regimens using these immunosuppressive agents have evolved with lower doses of the mTOR inhibitors and combination therapy. In the large TRANSFORM randomised control trial investigators compared everolimus plus reduced dose CNI to mycophenolic acid plus standard dose CNI (standard care) in patients with renal transplants and showed wound related adverse events were not statistically different (20.6% vs 17.3%; RR 1.19 95%CI 0.99 to 1.43).39 One limitation of this study was close monitor of everolimus concentrations and difficulties achieving the targeted plasma concentrations C0 between 3 and 8 ng/mL.39 Overall, review of the current literature is suggestive that mTOR inhibitors have a detrimental effect on wound healing, especially at higher doses, and that improved dosing regimens may lessen or mitigate this risk.
Antiproliferative Agents
There are three regularly used antiproliferative agents: Mycophenolate mofetil (MMF) and Mycophenolate sodium (MPS) (both inosine monophosphate dehydrogenase (IMPDH) inhibitors) and azathioprine.2,40 IMPDH inhibitors have a similar effect to mTOR inhibitors in terms of their mechanism of immunosuppression. In the body, MMF and MPS are converted into mycophenolic acid which blocks a portion of a pathway that is crucial for DNA synthesis, to decrease proliferation of T cells and B cells.2,5,40 MMF is used for its immunosuppressive effect in heart, kidney, and lung transplants.3,40 MPS is used for kidney transplants.40 Azathioprine is used as an immunosuppressive drug for kidney transplants and autoimmune diseases including rheumatoid arthritis, Crohn’s disease, and multiple sclerosis.22,41 In the body, azathioprine reacts with glutathione and is converted into 6-mercaptupurine after which additional metabolites are generated ultimately blocking purine synthesis and stimulation of T-cells.3,22
When a study compared two different doses of MMF in kidney transplant recipients, incidence of wounds requiring surgical intervention were not significantly different, similarly for wounds treated with local wound care.42 Based on review of article titles as part of our search, no studies regarding the sole effect of azathioprine on external wound healing in humans were found. When azathioprine was compared to a placebo in a rat study, the wounds of the rats who were on azathioprine took longer to heal than those on the placebo suggesting that azathioprine can have detrimental effects on wound healing, but the extent that it would affect humans is unclear.43
Anti-metabolite
Methotrexate is a commonly used folate antagonist immunosuppressive agent, with indications in many rheumatologic disorders. It also has antineoplastic activity in higher doses. Upon absorption, it enters the cell and is converted to methotrexate polyglutamates where it competes for dihydrofolate reductase thus preventing the transformation of folic acid for its use in the building of nucleic acids.6 Like other agents described, there is experimental animal studies with in vitro studies suggesting impairment in wound healing but these effects have not been borne out in clinical studies, particularly in post-surgical wounds.6 Thus, it is recommended this drug be continued postoperatively.
Corticosteroids/Glucocorticoids
Glucocorticoids prevent the formation of inflammatory chemicals like cytokines, cell adhesion molecules, and complement factors.3 By inhibiting interleukin-2 formation, glucocorticoids also prevent T cell proliferation and activation.22 They also impair monocytes and B cells.3,22 Glucocorticoids were the first antirejection drug created, but as time has passed, there has been a movement to phase them out due to their serious side effects.3,22 There is consensus that glucocorticoids are highly detrimental to wound healing since they interfere with many key stages of wound healing such as collagen deposition and synthesis, angiogenesis, fibroblast proliferation, growth factors, and phagocytosis among others.2,3,44,45
Practical considerations for health care providers
Persons with compromised immune systems (due to medications, co-morbidities or age extremes) require additional considerations for chronic wound management. Specific to immunosuppressive medications, health care providers should take a careful history not only of the medications and dosing (including changes in dosing), but also of the underlying conditions requiring these medications (e.g. autoimmune disorders, organ transplantation). As many immunosuppressive medications can impair wound healing, it is crucial for health care providers to assess healing potential early on to set and manage patient expectations. Early referral to medical or surgical specialists to assist with wound care and a team-based approach will be essential given the increased complexity of these individuals. In some cases where wounds are not healing, alternate goals of care for the wound may need to be set (e.g. maintenance or non-healable) if immunosuppressive doses cannot be reduced (assuming it is contributing to poor healing) and should be done in consultation with their primary or specialist care providers. As individuals and populations with comorbidities live longer, taking care of persons with chronic wounds on immunosuppressive medications will become increasingly common and must be recognised early by the wound care clinicians.
Discussion
With the ongoing advances in medicine, the need for immunosuppression in the context of transplant, autoimmune disease and malignancy has increased. In our review, we highlight the poverty of robust studies in this field and highlighted the mixed effects of various immunosuppression on wound healing. High quality evidence exists with respect to the deleterious effects of glucocorticoid therapy as well as mTOR therapy, particularly sirolimus on wound healing. Furthermore, when 4 studies compared sirolimus to either MMF or systemic tacrolimus, all the studies demonstrated sirolimus to be associated with an increased incidence of wound complications.35,36,46,47
The literature on agents such as systemic CNIs is mixed with some suggesting adverse effects on wounds and others suggesting benefit, necessitating additional study focusing directly on this question. Newer topical CNIs have shown little impact on delayed wound healing and in some cases benefit, but additional investigation is warranted for their use in chronic wounds directly. Reassuringly, antiproliferative agents, antimetabolite, and newer monoclonal antibiotics have not shown signal toward diminished healing. However, additional study is needed given the poverty of evidence on wound healing in mAB therapy. Overall, our review found the evidence in this area is dated with variable conclusions surrounding the effects of the immunosuppressant on wound healing. In addition, we found little evidence using human subjects. In general, when immunosuppressives are prescribed after transplants to prevent rejection, patients take more than one drug to effectively prevent rejection. Therefore, challenges exist in performing human studies evaluating the effects of individual drugs in isolation.
As we did not conduct a systematic review, certain articles may have been excluded. We did identify a few key reviews before conducting the search and ensured they were present in the search as one form of validation. As well, given the paucity of literature in this area particularly as it relates to the wound care field, a narrative review adds value to educate and increase awareness when working with individuals on these medications.
With the growing need for immunosuppression, additional study in this field is critical. Future directions include conducting more studies in animal subjects with newer classes of immunosuppressants to identify potential pathways to delayed wound healing and potential ways to mitigate such effects. In addition, more high-quality studies are required to evaluate both individual and combination immunotherapies to better understand the risks and how different immunosuppressants may impact wound healing. In order to explore immunosuppressants as a potential treatment for chronic or complex wounds, it is important for future studies to be conducted on a larger scale, control for confounding clinical factors, such as through randomised control trials.
Conclusions
In conclusion, immunosuppressants range from possibly beneficial to floridly deleterious in wound healing. While there is little conclusive evidence in this field, the effects of immunosuppressants on wound healing is worth exploring to better tailor immunosuppression to patients at risk for or experiencing chronic non-healing wounds. Reassuringly, our findings suggest not all immunosuppressants are harmful with some potentially offering benefit to wound treatment when conventional therapies has failed, opening up the possibility of a new treatment option for wounds.
Acknowledgements
University of Alberta Highschool Youth Researcher Summer Program.
Conflict of Interest
The authors declare no conflicts of interest.
Funding
The authors received no funding for this study.
Examinar a associação entre imunossupressores e a cicatrização de feridas: uma revisão narrativa
Aria Appoo, Brandon L Christensen, Ranjani Somayaji
DOI: 10.33235/wcet.43.4.32-39
Resumo
Objetivo Uma revisão da literatura recente para fornecer aos clínicos um entendimento da forma como as diferentes classes de imunossupressores afetam a cicatrização de feridas.
Fontes de dados Foi efetuada uma pesquisa bibliográfica na PubMed, no Google Scholar e na Biblioteca de Ciências da Saúde da Universidade de Calgary.
Seleção de estudos Os estudos escolhidos para inclusão foram inicialmente selecionados com base no título, utilizando palavras-chave como "medicação imunossupressora, cicatrização de feridas e imunossupressão" Se o título e/ou resumo contivessem estas palavras-chave e abordassem a cicatrização de feridas relacionada com medicamentos imunossupressores e tivessem sido publicados após 2000, estes eram incluídos na revisão. Quando não existiam dados humanos disponíveis para um imunossupressor (classe), foram incluídos estudos em animais.
Extração de dados Os artigos selecionados foram submetidos a uma revisão integral do texto e resumidos.
Síntese dos dados Os dados foram sintetizados de forma descritiva. Os corticosteroides e os inibidores de alvo mecanicista da rapamicina (mTOR) demonstram, de forma mais consistente, efeitos prejudiciais na cicatrização de feridas. Relativamente a outras classes de imunossupressores, as evidências são limitadas, encontrando-se descritos efeitos variáveis na cicatrização de feridas.
Conclusões São necessários estudos de maior qualidade para compreender melhor os efeitos dos imunossupressores na cicatrização de feridas, particularmente com o desenvolvimento de novas classes destes fármacos, de modo a identificar aqueles que apresentam um maior risco de prejudicar a cicatrização de feridas.
Introdução
Os imunossupressores são medicamentos com uma variedade de indicações, incluindo transplantes de órgãos sólidos e hematopoiéticos, bem como em doenças autoimunes. Funcionam suprimindo a atividade de vários dos componentes do sistema imunitário adaptativo, diminuindo assim a cascata de resposta inflamatória ao tecido normal do hospedeiro ou modulando a resposta de rejeição natural a materiais transplantados.1 As principais classes de imunossupressores são os corticosteroides/glucocorticóides,2,3 os inibidores da calcineurina,2,4,5 os inibidores de alvo mecanístico da rapamicina (mTOR),2,4 os anticorpos policlonais,2,4 os anticorpos monoclonais,2,4 e os agentes antiproliferativos.2 Para efeitos desta revisão, as feridas são definidas como uma abertura na pele resultante de uma cirurgia, traumatismo ou de doença suscetível de infeção.
O sistema imunitário desempenha um papel importante na prevenção de infeções, mas também no processo de cicatrização de feridas, com os efeitos inflamatórios a conduzirem à proliferação celular e à secreção de importantes componentes intra e extracelulares.6 Com os imunossupressores, o sistema imunitário é modulado, afetando potencialmente o tempo de cicatrização de uma ferida e a suscetibilidade a infecções.7 Com um número crescente de pacientes a tomar medicamentos imunossupressores, particularmente pacientes pós-cirúrgicos de transplantes, o efeito dos imunossupressores na cicatrização de feridas constitui uma questão importante a considerar. Este artigo de revisão tem como objetivo facultar aos médicos um entendimento da forma como as diferentes classes de imunossupressores afetam a cicatrização de feridas.
Materiais/métodos
Foi efetuada uma pesquisa bibliográfica entre 2000 e 2021, utilizando os nomes genéricos de uma série de imunossupressores utilizados habitualmente (glucocorticóides/corticosteroides, inibidores da mTOR, metotrexato, anticorpos monoclonais, anticorpos policlonais, inibidores da calcineurina, micofenolato, azatioprina), bem como os termos "cicatrização de feridas" e "imunossupressão". A principal base de dados pesquisada foi a PubMed. Esta informação foi complementada pelo Google Scholar e pela base de dados da Biblioteca de Ciências da Saúde da Universidade de Calgary. Sempre que possível, a pesquisa foi efetuada no seguinte formato "nome do imunossupressor [Termo MeSH]" e "cicatrização de feridas [Termo MeSH]". Se o nome do imunossupressor não estivesse disponível como um termo MeSH, então o termo foi pesquisado sem qualquer restrição. Os títulos dos artigos foram então analisados no que se refere à sua relevância para a revisão, com base no facto de a cicatrização de feridas ter sido descrita em relação à medicação/classe de imunossupressores. O resumo foi analisado de forma semelhante e incluído em conformidade na revisão. Se o artigo comparasse vários imunossupressores, discutisse os seus efeitos na cicatrização de feridas, medisse a cicatrização de feridas ou os efeitos deletérios nas feridas, era considerado relevante. Se os termos de pesquisa não identificaram estudos em seres humanos, foram incluídos estudos que se utilizaram animais para avaliar os efeitos imunossupressores na cicatrização de feridas. Quando não existiam dados disponíveis a partir de 2000, foi realizada uma pesquisa histórica para os medicamentos imunossupressores relevantes.
Todos os estudos incluídos foram resumidos descritivamente, incluindo o mecanismo de ação imunossupressor, os sujeitos do estudo e as evidências dos efeitos na cicatrização de feridas.
Resultados
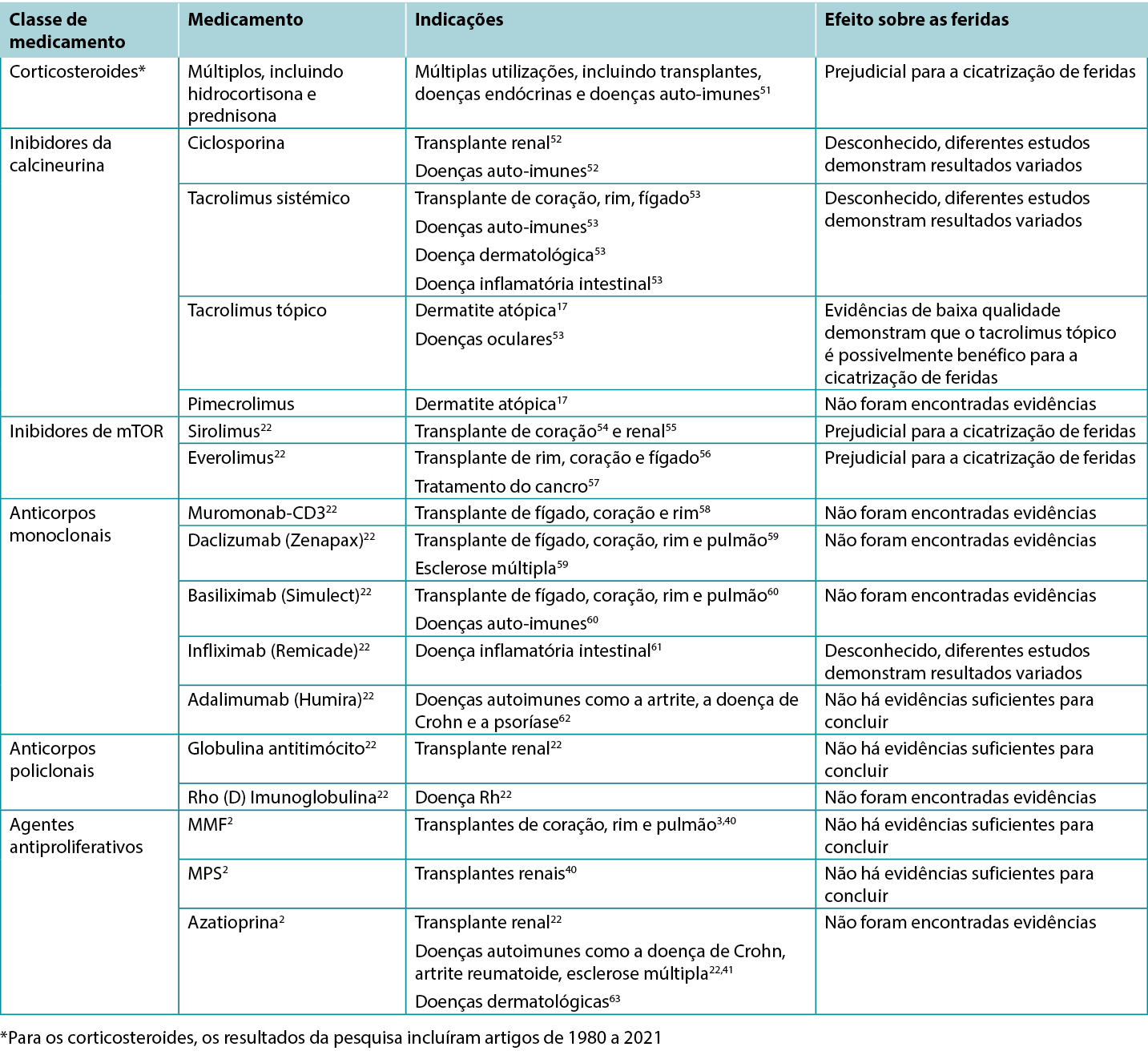
Os estudos selecionados relevantes para esta revisão foram utilizados para informar as várias categorias seguidamente descritas. Um total de 200 títulos e resumos de artigos foram inicialmente selecionados e 61 artigos foram incluídos para revisão. Os quadros de síntese que destacam os resultados dos estudos clínicos e em animais encontram-se resumidos no Tabela 1. As indicações específicas para vários imunossupressores, incluindo os seus possíveis impactos nas feridas, encontram-se descritas na Tabela 2.
Tabela 1. Estudos que comparam os efeitos de diferentes imunossupressores nas feridas
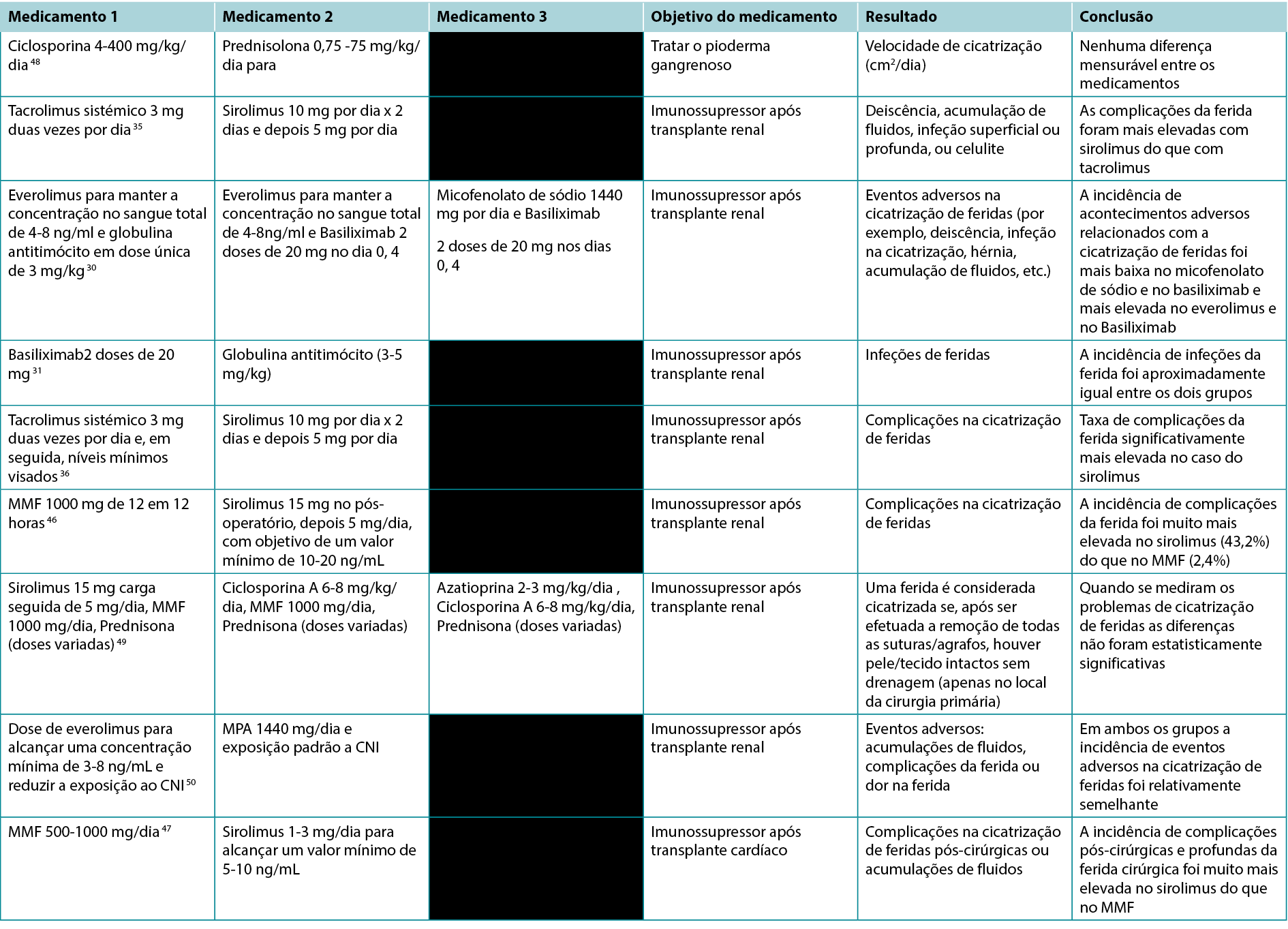
Tabela 2. Visão Geral das Indicações e dos Efeitos nas Feridas de Vários Imunossupressores
Inibidores da calcineurina
Os inibidores da calcineurina (CNI) são utilizados como imunossupressores para uma variedade de doenças autoimunes, transplantes de órgãos, doenças dermatológicas e feridas crónicas.8 Existem três tipos principais de CNI: ciclosporina (sistémica), tacrolimus (sistémica e tópica), pimecrolimus (tópica).9 Os CNI actuam ligando-se à parte da molécula de calcineurina que se encontra nas células humanas, impedindo assim a libertação de determinadas citocinas responsáveis pela ativação das células T.8 Por conseguinte, os CNI desativam um dos principais braços da resposta imunitária adaptativa do organismo.
Sistémico
Faltam estudos que incidam diretamente sobre os efeitos dos CNI na cicatrização de feridas em seres humanos; no entanto, foram realizados em animais muitos estudos científicos básicos. Dois desses estudos, realizados em ratos, compararam o efeito de várias doses de tacrolimus sistémico com um controlo, testando a resistência à rutura das feridas criadas durante a cirurgia. Um dos estudos efetuado em ratos concluiu que o tacrolimus não afecta a cicatrização de feridas10, enquanto que o outro estudo concluiu que o tacrolimus é prejudicial para a cicatrização de feridas.11 Ao mesmo tempo, os relatos de casos que utilizaram tacrolimus sistémico como tratamento para úlceras numa pessoa com líquen plano e pioderma gangrenoso demonstraram o sucesso do tratamento com esta terapêutica.12
Não foram encontrados estudos recentes em humanos sobre o efeito da ciclosporina sobre a cicatrização de feridas. Dois outros estudos efetuados com ratos também produziram resultados contraditórios. Estes estudos em ratos centraram-se nos efeitos da ciclosporina em diferentes marcadores do organismo que significam uma eficaz cicatrização das feridas. Um estudo que comparou a ciclosporina com a metilprednisona, demonstrou que a ciclosporina não teve qualquer efeito supressor nos vários marcadores inflamatórios e bioquímicos, em comparação com a terapêutica com glucocorticóides13, ao passo que um outro estudo demonstrou que a ciclosporina teve um efeito negativo nos marcadores14 Num estudo diferente, após receberem um transplante de pulmão, os cães foram designados para um fármaco imunossupressor específico ou para nenhum fármaco imunossupressor e, à semelhança do controlo, a ciclosporina A não demonstrou ter qualquer efeito significativo na cicatrização da ferida cirúrgica, medida pela força de rutura, em comparação com a imunossupressão com glucocorticoides e azatioprina.15 Em termos gerais, a literatura sobre os inibidores sistémicos da calcineurina e a cicatrização de feridas apresenta dados com uma heterogeneidade de comparadores e com resultados mistos na cicatrização de feridas.
Tópicos
Os inibidores da calcineurina (tacrolimus e pimecrolimus) são utilizados como pomadas tópicas mais frequentemente em doenças dermatológicas como a dermatite atópica, mas também em doenças dermatológicas crónicas como o pioderma gangrenoso.16-18 Alguns estudos de caso demonstraram que o tacrolimus é eficaz na cicatrização de úlceras complexas das pernas, no contexto de insuficiência venosa ou necrobiose lipoídica, quando as estratégias de tratamento regulares demonstraram ser ineficazes.19,20 Além disso, um estudo realizado em ratos com lesões cutâneas agudas, demonstrou que as feridas tratadas com tacrolimus tópico cicatrizaram tão rapidamente como o controlo (petrolato).21
Anticorpos monoclonais:
Existe uma variedade de diferentes terapias com anticorpos monoclonais (mAb), com indicações em transplantes e doenças auto-imunes, como a artrite reumatoide e a psoríase.22 De forma geral, os mAb funcionam ligando-se a diferentes recetores e a antigénios para inibir o efeito das citocinas e de outras vias de sinalização que ativam o sistema imunitário.22 Um pequeno estudo de coorte prospetivo entre pacientes com artrite reumatoide submetidos a cirurgia ortopédica demonstrou não existir um risco acrescido de infeções da ferida cirúrgica ou complicações de cicatrização em pacientes que tomavam infliximab, em comparação com a terapêutica convencional.23 Além disso, um relato de caso alega que o infliximab tópico foi útil na cicatrização de úlceras de perna resistentes ao tratamento padrão, sugerindo que a inibição do fator de necrose tumoral alfa é útil na cicatrização de feridas.24 Num relatório de um caso de tratamento de pioderma gangrenoso com infliximab, foram obtidos resultados semelhantes, resultando na melhoria da úlcera.25 A inibição do fator de necrose tumoral alfa demonstrou estar ainda mais associada à cicatrização de feridas em úlceras de perna venosas através da utilização de Adalimumab por via sistémica.26 No entanto, outro estudo que utilizou infliximab em feridas abdominais de ratazanas demonstrou que a resistência à tração era significativamente inferior nas feridas das ratazanas que tinham recebido infliximab, em comparação com as de controlo.27 Em geral, a até à data limitada literatura sobre o assunto, sugere que os resultados clínicos até agora são favoráveis em termos de cicatrização de feridas.
Anticorpos policlonais
Os anticorpos policlonais (pAb) são muito semelhantes aos mAb em termos de função, com um mecanismo de ação ligeiramente diferente.28,29 Ao contrário dos mAb, um grupo de anticorpos policlonais é criado a partir de muitas linhas diferentes de células B e dentro do grupo, diferentes pAb ligam-se a diferentes epítopos de um antigénio. Em contraste, os mAb provêm de uma única linha de células B e podem ligar-se apenas a um antigénio.28,29 Existem dois pAb principais: A globulina antitimócito e a globulina imunitária Rho (D).22 A globulina antitimócito, também conhecida como globulina antitimócito humano, é utilizada mais frequentemente como imunossupressor após o transplante renal e atua ligando-se a uma variedade de linfócitos e assim reduzindo o número de células T no organismo.22 A globulina imunitária Rho (D) é utilizada em gravidezes em que a mãe é Rh- e o feto é Rh+ e impede essencialmente a formação na mãe de anticorpos anti-Rh+.22
Foram encontrados poucos estudos sobre os efeitos dos pAb's na cicatrização de feridas. Dois estudos descreveram os efeitos da globulina antitimócito e do Basiliximab. O primeiro estudo, em pacientes com transplantes renais, em que ambos os fármacos foram combinados com everolimus, mostrou taxas mais elevadas de efeitos adversos na cicatrização de feridas com Basiliximab.30 O segundo estudo demonstrou que a incidência de infeções de feridas após o transplante renal era igual nos pacientes que tomavam Basiliximab versus globulina antitimócito.31 Uma vez que os glóbulos brancos desempenham um papel fundamental na cicatrização de feridas através da secreção das citocinas necessárias e da prevenção de infecções,32 seria razoável colocar a hipótese de a globulina antitimócitos poder afetar a cicatrização de feridas, uma vez que reduz o número de glóbulos brancos, assim como os seus mecanismos reguladores.
Inibidores de mTOR
Os inibidores de alvo mecanicista da rapamicina (mTOR) são fármacos imunossupressores que atuam através da interação com proteínas em vias de sinalização complexas de forma a impedir que as células passem para a fase S do ciclo celular e por conseguinte, suprimir a sua proliferação.3,22 O mTOR tem como alvo predominante as células T, mas também pode afetar as células B.3 Curiosamente, o mTOR pode causar um aumento da produção de determinadas citocinas inflamatórias, como a interleucina-6, e diminuir a produção de interleucina-10, uma citocina anti-inflamatória.3 Existem dois inibidores principais do mTOR: o sirolimus e o everolimus.3,22 Em geral, os inibidores do mTOR têm uma variedade de aplicações, incluindo a terapia do cancro.3,22 Como imunossupressores, são utilizados após os transplantes.3,22 O everolimus demonstrou inibir a proliferação de fibroblastos em modelos in vitro33, sugerindo que o everolimus poderia originar consequências negativas na cicatrização de feridas, uma vez que os fibroblastos são essenciais para a criação de uma matriz extracelular e para a criação de uma estrutura para outras células.34 Num estudo que comparou o sirolimus com o tacrolimus sistémico, o sirolimus apresentou uma taxa de complicações da ferida de 47%, em comparação com o tacrolimus, com apenas 8%.35 Isto é consistente com outro estudo de Larson et al, que demonstrou complicações da ferida mais elevadas com o sirolimus em comparação com o tacrolimus.36 Curiosamente, os pacientes obesos a tomar sirolimus tiveram taxas muito elevadas de complicações da ferida, o que levou o estudo a excluir todos os pacientes com obesidade.36 Em linha com os resultados anteriores, um estudo em ratos demonstrou que o aumento das doses de sirolimus diminui a resistência da ferida, sendo que os autores supõem que este efeito se deve a níveis mais baixos de VEGF e de óxido nítrico em ratos que recebem doses mais elevadas de sirolimus.37 Numa revisão, os autores concluíram que os inibidores do mTOR são prejudiciais para a cicatrização de feridas em doses elevadas, mas aparentam possuir um efeito neutro em doses baixas.38 Dadas as preocupações iniciais com os inibidores do mTOR e a cicatrização de feridas, os regimes que utilizam estes agentes imunossupressores evoluíram para doses mais baixas dos inibidores do mTOR e para terapia combinada. No grande ensaio de controlo aleatório TRANSFORM, os investigadores compararam o everolimus mais uma dose reduzida de CNI com o ácido micofenólico mais uma dose padrão de CNI (tratamento padrão) em pacientes com transplantes renais, demonstrando que os eventos adversos relacionados com a ferida não eram estatisticamente diferentes (20,6% vs 17,3%; RR 1,19 CI 95% 0,99 a 1,43).39 Uma limitação deste estudo foi a monitorização rigorosa das concentrações de everolimus e as dificuldades em atingir as concentrações plasmáticas pretendidas C0 entre 3 e 8 ng/mL.39 Em geral, a revisão da literatura atual sugere que os inibidores mTOR têm um efeito prejudicial na cicatrização de feridas, especialmente em doses mais elevadas e que regimes de dosagem melhorados podem diminuir ou atenuar este risco.
Agentes antiproliferativos
Existem três agentes antiproliferativos regularmente utilizados: O micofenolato mofetil (MMF) e o micofenolato de sódio (MPS) (ambos inibidores da inosina monofosfato desidrogenase (IMPDH)) e a azatioprina.2,40 Os inibidores da IMPDH têm um efeito semelhante ao dos inibidores da mTOR, em termos do seu mecanismo de imunossupressão. No organismo, o MMF e o MPS são convertidos em ácido micofenólico, o qual bloqueia uma parte de uma via crucial para a síntese de ADN, para diminuir a proliferação de células T e de células B.2,5,40 O MMF é utilizado pelo seu efeito imunossupressor em transplantes de coração, de rins e de pulmões.3,40 O MPS é utilizado em transplantes de rins.40 A azatioprina é utilizada como fármaco imunossupressor em transplantes renais e em doenças auto-imunes, incluindo artrite reumatoide, doença de Crohn e esclerose múltipla.22,41 No organismo, a azatioprina reage com o glutatião e é convertida em 6-mercaptupurina, após o que são gerados metabolitos adicionais que acabam por bloquear a síntese de purinas e também a estimulação das células T.3,22
Quando um estudo comparou duas doses diferentes de MMF em recetores de transplante renal, a incidência de feridas que necessitaram de intervenção cirúrgica não foi significativamente diferente, sendo similar às feridas tratadas com cuidados locais.42 Com base na revisão dos títulos dos artigos e como parte da nossa pesquisa, não foram encontrados estudos relativos ao efeito exclusivo da azatioprina na cicatrização de feridas externas em humanos. Num estudo com ratos, quando a azatioprina foi comparada com um placebo, as feridas dos ratos que tomaram a azatioprina demoraram mais tempo a cicatrizar do que as dos que tomaram o placebo, o que sugere que a azatioprina poderá apresentar efeitos prejudiciais na cicatrização de feridas, mas não é claro em que medida afetaria os seres humanos.43
Anti-metabolito
O metotrexato é um agente imunossupressor antagonista do folato comummente utilizado, com indicações em muitas doenças reumatológicas. Em doses mais elevadas tem também atividade antineoplásica. Ao ser absorvido, entra na célula e é convertido em poliglutamatos de metotrexato, passando a competir com a dihidrofolato redutase, impedindo assim a transformação do ácido fólico para a sua utilização na construção dos ácidos nucleicos.6 À semelhança de outros dos agentes descritos, existem estudos experimentais em animais, com estudos in vitro, que sugerem uma diminuição da cicatrização de feridas, mas estes efeitos não foram confirmados em estudos clínicos, nomeadamente em feridas pós-cirúrgicas.6 Por este motivo, recomenda-se a continuação deste fármaco no pós-operatório.
Corticosteroides/Glucocorticóides
Os glucocorticóides impedem a formação de substâncias químicas inflamatórias, como as citocinas, as moléculas de adesão celular e os fatores do complemento.3 Ao inibir a formação de interleucina-2, os glucocorticóides também impedem a proliferação e a ativação das células T.22 Também prejudicam os monócitos e as células B.3,22 Os glucocorticóides foram o primeiro fármaco anti-rejeição criado, mas, com o passar do tempo, tem havido um movimento para gradualmente os eliminar devido aos seus graves efeitos secundários.3,22 É consensual que os glucocorticóides são altamente prejudiciais para a cicatrização de feridas, uma vez que interferem com muitas fases-chave da cicatrização de feridas, tais como a deposição e a síntese de colagénio, angiogénese, proliferação de fibroblastos, fatores de crescimento e a fagocitose, entre outros.2,3,44,45
Considerações práticas para os prestadores de cuidados de saúde
As pessoas com sistemas imunitários comprometidos (devido a medicamentos, comorbilidades ou extremos etários) requerem considerações adicionais para o tratamento de feridas crónicas. Especificamente em relação aos medicamentos imunossupressores, os prestadores de cuidados de saúde devem elaborar um historial cuidadoso não só dos medicamentos e da dosagem (incluindo alterações na dosagem), mas também das doenças subjacentes que requerem estes medicamentos (por exemplo, doenças autoimunes, transplante de órgãos). Uma vez que muitos medicamentos imunossupressores podem prejudicar a cicatrização de feridas, é fundamental que numa fase inicial os prestadores de cuidados de saúde avaliem o potencial de cicatrização para definir e gerir as expectativas dos pacientes. Dada a complexidade acrescida destes indivíduos. o encaminhamento precoce para especialistas médicos ou cirúrgicos para auxiliar no tratamento de feridas e uma abordagem baseada em equipas será essencial. Nalguns casos em que as feridas não estão a cicatrizar, pode ser necessário definir objetivos alternativos para o tratamento da ferida (por exemplo, manutenção ou não cicatrização) se as doses de imunossupressores não puderem ser reduzidas (partindo do princípio de que estão a contribuir para uma cicatrização deficiente), o que deverá ser feito em consulta com os seus prestadores de cuidados primários ou especializados. À medida que os indivíduos e as populações com comorbilidades vivem durante mais tempo, cuidar de pessoas com feridas crónicas que tomam medicamentos imunossupressores tornar-se-á cada vez mais comum e deverá ser reconhecido precocemente pelos clínicos responsáveis pelo tratamento de feridas.
Discussão
Devido aos avanços contínuos da medicina, aumentou a necessidade de imunossupressão no contexto de transplantes, doenças autoimunes e malignidades. Na nossa revisão, salientámos a pobreza de estudos sólidos neste campo e destacámos os efeitos mistos de várias imunossupressões na cicatrização de feridas. Existem evidências da elevada qualidade na cicatrização de feridas relativamente aos efeitos deletérios da terapêutica com glucocorticoides, bem como da terapêutica com mTOR, em particular o sirolimus. Além disso, quando 4 estudos compararam o sirolimus com o MMF ou com o tacrolimus sistémico, todos os estudos demonstraram que o sirolimus estava associado a um aumento da incidência de complicações da ferida.35,36,46,47
A literatura sobre agentes como os CNIs sistémicos é mista, com alguns a sugerir efeitos adversos nas feridas e outros a sugerir benefícios, sendo necessário um estudo adicional que possa incidir diretamente sobre esta questão. Os CNIs tópicos mais recentes demonstraram ter pouco impacto na cicatrização retardada de feridas e, em alguns casos, benefícios, mas é necessária uma investigação adicional para a sua utilização direta em feridas crónicas. É tranquilizador o facto de os agentes antiproliferativos, os antimetabolitos e os antibióticos monoclonais mais recentes não terem mostrado sinais de diminuição da cicatrização. No entanto, dada a pobreza das evidências sobre a cicatrização de feridas na terapia com mAB são necessários estudos adicionais. Em geral, a nossa análise concluiu que as evidências nesta área se encontram desatualizadas, com conclusões variáveis sobre os efeitos do imunossupressor na cicatrização de feridas. Além disso, encontrámos poucas evidências que utilizassem seres humanos. Em geral, quando após os transplantes são prescritos imunossupressores para prevenir a rejeição, os pacientes tomam mais do que um medicamento para prevenir eficazmente a rejeição. Por conseguinte, existem desafios na realização de estudos em seres humanos que consigam avaliar os efeitos de medicamentos individuais isoladamente.
Como não realizámos uma revisão sistemática, alguns artigos podem ter sido excluídos. Antes de realizar a pesquisa identificámos algumas revisões-chave e garantimos que estavam presentes na pesquisa como uma forma de validação. Além disso, dada a escassez de literatura nesta área, particularmente no que diz respeito ao campo do tratamento de feridas, uma revisão narrativa acrescenta valor, para educar e aumentar a sensibilização, quando se trabalha com indivíduos que tomam estes medicamentos.
Com a crescente necessidade de imunossupressão, é fundamental um estudo adicional neste domínio. As direções futuras incluem a realização de mais estudos em animais com novas classes de imunossupressores para poder identificar potenciais vias para o atraso na cicatrização de feridas e potenciais formas de atenuar esses efeitos. Além disso, são necessários mais estudos de alta qualidade para avaliar imunoterapias individuais e combinadas, para compreender melhor os riscos e a forma como os diferentes imunossupressores podem afetar a cicatrização de feridas. A fim de explorar os imunossupressores como um potencial tratamento para feridas crónicas ou complexas, é importante que os estudos futuros sejam conduzidos em maior escala e controlem os fatores clínicos de confusão, por exemplo, através de ensaios de controlo aleatórios.
Conclusões
Em conclusão, na cicatrização de feridas os imunossupressores variam entre o possivelmente benéfico e o floridamente deletério. Embora neste campo existam poucas evidências conclusivas, vale a pena explorar os efeitos dos imunossupressores na cicatrização de feridas, de forma a adaptar melhor a imunossupressão aos pacientes em risco ou com feridas crónicas que não cicatrizam. Os nossos resultados sugerem que nem todos os imunossupressores são prejudiciais e que alguns podem apresentar benefícios no tratamento de feridas quando as terapias convencionais falham, abrindo a possibilidade de uma nova opção de tratamento para feridas.
Agradecimentos
Programa de verão para Jovens Investigadores do Ensino Secundário da Universidade de Alberta.
Conflito de interesses
Os autores declaram não existirem conflitos de interesse.
Financiamento
Os autores não receberam financiamento para este estudo.
Author(s)
Aria Appoo
Medical Student, University of Oxford, Oxford, UK
Brandon L Christensen
BMSc MD
Resident Physician, University of Calgary, Division of Infectious Diseases, Calgary, Alberta, Canada
Ranjani Somayaji
BScPT MD MPH
Assistant Professor, University of Calgary, Departments of Medicine, Microbiology, Immunology and Infectious Disease and Community Health Sciences, Calgary, Alberta, Canada
References
- Fireman M, DiMartini AF, Armstrong SC, Cozza KL. Immunosuppressants. Psychosomatics. 2004;45(4). doi:10.1176/appi.psy.45.4.354
- Taylor AL, Watson CJE, Bradley JA. Immunosuppressive agents in solid organ transplantation: Mechanisms of action and therapeutic efficacy. Crit Rev Oncol Hematol. 2005;56(1). doi:10.1016/j.critrevonc.2005.03.012
- Weltz A, Scalea J, Popescu M, Xu J, Bromberg JS. Mechanisms of Immunosuppressive Drugs. In: Kidney Transplantation. Springer New York; 2014. doi:10.1007/978-1-4939-0342-9_12
- Subramanian S, Trence DL. Immunosuppressive Agents: Effects on Glucose and Lipid Metabolism. Endocrinol Metab Clin North Am. 2007;36(4). doi:10.1016/j.ecl.2007.07.003
- Mika A, Stepnowski P. Current methods of the analysis of immunosuppressive agents in clinical materials: A review. J Pharm Biomed Anal. 2016;127. doi:10.1016/j.jpba.2016.01.059
- Pountos I, Giannoudis P V. Effect of methotrexate on bone and wound healing. Expert Opin Drug Saf. 2017;16(5):535-545. doi:10.1080/14740338.2017.1310839
- Willems MCM, van der Vliet JA, Lomme RMLM, Hendriks T. Tacrolimus Does Not Affect Early Wound Healing in a Rodent Model of Bowel Anastomoses and Abdominal Wall Closure. PLoS One. 2013;8(9). doi:10.1371/journal.pone.0076348
- Azzi JR, Sayegh MH, Mallat SG. Calcineurin Inhibitors: 40 Years Later, Can’t Live Without …. The Journal of Immunology. 2013;191(12). doi:10.4049/jimmunol.1390055
- Safarani OA, Patel J. Calcineurin Inhibitors. StatPearls Publishing; 2021.
- Willems MCM, van der Vliet JA, Lomme RMLM, Hendriks T. Tacrolimus Does Not Affect Early Wound Healing in a Rodent Model of Bowel Anastomoses and Abdominal Wall Closure. PLoS One. 2013;8(9). doi:10.1371/journal.pone.0076348
- Schäffer MR, Fuchs N, Proksch B, Bongartz M, Beiter T, Becker HD. TACROLIMUS IMPAIRS WOUND HEALING. Transplantation. 1998;65(6). doi:10.1097/00007890-199803270-00008
- The Effect of Tacrolimus on Lower Extremity Ulcers: A Case Study and Review of the Literature. Wound Manag Prev. 2008;54(4).
- Nemlander A, Ahonen J, Wiktorowicz K, et al. Effect of Cyclosporine on Wound Healing An Analysis With Viscous Cellulose Sponges. Transplantation. 1983;36(1):1-5.
- Petri J, Schurk S, Gebauer S, Haustein U. Cyclosporine A delays wound healing and apoptosis and suppresses activin beta-A expression in rats. European Journal of Dermatology. 1998;8(2):104-113.
- Goldberg M, Lima O, Morgan E, et al. A comparison between cyclosporin A and methylprednisolone plus azathioprine on bronchial healing following canine lung autotransplantation. J Thorac Cardiovasc Surg. 1983;85(6). doi:10.1016/S0022-5223(19)37469-0
- Sussman G. The use of topical calcineurin inhibitors in chronic wound management. Wound Practice & Research: Journal of the Australian Wound Management Association. 2000;26(3):140-145.
- Frazier W, Bhardwaj N. Atopic Dermatitis: Diagnosis and Treatment. Am Fam Physician. 2020;101(10):590-598.
- Lyon C, Stapleton M, Smith A, Mendelsohn S, Beck M, Griffiths C. Topical tacrolimus in the management of peristomal pyoderma gangrenosum. Journal of Dermatological Treatment. 2001;12(1). doi:10.1080/095466301750163518
- Ginocchio L, Draghi L, Darvishian F, Ross FL. Refractory Ulcerated Necrobiosis Lipoidica: Closure of a Difficult Wound with Topical Tacrolimus. Adv Skin Wound Care. 2017;30(10). doi:10.1097/01.ASW.0000521867.98577.a5
- Mackelfresh J, Soon S, Arbiser JL. Combination Therapy of Doxycycline and Topical Tacrolimus for Venous Ulcers. JAMA Dermatol. 2005;141(11). doi:10.1001/archderm.141.11.1476
- Namkoong S, Chung J, Yoo J, et al. Topical tacrolimus does not negatively impact acute skin wound healing. Exp Dermatol. 2013;22(5). doi:10.1111/exd.12131
- Khan MM. Immunopharmacology. Springer US; 2008. doi:10.1007/978-0-387-77976-8
- Bibbo C, Goldberg JW. Infectious and Healing Complications after Elective Orthopaedic Foot and Ankle Surgery during Tumor Necrosis Factor-Alpha Inhibition Therapy. Foot Ankle Int. 2004;25(5). doi:10.1177/107110070402500510
- Streit M, Beleznay Z, Braathen LR. Topical application of the tumour necrosis factor-alpha antibody infliximab improves healing of chronic wounds. Int Wound J. 2006;3(3). doi:10.1111/j.1742-481X.2006.00233.x
- Hewitt D, Tait C. Use of infliximab in pyoderma gangrenosum. Australasian Journal of Dermatology. 2007;48(2). doi:10.1111/j.1440-0960.2007.00344.x
- Fox JD, Baquerizo-Nole KL, Keegan BR, et al. Adalimumab treatment leads to reduction of tissue tumor necrosis factor-alpha correlated with venous leg ulcer improvement: a pilot study. Int Wound J. 2016;13(5). doi:10.1111/iwj.12497
- Lopes JV, Freitas LAM de, Marques RD, Bocca AL, Sousa JB de, Oliveira PG de. Analysis of the tensile strength on the healing of the abdominal wall of rats treated with infliximab. Acta Cir Bras. 2008;23(5). doi:10.1590/S0102-86502008000500009
- Larrañaga MD, Lewis S, Richard J, Robert A, eds. Polyclonal Antibodies. In: Hawley’s Condensed Chemical Dictionary. 16th ed. Wiley; 2016.
- Johnson M. Monoclonal Antibodies. In: Longe JL, ed. Gale Encyclopedia of Nursing and Allied Health. 4th ed. Credo Reference; 2018.
- Ueno P, Felipe C, Ferreira A, et al. Wound Healing Complications in Kidney Transplant Recipients Receiving Everolimus. Transplantation. 2017;101(4). doi:10.1097/TP.0000000000001392
- Patel S, Pankewycz O, Kohli R, et al. Obesity in Renal Transplantation: The Role of Induction Therapy on Long-Term Outcomes. Transplant Proc. 2011;43(2). doi:10.1016/j.transproceed.2011.01.040
- Kordestani SS. Atlas of Wound Healing. (Abyaneh S, Fayyazbakhsh, eds.). Elsevier; 2019.
- Azzola A, Havryk A, Chhajed P, et al. Everolimus and mycophenolate mofetil are potent inhibitors of fibroblast proliferation after lung transplantation1. Transplantation. 2004;77(2). doi:10.1097/01.TP.0000101822.50960.AB
- P. B. Wound healing and the role of fibroblasts. J Wound Care. 2013;22(8). doi:10.12968/jowc.2013.22.8.407
- Dean PG, Lund WJ, Larson TS, et al. Wound-Healing Complications After Kidney Transplantation: A Prospective, Randomized Comparison Of Sirolimus And Tacrolimus1. Transplantation. 2004;77(10). doi:10.1097/01.TP.0000123082.31092.53
- Larson TS, Dean PG, Stegall MD, et al. Complete Avoidance of Calcineurin Inhibitors in Renal Transplantation: A Randomized Trial Comparing Sirolimus and Tacrolimus. American Journal of Transplantation. 2006;6(3). doi:10.1111/j.1600-6143.2005.01177.x
- Schäffer M, Schier R, Napirei M, Michalski S, Traska T, Viebahn R. Sirolimus impairs wound healing. Langenbecks Arch Surg. 2007;392(3). doi:10.1007/s00423-007-0174-5
- Nashan B, Citterio F. Wound Healing Complications and the Use of Mammalian Target of Rapamycin Inhibitors in Kidney Transplantation. Transplantation. 2012;94(6). doi:10.1097/TP.0b013e3182551021
- Citterio F, Henry M, Kim DY, et al. Wound healing adverse events in kidney transplant recipients receiving everolimus with reduced calcineurin inhibitor exposure or current standard-of-care: Insights from the 24 month TRANSFORM study. Expert Opin Drug Saf. Published online 2020:1339-1348. doi:10.1080/14740338.2020.1792441
- Staatz CE, Tett SE. Clinical Pharmacokinetics and Pharmacodynamics of Mycophenolate in Solid Organ Transplant Recipients. Clin Pharmacokinet. 2007;46(1). doi:10.2165/00003088-200746010-00002
- Casetta I, Iuliano G, Filippini G. Azathioprine for multiple sclerosis. Cochrane Database of Systematic Reviews. Published online October 17, 2007. doi:10.1002/14651858.CD003982.pub2
- Flechner SM, Feng J, Mastroianni B, et al. The Effect of 2-Gram Versus 1-Gram Concentration Controlled Mycophenolate Mofetil on Renal Transplant Outcomes Using Sirolimus-Based Calcineurin Inhibitor Drug-Free Immunosuppression. Transplantation. 2005;79(8). doi:10.1097/01.TP.0000155430.52845.51
- Ginestal R, Pérez-Köhler B, Pérez-López P, et al. Comparing the influence of two immunosuppressants (fingolimod, azathioprine) on wound healing in a rat model of primary and secondary intention wound closure. Wound Repair and Regeneration. 2019;27(1). doi:10.1111/wrr.12685
- Wicke C. Effects of Steroids and Retinoids on Wound Healing. Archives of Surgery. 2000;135(11). doi:10.1001/archsurg.135.11.1265
- Anstead G. Steroids, retinoids, and wound healing. Adv Wound Care (New Rochelle). 1998;11(6):277-285.
- Valente JF, Hricik D, Weigel K, et al. Comparison of Sirolimus vs. Mycophenolate Mofetil on Surgical Complications and Wound Healing in Adult Kidney Transplantation. American Journal of Transplantation. 2003;3(9). doi:10.1034/j.1600-6143.2003.00185.x
- Kuppahally S, Al-Khaldi A, Weisshaar D, et al. Wound Healing Complications with De Novo Sirolimus Versus Mycophenolate Mofetil-Based Regimen in Cardiac Transplant Recipients. American Journal of Transplantation. 2006;6(5p1). doi:10.1111/j.1600-6143.2006.01282.x
- Ormerod AD, Thomas KS, Craig FE, et al. Comparison of the two most commonly used treatments for pyoderma gangrenosum: results of the STOP GAP randomised controlled trial. BMJ. 2015;350(jun12 3). doi:10.1136/bmj.h2958
- Flechner SM, Zhou L, Derweesh I, et al. The impact of sirolimus, mycophenolate mofetil, cyclosporine, azathioprine, and steroids on wound healing in 513 kidney-transplant recipients. Transplantation. 2003;76(12). doi:10.1097/01.TP.0000093502.26208.42
- Citterio F, Henry M, Kim DY, et al. Wound healing adverse events in kidney transplant recipients receiving everolimus with reduced calcineurin inhibitor exposure or current standard-of-care: insights from the 24-month TRANSFORM study. Expert Opin Drug Saf. 2020;19(10). doi:10.1080/14740338.2020.1792441
- Kapugi M, Cunningham K. Corticosteroids. Orthopaedic Nursing. 2019;38(5):336-339. doi:10.1097/NOR.0000000000000595
- Ponticelli C. Cyclosporine: From Renal Transplantation to Autoimmune Diseases. Ann N Y Acad Sci. 2005;1051(1):551-558. doi:10.1196/annals.1361.099
- Akar Y, Yucel G, Durukan AH, Yucel I, Arici G. Laboratory Science. Systemic toxicity of tacrolimus given by various routes and the response to dose reduction. Clin Exp Ophthalmol. 2005;33(1):53-59. doi:10.1111/j.1442-9071.2005.00942.x
- Kurian K, Addisu A. Sirolimus: A Novel Immunosuppressive Drug in Heart Transplantation. Recent Pat Cardiovasc Drug Discov. 2009;4(3):187-191. doi:10.2174/157489009789152294
- Sehgal SN. Sirolimus: its discovery, biological properties, and mechanism of action. Transplant Proc. 2003;35(3):S7-S14. doi:10.1016/S0041-1345(03)00211-2
- van Gelder T, Fischer L, Shihab F, Shipkova M. Optimizing everolimus exposure when combined with calcineurin inhibitors in solid organ transplantation. Transplant Rev. 2017;31(3):151-157. doi:10.1016/j.trre.2017.02.007
- Falkowski S, Woillard JB. Therapeutic Drug Monitoring of Everolimus in Oncology: Evidences and Perspectives. Ther Drug Monit. 2019;41(5):568-574. doi:10.1097/FTD.0000000000000628
- Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases. LiverTox: Clinical and Research Information on Drug-Induced Liver Injury.; 2020.
- Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases. LiverTox: Clinical and Research Information on Drug-Induced Liver Injury.; 2017. Accessed February 10, 2022. https://www-ncbi-nlm-nih-gov.ezproxy.lib.ucalgary.ca/books/NBK548018/
- Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases. LiverTox: Clinical and Research Information on Drug-Induced Liver Injury.; 2017. Accessed February 10, 2022. https://www-ncbi-nlm-nih-gov.ezproxy.lib.ucalgary.ca/books/NBK548587/
- Lichtenstein L, Ron Y, Kivity S, et al. Infliximab-Related Infusion Reactions: Systematic Review. J Crohns Colitis. 2015;9(9):806-815. doi:10.1093/ecco-jcc/jjv096
- Tracey D, Klareskog L, Sasso EH, Salfeld JG, Tak PP. Tumor necrosis factor antagonist mechanisms of action: A comprehensive review. Pharmacol Ther. 2008;117(2):244-279. doi:10.1016/j.pharmthera.2007.10.001
- Chavez-Alvarez S, Herz-Ruelas M, Villarreal-Martinez A, Ocampo-Candiani J, Garza-Garza R, Gomez-Flores M. Azathioprine: its uses in dermatology. An Bras Dermatol. 2020;95(6):731-736. doi:10.1016/j.abd.2020.05.003



