Volume 41 Number 1
Comprehensive treatment, including topical care, for severe facial burn
Beihua Xu, Yajuan Weng and Suping Bai
Keywords dressing, Wound care, burn, Aquacel Ag
For referencing Xu B et al. Comprehensive treatment, including topical care, for severe facial burn. WCET® Journal 2021;41(1):16-20
DOI https://doi.org/10.33235/wcet.41.1.16-20
Abstract
Background The face is the area central to a person’s identity that provides our most expressive means of communication. Facial burns are extremely serious medical problems. Topical interventions are currently the cornerstone of treatment of facial burns.
Case The authors report a 45-year-old woman who presented with a 1-hour old, 90% total body surface area (TBSA), including a mixture of deep II° and III° burns to her face. A silver impregnated dressing was used to care for the facial burn wounds.
Conclusion The silver impregnated dressing AQUACEL® Ag Hydrofiber® was found to be useful in nursing the facial burn wounds in this case.
Introduction
Burn injuries are an important health problem worldwide. In the USA, burns result in 45,000 admissions per year, of which more than 25,000 admissions are to hospitals with specialised burn centres1.
The head and neck area has been identified as the site most frequently affected by thermal injuries1. Facial burns are extremely serious due to the abundance of nerves and blood vessels2. In addition, complications such as facial scar hyperplasia, minor mouth deformity, upper eyelid ectropion and reduced or total lack of facial expressions can occur, resulting in psychological trauma and increased treatment costs3. Adequate facial burn care can improve the physical function and burned tissue recovery and relieve the psychological burden of patients4. A wide variety of agents are available for treatment of burn wounds, including ointments, creams and biological and non-biological dressings5.
Currently, there is no consensus on the optimal topical interventions for burn wound coverage to prevent or control infection or to enhance wound healing and minimise life-long scarring. Here, the authors report the case of a 45-year-old female case with a 1-hour old, 90% total body surface area (TBSA), including a mixture of deep II° and III° flame burns, cared for with a silver impregnated dressing with a satisfactory effect.
Background
The patient suffered flame burns due to ignition of a gas leakage. She stayed at home alone for 1 hour post-injury, refusing treatment, although there was no evidence of altered mental status at the time of injury. On arrival at her home, her family called emergency services, and she was sent to hospital.
Physical examination showed a body temperature of 36.2°C, a heart rate of 90 beats/min, a respiratory rate of 20 breaths/min, and a blood pressure of 168/104mmHg. The medical history surrounding the current facial burn wound was presented by the patient herself. The pain in burn wounds reached a score of 0–3/10 on the Visual Analogue Scale6. The Generalized Anxiety Disorder 7-Item (GAD-7) Scale7 showed a score of 18, which meant the patient exhibited signs of severe anxiety. She had slightly fidgety and cold extremities and was thirsty, yet no fever or tachycardia or confusion. Her current and past medical history found no heart disease or lung disease or epidemiological history of COVID-19.
The overall percentage of burnt skin on the patient’s body was estimated by the Rule of 9s8. Burns spanned the face (4% II°) (upper row, Figure 1 shows the facial wound image on admission), neck (3% II°), anterior trunk (12% II°), posterior trunk (13% II°), bilateral upper arms (4% II°, 3% III°), bilateral forearms (3% II°, 3% III°), bilateral hands (2% II°, 1% III°), buttocks (4% II°), bilateral thighs (11% II°, 10% III°), bilateral legs (13% III°), and feet (4% III°), a total of 56% II° and 34% III°. The only unburned area seen was genitalia skin. There were small amounts of purulent secretions near the eyes, and the left auricle skin was intact; however, there was crust was inside the auricle. The skin of the right auricle was ruptured, and there was blood and purulent secretions in the auricle and ear canal. Though the skin condition around both eyes was poor, the eyeballs were not injured.
Further intensive examination showed burns of varying degree with the epidermal layer; these were moist, mostly hyperaemic and blanching with significant swelling. Vibrissa and hair on the scalp were partially scorched. Besides deep II° to III° burns, the patient was also diagnosed with inhalation injury and (hypovolaemic) burn shock.
Clinical management
Upon the diagnoses, the patient was placed on a suspended bed, with a room temperature of 25°C and humidity 60%. The standard wound care regimen for burn wounds in the authors’ hospital of broad-spectrum intravenous antibiotics was implemented for all burn wounds sustained. On day 1 (the next day after admission), and on days 4, 7, 11 and 18, the patient received excision, debridement and allografts to affected burn tissue with the exception of the face.
Assessment and management of facial burn wounds
Regarding the facial burns, the patient received initial treatment in the form of a thorough face wash with sterile 0.9% saline and removal of debris. The face was then dried with sterile gauze. Hair in the burned area was shaved off with electric clippers to facilitate wound assessment and management.
The wound care specialty team, including enterostomal therapists (ETs) and wound care nurses, collectively assessed the patient’s facial burns and identified several salient issues as indicated in Table 1. The wound care specialty team confirmed that the priorities of nursing care for this case were improving the skin integrity of burned skin through the application of an appropriate dressing to facilitate wound healing and minimise scarring, decreasing wound exudate and associated burn pain, and liaising with allied health professionals to assist in preventing malnutrition from hypermetabolism and trauma-induced anxiety. ET/wound care nurses alone would not be able to address pain, hypermetabolism or anxiety. The management of burn wounds is multidisciplinary.
Table 1. Assessment of patient’s facial wound
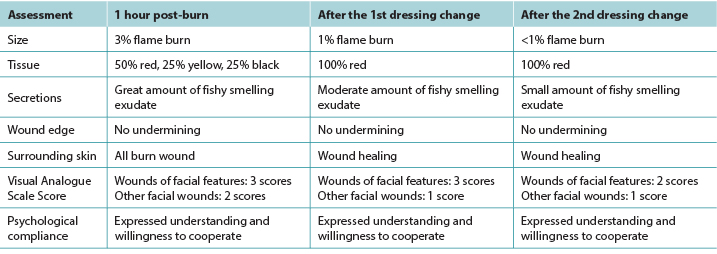
The first facial dressing was on day 0 (admission). The aim was to debride all non-viable burned tissue, to control the infection, and to implement effective exudate management. Before commencing the dressing procedure the patient was informed of the purpose of the facial wound care and the processes involved. Sterile gauze soaked in sterile water for injection was used to apply wet compresses to the face to moisten and clean the wound and facilitate easy removal of the gauze from the face to reduce the patient’s pain and discomfort. Conservative sharp wound debridement with sterile sharp instruments and forceps was then undertaken to clear facial eschar and necrotic tissue. Next, gauze was used to re-clean the facial wound. Finally, a silver dressing (AQUACEL® Ag Hydrofiber®, ConvaTec Ltd., UK) was chosen as the primary interface dressing. In order to permit eyelid movement, the eyelids were not covered with Aquacel® Ag sheets. The next day the patient’s facial wound dressings were fixed to the wound without displacement. A small amount of black exudate on the dressing was found. The patient had no complaints (upper row, Figure 1). The dressings were checked every day.
The second dressing change occurred on day 5. We found the wound bed had less necrotic tissue, exudate and odour were less, and the periwound skin had improved as per Table 1. The facial contour was more discernible because there was less swelling. The dressings were slowly removed to enable reassessment of the facial wound. The nursing regimen was repeated as for the first dressing. On day 6, the patient’s facial wound was observed, and only a small amount of exudate was found in the auricle. A sterile dry cotton ball was placed in the auricle. The patient was inspected and the dressing replaced as needed (middle row, Figure 1). The dressings were checked every day.
The clinical characteristics and improved condition of the facial wounds before the third dressing change on day 12 are listed in Table 1. The wound management regimen was assessed as being effective as the burn wounds continued to improve. Less dressing product was being applied, thereby exposing more of the face (lower row, Figure 1). The wound management goals of care remained the same: debriding to the maximum extent, controlling the infection, and implementing effective exudate management. The dressing regimen remained unchanged. There was a small amount of dry scab in the auricle, therefore the sterile dry cotton ball was not needed. The dressings were checked every day.
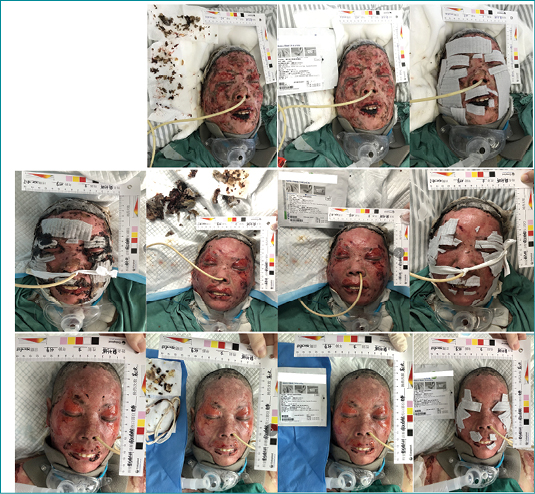
Figure 1. Face wound images
Upper: images before and after the 1st dressing change
Middle: images before and after the 2nd dressing change
Lower: images before and after the 3rd dressing change
After the three facial wound dressing changes, the patient’s facial wounds had healed significantly (Figure 2).
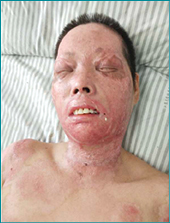
Figure 2. After the three dressing changes
Discussion
Approximately two-thirds of communication is non-verbal, mediated principally by facial expression that also allows for individual identity. The healing of facial wounds is of great significance to patients, and effective intervention can reduce the chance of disfigurement. It is necessary to customise a personalised nursing plan according to the specific injury and condition of the patient’s wound.
Facial wound healing is affected by patient-related factors, the characteristics of the wound, and associated cellular repair processes with overlapping problems of microcirculation, local immunity, and dressing methods. The desired result is healing with minimal scarring and no functional defects2.
In this case, most facial tissue was lost from heat coagulation of the protein within the tissue from the gas explosion and resultant flames. The extent of tissue loss, however, was progressive and resulted from the release of local mediators, changes in blood flow, tissue oedema, and infection. Multiple difficulties for wound care were observed. First, assessment of facial wounds with cultures found Gram-positive bacterial (Staphylococcus aureus and extensively drug-resistant Acinetobacter baumannii) infections. Second, the patient on admission was in a period of extensive tissue dissolution. The necrotic tissue was dissolving, and there was massive amounts of bloody and purulent exudate on the local area. The exudate spread to the concave parts of the face, and the eyes and ears of the patient were likely to be further compromised. Third, facial blood vessels and nerves are richer than other areas of the body. Carelessness during the administration of wound healing interventions can easily result in severe sequelae such as scar hyperplasia, decreased or loss of facial features. Fourth, the newly deposited granulation tissue was friable and prone to bleeding when touched. Fifth, the TBSA was large and deep and, in response, the body was hypermetabolic which resulted in prolonged wound healing. And last, in this accident, her son was also injured. The patient was less worried about her own condition and more about her son’s.
An effective dressing should be cheap, alleviate pain, prevent infection, be easy to handle, permit easy and early mobilisation, have no toxicity, cause no allergic reactions, and facilitate wound healing with a cosmetically acceptable scar.
Sodium carboxymethyl cellulose, silver impregnated antimicrobial dressing is a soft, sterile, non-woven pad or ribbon dressing composed of sodium carboxymethylcellulose and 1.2% ionic silver which allows for a maximum of 12mg of silver for a 4x4 inch dressing. The silver in the dressing kills wound bacteria held in the dressing9. Caruso et al. compared the effect of Aquacel® Ag and that of silver sulphadiazine in the treatment of partial-thickness burns and observed that there was less pain and less anxiety during dressing changes with Aquacel® Ag and also that fewer analgesics and narcotics were used in patients treated with Aquacel® Ag10. Hindy11 concluded that Aquacel® Ag was found to be comparable to moist exposed burn ointment (MEBO), particularly allowing more rapid healing, and was psychologically less traumatic for those who cannot tolerate strong odour of dressings.
In this case, the dressing facilitated facial wound healing. However, these dressings are expensive, and the cost of each dressing change was not cheap, however, Robinson et al.12 reported that a cost-benefit study of the hydrofibre dressing demonstrated a significant saving of clinical time, owing to the fact that the largest component in the cost-benefit equation was staff time. The patient in this case attached great importance to family, had a high degree of compliance, and was willing to communicate so that pain and psychological problems could be identified and resolved in a timely manner.
A complication in this case was the amount of exudate from autolysing necrotic tissue which could not be estimated in advance, thereby limiting protective measures. Therefore, more clinical factors and potential for such complications to arise should be considered in the assessment and ongoing evaluation of wound healing to allow for more proactive measures to facilitate wound healing and meet nursing goals. The cost of dressing for wounds is high, and the affordability of patients and their families should be considered in the subsequent nursing process.
But still there are possible solutions. According to hospital policy, the manufacturer of the dressing is supposed to negotiate with medical insurance department to cover part of the fee. In practice, wound care nurses may be able to cut the dressings if this is in accordance with manufacturer guidelines. The cutting of the dressing into pieces instead of applying the dressing in one piece is mainly for two reasons. First, the facial contour is irregular, and cut dressings fit the size and shape of the burn wound better. Second, cutting the dressings reduces the fees for patients. In this case, it was identified that cutting the dressings did not incur any adverse effects or compromise wound healing of the facial burn.
Facial features are more sensitive to pain due to abundance of nerves2. In this case scenario, wound debridement and dressing changes caused pain which can easily cause poor coordination of patient care and place a heavy psychological burden on nursing staff, and slow down the process of facial wound care. By digitally assessing the location, nature and duration of wound pain, individualised pain care measures are formulated according to the characteristics of the patient, with psychological intervention as the mainstay. Before each dressing change, the authors discussed the procedure with the patient and told her the actions that indicated pain such as opening her mouth or nodding. During the dressing procedure, the patient was informed of the current dressing procedure steps, the site where debridement would be performed, and how much necrotic tissue was likely to be removed, so that the patient was psychologically prepared to cooperate with the dressing procedure. The dressing procedure was suspended when the patient sent a signal of pain.
The environment directly affects the psychological activities of patients, and creating a beautiful and comfortable environment has a good impact on the psychology of patients. The ward environment was clean and bright, with a temperature of 25°C and a humidity of 60%.
Establishing a good nurse–patient relationship is the key to the effectiveness of psychological care. Using polite language, being sincere, natural, gentle, calm, having friendly conversations yet being serious about the dressing process, always being optimistic and having a cheerful mood, paying attention to the attitude of dealing with others and your appearance, having a good demeanour and posture are all conducive to building respect, trust and cooperation.
Psychological support was applied everyday, providing psychological comfort, persuasion and guidance to patients to achieve the purpose of treatment. The authors strived for the close cooperation of family members and friends.
Conclusion
Burn injuries are an important health problem worldwide. Facial burns are extremely serious due to the abundance of nerves and blood vessels. This case study reports a case of a 45-year-old female case with a 1-hour old, 90% TBSA, including a mixture of deep II° and III° flame burns, cared for with a silver impregnated dressing, AQUACEL® Ag Hydrofiber®, with a satisfactory effect. Further studies are needed in order to find the ideal dressing for facial burn management.
Acknowledgements
We thank the patient’s family, the surgical team and the nursing staff involved in the surgery and care.
Conflict of Interest
The authors declare no conflicts of interest.
Funding
This work was funded by grant from Guiding Program for Science and Technology of Changzhou Health Commission (WZ201905, to Beihua Xu).
Traitement complet, y compris les soins topiques, pour les brûlures faciales graves
Beihua Xu, Yajuan Weng and Suping Bai
DOI: https://doi.org/10.33235/wcet.41.1.16-20
Résumé
Contexte Le visage est la zone centrale de l’identité d’une personne qui constitue notre moyen de communication le plus expressif. Les brûlures faciales sont des problèmes médicaux extrêmement graves. Les interventions topiques sont actuellement la pierre angulaire du traitement des brûlures du visage.
Cas Les auteurs rapportent le cas d’une femme de 45 ans qui s’est présentée avec une brûlure datant d’une heure, d’une surface corporelle totale (SCT) de 90%, comprenant un mélange de brûlures profondes de 2e et 3e degrés au visage. Un pansement imprégné d’argent a été utilisé pour soigner les brûlures faciales.
Conclusion Le pansement imprégné d’argent AQUACEL® Ag Hydrofiber® s’est avéré utile pour soigner les brûlures du visage dans ce cas.
Introduction
Les brûlures constituent un problème de santé important dans le monde entier. Aux États-Unis, les brûlures entraînent 45 000 hospitalisations par an, dont plus de 25 000 dans des hôpitaux dotés de centres spécialisés dans le traitement des grands brûlés1.
La région de la tête et du cou a été identifiée comme la zone la plus fréquemment touchée par les blessures thermiques1. Les brûlures faciales sont extrêmement graves en raison de l’abondance des nerfs et des vaisseaux sanguins2. En outre, des complications telles que l’hyperplasie des cicatrices faciales, une déformation mineure de la bouche, l’ectropion de la paupière supérieure et la réduction ou l’absence totale d’expressions faciales peuvent survenir, entraînant un traumatisme psychologique et une augmentation des coûts du traitement3. Des soins adéquats pour les brûlures du visage peuvent améliorer la fonction physique, la récupération des tissus brûlés et soulager la charge psychologique des patients4. Une grande variété de matériels est disponible pour le traitement des brûlures, notamment des pommades, des crèmes et des pansements biologiques et non biologiques5.
Actuellement, il n’y a pas de consensus sur les interventions topiques optimales pour la couverture des brûlures afin de prévenir ou de contrôler l’infection, d’améliorer la cicatrisation et de réduire lla durée de vie des cicatrices. Les auteurs rapportent ici le cas d’une femme de 45 ans présentant une surface corporelle totale (STC) de 90%, datant d’une heure, comprenant un mélange de brûlures profondes par flamme de 2e et 3e degrés soignée avec un pansement à l’argent avec un effet satisfaisant.
Contexte
La patiente souffrait de brûlures dues aux flammes produites parune fuite de gaz. Elle est restée seule à la maison pendant une heure après la blessure, refusant tout traitement, bien qu’il n’y ait aucune preuve d’altération de son état mental au moment de la blessure. En arrivant à son domicile, sa famille a appelé les services d’urgence, et elle a été envoyée à l’hôpital.
L’examen physique a révélé une température corporelle de 36,2°C, une fréquence cardiaque de 90 battements/min, une fréquence respiratoire de 20 respirations/min et une pression sanguine de 168/104mmHg. L’histoire médicale concernant la brûlure faciale actuelle a été présentée par la patiente elle-même. La douleur des brûlures atteint un score de 0-3/10 sur l’échelle visuelle analogique6. L’échelle du trouble d’anxiété généralisée à 7 éléments (GAD-7) a révélé un score de 18, ce qui signifie que la patiente présentait des signes d’anxiété sévère. Elle avait les extrémités légèrement agitées et froides et avait soif, mais pas de fièvre ni de tachycardie, ni de confusion. Son histoire médicale actuelle et passée n’ont révélé aucune maladie cardiaque ou pulmonaire ni aucun antécédent épidémiologique de COVID-19.
Le pourcentage global de peau brûlée sur le corps de la patiente a été estimé avec la règle de 9s 8. Les brûlures s’étendaient au visage (4% du 2e degré) (rangée supérieure, la figure 1 montre l’image de la plaie faciale à l’admission), au cou (3% du 2e degré), au tronc antérieur (12% du 2e degré), au tronc postérieur (13% du 2e degré), aux bras supérieurs bilatéraux (4% du 2e degré, 3% du 3e degré), avant-bras bilatéraux (3% du 2e degré, 3% du 3e degré), mains bilatérales (2% du 2e degré, 1% du 3e degré), fessier (4% du 2e degré), cuisses bilatérales (11% du 2e degré, 10% du 3e degré), jambes bilatérales (13% du 3e degré), et pieds (4% du 3e degré), soit un total de 56% du 2e degré et 34% du 3e degré. La seule zone non brûlée constatée était la peau des organes génitaux. Il y avait de petites quantités de sécrétions purulentes près des yeux, et la peau de l’auricule gauche était intacte; cependant, il y avait une croûte à l’intérieur de l’auricule. La peau de l’auricule droit était rompue, et il y avait du sang et des sécrétions purulentes dans l’auricule et le canal auditif. Bien que l’état de la peau autour des deux yeux soit mauvais, les globes oculaires n’ont pas été blessés.
Un examen plus approfondi a montré des brûlures de degré variable au niveau de la couche épidermique; celles-ci étaient humides, le plus souvent hyperémiques et blanchissantes avec un gonflement important. Les vibrisses et les cheveux du cuir chevelu ont été partiellement brûlés. Outre des brûlures profondes du 2e et du 3e degrés, le patient présentait également des lésions par inhalation et un choc (hypovolémique) dû aux brûlures.
Prise En Charge Clinique
Une fois les diagnostics posés, la patiente a été placé sur un lit suspendu, avec une température ambiante de 25°C et une humidité de 60%. Le projet de soins standard des brûlures de l’hôpital des auteurs, à savoir des antibiotiques intraveineux à large spectre, a été mis en œuvre pour toutes les plaies de brûlures subies. Le jour 1 (le lendemain de l’’hospitalisation), et les jours 4, 7, 11 et 18, le patient a fait l’objet d’une excision, d’une détersion et d’allogreffes des tissus brûlés affectés, à l’exception du visage.
Évaluation Et Prise En Charge Des Brûlures Faciales
En ce qui concerne les brûlures faciales, la patiente a reçu un traitement initial sous la forme d’un lavage complet du visage avec une solution saline stérile à 0,9% et l’élimination des débris. Le visage a ensuite été séché avec une gaze stérile. Les cheveux de la zone brûlée ont été rasés à l’aide d’une tondeuse électrique afin de faciliter l’évaluation et le traitement des plaies.
L’équipe spécialisée dans les soins des plaies, y compris les Sstomathérapeutes(ET) et les infirmières et infirmiers en soins des plaies, a évalué collectivement les brûlures faciales du patient et a identifié plusieurs problèmes saillants, comme indiqué dans le tableau 1. L’équipe spécialisée dans les soins des plaies a confirmé que les priorités des soins infirmiers pour ce cas étaient d’améliorer l’intégrité de la peau brûlée par l’application d’un pansement approprié pour faciliter la cicatrisation et réduire les cicatrices, de diminuer l’exsudat de la plaie et la douleur associée à la brûlure, et d’assurer la liaison avec les professionnels paramédicaux pour aider à prévenir la malnutrition due à l’hypermétabolisme et à l’anxiété induite par le traumatisme. Les infirmières et infirmiers stomathérapeutes spécialisés dans les soins des plaies ne pourraient pas, à eux seuls, traiter la douleur, l’hypermétabolisme ou l’anxiété. La prise en charge des brûlures est multidisciplinaire.
Tableau 1. Évaluation des plaies faciales du patient
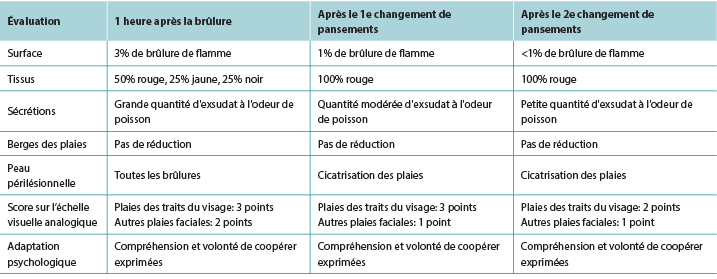
Le premier pansement facial a été effectué le jour 0 (hospitalisation). L’objectif était de débrider tous les tissus brûlés non viables, de contrôler l’infection et de mettre en place une prise en charge efficace des exsudats. Avant de commencer la procédure de pansement, la patiente a été informée de l’objectif du soin des plaies faciales et des processus engagés. De la gaze imbibée d’eau stérile pour injection a été utilisée pour appliquer des compresses humides sur le visage afin d’humidifier et de nettoyer la plaie et de faciliter le retrait de la gaze du visage pour réduire la douleur et l’inconfort du patient. Une détersion conservatrice des plaies à l’aide d’instruments tranchants et de pinces stériles a ensuite été entrepris pour éliminer les escarres et les tissus nécrotiques du visage. Ensuite, une gaze a été utilisée pour nettoyer à nouveau les plaies faciales. Enfin, un pansement à l’argent (AQUACEL® Ag Hydrofiber®, ConvaTec Ltd., UK) a été choisi comme pansement d’interface primaire. Afin de permettre le mouvement des paupières, les paupières n’ont pas été recouvertes de pansements Aquacel® Ag. Le lendemain, les pansements de la plaie faciale de la patiente étaient fixés à la plaie sans déplacement. Une petite quantité d’exsudat noir a été trouvée sur le pansement. La patiente ne s’est pas plainte (rangée supérieure, figure 1). Les pansements étaient vérifiés tous les jours.
Le deuxième changement de pansement a eu lieu le jour 5. Nous avons constaté que le lit de la plaie présentait moins de tissus nécrotiques, que l’exsudat et l’odeur étaient moindres, et que la peau périlésionnelle s’était améliorée, comme le montre le tableau 1. Le contour du visage était plus discernable car le gonflement était moindre. Les pansements ont été retirés lentement pour permettre une réévaluation des plaies faciales. Le projet de soins a été répété comme pour le premier pansement. Le sixième jour, les plaies faciales de la patiente ont été observées, et seule une petite quantité d’exsudat a été trouvée dans l’auricule. Une boule de coton sec et stérile a été placée dans l’auricule. La patiente a été inspectée et les pansements ont été remplacés si nécessaire (rangée du milieu, figure 1). Les pansements étaient vérifiés tous les jours.
Les caractéristiques cliniques et l’amélioration de l’état des plaies faciales avant le troisième changement de pansement au jour 12 sont répertoriées dans le tableau 1. Le projet de traitement des plaies a été jugé efficace car les brûlures ont continué à s’améliorer. La quantité de pansement appliquée était moindre, ce qui exposait davantage le visage (rangée inférieure, figure 1). Les objectifs de soins des plaie ssont restés les mêmes: déterger au maximum, contrôler l’infection et mettre en place une prise en pcharge efficace des exsudats. Le projet de pansement est resté inchangé. Il y avait une petite quantité de croûte sèche dans l’auricule, donc la boule de coton stérile sèche n’était pas nécessaire. Les pansements étaient vérifiés tous les jours.

Figure 1. Images des plaies faciales
En haut: images avant et après le 1er changement de pansement
Milieu: images avant et après le 2e changement de pansement
En bas: images avant et après le 3e changement de pansement
Après les trois changements de pansements des la plaies faciales, les plaies faciales de la patiente avaient cicatrisé de manière significative (figure 2).

Figure 2. Après les trois changements de pansement
Discussion
Environ deux tiers de la communication est non verbale, principalement par le biais de l’expression faciale, qui permet également l’identité individuelle. La cicatrisation des plaies faciales revêt une grande importance pour les patients, et une intervention efficace peut réduire les risques de défiguration. Il est nécessaire d’établir un plan de soins infirmiers personnalisé en fonction des caractéristiques des blessures et de l’état des plaies du patient.
La cicatrisation des plaies faciales est affectée par des facteurs liés au patient, les caractéristiques des plaies et les processus de réparation cellulaire associés, avec des problèmes de microcirculation, d’immunité locale et de méthodes de pansement qui se chevauchent. Le résultat souhaité est une cicatrisation avec une cicatrice minimale et sans défaut fonctionnel2.
L’étendue de la perte de tissus, cependant, était progressive et résultait de la libération de médiateurs locaux, de changements dans le flux sanguin, d’œdèmes tissulaires et d’infections. De multiples difficultés dans le soin des plaies ont été observées. Tout d’abord, l’évaluation des plaies faciales lors de la mise en culture a révélé des infections bactériennes à Gram positif (Staphylococcus aureus et Acinetobacter baumannii extrêmement résistant aux médicaments). Deuxièmement, le patient au moment de l’hospitalisation était en période de dissolution étendue des tissus. Le tissu nécrotique se dissolvait et la zone locale présentait des quantités massives d’exsudat sanglant et purulent. L’exsudat s’est étendu aux parties concaves du visage, et les yeux et les oreilles du patient risquaient d’être davantage compromis. Troisièmement, les vaisseaux sanguins et les nerfs du visage sont plus riches que ceux des autres zones du corps. Une négligence durant les interventions de cicatrisation peut facilement entraîner des séquelles graves telles que l’hyperplasie des cicatrices, la réduction ou la perte des traits du visage. Quatrièmement, les tissus de granulation nouvellement déposés était friable et avait tendance à saigner au toucher. Cinquièmement, la STC brûlée était étendue et profonde et, en réponse, le corps était hypermétabolique, ce qui a entraîné une cicatrisation prolongée. Et enfin, dans cet accident, son fils a également été blessé. La patiente s’inquiétait moins de son propre état et davantage de celui de son fils.
Un pansement efficace doit être bon marché, soulager la douleur, prévenir l’infection, être facile à manipuler, être accessible facilement et rapidement, ne présenter aucune toxicité, ne provoquer aucune réaction allergique et faciliter la cicatrisation de la plaie avec une cicatrice acceptable sur le plan esthétique.
Le pansement antimicrobien à l’argent et de carboxyméthylcellulose sodique est une compresse ou un ruban souple, stérile et non tissé composé de carboxyméthylcellulose sodique et de 1,2% d’argent ionique, ce qui permet d’obtenir un maximum de 12 mg d’argent pour un pansement de 3,5 par 3,5 cm (4 x 4 pouces). L’argent contenu dans le pansement tue les bactéries de la plaie retenues dans le pansement9. Caruso et al. ont comparé l’effet d’Aquacel® Ag et celui de la sulfadiazine d’argent dans le traitement des brûlures semi-profondes et ont observé que la douleur et l’anxiété étaient moindres pendant les changements de pansement avec Aquacel® Ag et que moins d’analgésiques et de narcotiques étaient utilisés chez les patients traités avec Aquacel® Ag10. Hindy11 a conclu qu’Aquacel® Ag s’est avéré comparable à une pommade humide pour brûlures exposées (MEBO), permettant notamment une guérison plus rapide, et qu’il était psychologiquement moins traumatisant pour les personnes qui ne peuvent pas tolérer l’odeur forte des pansements.
Dans ce cas, le pansement a facilité la cicatrisation des plaies faciales. Cependant, ces pansements sont coûteux et le coût de chaque exemplaire changé n’était pas bon marché. Cependant, Robinson et al.12 ont rapporté qu’une étude coût-bénéfice du pansement hydrofibre a démontré un gain significatif de temps clinique, du fait que le composant le plus important dans l’équation coût-bénéfice était le temps de travail du personnel. Dans ce cas, la patiente attachait une grande importance à la famille, avait un haut degré de coopération aux soins et était disposée à communiquer afin que la douleur et les problèmes psychologiques soient identifiés et résolus en temps utile.
Une complication dans ce cas était la quantité d’exsudat provenant de l’autolyse des tissus nécrosés qui ne pouvait pas être estimée à l’avance, limitant ainsi les mesures de protection. Par conséquent, il convient de prendre en compte davantage de facteurs cliniques et le potentiel d’apparition de telles complications dans l’évaluation et l’appréciation continue de la cicatrisation des plaies afin de permettre plus de mesures proactives pour faciliter la cicatrisation des plaies et atteindre les objectifs des soins infirmiers. Le coût des pansements pour les plaies est élevé, et leur accessibilité pour les patients et leurs familles doit être prise en compte dans le processus ultérieur de soins infirmiers.
Mais il existe tout de même des solutions possibles. Selon la politique de l’hôpital, le fabricant du pansement est censé négocier avec le service d’assurance médicale pour couvrir une partie des frais. En pratique, les infirmières et infirmiers chargés des soins des plaies peuvent être en mesure de découper les pansements si cela est conforme aux directives du fabricant. Le fait de découper le pansement en morceaux au lieu de l’appliquer en une seule fois se justifie pour deux raisons principales. Tout d’abord, le contour du visage est irrégulier, et les pansements découpés épousent mieux l’étendue et la forme des brûlures. Deuxièmement, le fait de découper les pansements réduit les frais pour les patients. Dans ce cas, il a été établi que le fait de découper les pansements n’a entraîné aucun effet indésirable et n’a pas compromis la cicatrisation des brûlures faciales.
Les traits du visage sont plus sensibles à la douleur en raison de l’abondance de nerfs2. Dans ce cas de figure, la détersion des plaies et les changements de pansement ont provoqué des douleurs qui pourraient facilement entraîner une mauvaise coordination des soins au patient, faire peser une lourde charge psychologique sur le personnel infirmier et ralentir le processus de soins des plaies faciales. En évaluant numériquement la localisation, la nature et la durée de la douleur liée à la plaie, des mesures de traitement de la douleur individualisées sont formulées en fonction des caractéristiques du patient, l’intervention psychologique en constituant le pilier. Avant chaque changement de pansement, les auteurs ont discuté de la procédure avec la patiente et lui ont précisé quels gestes indiquaient une douleur, comme ouvrir la bouche ou hocher la tête. Au cours de la procédure de pansement, la patiente était informée des étapes de la procédure de pansement en cours, de la zone où la détersion serait effectué et de la quantité de tissu nécrotique susceptible d’être retirée, afin que la patiente soit psychologiquement préparée à coopérer à la procédure de pansement. La procédure de pansement était interrompue lorsque la patiente envoyait un signal de douleur.
L’environnement affecte directement les activités psychologiques des patients, et la création d’un environnement beau et confortable a un bon impact sur la psychologie des patients. L’environnement du service était propre et lumineux, avec une température de 25°C et une humidité de 60%.
L’établissement d’une bonne relation infirmière-patient ou infirmier-patient est la clé de l’efficacité des soins psychologiques. Utiliser un langage poli, être sincère, naturel, doux, calme, avoir des conversations amicales tout en étant sérieux dans le processus de pansement, être toujours optimiste et d’humeur joyeuse, faire attention à l’attitude dans les relations avec les autres et à son apparence, avoir un bon comportement et une bonne posture sont autant d’éléments qui favorisent le respect, la confiance et la coopération.
Le soutien psychologique était pratiqué tous les jours, apportant du réconfort psychologique, de la conviction et des conseils à la patiente pour atteindre l’objectif du traitement. Les auteurs se sont efforcés d’obtenir l’étroite collaboration des membres de la famille et des amis.
Conclusion
Les brûlures constituent un problème de santé important dans le monde entier. Les brûlures faciales sont extrêmement graves en raison de l’abondance de nerfs et ds vaisseaux sanguins. Cette étude de cas rapporte le cas d’une femme de 45 ans présentant des brûlures datant d’1 heure, de 90% de la surface corporelle totale (STC), comprenant un mélange de brûlures profondes par flamme de 2e et 3e degrés, soignées avec un pansement à l’argent, AQUACEL® Ag Hydrofiber®, avec un effet satisfaisant. D’autres études sont nécessaires afin de trouver le pansement idéal pour la prise en charge des brûlures faciales.
Remerciements
Nous remercions la famille du patient, l’équipe chirurgicale et le personnel infirmier qui ont participé à l’intervention chirurgicale et aux soins.
Conflit D’intérêt
Les auteurs ne déclarent aucun conflit d’intérêt.
Financement
Ce travail a été financé par une subvention du
Author(s)
Beihua Xu
Registered Nurse, Wound Care Nurse
Wound Care Clinic, The Third Affiliated Hospital of Soochow University (The First People’s Hospital of Changzhou), Jiangsu Province,
P. R. China
Yajuan Weng* MNurs Sci, MBusAdmin
Registered Nurse, Enterostomal Therapist, Chief Nurse Executive
Education Committee Chairperson WCET®
Wound Care Clinic, The Third Affiliated Hospital of Soochow University (The First People’s Hospital of Changzhou), Jiangsu Province,
P. R. China
Email faith830406@hotmail.com
Suping Bai*
Registered Nurse, Enterostomal Therapist, Chief Nurse
Department of Burn and Plastic Surgery, Affiliated Hospital of Jiangsu University, Zhenjiang, Jiangsu Province, P. R. China
Email bosuping@163.com
* Corresponding authors
References
- American Burn Association. Burn incidence and treatment in the United States; 2016 [cited 2016 Aug 17]. Available from: www.ameriburn.org/ resources_factsheet.php
- Singer AJ, Boyce ST. Burn wound healing and tissue engineering. J Burn Care Res 2017;38:e605–e613.
- Jeschke MG, van Baar ME, Choudhry MA, Chung KK, Gibran NS, Logsetty S. Burn injury. Nature Rev 2020;6:11.
- Spence RJ. The challenge of reconstruction for severe facial burn deformity. Plastic Surg Nurs 2008;28:71–76; quiz 77–78.
- Palmieri TL, Greenhalgh DG. Topical treatment of pediatric patients with burns. Am J Clin Dermatol 2002(8):529–34.
- Raghavan R, Sharma PS, Kumar P. Abacus VAS in burn pain assessment. Clin J Pain 1999;15:238.
- Spitzer RL, Kroenke K, Williams JB, Lowe B. A brief measure for assessing generalized anxiety disorder: the GAD-7. Arch Intern Med 2006;166:1092–1097.
- Thom D. Appraising current methods for preclinical calculation of burn size: a pre-hospital perspective. Burns 2017;43:127–136.
- Caruso DM, Foster KN, Hermans MH, Rick C. Aquacel Ag in the management of partial-thickness burns: results of a clinical trial. J Burn Care Rehab 2004;25:89–97.
- Caruso DM, Foster KN, Blome-Eberwein SA, et al. Randomized clinical study of Hydrofiber dressing with silver or silver sulfadiazine in the management of partial-thickness burns. J Burn Care Res 2006;27:298–309.
- Hindy A. Comparative study between sodium carboxymethyl-cellulose silver, moist exposed burn ointment, and saline-soaked dressing for treatment of facial burns Annal Burn Fire Disaster 2009;22:131–137.
- Robinson BJ. The use of a hydrofibre dressing in wound management. J Wound Care 2000;9:32–34.
