Volume 44 Number 1
Wound bed preparation 2024: Delphi consensus on foot ulcer management in resource-limited settings
Hiske Smart, R Gary Sibbald, Laurie Goodman, Elizabeth A Ayello, Reneeka Jaimangal, John H Gregory, Sadanori Akita, Afsaneh Alavi, David G Armstrong, Helen Arputhanathan, Febe Bruwer, Jeremy Caul, Beverley Chan, Frans Cronje, Belen Dofitas, Jassin Hamed, Catherine Harley, Jolene Heil, Mary Hill, Devon Jahnke, Dale Kalina, Chaitanya Kodange, Bharat Kotru, Laura Lee Kozody, Stephan Landis, Kimberly LeBlanc, Mary MacDonald, Tobi Mark, Carlos Martin, Dieter Mayer, Christine Murphy, Harikrishna Nair, Cesar Orellana, Brian Ostrow, Douglas Queen, Patrick Rainville, Erin Rajhathy, Gregory Schultz, Ranjani Somayaji, Michael C Stacey, Gulnaz Tariq, Gregory Weir, Catharine Whiteside, Helen Yifter, Ramesh Zacharias
Keywords Diabetes, wound bed preparation, low-resource settings, foot ulcer, rural, delphi consensus, low- and middle-income countries, innovation
For referencing Smart H et al. Wound bed preparation 2024: Delphi consensus on foot ulcer management in resource-limited settings. WCET® Journal 2024;44(1):13-35.
DOI 10.33235/wcet.44.1.13-35
Abstract
Background Chronic wound management in low-resource settings deserves special attention. Rural or underresourced settings (ie, those with limited basic needs/healthcare supplies and inconsistent availability of interprofessional team members) may not be able to apply or duplicate best practices from urban or abundantly resourced settings.
Objective The authors linked world expertise to develop a practical and scientifically sound application of the wound bed preparation model for communities without ideal resources.
Methods A group of 41 wound experts from 15 countries reached a consensus on wound bed preparation in resource-limited settings.
Results Each statement of 10 key concepts (32 substatements) reached more than 88% consensus.
Conclusions The consensus statements and rationales can guide clinical practice and research for practitioners in low-resource settings. These concepts should prompt ongoing innovation to improve patient outcomes and healthcare system efficiency for all persons with foot ulcers, especially persons with diabetes.
General purpose
To review a practical and scientifically sound application of the wound bed preparation model for communities without ideal resources.
Target audience
This continuing education activity is intended for physicians, physician assistants, nurse practitioners, and nurses with an interest in skin and wound care.
Learning objectives/putcomes
After participating in this educational activity, the participant will:
- Summarise issues related to wound assessment.
- Identify a class of drugs for the treatment of type II diabetes mellitus that has been shown to improve glycemia, nephroprotection, and cardiovascular outcomes.
- Synthesise strategies for wound management, including treatment in resource-limited settings.
- Specify the target time for edge advancement in chronic, healable wounds.
Introduction
A framework for wound bed preparation (WBP) was introduced in 2000 to emphasise treating the whole person as a foundation of optimal local wound care.1 As this has evolved into an international framework, it became clear that not all wounds are healable. These concepts of maintenance and nonhealable wounds led to revisions of local wound care principles and WBP expansion. The importance of integrated coordinated care with nurses, doctors, and allied healthcare professionals working together to optimise patient care outcomes and healthcare system utilisation was paramount in further WBP developments.
This article focuses on applying the WBP framework to manage foot-related wounds, particularly in persons with diabetes (PWDs), leprosy-related neuropathic foot ulcers, and other complications that include neuropathy and vascular disease. Several parameters are critical to PWDs, including poor glycemic control, BP changes, high cholesterol, inadequate plantar pressure redistribution, infections, and lack of exercise. The effects of smoking are also particularly detrimental to saving limbs and lives of PWDs.
Critical for this article is a set definition for resource-restricted settings, including low resource availability; lacking or restricted funding; remote, isolated, or rural settings; and Indigenous populations. These terms all relate to healthcare settings that may have challenges accessing supplies, equipment, specialists, and advanced wound care competencies and skills. Low-resource settings can be present anywhere in the world and are not limited to lower-income or developing countries.
The Delphi process underpinning this work expanded and developed the WBP framework in its current format. Forty-one authors drawn from 15 countries took part in the Delphi process, which occurred over two rounds using a four-part Likert-type scale (1, strongly agree; 2, agree; 3, disagree; 4, strongly disagree). The first round consisted of 29 statements. Although all statements exceeded the desired 80% consensus level, there were 299 comments considered by the lead group of authors. A professional editor was employed to improve the comprehension and grammatical accuracy of the statements before a Delphi round 2 was deployed with 32 constructed statements. All statements exceeded 88% consensus level.
In round 2, 14 statements achieved 100% consensus. One statement stood out and was rated as “strongly agree” by all Delphi panel members: 10C. Establish timely and effective communication that includes the patient and all interprofessional wound care team members for improved healthcare system wound outcomes. In parallel, each of the international wound experts worked in groups to develop the manuscript content. Refer to Supplemental Table 1 (http://links.lww.com/NSW/A176) for the consensus statements.
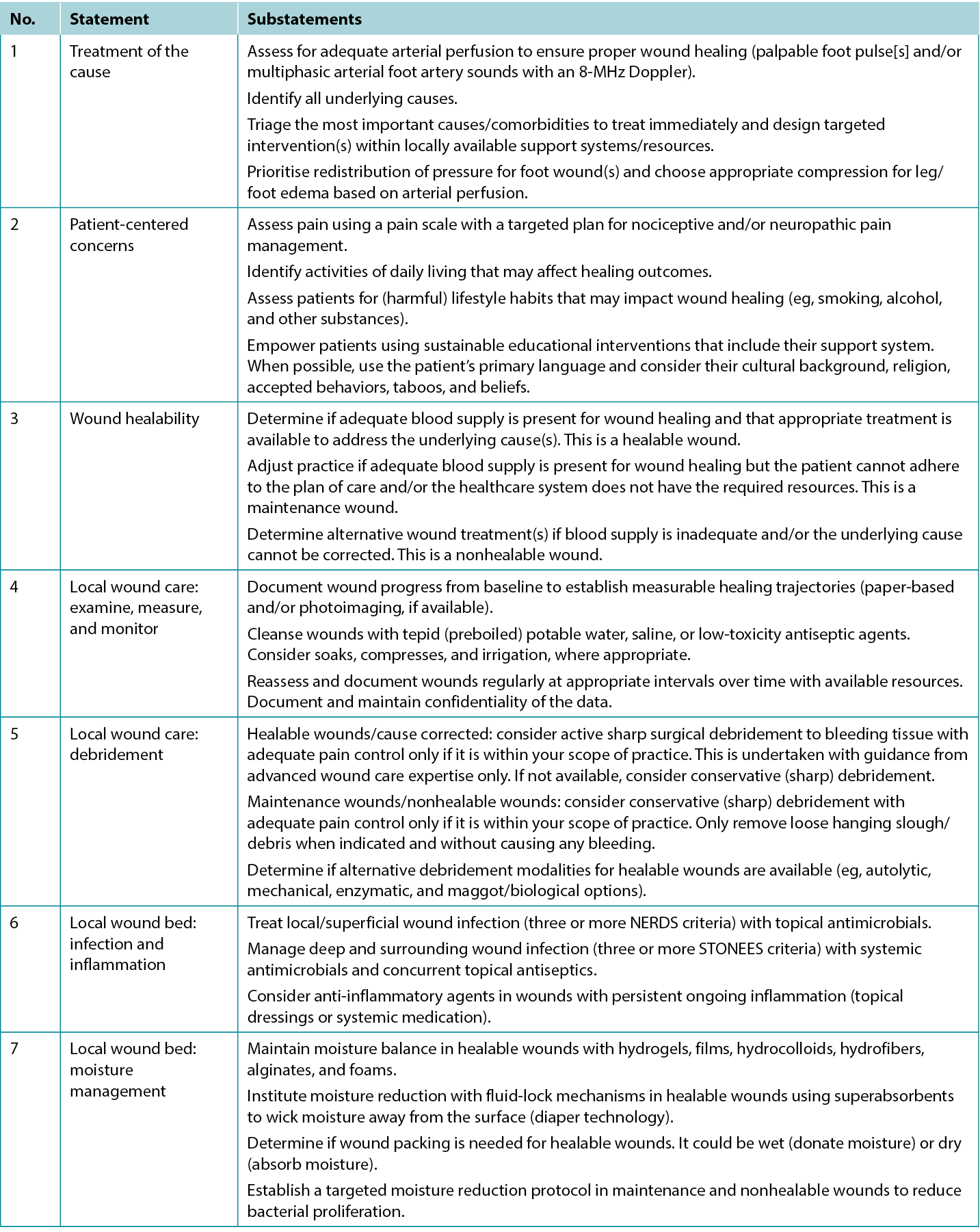
The consensus aimed to set a scientifically based minimal standard of care that could be optimised for available resources. Refer to Table 1 for the 10 key steps and 32 substatements for wounds in limited-resource environments. This consensus process updated the framework for WBP to be applicable regardless of resource availability. In addition, it also includes the concepts of healing trajectories and healthcare system change for the first time (Figure 1).
The remainder of this report will highlight the 10 consensus statements and discuss the rationale for each statement.
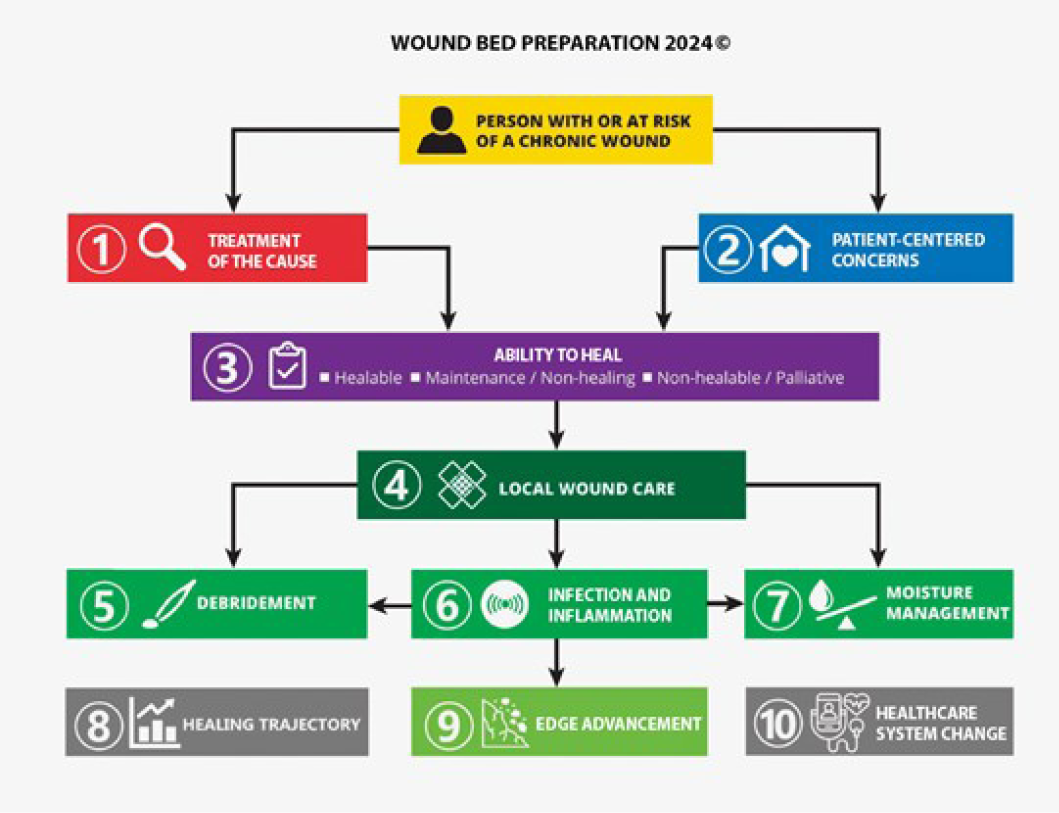
Figure 1. Wound bed preparation 2024. ©WoundPedia 2023
Table 1. Wound bed preparation for wounds below the knee in environments with limited resource availability

Statement 1: treatment of the cause
1A. Assess for adequate arterial perfusion to ensure proper wound healing (palpable foot pulse[s] and/or multiphasic arterial foot artery sounds with an 8-MHz Doppler)
To determine lower-limb blood flow, find a palpable foot pulse(s) as a vital first action. Start with the dorsalis pedis and/or the posterior tibial pulses. If an 8-MHz handheld Doppler is available, confirm multiphasic flow patterns (biphasic/triphasic). Refer to vascular specialists when a monophasic or absent Doppler sound is observed or foot pulses are not palpable. Other signs of inadequate arterial perfusion are lower limb pain at rest and ischemic limb changes (cold extremity with dependent rubor that blanches on elevation).
Persons with diabetes are susceptible to microvascular issues (peripheral neuropathy, Charcot foot changes) and macrovascular complications including peripheral arterial disease (PAD). These conditions contribute to calluses, foot ulcers, and mixed tissue loss. Because up to 50% of susceptible populations experience both diabetes and PAD,2 timely identification of PAD is critical (using physical examination and vascular tests) because it is a major risk factor for poor ulcer healing and amputation. If detected, immediate revascularisation (angioplasty or vascular bypass) is vital to restore proper arterial flow to the foot. Additional assessment may include capillary refill time, a Buerger blanching test (pale on elevation, bright red rubor on dependency), and claudication with walking.
Vascular examination. In cases of arterial insufficiency, the extremity is often cool to the touch because of insufficient nutrient and oxygen supply (Table 2). Severe cases may manifest tissue necrosis presenting as ulcers, macerated toe webs (often with secondary infection), fissures, or gangrene. Other severe case indicators include pallor upon leg elevation, exercise-induced claudication that resolves with rest, dependent cyanosis or rubor, and muscle atrophy. Notably, lower extremity edema is more indicative of venous rather than arterial issues. Arterial lesions are generally punched out, with a deep base that often contains tendons, whereas venous ulcers show irregular border morphology with a shallow granulation tissue base.3
Table 2. Vascular supply needed for tissue healing
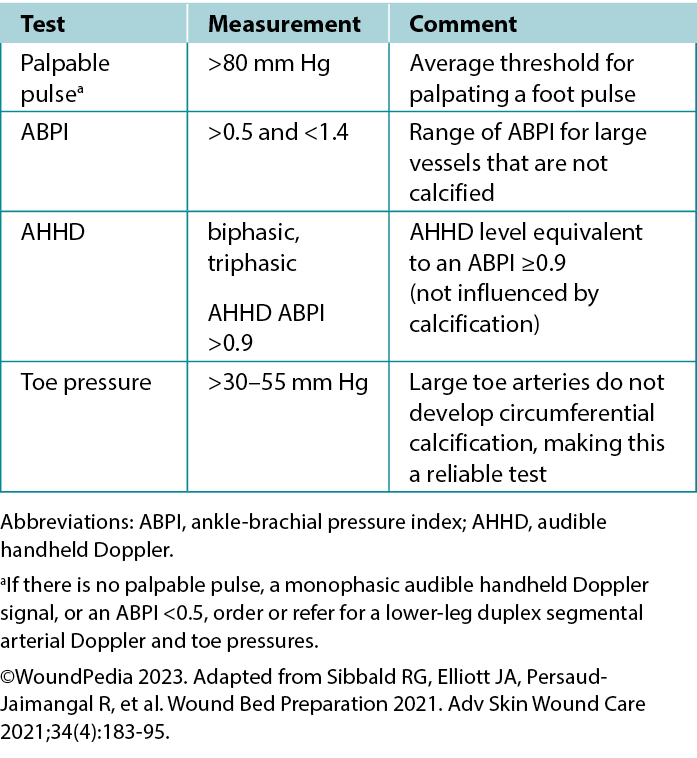
Ankle-brachial pressure index (ABPI) examination. The ABPI measures the ratio of ankle systolic BP divided by the brachial systolic BP using an 8-MHz Doppler. The procedure involves using a BP cuff and recording systolic BP when arterial sounds reappear after cuff inflation. However, factors such as edema, inflammation, and arterial calcification can affect its accuracy. If an 8-MHz Doppler cannot be afforded/obtained, early referral to a tertiary assessment center becomes the priority in cases where the absent foot pulses are present. In certain healthcare settings, an ABPI is still required as vital quantification assessment before beginning any lower limb intervention.
Audible handheld Doppler (AHHD) examination. An AHHD can easily be added as an additional parameter in certain settings, should providers choose a simpler and faster test (not influenced by calcification, no need to squeeze a painful calf, and no need to be recumbent for 20 minutes). The AHHD assessment also can provide accurate results in case of large toe amputation and be recorded as an MP3 or MP4 file and transferred for remote verification of the signal interpretation.
Healthcare professionals should apply gel on the appropriate foot pulse sites with an 8-MHz Doppler probe positioned at a 45° angle to the skin on the dorsalis pedis, posterior tibial, and peroneal arteries. The acquired Doppler signals/waveforms can then be analysed (either by audible sound or visual tracings): A comprehensive tutorial on the AHHD procedure is available online at https://journals.lww.com/aswcjournal/Pages/videogallery.aspx?videoId=20. Optimise signal quality with careful repositioning of the probe to obtain the loudest or most multiphasic signal.
A monophasic or absent waveform warrants a comprehensive vascular assessment, including a Duplex segmental lower leg arterial Doppler in the vascular laboratory. A multiphasic waveform typically indicates the absence of peripheral vascular disease.4 In PWDs, interpret the ABPI ratio with caution (due to arteriosclerosis or arterial calcification); AHHD multiphasic findings are a preferable choice to confirm adequate blood supply for wound healing. A multiphasic waveform (biphasic, triphasic) suggests an AHHD value equivalent to a normal ABPI ≥0.9.
Although AHHD is effective in excluding arterial disease, it may not identify existing segmental perfusion deficits—islands of ischemia or angiosome defects.5 Therefore, physical examination of the foot and lower limb is vital for a conclusive diagnosis. Healthcare professionals can record AHHD signals and transmit them to specialists, facilitating either synchronous or asynchronous assessments remotely. Synchronous assessments enable real-time patient involvement and prompt decision-making.
Chronic venous insufficiency. Chronic venous insufficiency may coexist in PWDs and those with foot ulcers. It mainly affects the lower limbs and impairs the return of deoxygenated blood to the heart and lungs. This condition often arises from venous valve dysfunction that can be triggered by factors including pregnancy or weight gain. Symptoms commonly include varicose veins, edema, skin discoloration from hemosiderin, lipodermatosclerosis, and venous ulcers.6 These ulcers can be any size (from small to circumferential) and form quickly over areas of venous pooling, usually on the medial aspects of the lower limbs.
The cornerstone of treatment for venous ulcers is compression therapy. This compensates for valve dysfunction by enhancing the peristaltic action of the calf muscle pump. Additional measures include leg elevation and walking. Venous ablative procedures may be considered when ulcers are attributed to superficial veins. Untreated venous edema can delay foot ulcer healing.7
For the medical optimisation of PAD, key strategies include optimal BP control, initiating cholesterol medication, and, often, starting statin therapy. Recent studies also recommend treating patients with PAD and concurrent coronary artery disease or carotid disease using a combination of low-dose aspirin (91-100 mg PO daily) and low-dose rivaroxaban (2.5 mg PO BID).8 Additional modifiable factors are smoking cessation and walking or exercise programs. For patients with a foot ulcer (especially in PWDs), appropriate plantar pressure redistribution or offloading is essential.
1B. Identify all underlying causes
Foot complications are of great concern to PWDs and represent a significant burden of disease to healthcare systems. A holistic approach is represented by the mnemonic AIM (assessment, identification, management) and focuses on treating or mitigating the underlying cause of diabetic foot issues, especially neuropathy. The application of a focused assessment approach as a baseline standard of care (VIPS: vascular, infection, pressure, surgical debridement) is crucial in preventing severe complications, including foot ulcerations, lower limb amputations, and an increased incidence of early/preventable death. Some critical foot-related elements in resource-challenged settings include late presentations to formal care, delayed diagnosis,9 barefoot walking, neglected wounds, and the absence of preventive foot care. A hospital-based observational analysis conducted in Ethiopia identified several factors contributing to diabetic foot complications;10 these included high humidity, foot deformity, neuropathy, unidentified active ulcers, inadequate or ill-fitting footwear, poor foot hygiene (eg, foot and toenail fungus), and lack of foot care awareness. A systematic review on plantar ulcers among patients with leprosy (n = 7 studies) identified the following risk factors for developing ulcers: inability to feel a 10 g monofilament on sensory testing, severe foot deformities or hyperpronation, lower education, and unemployment.11 Addressing these challenges in any resource-challenged environment requires a multipronged approach that may include patient and healthcare professional education, early detection, access to care, footwear programs, and community engagement.
Regular and thorough foot assessments include detecting neuropathy (loss of protective sensation), vascular issues (poor or absent lower limb blood circulation), signs of infection, areas of high pressure (callus formation), and friction (blisters, often with hemorrhagic components) to facilitate timely interventions. The simplified 60-second screening tool may be a valuable means to quickly assess, stratify, and follow up patients based on their risk levels without significant cost.12 Patients with a history of ulceration, amputation, peripheral vascular surgery, or Charcot neuroarthropathy are at the highest risk for skin breakdown and should receive additional attention to prevent ulceration and further complications.
To detect infection, the NERDS (superficial wound infection: nonhealing, exudate, red friable granulation tissue, debris, smell) or STONEES (deep and surrounding wound infection: size increased, 3 °F temperature warmer, os [probe to bone], new areas of breakdown, erythema >2, exudate, smell) criteria along with using noncontact infrared thermometry can be helpful.13 Elevated temperatures of 3 °F compared with the opposite limb may signal inflammation and a foot at a higher risk of ulceration.13 A comparative change of 1.67 °C is difficult to measure clinically. This same finding in a person with a lower leg or foot ulcer is eight times more likely to signify deep and surrounding infection when accompanied by two or more additional STONEES criteria.13
Patients with neuropathy without an ulcer and presenting with a hot swollen foot could have acute Charcot neuroarthropathy. Infrared thermometry is a valuable assessment tool in these cases: acute Charcot feet may be 8 to 15 °F warmer than the mirror image on the opposite foot. These patients require a comprehensive medical history, physical examination, and radiographic images to facilitate early detection. Further actions include the application of a total contact cast for stabilisation and complete plantar pressure offloading with a wheelchair to prevent further bone deterioration and prevent lower limb amputation (Table 3).
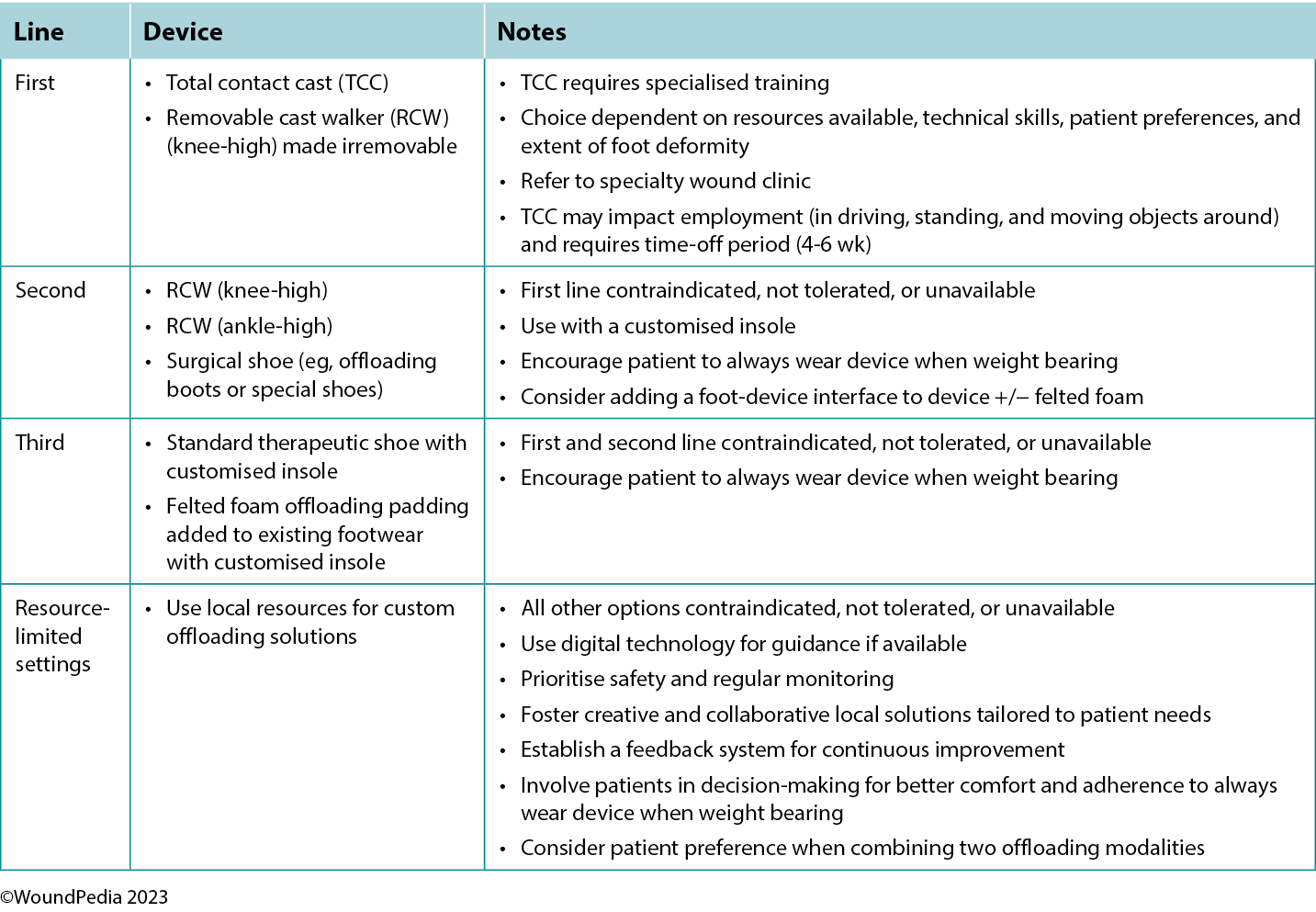
Table 3. Offloading interventions for a plantar diabetic/neuropathic foot wound28
Callus formation in PWDs is positively correlated with pressure and shear stress. In individuals with diabetic neuropathy, various factors including foot deformities, limited joint mobility, repetitive stress during walking, and poorly fitting shoes can increase the risk of callus formation.14 Moreover, the presence of calluses can pose a significant risk because repetitive trauma may lead to subcutaneous hemorrhage and eventually progress to ulceration. Provide tailor-made pressure redistribution devices (soft insoles, cobbler interventions to adapt shoes, and reduced barefoot walking) to prevent subsequent callous-to-ulcer progression.
Different etiologic causes may lead to foot ulcers in PWDs: neuropathic because of peripheral neuropathy, ischemic associated with PAD, or a combination of both—neuroischemic foot complications. The presence of diabetic neuropathy is established from medical history; physical examination (5.07/10 g monofilament test); altered sensation distributed symmetrically in both limbs (stocking and glove distribution); and burning, stinging, shooting, or stabbing pain.
1C. Triage the most important causes/comorbidities to treat immediately and design targeted intervention(s) within locally available support systems/resources
A diabetic foot ulcer (DFU) occurs in 25% to 34% of PWDs and is one of the most feared complications, potentially leading to lower limb amputation, severe disability, and reduced life expectancy.15 Multifactorial in origin, diabetes-related peripheral neuropathy and PAD leave feet highly vulnerable to traumatic injury. Access to timely diagnosis and intervention are determinant factors in effective management and limb preservation.
Chronic hyperglycemia measured by elevated hemoglobin A1c (HbA1c) is a major risk factor for sensory, motor, and autonomic neuropathy. Both PAD and dry skin increase foot vulnerability to infection and delayed healing, all contributing to poor outcomes. Chronic kidney disease adds to the risk.16 Recent studies of continuous glucose monitoring report that high glucose variability (reduced time to target range levels) may additionally contribute to long-term complications.17
Up to 50% of PWDs will develop neuropathy with no known cure. Management includes proper daily foot inspections for evidence of trauma or infection, foot care, and effective glucose control.18 In addition to neuropathy, PAD contributes equally to DFUs; PAD is largely asymptomatic and may remain underdiagnosed and untreated for a prolonged period. Individuals with diabetes have more than a twofold increased prevalence of PAD compared with those without.19 A systematic review of community-based studies for global prevalence and risk factors for PAD ranked diabetes highest next to smoking.20
The European Society of Hypertension recommends providers and patients target a systolic BP less than 130 mm Hg and diastolic BP less than 80 mm Hg. In PWDs, systolic BP should not fall less than 120 mm Hg to prevent reduced blood flow to vital organs and lower limbs.21 Although diuretics, calcium-channel blockers, angiotensin-converting enzyme inhibitors, angiotensin receptor blockers, and β-blockers can all be used, angiotensin-converting enzyme inhibitors and angiotensin receptor blockers reduce cardiovascular events.22,23 Recently, SGLT2 inhibitors have shown excellent results in improving glycemia, nephroprotection, and cardiovascular outcomes.24 In addition, DFU incidence is reduced by early detection of PAD with lifestyle modifications.17
The complexity of managing a DFU requires an interprofessional team approach to identify biological, social, geographic, and cultural determinants of health. In Denmark, PWDs are registered by region with access to specialised clinics with interprofessional wound care teams. Lower limb amputation rates have declined significantly due to improved diabetes care, regular foot inspection, better self-care, and timely treatment.25 In more geographically dispersed diverse populations (eg, Ontario, Canada), significant disparities in amputation rates exist, highest in rural regions where timely prevention such as revascularisation surgery and foot care specialists are underserviced or absent.
The most vulnerable persons for diabetic foot-related amputations in Canada are Indigenous people, immigrants, and persons living in rural and northern regions.26 The Indigenous Diabetes Health Circle provides a culturally sensitive approach to local Ontario First Nations communities with education and knowledge about diabetes, wellness, and self-management. Its holistic foot care program supports a continuum of services that connects community members to Indigenous agency partners and local healthcare professionals and is proven to reduce DFU incidence and prevent amputations.27
1D. Prioritise redistribution of pressure for foot wound(s) and choose appropriate compression for leg/foot edema based on arterial perfusion
The criterion standard for plantar pressure redistribution devices is the total contact cast or the removable cast walker made irremovable.28 Even in healthcare systems in which these offloading modalities are readily available, less than 10% of eligible patients are fitted for and adherent to the use of these devices.29
Offloading is paramount to healing foot ulcers (Table 3). The aim is to select the best device for the patient incorporating patient-centered concerns, the goals of care, and best practice evidence. Consider creative solutions to repurpose local materials such as soft felted inserts for offloading in resource-limited settings. It is important to establish an early surveillance program between the patient and healthcare professional to monitor and ensure the desired offloading outcomes. Healthcare professionals need to evaluate the effectiveness of the devices and continually make modifications as needed through established follow-up. In regions lacking specialised practitioners, empowering healthcare workers with competencies in basic offloading can bridge this gap.
Statement 2: patient-centred concerns
2A. Assess pain using a pain scale with a targeted plan for nociceptive and/or neuropathic pain management
The perception of pain involves a stimulus that may be physical or chemical. There are two main types of pain: nociceptive and neuropathic (Table 4). Wound-related pain is an important component of patient-centered concerns that is often undervalued by healthcare professionals. By the late 1990s, wound pain was a focus for healthcare professionals with the launch of a pivotal position document focused on wound pain.30 The document recognised and focused on the distress of chronic wound pain and its influence on patients’ health-related quality of life. The management of wound pain was then integrated into the WBP framework.1,31
Table 4. Pain types and responses30
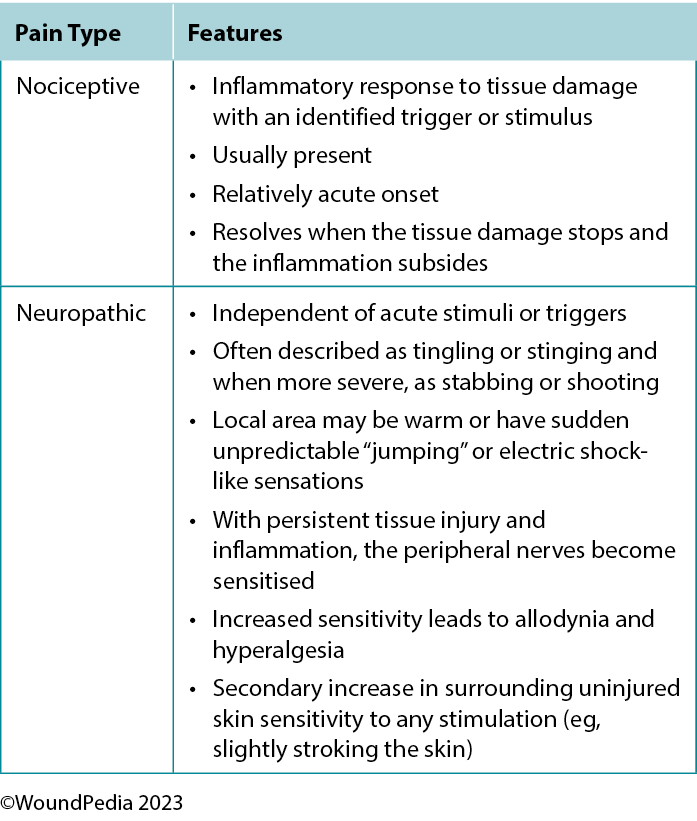
Pain can play a significant role in the total management of persons with wounds and their ultimate healing success.32 Pain signals associated with injury play an important function in patient wellness and as such must be acknowledged through adequate assessment and management. For example, pain or any change in pain is a key predictor of wound infection and one of the four cardinal signs of inflammation.1 Unresolved pain is often associated with delayed wound closure.
Assessment. A pain history is essential to wound pain management.32 Assessment must include the nature, onset, duration, and exacerbating and relieving factors. This will help determine the cause of the pain and direct its management. Pain intensity can be reliably measured using validated pain scales. A verbally administered 0- to 10-point numerical rating scale is a good first choice for measuring pain numerical intensity. Most patients can function with a pain level of 3 to 4 out of 10.33
Patients with persistent pain should be reassessed regularly for improvement, deterioration, and adherence to medication regimens. The use of a pain diary with entries regarding pain intensity, medications used, mood, and response to treatment may be a good management strategy. For individuals with communication limitations, the pain scale should incorporate pictures for easy recognition.
Management. The management of wound pain can be integrated into the WBP framework: treat the cause and address local wound factors and patient-centered concerns.3 Treating the cause should determine the correct diagnosis and initiate treatment of the wound pain. Patient-centered concerns must focus on what the patient sees as the primary reasons and resolutions for the pain. Patient anticipatory pain and suffering can be just as disruptive to quality of life as the actual experience of pain.
Multiple pain management strategies exist and are not always pharmaceutical (Table 5). Consider total patient management, including all aspects of WBP, in choosing a management strategy. Remember: pain is what the patient says it is.34
Table 5. Pain management strategies
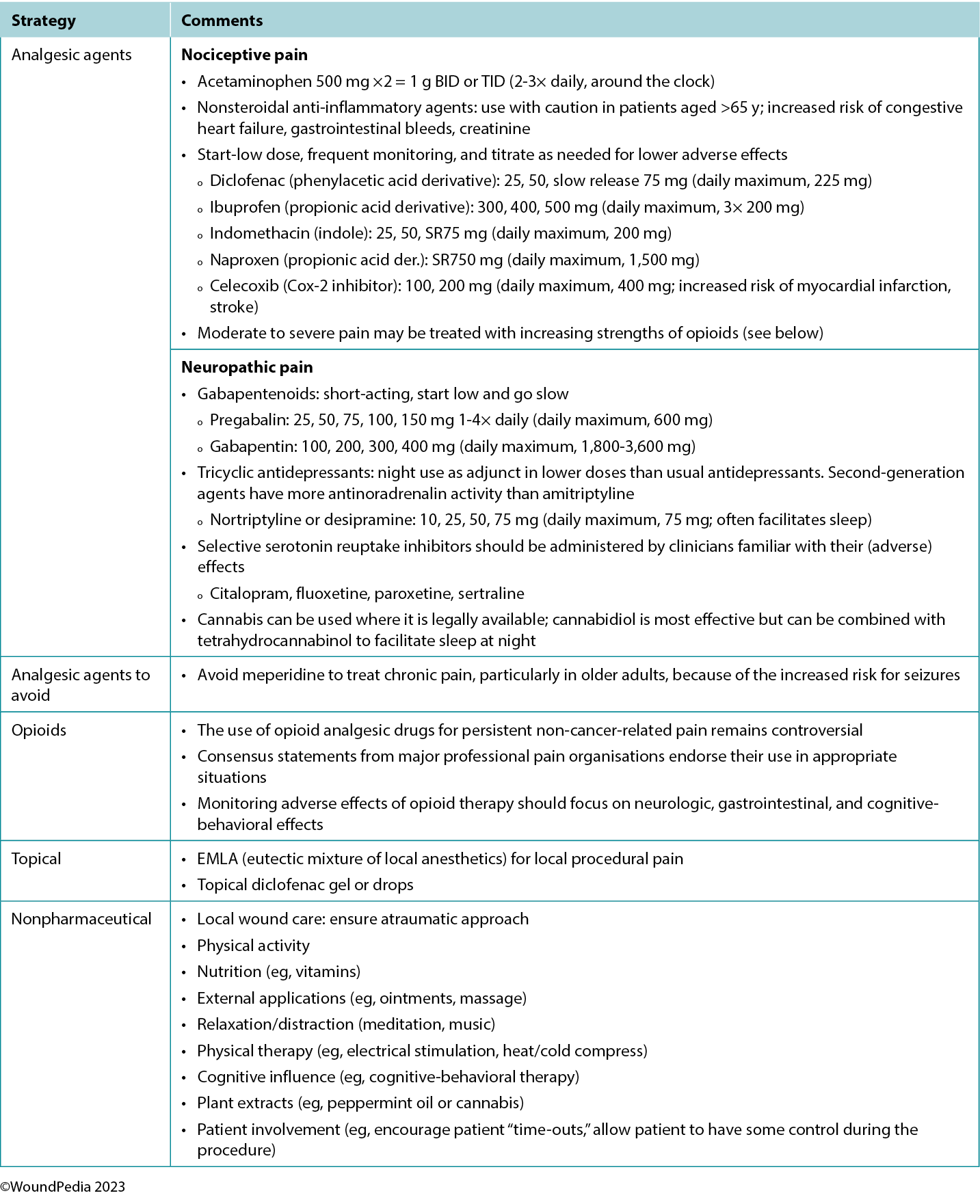
Assessment and management given limited resources. In regions with limited resources, assessment remains possible because it requires no costly tools. Most pain scales are freely available despite some initial cost relative to education and training of practitioners.31 Treatment options for pain in resource-restricted environments may be more practical if driven with nonpharmacologic methods (Table 5). Some of these options may also be more socially acceptable or already practiced culturally (eg, meditation, plant-based treatments) and particularly applicable in nociceptive pain management. Implementing such strategies can then preserve pharmaceutical management for those with pain that cannot be managed by nonpharmacologic means (eg, neuropathic pain).35
2B. Identify activities of daily living that may affect healing outcomes
2C. Assess patients for (harmful) lifestyle habits that may impact wound healing (eg, smoking, alcohol, and other substances)
2D. Empower patients using sustainable educational interventions that include their support system. When possible, use the patient’s primary language and consider their cultural background, religion, accepted behaviors, taboos, and beliefs
In resource-limited environments, patient-centered concerns and barriers to clinical outcomes are crucial for providers to understand and address within the context of cultural, spiritual, and religious beliefs of the respective community.
Wound healing disparities exist among Indigenous populations across the globe. These disparities are often rooted in historical and ongoing socioeconomic, cultural, and healthcare-related factors. Cultural diversity and societal pressure also often dictate formal resource allocation processes to certain health sectors. Some key barriers to wound healing among Indigenous populations include historical trauma, socioeconomic disparities, limited access to healthcare, cultural barriers, chronic health conditions, cultural healing practices, geographic isolation, and healthcare system bias.36 Many cultures have an honor system in managing their sick, older adult, and chronically ill members. These principles are easier upheld if sufficient resources are available to maintain them.
Many studies have identified a major medical illness as one of the core reasons a family can incur large debts.37,38 Even in government-run clinics, additional dressing materials or medicines may be charged to the family. Patients and family members may therefore resort to alternative treatment methods (nonallopathic medicine) from local/Indigenous/traditional healers. Although often less costly, these healers may not have the necessary skills or expertise in managing chronic wounds, leading to deterioration.
Loss of independent mobility because of wound chronicity is another major factor that impacts attendance and regular follow-up. Transport availability varies in resource-restricted environments, and walking may be the only way to access a public transport pick-up point. Secluded rural environments are often affected the most and require traveling significant distances to reach a formal healthcare facility.
The social health of the family environment and willingness to incorporate a person with healthcare needs can drive the quality of care/self-care rendered as well as patient safety within a home environment. Because of the social structure and milieu in various countries, family support and social support may differ by culture. Often, as time passes, the financial burden increases; patient independence and activities of daily living (ADLs) achievement deteriorates; dressing changes become more challenging; and caregivers become stressed, fatigued, and exhausted.39 Late referrals and critical/terminal patient conditions when eventually presenting to formal care are additional aggravating social and behavioral factors that can compound poor wound healing outcomes.
Individuals with wounds treated at home need a designated space to themselves. Wound odor, persistent pain, and a different routine are the main stressors on both the patient and family in settings where space is at a premium. The mere presence of a major skin wound already negatively impacts the patient’s own social interactions, relationships, sexuality, and self-confidence. This leads to progressive anxiety and depression that may bring about pessimism regarding perceived treatment benefits. Subsequently, patients have lowered self-efficacy that is often associated with further wound deterioration including eventual lower-extremity amputations.40
The real challenge occurs when lifestyle modifications are needed. This often requires additional resources or tailor-made education to construct self-care plans.40,41 The need for health education and lifestyle modification interventions to have clear rationales cannot be overemphasised. Lifestyle interventions may become a financial, social, and logistical challenge, first to acquire and then to maintain within any restricted living domain. Further, it is a vital step to ensure that any financial help received is correctly allocated to the family member with a wound.
A biopsychosocial approach is necessary in managing wound care for patients in resource-restricted environments. The wound care team, beyond managing the wound, must address the social stressors/factors affecting the patient. Each patient will need a unique, mutually agreed-upon management plan that fits their constraints (medical, financial, family, social, and emotional support).40
Statement 3: ability to heal
3A. Healable wound: Determine if adequate blood supply is present for wound healing and that appropriate treatment is available to address the underlying cause(s)
3B. Maintenance wound: Adjust practice if adequate blood supply is present for wound healing but the patient cannot adhere to the plan of care and/or the healthcare system does not have the required resources
3C. Nonhealable wound: Determine alternative wound treatment(s) if blood supply is inadequate and/or the underlying cause cannot be corrected
The process of determining the healing classification of a wound begins with a thorough patient history and physical examination. Identifying the underlying cause(s) of the wound is important. Addressing the underlying cause(s) is the first step to developing an achievable management plan.
In some cases, chronic wounds may also become stalled and fail to achieve the wound edge advancement over the set time; these are known as hard-to-heal wounds. They often fall into the maintenance category but, with additional assessment, may be healable with a re-evaluation of the patient, history, causes, and treatment plan.3,42
Patient-centered concerns and expectations need to be identified, compared with, and aligned with institutional/clinician resource availability, skills, and immediate intervention options that are available.3,42 The management plan is based on the assigned healing classification, which may change.
Protect nonhealable wounds against tissue loss, deep and surrounding wound infection, and general deterioration from a wet wound environment. Decreasing moisture is a priority. Maintenance wounds also need protection against further tissue losses with dry wound bed management and local infection controls as the mainstay. Tissue protection may also be a temporary measure until resources become available and additional patient factors are controlled to achieve full optimisation.
Stalled but healable wounds (hard-to-heal) need a second chance to achieve edge advancement with urgency in reassessment and interprofessional team intervention as the highest priorities.3,42
Statement 4: local wound care: examine, measure and monitor
4A. Document wound progress from baseline to establish measurable healing trajectories (paper-based and/or photoimaging, if available).
4B. Cleanse wounds with tepid (preboiled) potable water, saline, or low-toxicity antiseptic agents. Consider soaks, compresses, and irrigation, where appropriate.
4C. Reassess and document wounds regularly at appropriate intervals over time with available resources. Document and maintain confidentiality of the data.
Wound assessment documentation is an integral component of healthcare practice. It is instrumental in ensuring the delivery of high-quality patient care, monitoring wound status, and providing direction for any changes in wound interventions. The comprehensive and accurate recording of wound assessments is essential to ensure improved patient outcomes, effective communication among healthcare professionals, and legal and regulatory compliance.43
Monitoring progress. Wound assessment documentation serves as a historical record of the wound’s progression over time. By regularly documenting wound characteristics, including size, depth, color, exudate, infection, tissue type, and so on, healthcare professionals can track changes, identify potential complications, and adjust treatment plans. If photo documentation is used, obtain patient consent according to organisational policy, ensure appropriate technique with adequate lighting and appropriate distance from the wound, and include a measuring guide in the photo.44 This ongoing evaluation is critical for evaluating the effectiveness of interventions and making informed decisions regarding wound management. When measuring surface area or volume, it is imperative to use a consistent technique regardless of technology.
Communication. Accurate wound assessments facilitate effective communication among healthcare professionals. When all team members have access to consistent and up-to-date wound documentation, they can work together to develop and implement a coordinated care plan, ensuring patients receive the best possible treatment. It is vital to use consistent terminology that is common to all disciplines. The International Classification of Diseases medical classification system is an example of a globally applicable standard.45
Legal and regulatory compliance. Proper wound assessment and documentation are essential to meet legal and regulatory requirements. Inaccurate or incomplete records can lead to legal issues and negatively impact a healthcare professional’s practice, even in resource-limited environments.
Reimbursement. In many healthcare systems, proper wound assessment documentation is tied to reimbursement-based funding models. Accurate and detailed records are often necessary to justify the use of specific wound care products or procedures and ensure organisations receive adequate reimbursement for services rendered.
Research and quality improvement. Wound assessment data are a valuable resource for research and quality improvement initiatives. This continuous learning process helps improve global wound care and patient outcomes.
Patient-centered care. Proper wound assessment and documentation are an essential component of patient-centered care. It ensures that patients’ conditions are thoroughly evaluated and their treatment plans are tailored to their specific needs. When patients observe that their healthcare provider is committed to documenting and monitoring their wounds, it can enhance trust and patient satisfaction.
To promote language consistency and enhance data clarity, an increasing number of enterprises are creating electronic wound assessment software and applications to reduce the time required for thorough documentation.43 These programs and applications (some more affordable than others) can provide the healthcare team with a structured set of parameters to ensure all clinical features are documented, thereby enhancing overall communication.46 Although these tools are an asset to healthcare professionals, they are not without risk, such as incorrect copying and pasting from previous reports/consult notes or patient data security risks. In areas where such programs and applications are not available, updating
the patient and providing written assessment and intervention plans may be warranted.
Statement 5: local wound care: debridement
5A. Healable wounds/cause corrected: Consider active sharp surgical debridement to bleeding tissue with adequate pain control only if it is within your scope of practice. This is undertaken with guidance from advanced wound care expertise only. If not available, consider conservative (sharp) debridement
5B. Maintenance wounds/nonhealable wounds: Consider conservative (sharp) debridement with adequate pain control only if it is within your scope of practice. Only remove loose hanging slough/debris when indicated and without causing any bleeding
5C. Determine if alternative debridement modalities for healable wounds are available (eg, autolytic, mechanical, enzymatic, and maggot biological options)
Debridement is an important process in the WBP paradigm to remove necrotic tissue and other biomaterials, including biofilm, in healable wounds and prevent odor and infection in maintenance wounds. For all wounds located below the knee, communicate the outcomes of any vascular testing (eg, ABPI, waveform) to all members of the interprofessional team, and document accordingly before attempting debridement because many types may be deleterious to the wound bed with reduced vascular supply.
For healable wounds, local wound bed interventions are best determined via the WBP paradigm based on the patient and wound characteristics. Consider surgical debridement (to bleeding tissue) as a first-line intervention. However, in many rural and remote regions, access to a skilled healthcare professional with the necessary education, knowledge, and judgment for this procedure may not exist.
Conservative (sharp) debridement (without causing bleeding) requires advanced knowledge and skills and is more suitable for nonacute care or specialty clinic settings. Only remove loose hanging or unattached debris from the wound without causing trauma to the wound bed.
Clinical sterile maggot debridement therapy is a limited treatment modality in resource-restricted environments, except in cases of accidental exposure. Maggot infestation is often discovered during dressing changes. Good debridement outcomes may result from accidental maggot therapy, particularly if the larvae are from the highly selective Lucilia sericata/cuprina bottlefly source, as they focus on devitalised tissue as their food source.47,48 Detrimental outcomes may present if the infestation is from the ordinary housefly (Musca domestica) or other invader species, as those larvae may indiscriminately destroy healthy tissue.47,48
Healthcare professionals should assess alternative methods of debridement (eg, autolytic, enzymatic, mechanical) for community sectors, including primary care, home care, and long-term care. Within available resources it is vital to consider patient safety, assess environmental factors, and identify barriers to wound healing before initiating debridement.
Appropriate debridement protocols for maintenance and nonhealable wounds differ significantly from those for healable wounds. Although moist wound healing provides an optimal environment for wound healing, it is a form of debridement (autolytic) that may be detrimental to nonhealable and maintenance wounds. Debridement is generally not a suitable intervention for stable maintenance or nonhealable wounds, because the goal is to keep those dry and free of infection.49 Consider debridement only when a maintenance or nonhealable wound becomes unstable to remove infected or necrotic wound debris in the most atraumatic manner possible.
Patient goals typically include enhancing comfort, minimising wound-related odor, reducing pain, and improving ADLs. Keeping the wound dry enables the formation of a protective layer, whereas debridement carries the risk of removing this protective layer and introducing pathogenic organisms.
Statement 6: local wound care: infection and inflammation
6A. Treat local/superficial wound infection (three or more NERDS criteria) with topical antimicrobials
6B. Manage deep and surrounding wound infection (three or more STONEES criteria) with systemic antimicrobials and concurrent topical antiseptics
6C. Consider anti-inflammatory agents in wounds with persistent ongoing inflammation (topical dressings or systemic medication)
The validated NERDS and STONEES criteria can guide the assessment and treatment of infection and inflammation in chronic wounds.50 Base the diagnosis of infection on clinical signs and symptoms rather than superficial wound swabs, which should be used only to guide antimicrobial selection in the event of an infection. If deep and surrounding tissue infection is suspected, identify the bacterial species and their sensitivity to commonly used antibacterial agents to help guide systemic antimicrobial use. This is especially true if a deep and surrounding infection is not responding to the empiric treatment.
The best tissue samples for wound bed culture swabs are obtained after cleaning the wound with potable water or saline and sampling the wound base without debris. A culture from tissue samples using a curette or other biopsy technique is most likely to represent the organisms in the wound tissue. Alternately, a semiquantitative swab technique using the Levine method can correlate to tissue biopsies.51 The swab is placed on granulation tissue and pressed enough to extract wound exudate and then rotated 360° to cover all surfaces of the swab. Placing the swab in the transport media to premoisten it prior to placing the swab on the skin may increase the bacterial yield for patients with low-exudate wounds.52
Pathogenic bacteria may infiltrate to the bone and cause osteomyelitis, which derails healing potential and is challenging to cure. A bone biopsy is the criterion standard to diagnose suspected osteomyelitis, because superficial cultures do not access the deep bone tissue, and imaging is limited by variable specificity.53 However, a bone biopsy may be uncomfortable, is dependent on skilled clinicians, and may extend the tissue damage. For these reasons, it frequently is not a feasible option, even more so if resources are scarce.
When deep wound infection is confirmed, antimicrobial dressings are appropriate to locally support systemic antibiotic therapy and prevent spread to the deep and surrounding compartment from surface bacteria. The five most common choices of antimicrobial dressings are silver, polyhexamethylene biguanide, iodine, methylene blue/crystal violet, and honey. Of these, silver and honey have additional anti-inflammatory properties.54
In some wounds, broad-spectrum antiseptics are applied for short-term rapid bacterial burden reduction to support systemic antibiotics. When the risk of infection outweighs the cytotoxic properties, low-cost povidone-iodine-moistened gauze changed daily over exposed bone can reduce surface bacteria. This is a short-term strategy accompanied by clinical evaluation for serum thyroid function levels especially when wound surfaces are large. However, with the newer low-toxicity antiseptics, other options are now available that are less aggressive but equally effective.
In general, wounds in immunocompetent patients that present for less than 1 month are treated with agents for Gram-positive coverage. Polymicrobial infections (typically seen in PWDs) or wounds longer than 1 month in duration call for broad-spectrum agents with Gram-positive, Gram-negative, and anaerobic coverage because these patients are often also immunocompromised.55
Cytotoxic agents may be appropriate for nonhealable wounds if the need for topical antimicrobial action is greater than the tissue toxicity. Antiseptics are generally preferred over topical antibiotics as part of antibiotic stewardship because of a lower risk of systemic bacterial resistance and adverse effects associated with contact irritant or contact allergic dermatitis.54
6D. Gently cleanse the wound with low-toxicity solutions (water, saline, noncytotoxic antiseptic agents).
The cleansing solution used depends on the characteristics of the wound and availability in practice. There is poor consensus in the literature on wound cleansing recommendations. An updated 2021 Cochrane review on cleansing solutions of venous leg ulcers concluded that there is a lack of randomised controlled trial evidence “to guide decision-making about the effectiveness of wound cleansing compared with no cleansing and the optimal approaches to cleansing of venous leg ulcers.”56 However, general wound care principles involve low-toxicity solutions including potable or preboiled water, saline, and other wound-friendly antiseptic agents.57 This avoids cytotoxic effects and damage to healthy granulation tissue in healable wounds.
Acetic acid diluted to 0.5% to 1.0% or hypochlorous acid can also be used in some cases in which an acidic environment is preferred (eg, for topical treatment of Pseudomonas aeruginosa).58 Based on the healability classification of the wound, antiseptic agents with some tissue cytotoxicity may be used after a positive risk-benefit assessment. This includes agents such as low-concentration chlorhexidine or its derivative polyhexamethylene biguanide and povidone-iodine. This may be beneficial in cases of maintenance and nonhealable wounds that have a high potential for infection. Further, these agents can be used to manage odor and exudate in addition to controlling bioburden. In resource-limited environments, consider wound hygiene measures and how solutions are prepared, stored, and distributed to patients to prevent cross-contamination.
There is emerging interest in the use of surfactants to remove biofilms that often exist within wound debris and have two surfaces of different viscosity (Supplemental Table 2, http://links.lww.com/NSW/A177). Wound irrigation remains a controversial topic for use in chronic wounds. However, expert opinion is not to irrigate wounds if the base of the wound is not visible to avoid accumulation of the irrigation solution in closed spaces and accidental enlargement of the wound.57 Irrigate wounds with an adequate solution volume (50-100 mL per centimeter of wound length).59
Statement 7: local wound care: moisture management
7A. Maintain moisture balance in healable wounds with hydrogels, films, hydrocolloids, hydrofibers, alginates, and foams
7B. Institute moisture reduction with fluid-lock mechanisms in healable wounds using superabsorbents to wick moisture away from the surface (diaper technology)
7C. Determine if wound packing is needed for healable wounds. It could be wet (donate moisture) or dry (absorb moisture)
7D. Establish a targeted moisture reduction protocol in maintenance and nonhealable wounds to reduce bacterial proliferation
Maintaining moisture balance is complex and depends on the wound type and healing classification. Consider moisture balance, infection control, and patient education in selection of dressing materials.60 Incorporating and tailoring moisture management strategies to the specific wound type and the resources available can optimise patient outcomes and minimise complications (Table 6).3,54 Further research and clinical studies should continue to refine our understanding of wound moisture management to enhance wound care practices in the future.3,54
Table 6. Goals of moisture management based on wound healability3,42,54
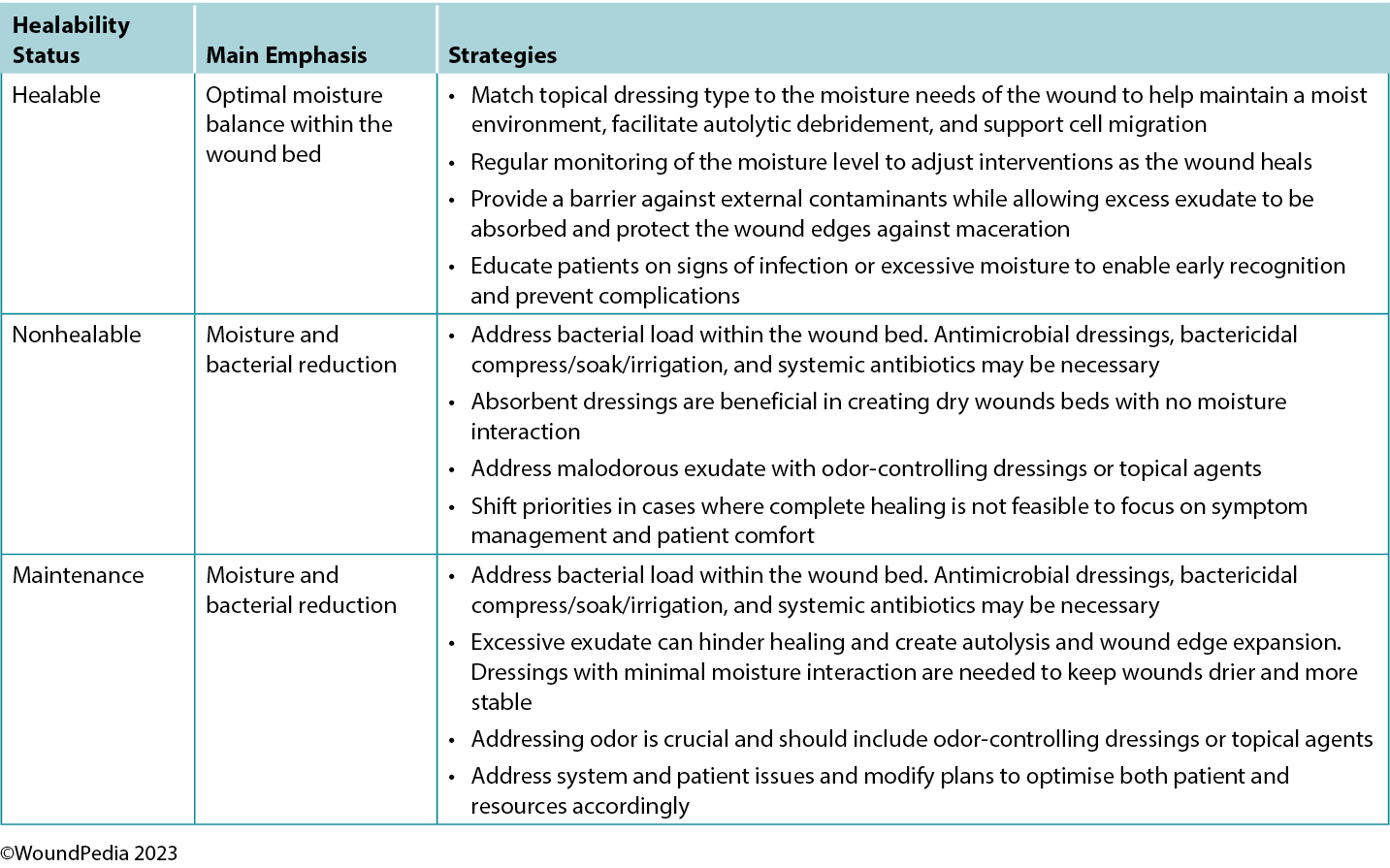
In general, as the level of exudate increases, so should the moisture absorbency or transferring capability of the dressing.3 Moisture-balance dressing options can be combined with antibacterial and anti-inflammatory properties to further meet the wound needs.
The choice of dressing for maintenance and nonhealable wounds should prioritise comfort while avoiding fluid donation to the wound bed and maceration of the wound edges. These wounds require regular reassessment for any progress or deterioration and should be managed to reduce bacterial load. Depending on wound evolution and characteristics over time, dressings may need to be adapted.
Statement 8: Healing trajectory
8A. Consider that healable wounds should be at least 20% to 40% smaller by week 4 to heal by week 12. If factors are present that affect healing time (poor glycemic control, for example), additional healing time may be required
8B. Allocate additional time to healing beyond 12 weeks in healable wounds if there are limited available resources, and continue with consistent care
8C. Prioritise referral to specialist centers (when available) for diagnostic testing and/or a skin biopsy, especially when faced with severe resource restrictions
Wound healing trajectories are useful and necessary for evaluating the needed time to heal, especially using clinical data (measurements) for both acute and chronic wounds. The healing trajectory is based on accurate and consistent wound measurements that determine the wound surface area closure over time. This helps to distinguish wound progression, stalled wounds, and worsening wound status.
Healable acute wounds should be completely closed within 30 days. Expect chronic healable wounds to have a 20% to 40% edge advancement at 30 days (4 weeks) and to close within 12 weeks.3,42,61,62 Nonhealable wounds have no defined time allocated to close, no edge advancement is expected, and all initiated steps are to prevent further deterioration. Maintenance wounds are not expected to heal nor deteriorate, and wound healing may progress slowly without a fixed time expectation unless patient/institution/system optimisation is achieved.
Re-evaluate hard-to-heal wounds periodically for alternate diagnoses. In these cases, consider wound biopsy, further investigation, and/or referral to an interprofessional assessment team. A healing trajectory can be assessed in the first 4 to 8 weeks to predict if a wound is likely to heal by week 12, provided there are no new complicating factors.63 Changes in the wound, the individual, or the environment may necessitate the reclassification of a wound to the maintenance or nonhealable category.
Statement 9: Edge advancement
9A. Consider locally constructed active modalities according to the required mechanism of action and the specific indications for initiating an adjunctive therapy to support wound healing
9B. Decide on adjunctive therapies through an interprofessional team approach and include a prior risk-to-benefit analysis
Select adjunctive therapies according to healability. Initiate these as soon as possible after injury in persons with major trauma to prevent sequelae of long chronicity. Select modalities using an interprofessional team approach based on what is available and the physical mechanism required (while ensuring trauma tissue healability). In hard-to-heal wounds, the wound may need a second chance to heal after reassessment.42 Ensure informed consent is a part of adjunctive therapy decisions.
A risk-to-benefit and cost-effectiveness analysis is helpful and will add in system sustainability. The key to effective adjunctive modality decisions is based on the risk it poses to initiate the therapy (physical discomfort, financial hardship, patient adherence) versus the benefit it will provide (tissue oxygenation, wound contraction, edema reduction, cellular reactivation).42,64 The best risk-benefit decisions are made within an interprofessional team including the patient, ensuring group commitment and treatment completion within optimal use of resources.
Optimising resources, or the slight repurposing thereof, may lead to creative strategies in the hands of interprofessional teams to tailor-make solutions to ensure all patients are optimally treated despite resource restrictions.
Surgery. Even in the most restricted environments, this is the one modality that is mostly available within a medical catchment area, often in tertiary care settings with referrals received from primary care clinics to provide debridement, general surgery with primary/tertiary intention closure, skin grafts, and/or amputations.
Skin grafts may be available in resource-restricted environments as an advanced modality to achieve tissue closure to reduce healing times and prevent recurrent deep wound infections. The procedure can minimise the extensive use of dressing materials over a prolonged period and reduce primary care chronic wound workload. Skin graft decisions are often made to preserve body functionality and promote early wound closure above aesthetic outcomes.65 However, avoid skin grafts for ischemic wounds and most venous stasis ulcers; consider them only in wounds where a favorable outcome could be expected.66,67
Electrical stimulation. Wound healing can be accelerated by enhancing the natural electrical current present in injured skin. In resource-limited environments, this modality should be investigated for wound healing because of its high-level evidence base and availability of devices of this nature (direct current, alternating current, low-intensity direct current, pulsed electromagnetic fields, high-voltage pulsed current, and transcutaneous electrical nerve stimulation devices). The evidence supports increased cellular proliferation and increased microcapillary perfusion, as well as a reduction in bacterial burden and infection on treated wound beds.68
Wall-mounted negative-pressure wound therapy. This can give the healthcare professional control over exudate management and accuracy in fluid replacement for inpatients with high exudate and large tissue defects. Start with the lowest possible pressure (minus 50-80 mm Hg). The patient becomes bedbound for the modality to be maintained, and the base layer (often gauze or petrolatum-impregnated dressings) needs to be replaced at least daily. This, together with starting on the lowest possible negative-pressure setting, will prevent mechanical trauma to the wound bed from tissue adherence and traumatic dressing removal in cases where nonadherent base layers are not available.69 There are now disposable negative-pressure wound therapy devices designed for use in the community as well as do-it-yourself options that can render acceptable clinical outcomes.70,71
Breathing high-flow, highly concentrated oxygen. Oxygen is often overlooked as a legitimate wound healing modality.72 Ironically, it is rarely used, although nearly all formal healthcare settings have copious amounts of oxygen available, even in relatively resource-poor environments. The availability of oxygen concentrators has also increased because of the COVID-19 pandemic, making oxygen administration also a possibility on an outpatient basis in home-based settings.73 Although hyperbaric oxygenation is the most effective means of increasing plasma oxygen concentration and tissue oxygen delivery, this modality is not always readily available. However, providing normobaric (ward) oxygenation still produces a 7.5-fold increase in plasma-borne oxygen (ie, from 0.3 mL/dL to 2.3 mL/dL; Table 7).74 Moreover, intermittent inhalation of 100% oxygen in patients without chronic obstructive pulmonary disorder (eg, 6 hours on/2 hours off by nonrebreather mask) over 3 to 4 days is not harmful to the lungs and may provide significant additional oxygen substrate, while the intermittent increase and decrease in oxygen delivery activate the expression of hypoxia-inducible factor (a strong stimulus for angiogenesis).75 This would suggest that in lieu of hyperbaric oxygen therapy, normobaric oxygen is justified for mitigating conditions on the FDA-approved list of indications for hyperbaric oxygen (Table 7).76 This may include tissue reperfusion injuries (eg, crush injuries, compartment syndromes before and after surgical release); bacterial toxin inhibition (ie, infective myonecrosis or other anaerobic infections); or large-tissue defects (after debridement to maintain the reactivated inflammatory response for up to 48 hours). Normobaric oxygen provides 50% of the Po2 of typical hyperbaric oxygen therapy (at 2 atmospheres); however, many of the pharmacologic effects of oxygen are achieved only under hyperbaric dosages.77,78
Table 7. Normobaric oxygen therapy mechanisms and delivery systems
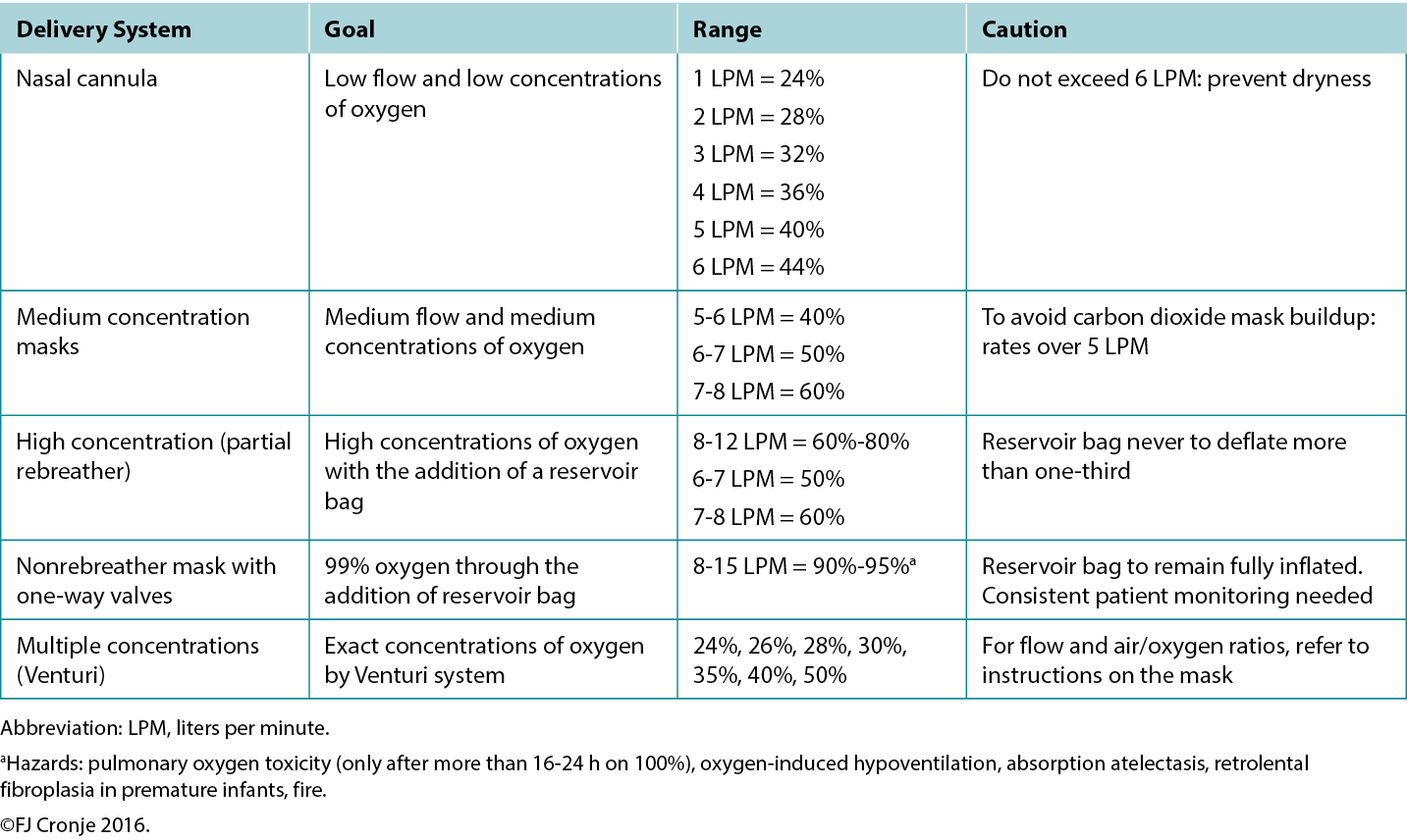
Note that topical oxygen administration directly to a wound does not have the same physiologic effects attributed to systemic oxygen delivery.79 Topical oxygen delivery systems remain subject to ongoing research to determine their beneficial actions beyond improved epithelialisation and possibly a mild antiseptic effect.64 The latter effect has also been attributed to ozone therapy.80 A systematic review completed in 2018 indicated that these therapies could potentially elicit mild oxidative stress or disinfection but that the risk of toxicity due to uncontrolled reactive oxygen species is high.81 Within the limited-resource environment, these devices and use thereof are likely uncontrolled.
Statement 10: Healthcare system change
10A. Facilitate evidence-informed, culturally competent, and equitable care for all patients
10B. Improve provider skills for wound management competency to enhance patient outcomes
10C. Establish timely and effective communication that includes the patient and all interprofessional wound care team members for improved healthcare system wound outcomes
Globally, chronic wound management consumes a significant portion of healthcare resources; preventive care represents the most cost-effective strategy for reducing healthcare system expenditures. There are numerous approaches to integrating preventive care into practice. For instance, DFUs are notorious for leading to high amputation rates and morbidity worldwide, even though many DFUs are preventable. Although diabetes was initially believed to be most prevalent in developed countries, it is noteworthy that 80% of diabetes-related deaths occur in countries with limited resources.82 A validated screening tool, an educated and available interprofessional team, and the implementation of prevention algorithms can be used in countries regardless of the availability of resources.83-85 Other organisational strategies that could be implemented include the following.
Patient navigation. Managing a DFU requires continual support from a circle of care that includes family members and healthcare professionals (including home care and wound care) working as a team. Timely access to both health and social services is often necessary to prevent and heal DFUs. Regionalised, community-based integrated diabetes services linked to interprofessional wound care clinics are proving to be most successful.86
One effective way to ensure optimal and timely care is patient navigation. This concept is adaptable to all healthcare sectors and can improve the timely diagnosis and treatment of wound infections, optimise pain management, and increase access to specialised care, thereby expediting wound closure rates.87 Patient navigation is becoming a vital component of integrated care, facilitating seamless transition between sectors and enhanced clinical outcomes. Further, it is accompanied by a boost in morale for both patient and healthcare professional, decreased nonacute hospital admissions or readmissions, enhanced patient quality of life, and improved adherence to treatment protocols. All these factors combined generate significant cost savings to healthcare systems.87,88
A critical element of successful patient navigation programs is the inclusion of a comprehensive and systematic approach to guide healthcare professionals in assessing and delivering care to each individual patient (eg, the WBP framework). These pathways do not need to be complicated or time consuming, but should ensure specific criteria are met, including regular foot care for those at high risk of amputation, glycemic control to an HbA1c less than 9%, and a BP less than 130/90 mm Hg.23,89
Policy interventions. Organisational policies that detail and provide guidance on best practice interventions and pathways are crucial for the successful and sustainable implementation of wound care protocols. Base these policies on current published guidelines for each specific wound type and translate them into the environment they need to serve. The institution needs to accept them as standards of practice and be approved as such to serve as evidence-based care in environments in which other guidelines may not be successfully adopted because of cultural or language translation challenges. Further, these policies must clearly outline the process for entering and using data, as ongoing quality improvement initiatives are based on data to improve and maintain effective care processes.
Adapted wound care. Although the delivery of care should be adapted to the unique needs of each healthcare sector, certain concepts should be standard, particularly those that enhance effective communication both within and across sectors. The increased adoption of digital technology expedites assessments, enhances access to specialised care, and optimises the allocation of limited resources.90 Where adaptations are implemented as care processes, these practices should be well documented as care standards and be easily accessible to ensure consistency and continuity of care within respective institutions.
Delphi consensus highlights
Some important comments from the panel:
- The ability to heal (healability) is a changeable modality and not to be seen as a static classification as patient condition, circumstances, and choices drive the classification allocation process (3A).
- The adjustment of practice as required in maintenance wounds incorporates the establishment of a conservative wound bed approach, with attention to the allowances the patient is willing to make within their life choices to slowly ensure patient optimisation and subsequently increase host competence (3B).
- When the method of patient documentation is agreed upon within an institution, it should be uniformly used to prevent communication gaps between providers that may inadvertently cause a negative impact on patient care outcomes (4A).
- Antiseptic mouth washes suitable for mucosa are often also friendly for use on a wound bed (4B). This may be considered off-label use.
- The choice for topical bacterial burden control should be on topical (low) toxicity antiseptics (the five most important ones), depending on the ability to heal and bacterial burden priorities to be addressed. Refrain from using topical antibiotic preparations, ointments, and creams on chronic wounds because those preparations are often focused only on Gram-positive organisms and would allow Gram-negative and anaerobic organisms on the wound bed to multiply freely. Further, topical antibiotic preparations need only one mutation to create systemic resistance to the targeted organism. Topical antibiotics are often in a carrier medium that is associated with contact irritant or contact allergic dermatitis (6A and 6B).
- When a healable wound has a significant moisture burden and remains in need of superabsorbent dressings to control the moisture balance of the wound bed, the wound needs thorough reassessment to ensure all underlying causes have been corrected for (7B).
- In establishing an interprofessional team, use any means of communication to build and maintain such a team as that could significantly optimise local capacity despite distances between providers and specialists to increase clinical outcomes despite local limitations (9B).
Conclusions
Optimise chronic wound care in resource-limited environments by initiating small adaptations and creative interventions without compromise to the core principles of care required. Interprofessional wound care teams can serve as a virtual resource to isolated and remote communities to improve clinical outcomes. All of the critical elements for (diabetic) foot management and care can easily be incorporated into diverse environments by increasing local capacity and providing clinician education and culturally appropriate patient empowerment.
Practice pearls
- The holistic care of PWDs includes the optimisation of HbA1c levels, BP, cholesterol levels, and drugs with cardiac- and renal-protective properties.
- The audible handheld 8-MHz Doppler pulse signal is a suitable bedside test for arterial blood supply to the lower limbs. It can be performed as a modification of the traditional ABPI, and the pulse sounds are easy verifiable by remote expert team members using MP3 or MP4 recordings from a cellphone.
- The NERDS and STONEES mnemonics can guide diagnosis and treatment of local/deep and surrounding infection, including an oral antibiotic indication for osteomyelitis.
- Plantar pressure redistribution can be accomplished from innovative, less costly alternatives such as soft felted simple inserts, to the total contact cast and removable cast walker made irremovable if the latter are unavailable or unsuitable for patient preferences or ADLs.
- Integrated coordinated care teams can connect with virtual expertise by equipping healthcare professionals with skills in patient navigation.
- Toolkits containing enablers for practice along with 8-MHz Dopplers and infrared thermometers can facilitate care in resource-limited settings.
Conflict of Interest
The authors declare no conflicts of interest.
Funding
The authors received no funding for this study.
Preparación del lecho de la herida 2024: Consenso Delphi sobre el tratamiento de las úlceras del pie en entornos con recursos limitados
Hiske Smart, R Gary Sibbald, Laurie Goodman, Elizabeth A Ayello, Reneeka Jaimangal, John H Gregory, Sadanori Akita, Afsaneh Alavi, David G Armstrong, Helen Arputhanathan, Febe Bruwer, Jeremy Caul, Beverley Chan, Frans Cronje, Belen Dofitas, Jassin Hamed, Catherine Harley, Jolene Heil, Mary Hill, Devon Jahnke, Dale Kalina, Chaitanya Kodange, Bharat Kotru, Laura Lee Kozody, Stephan Landis, Kimberly LeBlanc, Mary MacDonald, Tobi Mark, Carlos Martin, Dieter Mayer, Christine Murphy, Harikrishna Nair, Cesar Orellana, Brian Ostrow, Douglas Queen, Patrick Rainville, Erin Rajhathy, Gregory Schultz, Ranjani Somayaji, Michael C Stacey, Gulnaz Tariq, Gregory Weir, Catharine Whiteside, Helen Yifter, Ramesh Zacharias
DOI: 10.33235/wcet.44.1.13-35
Resumen
Antecedentes El tratamiento de heridas crónicas en entornos de bajos recursos merece especial atención. Es posible que los entornos rurales o con escasos recursos (por ejemplo, aquellos con necesidades básicas/suministros sanitarios limitados y disponibilidad irregular de miembros de equipos interprofesionales) no puedan aplicar o duplicar las mejores prácticas de los entornos urbanos o con abundantes recursos.
Objetivo Los autores unieron la experiencia mundial para desarrollar una aplicación práctica y científicamente sólida del modelo de preparación del lecho de la herida para comunidades sin recursos ideales.
Métodos Un grupo de 41 expertos en heridas de 15 países llegó a un consenso sobre la preparación del lecho de la herida en entornos con recursos limitados.
Resultados Cada enunciado de 10 conceptos clave (32 subenunciados) alcanzó más del 88% de consenso.
Conclusiones Las declaraciones de consenso y las justificaciones pueden orientar la práctica clínica y la investigación para los profesionales en entornos de bajos recursos. Estos conceptos deberían impulsar la innovación continua para mejorar los resultados de los pacientes y la eficiencia del sistema sanitario para todas las personas con úlceras de pie, especialmente las personas con diabetes.
Proposito general
Revisar una aplicación práctica y científicamente sólida del modelo de preparación del lecho de la herida para comunidades sin recursos ideales.
Publico objetivo
Esta actividad de formación continua está dirigida a médicos, asistentes médicos y personal de enfermería con interés en el cuidado de la piel y las heridas.
Objetivos/resultados del aprendizaje
Después de participar en esta actividad educativa, el participante:
1. Resumir las cuestiones relacionadas con la evaluación de heridas.
2. Identificar una clase de fármacos para el tratamiento de la diabetes mellitus tipo II que haya demostrado mejorar la glucemia, la nefroprotección y los resultados cardiovasculares.
3. Sintetizar estrategias para el tratamiento de heridas, incluido el tratamiento en entornos con recursos limitados.
4. Especificar el tiempo objetivo para el avance de los bordes en heridas crónicas curables.
Introducción
En el año 2000 se introdujo un marco para la preparación del lecho de la herida (WBP) con el fin de hacer hincapié en el tratamiento integral de la persona como base de un cuidado local óptimo de las heridas.1 A medida que este marco ha ido evolucionando hasta convertirse en un marco internacional, ha quedado claro que no todas las heridas son curables. Estos conceptos de heridas de mantenimiento y no curables condujeron a la revisión de los principios locales de cuidado de heridas y a la expansión de la WBP. La importancia de una atención integrada y coordinada en la que enfermeros, médicos y otros profesionales sanitarios trabajen juntos para optimizar los resultados de la atención al paciente y la utilización del sistema sanitario fue primordial para seguir desarrollando la WBP.
Este artículo se centra en la aplicación del marco de la WBP para tratar las heridas relacionadas con los pies, especialmente en personas con diabetes (PWD), úlceras neuropáticas del pie relacionadas con la lepra y otras complicaciones que incluyen la neuropatía y la enfermedad vascular. Varios parámetros son críticos para las PWD, como el mal control glucémico, los cambios de BP, el colesterol elevado, la redistribución inadecuada de la presión plantar, las infecciones y la falta de ejercicio. Los efectos del tabaco también son especialmente perjudiciales para salvar las extremidades y la vida de PWD.
Para este artículo es fundamental establecer una definición de los entornos con recursos limitados, incluida la baja disponibilidad de recursos, la falta o restricción de financiación, los entornos remotos, aislados o rurales, y las poblaciones indígenas. Todos estos términos se refieren a entornos sanitarios que pueden tener dificultades para acceder a suministros, equipos, especialistas y competencias y habilidades avanzadas en el cuidado de heridas. Los entornos de bajos recursos pueden estar presentes en cualquier parte del mundo y no se limitan a los países de renta baja o en vías de desarrollo.
El proceso Delphi en el que se basó este trabajo amplió y desarrolló el marco WBP en su formato actual. Cuarenta y un autores procedentes de 15 países participaron en el proceso Delphi, que se desarrolló en dos rondas utilizando una escala tipo Likert de cuatro partes (1, totalmente de acuerdo; 2, de acuerdo; 3, en desacuerdo; 4, totalmente en desacuerdo). La primera ronda constaba de 29 declaraciones. Aunque todas las declaraciones superaron el nivel de consenso deseado del 80%, hubo 299 comentarios considerados por el grupo principal de autores. Se recurrió a un editor profesional para mejorar la comprensión y la precisión gramatical de las declaraciones antes de pasar a la ronda Delphi 2, con 32 declaraciones construidas. Todas las declaraciones superaron el nivel de consenso del 88%.
En la ronda 2, 14 declaraciones alcanzaron un consenso del 100%. Una declaración destacó y fue calificada como "totalmente de acuerdo" por todos los miembros del grupo Delphi: 10C. Establecer una comunicación oportuna y eficaz que incluya al paciente y a todos los miembros del equipo interprofesional de cuidado de heridas para mejorar los resultados del sistema sanitario en relación con las heridas. Paralelamente, cada uno de los expertos internacionales en heridas trabajó en grupos para desarrollar el contenido del manuscrito. Consulte las declaraciones consensuadas en la Tabla suplementaria 1 (http://links.lww.com/NSW/A176).
El objetivo del consenso era establecer un nivel mínimo de asistencia con base científica que pudiera optimizarse en función de los recursos disponibles. En la tabla 1 figuran los 10 pasos clave y los 32 sustitutos para las heridas en entornos con recursos limitados. Este proceso de consenso actualizó el marco de la WBP para que fuera aplicable independientemente de la disponibilidad de recursos. Además, incluye por primera vez los conceptos de trayectorias de curación y cambio del sistema sanitario (Figura 1).
El resto de este informe destacará las 10 declaraciones de consenso y analizará la justificación de cada una de ellas.

Figura 1. Preparación del lecho de la herida 2024. ©WoundPedia 2023
Tabla 1. Preparación del lecho de la herida para heridas por debajo de la rodilla en entornos con disponibilidad limitada de recursos
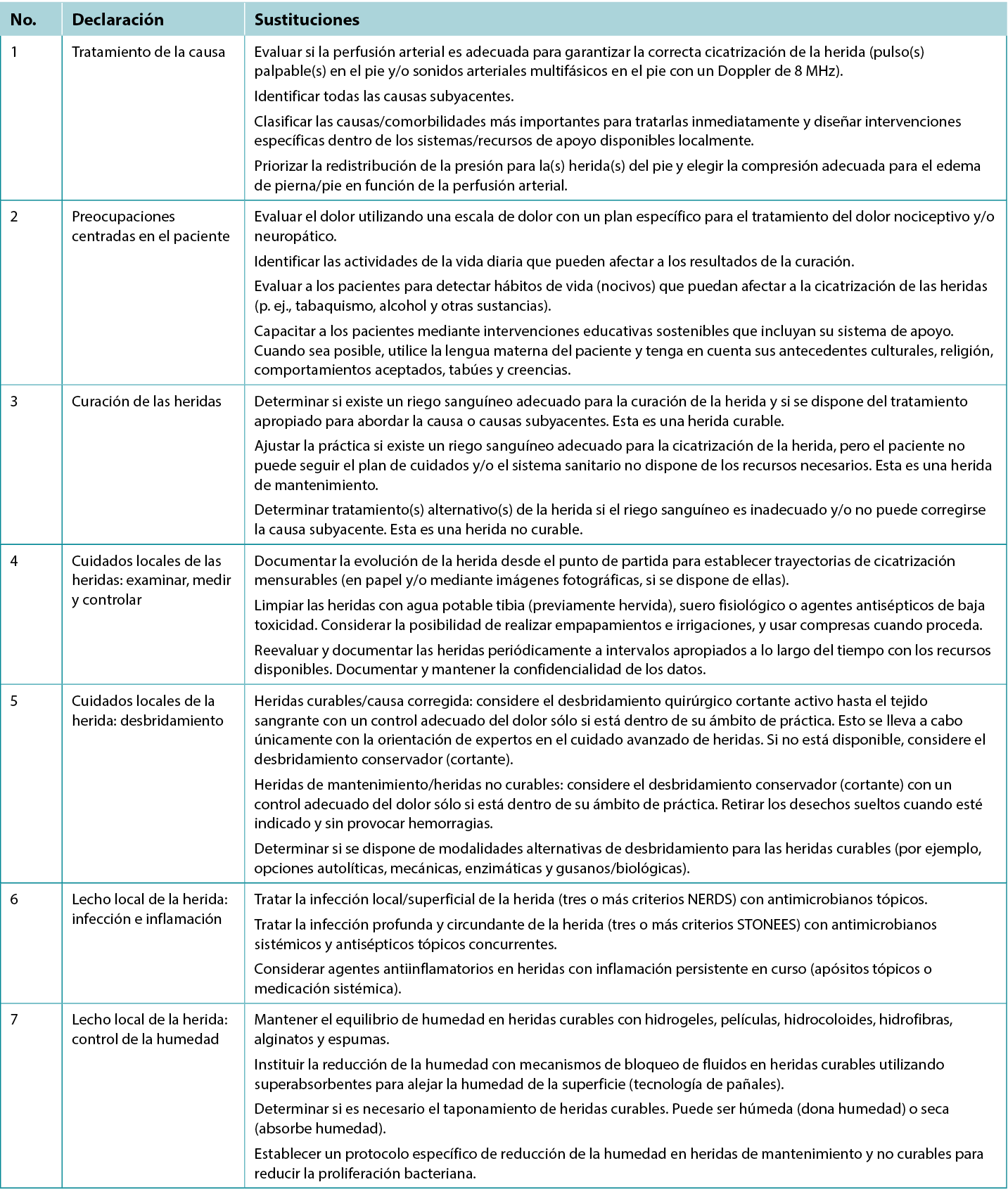

Declaración 1: tratamiento de la causa
1A. Evaluar si existe una perfusión arterial adecuada para garantizar la correcta cicatrización de la herida (pulso(s) palpable(s) en el pie y/o sonidos arteriales multifásicos en el pie con un Doppler de 8 MHz)
Para determinar el flujo sanguíneo de las extremidades inferiores, la primera acción vital es encontrar el pulso palpable del pie. Empezar con los pulsos dorsales del pie y/o tibial posterior. Si se dispone de un Doppler portátil de 8 MHz, confirmar los patrones de flujo multifásico (bifásico/trifásico). Remitir a los especialistas vasculares cuando se observe un sonido Doppler monofásico o ausente o no se palpen los pulsos del pie. Otros signos de perfusión arterial inadecuada son el dolor de las extremidades inferiores en reposo y los cambios isquémicos de las extremidades (extremidad fría con rubor dependiente que palidece al elevarla).
Las personas con diabetes son susceptibles de sufrir problemas microvasculares (neuropatía periférica, alteraciones del pie de Charcot) y complicaciones macrovasculares, incluida la enfermedad arterial periférica (PAD). Estas afecciones contribuyen a la aparición de callosidades, úlceras en los pies y pérdida de tejido mixto. Dado que hasta el 50% de las poblaciones susceptibles padecen tanto diabetes como PAD,2 la identificación oportuna de la EAP es fundamental (mediante exploración física y pruebas vasculares) porque es un factor de riesgo importante para la mala cicatrización de las úlceras y la amputación. Si se detecta, la revascularización inmediata (angioplastia o bypass vascular) es vital para restablecer el flujo arterial adecuado al pie. La evaluación adicional puede incluir el tiempo de relleno capilar, una prueba de blanqueamiento de Buerger (palidez en la elevación, rubor rojo brillante en la dependencia) y claudicación al caminar.
Examen vascular. En los casos de insuficiencia arterial, la extremidad suele estar fría al tacto debido a un aporte insuficiente de nutrientes y oxígeno (Tabla 2). Los casos graves pueden manifestar necrosis tisular en forma de úlceras, maceración de las membranas de los dedos (a menudo con infección secundaria), fisuras o gangrena. Otros indicadores de casos graves son la palidez al elevar la pierna, la claudicación inducida por el ejercicio que se resuelve con el reposo, la cianosis o rubor dependiente y la atrofia muscular. En particular, el edema de las extremidades inferiores es más indicativo de problemas venosos que arteriales. Las lesiones arteriales suelen ser punzantes, con una base profunda que a menudo contiene tendones, mientras que las úlceras venosas muestran una morfología de bordes irregulares con una base de tejido de granulación poco profunda.3
Tabla 2. Suministro vascular necesario para la curación de los tejidos
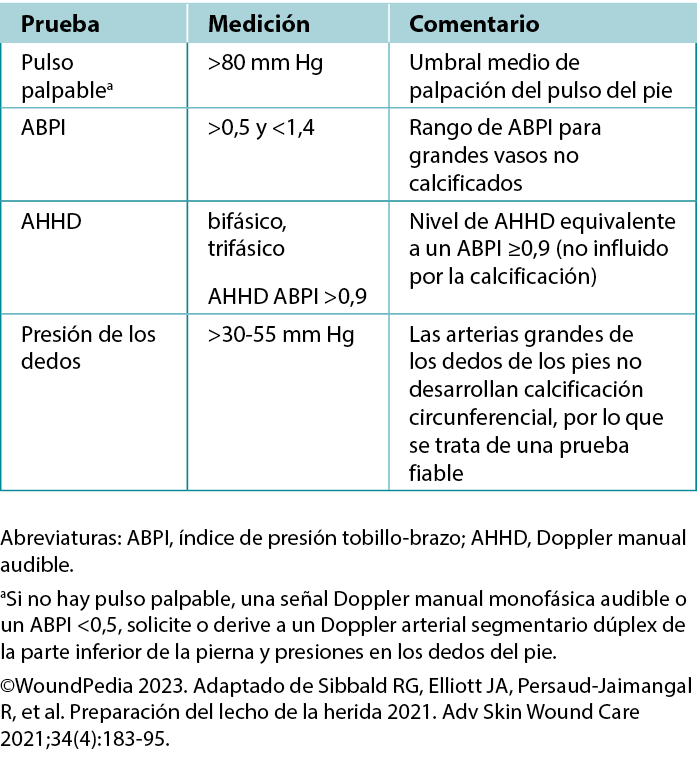
Examen del índice de presión tobillo-brazo (ABPI). El ABPI mide la relación entre la PA sistólica del tobillo dividida por la PA sistólica braquial mediante un Doppler de 8 MHz. El procedimiento consiste en utilizar un manguito de PA y registrar la PA sistólica cuando reaparecen los ruidos arteriales tras el inflado del manguito. Sin embargo, factores como el edema, la inflamación y la calcificación arterial pueden afectar a su precisión. Si no se puede permitir/obtener un Doppler de 8 MHz, la derivación precoz a un centro de evaluación terciaria se convierte en la prioridad en los casos en los que los pulsos del pie están ausentes. En determinados entornos sanitarios, se sigue exigiendo un ABPI como evaluación de cuantificación vital antes de iniciar cualquier intervención en las extremidades inferiores.
Examen Doppler manual audible (AHHD). El AHHD puede añadirse fácilmente como parámetro adicional en determinados contextos, en caso de que los proveedores opten por una prueba más sencilla y rápida (sin influencia de la calcificación, sin necesidad de apretar una pantorrilla dolorida y sin necesidad de estar en decúbito durante 20 minutos). La evaluación AHHD también puede proporcionar resultados precisos en caso de amputación de un dedo gordo y grabarse como archivo MP3 o MP4 y transferirse para la verificación remota de la interpretación de la señal.
Los profesionales sanitarios deben aplicar el gel en los puntos apropiados del pulso del pie con una sonda Doppler de 8 MHz colocada en un ángulo de45° con respecto a la piel en las arterias dorsales del pie, tibial posterior y peronea.
A continuación, pueden analizarse las señales/formas de onda Doppler adquiridas (mediante sonido audible o trazados visuales): Encontrará un tutorial completo sobre el procedimiento AHHD en https://journals.lww.com/aswcjournal/Pages/videogallery.aspx?videoId=20. Optimice la calidad de la señal con un cuidadoso reposicionamiento de la sonda para obtener la señal más fuerte o multifásica.
Una forma de onda monofásica o ausente justifica una evaluación vascular exhaustiva, incluido un Doppler arterial segmentario dúplex de la parte inferior de la pierna en el laboratorio vascular. Una forma de onda multifásica suele indicar la ausencia de enfermedad vascular periférica.4 En las PWD, hay que interpretar el cociente ABPI con precaución (debido a arteriosclerosis o calcificación arterial); los hallazgos multifásicos de AHHD son una opción preferible para confirmar un aporte sanguíneo adecuado para la cicatrización de heridas. Una forma de onda multifásica (bifásica, trifásica) sugiere un valor de AHHD equivalente a un ABPI normal ≥0,9.
Aunque el AHHD es eficaz para excluir la enfermedad arterial, es posible que no identifique los déficits de perfusión segmentarios existentes -islas de isquemia o defectos angiosómicos.5 Por lo tanto, la exploración física del pie y la extremidad inferior es vital para un diagnóstico concluyente. Los profesionales sanitarios pueden grabar las señales de AHHD y transmitirlas a los especialistas, lo que facilita las evaluaciones síncronas o asíncronas a distancia. Las evaluaciones sincrónicas permiten la participación del paciente en tiempo real y una rápida toma de decisiones.
Insuficiencia venosa crónica. La insuficiencia venosa crónica puede coexistir en las PWD y en aquellas con úlceras en los pies. Afecta principalmente a las extremidades inferiores y dificulta el retorno de la sangre desoxigenada al corazón y los pulmones. Esta afección suele deberse a una disfunción de la válvula venosa que puede desencadenarse por factores como el embarazo o el aumento de peso. Los síntomas suelen incluir varices, edema, decoloración de la piel por hemosiderina, lipodermatoesclerosis y úlceras venosas.6 Estas úlceras pueden ser de cualquier tamaño (desde pequeñas a circunferenciales) y se forman rápidamente sobre zonas de acumulación venosa, normalmente en la cara medial de las extremidades inferiores.
La piedra angular del tratamiento de las úlceras venosas es la terapia de compresión. Esto compensa la disfunción valvular al potenciar la acción peristáltica de la bomba muscular de la pantorrilla. Otras medidas adicionales son la elevación de las piernas y caminar. Los procedimientos de ablación venosa pueden considerarse cuando las úlceras se atribuyen a venas superficiales. El edema venoso no tratado puede retrasar la cicatrización de la úlcera del pie.7
Para la optimización médica de la PAD, las estrategias clave incluyen el control óptimo de la PA, la iniciación de la medicación para el colesterol y, a menudo, el inicio del tratamiento con estatinas. Estudios recientes también recomiendan tratar a los pacientes con PAD y enfermedad coronaria o carotídea concurrentes con una combinación de dosis bajas de aspirina (91-100 mg PO al día) y dosis bajas de rivaroxabán (2,5 mg PO BID).8 Otros factores modificables son dejar de fumar y los programas de caminar o hacer ejercicio. Para los pacientes con una úlcera en el pie (especialmente en las PWD), es esencial una redistribución o descarga adecuada de la presión plantar.
1B. Identificar todas las causas subyacentes
Las complicaciones de los pies son motivo de gran preocupación para las PWD y representan una importante carga de morbilidad para los sistemas sanitarios. Un enfoque holístico está representado por el mnemotécnico AIM (evaluación, identificación, gestión) y se centra en tratar o mitigar la causa subyacente de los problemas del pie diabético, especialmente la neuropatía. La aplicación de un enfoque centrado en la evaluación como norma básica de atención (VIPS: vascular, infección, presión, desbridamiento quirúrgico) es crucial para prevenir complicaciones graves, como ulceraciones del pie, amputaciones de miembros inferiores y una mayor incidencia de muerte temprana/prevenible. Algunos elementos críticos relacionados con los pies en entornos con escasez de recursos incluyen la presentación tardía a la atención formal, el retraso en el diagnóstico,9 caminar descalzo, las heridas desatendidas y la ausencia de cuidados preventivos de los pies. Un análisis observacional hospitalario realizado en Etiopía identificó varios factores que contribuyen a las complicaciones del pie diabético10, entre los que se incluyen la elevada humedad, la deformidad del pie, la neuropatía, las úlceras activas no identificadas, el calzado inadecuado o mal ajustado, la higiene deficiente de los pies (p. ej., hongos en pies y uñas de los pies) y la falta de concienciación sobre el cuidado de los pies. Una revisión sistemática sobre las úlceras plantares en pacientes con lepra (n = 7 estudios) identificó los siguientes factores de riesgo para el desarrollo de úlceras: incapacidad para sentir un monofilamento de 10 g en una prueba sensorial, deformidades graves del pie o hiperpronación, bajo nivel educativo y desempleo.11 Para abordar estos retos en cualquier entorno con recursos limitados se requiere un enfoque múltiple que puede incluir la educación del paciente y del profesional sanitario, la detección precoz, el acceso a la atención, los programas de calzado y la participación de la comunidad.
Las evaluaciones periódicas y exhaustivas de los pies incluyen la detección de neuropatía (pérdida de sensibilidad protectora), problemas vasculares (circulación sanguínea deficiente o inexistente en las extremidades inferiores), signos de infección, zonas de alta presión (formación de callos) y fricción (ampollas, a menudo con componentes hemorrágicos) para facilitar las intervenciones oportunas. La herramienta de cribado simplificada de 60 segundos puede ser un medio valioso para evaluar, estratificar y realizar un seguimiento rápido de los pacientes en función de sus niveles de riesgo sin un coste significativo.12 Los pacientes con antecedentes de ulceración, amputación, cirugía vascular periférica o neuroartropatía de Charcot son los que presentan un mayor riesgo de ruptura de la piel y deben recibir atención adicional para prevenir la ulceración y otras complicaciones.
Para detectar la infección, pueden ser útiles los criterios NERDS (infección superficial de la herida: no cicatriza, exudado, tejido de granulación rojo y friable, restos, olor) o STONEES (infección profunda y circundante de la herida: aumento de tamaño, temperatura 3 °F más alta, os [sonda al hueso], nuevas zonas de ruptura, eritema >2, exudado, olor) junto con el uso de termometría infrarroja sin contacto. 13 Las temperaturas elevadas de 3 °F en comparación con la extremidad opuesta pueden indicar inflamación y un pie con mayor riesgo de ulceración.13 Un cambio comparativo de 1,67 °C es difícil de medir clínicamente. Este mismo hallazgo en una persona con una úlcera en la parte inferior de la pierna o el pie es ocho veces más probable que signifique una infección profunda y circundante cuando va acompañado de dos o más criterios STONEES adicionales.13
Los pacientes con neuropatía sin úlcera y que presentan un pie hinchado y caliente podrían tener una neuroartropatía de Charcot aguda. La termometría infrarroja es una valiosa herramienta de evaluación en estos casos: los pies de Charcot agudos pueden estar entre 8 y 15 °F más calientes que la imagen especular del pie opuesto. Estos pacientes requieren una historia clínica completa, un examen físico e imágenes radiográficas para facilitar la detección precoz. Otras medidas incluyen la aplicación de una escayola de contacto total para la estabilización y la descarga completa de la presión plantar con una silla de ruedas para evitar un mayor deterioro óseo y prevenir la amputación de las extremidades inferiores (Tabla 3).
Tabla 3. Intervenciones de descarga para una herida plantar de pie diabético/neuropático28
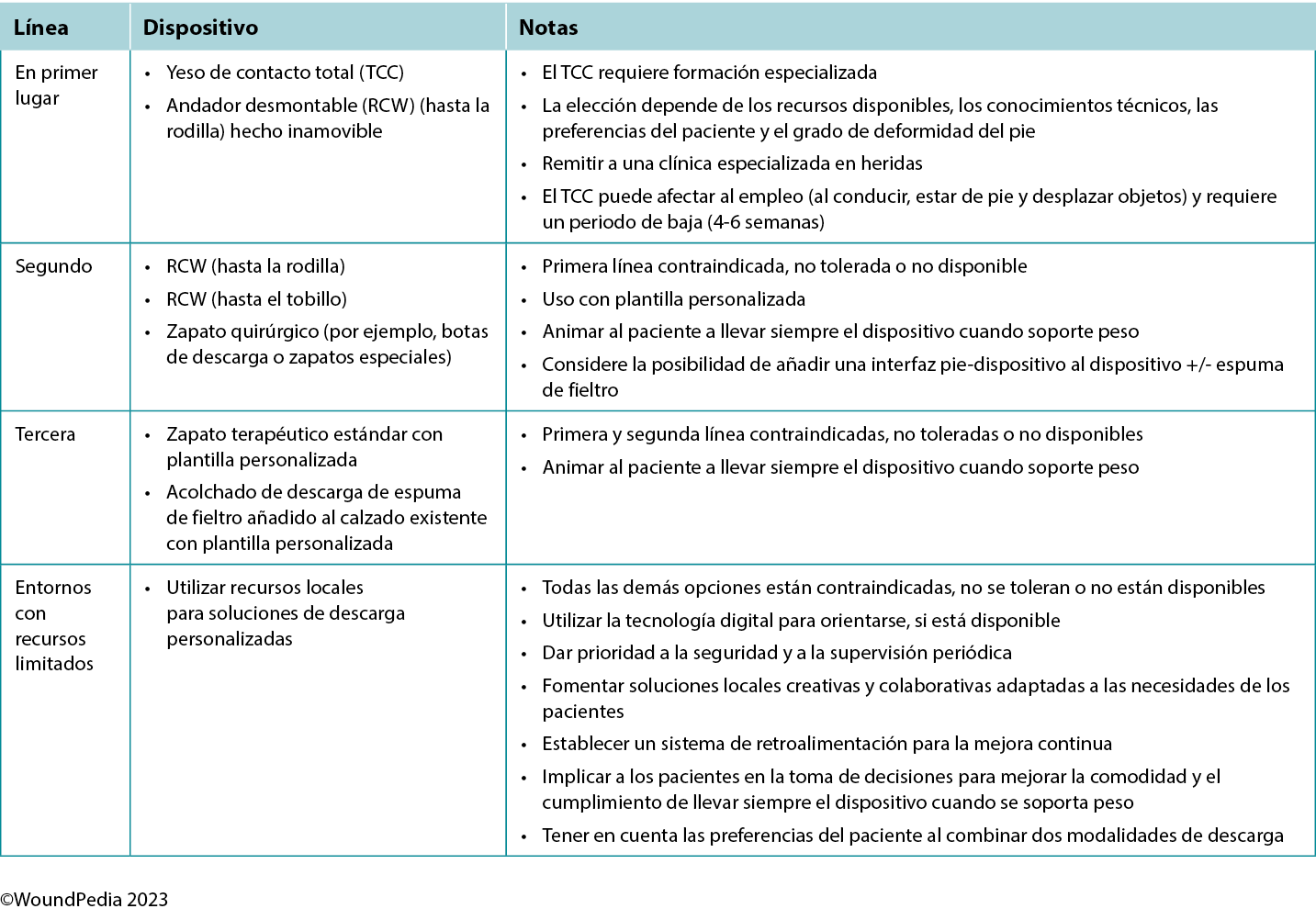
La formación de callos en las PWD está positivamente correlacionada con la presión y la tensión de cizallamiento. En las personas con neuropatía diabética, diversos factores, como las deformidades del pie, la movilidad limitada de las articulaciones, el estrés repetitivo durante la marcha y el calzado inadecuado, pueden aumentar el riesgo de formación de callos.14 Además, la presencia de callos puede suponer un riesgo importante, ya que los traumatismos repetitivos pueden provocar hemorragias subcutáneas y, con el tiempo, progresar a ulceración. Proporcionar dispositivos de redistribución de la presión a medida (plantillas blandas, intervenciones de zapatero para adaptar el calzado y reducción de la marcha descalza) para prevenir la posterior progresión de callosidad a úlcera.
Diferentes causas etiológicas pueden provocar úlceras en los pies de las PWD : neuropáticas debido a una neuropatía periférica, isquémicas asociadas a la arteriopatía periférica o una combinación de ambas: complicaciones neuroisquémicas del pie. La presencia de neuropatía diabética se establece a partir de la historia clínica; la exploración física (prueba del monofilamento de 5,07/10 g); la alteración de la sensibilidad distribuida simétricamente en ambas extremidades (distribución en medias y guantes); y el dolor ardiente, con escozor, punzante o con pinchazos.
1C. Clasificar las causas/comorbilidades más importantes para tratarlas inmediatamente y diseñar intervenciones específicas dentro de los sistemas/recursos de apoyo disponibles a nivel local
La úlcera del pie diabético (DFU) afecta a entre el 25% y el 34% de las personas con diabetes y es una de las complicaciones más temidas, ya que puede conducir a la amputación de las extremidades inferiores, a una discapacidad grave y a una reducción de la esperanza de vida.15 De origen multifactorial, la neuropatía periférica relacionada con la diabetes y la arteriopatía periférica hacen que los pies sean muy vulnerables a las lesiones traumáticas. El acceso a un diagnóstico y una intervención oportunos son factores determinantes para un tratamiento eficaz y la conservación de las extremidades.
La hiperglucemia crónica medida por la elevación de la hemoglobina A1c (HbA1c) es un importante factor de riesgo de neuropatía sensorial, motora y autonómica. Tanto la PAD como la sequedad cutánea aumentan la vulnerabilidad de los pies a las infecciones y retrasan la cicatrización, lo que contribuye a empeorar la situación. Las enfermedades renales crónicas aumentan el riesgo.16 Estudios recientes sobre la monitorización continua de la glucosa informan de que la alta variabilidad de la glucosa (tiempo reducido hasta alcanzar los niveles del intervalo objetivo) puede contribuir además a las complicaciones a largo plazo.17
Hasta el 50% de las PWD desarrollarán una neuropatía sin cura conocida. El tratamiento incluye la inspección diaria de los pies para detectar traumatismos o infecciones, el cuidado de los pies y la administración eficaz de glucosa.18 Además de la neuropatía, la PAD también contribuye a las DFU; la PAD es en gran medida asintomática y puede permanecer infradiagnosticada y sin tratar durante un periodo prolongado. La prevalencia de la PAD es más del doble en las personas diabéticas que en las que no la padecen.19 En una revisión sistemática de estudios comunitarios sobre la prevalencia global y los factores de riesgo de la PAD, la diabetes ocupó el primer lugar, junto con el tabaquismo.20
La Sociedad Europea de Hipertensión recomienda a proveedores y pacientes que se fijen como objetivo una PA sistólica inferior a 130 mm Hg y una PA diastólica inferior a 80 mm Hg. En las PWD, la PA sistólica no debe ser inferior a 120 mm Hg para evitar una reducción del flujo sanguíneo a los órganos vitales y las extremidades inferiores.21 Aunque pueden utilizarse diuréticos, antagonistas del calcio, inhibidores de la enzima convertidora de angiotensina, antagonistas de los receptores de angiotensina y bloqueadores beta, los inhibidores de la enzima convertidora de angiotensina y los antagonistas de los receptores de angiotensina reducen los episodios cardiovasculares.22,23 Recientemente, los inhibidores de SGLT2 han mostrado excelentes resultados en la mejora de la glucemia, la nefroprotección y los resultados cardiovasculares. 24 Además, la incidencia de DFU se reduce mediante la detección precoz de la PAD con modificaciones del estilo de vida.17
La complejidad de la gestión de una DFU requiere un enfoque de equipo interprofesional para identificar los determinantes biológicos, sociales, geográficos y culturales de la salud. En Dinamarca, las PWD están registradas por regiones y tienen acceso a clínicas especializadas con equipos interprofesionales para el cuidado de heridas. Las tasas de amputación de miembros inferiores han disminuido significativamente gracias a la mejora de la atención diabética, la inspección periódica de los pies, la mejora del autocuidado y el tratamiento oportuno.25
En poblaciones más dispersas geográficamente (p. ej., Ontario, Canadá), existen disparidades significativas en las tasas de amputación, más elevadas en las regiones rurales donde la prevención oportuna, como la cirugía de revascularización y los especialistas en el cuidado de los pies, están desatendidas o ausentes.
Las personas más vulnerables a las amputaciones relacionadas con el pie diabético en Canadá son los indígenas, los inmigrantes y las personas que viven en regiones rurales y septentrionales.26 El Círculo de Salud para la Diabetes Indígena ofrece un enfoque culturalmente sensible a las comunidades locales de las Primeras Naciones de Ontario con educación y conocimientos sobre diabetes, bienestar y autocontrol. Su programa holístico de cuidado de los pies apoya una serie continua de servicios que conecta a los miembros de la comunidad con agencias indígenas asociadas y profesionales sanitarios locales, y ha demostrado que reduce la incidencia de DFU y previene las amputaciones.27
1D. Priorizar la redistribución de la presión para la(s) herida(s) del pie y elegir la compresión adecuada para el edema de pierna/pie en función de la perfusión arterial
El criterio estándar para los dispositivos de redistribución de la presión plantar es la escayola de contacto total o el andador de escayola desmontable hecho inamovible.28 Incluso en los sistemas sanitarios en los que estas modalidades de descarga están fácilmente disponibles, menos del 10% de los pacientes que cumplen los requisitos están equipados con estos dispositivos y los utilizan.29
La descarga es primordial para curar las úlceras del pie (Tabla 3). El objetivo es seleccionar el mejor dispositivo para el paciente, teniendo en cuenta las preocupaciones del paciente, los objetivos de la asistencia y las pruebas de las mejores prácticas. Estudiar soluciones creativas para reutilizar materiales locales, como las plantillas de fieltro blando para descargar en entornos con recursos limitados. Es importante establecer un programa de vigilancia precoz entre el paciente y el profesional sanitario para controlar y garantizar los resultados de descarga deseados. Los profesionales sanitarios deben evaluar la eficacia de los dispositivos y realizar continuamente las modificaciones necesarias mediante un seguimiento establecido. En las regiones que carecen de profesionales especializados, dotar al personal sanitario de competencias en descarga básica puede colmar esta deficiencia.
Declaración 2: preocupaciones centradas en el paciente
2A. Evaluar el dolor utilizando una escala de dolor con un plan específico para el tratamiento del dolor nociceptivo y/o neuropático
La percepción del dolor implica un estímulo que puede ser físico o químico. Existen dos tipos principales de dolor: nociceptivo y neuropático (Tabla 4). El dolor relacionado con las heridas es un componente importante de las preocupaciones centradas en el paciente que los profesionales sanitarios suelen infravalorar. A finales de la década de 1990, el dolor de las heridas se convirtió en el centro de atención de los profesionales sanitarios con el lanzamiento de un documento de posición fundamental centrado en el dolor de las heridas.30 El documento reconocía y se centraba en la angustia del dolor crónico de las heridas y su influencia en la calidad de vida relacionada con la salud de los pacientes. El tratamiento del dolor de las heridas entonces se integró en el marco de la WBP.1,31
Tabla 4. Tipos de dolor y respuestas30
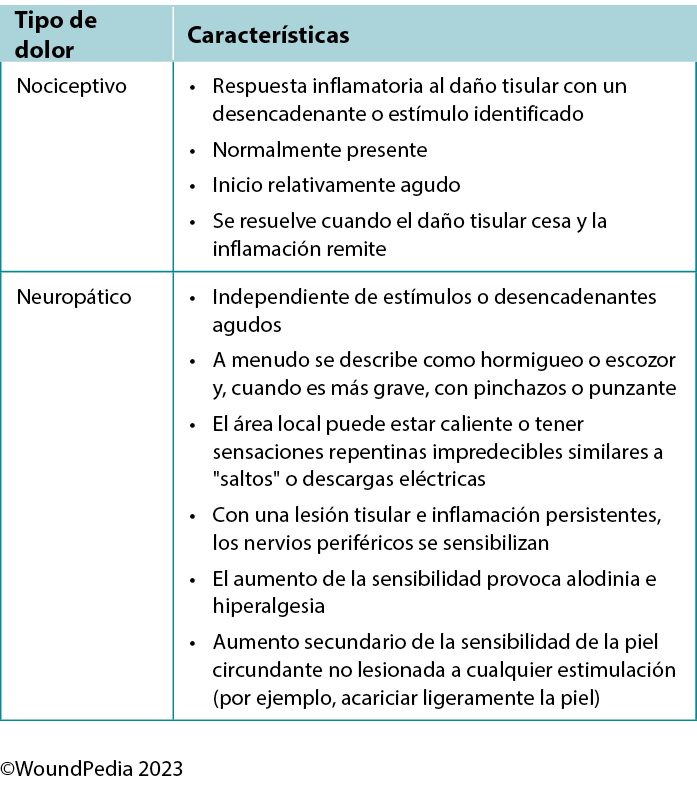
El dolor puede desempeñar un papel importante en el tratamiento total de las personas con heridas y en el éxito final de su curación.32 Las señales de dolor asociadas a las lesiones desempeñan una función importante en el bienestar del paciente y, como tales, deben reconocerse mediante una evaluación y un tratamiento adecuados.. Por ejemplo, el dolor o cualquier cambio en el dolor es un factor predictivo clave de la infección de la herida y uno de los cuatro signos cardinales de la inflamación.1 El dolor no resuelto se asocia a menudo con un retraso en el cierre de la herida.
Evaluación. La anamnesis del dolor es esencial para el tratamiento del dolor de la herida.32 La evaluación debe incluir la naturaleza, el inicio, la duración y los factores de exacerbación y alivio. Esto ayudará a determinar la causa del dolor y a orientar su tratamiento. La intensidad del dolor puede medirse de forma fiable utilizando escalas de dolor validadas. Una escala de valoración numérica de 0 a 10 puntos administrada verbalmente es una buena primera opción para medir la intensidad numérica del dolor. La mayoría de los pacientes pueden funcionar con un nivel de dolor de 3 a 4 sobre 10.33
Los pacientes con dolor persistente deben ser reevaluados periódicamente para comprobar su mejoría, deterioro y cumplimiento de los regímenes de medicación. El uso de un diario del dolor con anotaciones sobre la intensidad del dolor, los medicamentos utilizados, el estado de ánimo y la respuesta al tratamiento puede ser una buena estrategia de gestión. Para las personas con limitaciones de comunicación, la escala de dolor debe incorporar imágenes para facilitar su reconocimiento.
Gestión. El tratamiento del dolor de la herida puede integrarse en el marco de la WBP: tratar la causa y abordar los factores locales de la herida y las preocupaciones centradas en el paciente.3
El tratamiento de la causa debería determinar el diagnóstico correcto e iniciar el tratamiento del dolor de la herida. Las preocupaciones centradas en el paciente deben centrarse en lo que el paciente considera las principales razones y resoluciones del dolor. El dolor y el sufrimiento anticipados por el paciente pueden ser tan perjudiciales para la calidad de vida como la experiencia real del dolor.
Existen múltiples estrategias de tratamiento del dolor y no siempre son farmacéuticas (Tabla 5). A la hora de elegir una estrategia de tratamiento, hay que tener en cuenta el tratamiento total del paciente, incluidos todos los aspectos de la WBP. Recuerde: el dolor es lo que el paciente dice que es.34
Tabla 5. Estrategias para el tratamiento del dolor
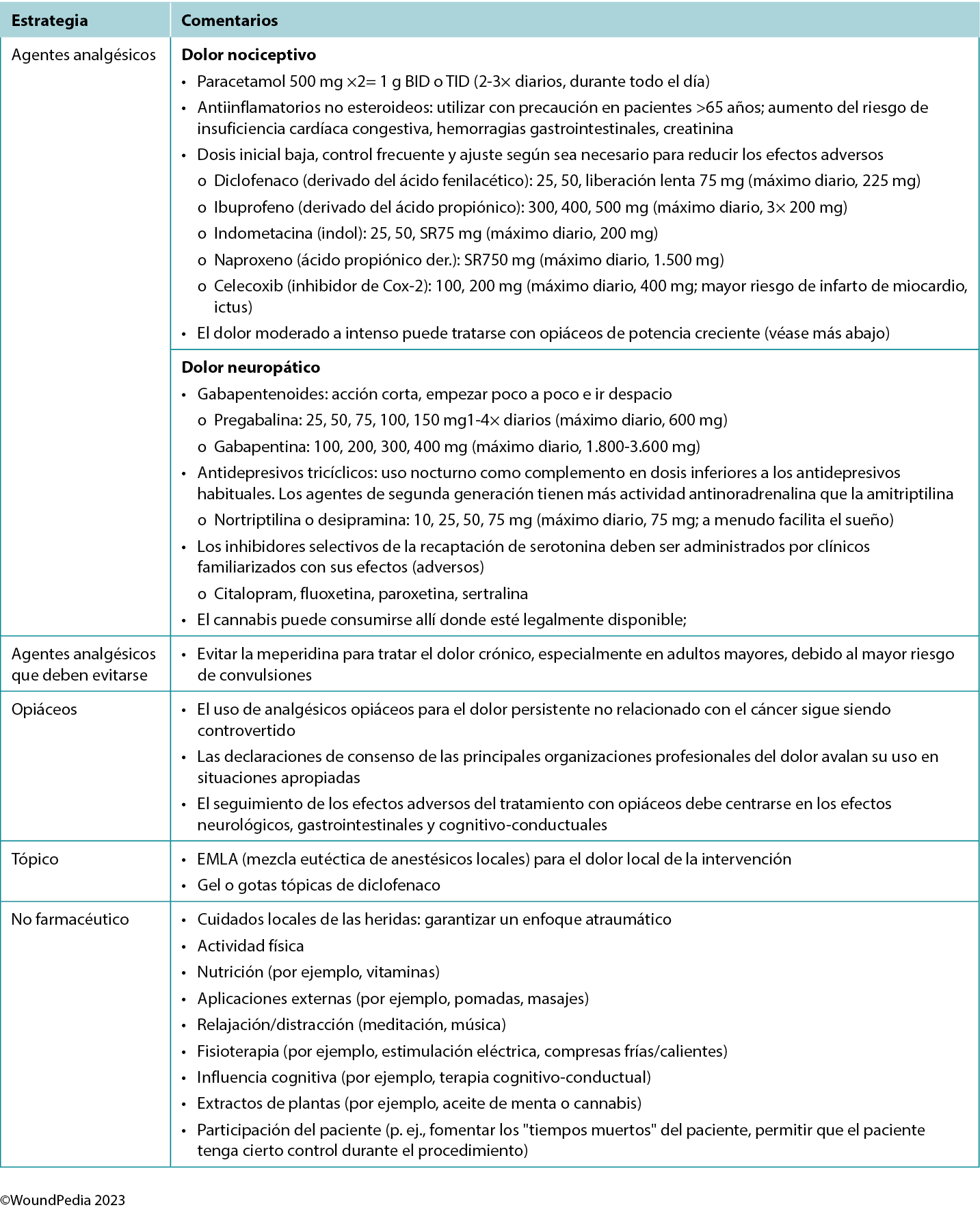
Evaluación y gestión con recursos limitados. En regiones con recursos limitados, la evaluación sigue siendo posible porque no requiere herramientas costosas. La mayoría de las escalas de dolor son de libre acceso, a pesar de cierto coste inicial en relación con la educación y la formación de los profesionales.31 Las opciones de tratamiento del dolor en entornos con recursos limitados pueden ser más prácticas si se impulsan con métodos no farmacológicos (Tabla 5). Algunas de estas opciones también pueden ser socialmente más aceptables o ya practicadas culturalmente (por ejemplo, la meditación, los tratamientos basados en plantas) y especialmente aplicables en el tratamiento del dolor nociceptivo. La aplicación de estas estrategias puede preservar el tratamiento farmacológico para las personas con dolor que no puede tratarse por medios no farmacológicos (por ejemplo, dolor neuropático).35
2B. Identificar las actividades de la vida diaria que pueden afectar a los resultados de la curación
2C. Evaluar a los pacientes para detectar hábitos de vida (nocivos) que puedan afectar a la cicatrización de las heridas (p. ej., tabaquismo, alcohol y otras sustancias)
2D. Capacitar a los pacientes mediante intervenciones educativas sostenibles que incluyan su sistema de apoyo. Cuando sea posible, utilice la lengua materna del paciente y tenga en cuenta sus antecedentes culturales, religión, comportamientos aceptados, tabúes y creencias
En entornos con recursos limitados, las preocupaciones centradas en el paciente y las barreras a los resultados clínicos son cruciales para que los proveedores las comprendan y aborden en el contexto de las creencias culturales, espirituales y religiosas de la comunidad respectiva.
Existen disparidades en la curación de heridas entre las poblaciones indígenas de todo el mundo. Estas disparidades suelen tener su origen en factores socioeconómicos, culturales y sanitarios históricos y actuales. La diversidad cultural y la presión social también suelen dictar los procesos formales de asignación de recursos a determinados sectores sanitarios. Algunos de los principales obstáculos para la cicatrización de heridas entre las poblaciones indígenas son los traumas históricos, las disparidades socioeconómicas, el acceso limitado a la asistencia sanitaria, las barreras culturales, los trastornos crónicos de salud, las prácticas curativas culturales, el aislamiento geográfico y los prejuicios del sistema sanitario.36 Muchas culturas tienen un sistema de honor en la gestión de sus miembros enfermos, adultos mayores y enfermos crónicos. Estos principios se mantienen más fácilmente si se dispone de recursos suficientes para mantenerlos.
Muchos estudios han identificado una enfermedad médica grave como una de las principales razones por las que una familia puede contraer grandes deudas.37,38 Incluso en las clínicas gestionadas por el gobierno, se pueden cobrar a la familia materiales de vendaje o medicamentos adicionales. Por ello, los pacientes y sus familiares pueden recurrir a métodos de tratamiento alternativos (medicina no alopática) de curanderos locales/indígenas/tradicionales. Aunque suelen ser menos costosos, estos curanderos pueden carecer de las habilidades o los conocimientos necesarios para tratar las heridas crónicas, lo que provoca su deterioro.
La pérdida de movilidad independiente debido a la cronicidad de la herida es otro factor importante que influye en la asistencia y el seguimiento regular. La disponibilidad de transporte varía en entornos con recursos limitados, y caminar puede ser la única forma de acceder a un punto de recogida de transporte público. Los entornos rurales aislados suelen ser los más afectados y requieren recorrer distancias considerables para llegar a un centro sanitario oficial.
La salud social del entorno familiar y la voluntad de incorporar a una persona con necesidades sanitarias pueden impulsar la calidad de los cuidados/autocuidados prestados, así como la seguridad del paciente en un entorno domiciliario. Debido a la estructura social y al entorno de los distintos países, el apoyo familiar y social puede variar según la cultura. A menudo, a medida que pasa el tiempo, la carga económica aumenta; la independencia del paciente y el logro de las actividades de la vida diaria (ADL) se deterioran; los cambios de apósito se vuelven más difíciles; y los cuidadores se estresan, fatigan y agotan.39 Las derivaciones tardías y las condiciones críticas/terminales del paciente cuando finalmente se presenta a la atención formal son factores sociales y de comportamiento agravantes adicionales que pueden agravar los malos resultados de la cicatrización de heridas.
Las personas con heridas tratadas en casa necesitan un espacio designado para ellas. El olor de las heridas, el dolor persistente y una rutina diferente son los principales factores de estrés tanto para el paciente como para la familia en entornos donde el espacio es escaso. La mera presencia de una herida cutánea importante ya repercute negativamente en las interacciones sociales, las relaciones, la sexualidad y la autoestima del propio paciente. Esto conduce a una ansiedad y depresión progresivas que pueden provocar pesimismo respecto a los beneficios percibidos del tratamiento. Posteriormente, los pacientes sufren una disminución de su autoeficacia, que a menudo se asocia a un mayor deterioro de la herida, incluidas amputaciones de las extremidades inferiores.40
El verdadero reto se plantea cuando es necesario modificar el estilo de vida. Esto suele requerir recursos adicionales o una formación a medida para elaborar planes de autocuidado.40,41 Nunca se insistirá lo suficiente en la necesidad de que las intervenciones de educación sanitaria y modificación del estilo de vida tengan una justificación clara. Las intervenciones en el estilo de vida pueden convertirse en un reto económico, social y logístico, primero para adquirirlas y luego para mantenerlas dentro de cualquier ámbito de vida restringido. Además, es un paso vital para garantizar que cualquier ayuda económica recibida se asigna correctamente al miembro de la familia con una herida.
Es necesario un enfoque biopsicosocial en la gestión del cuidado de las heridas de pacientes en entornos con recursos limitados. El equipo de tratamiento de heridas, además de tratar la herida, debe ocuparse de los factores de estrés social que afectan al paciente. Cada paciente necesitará un plan de tratamiento único, acordado mutuamente y adaptado a sus limitaciones (médicas, económicas, familiares, sociales y de apoyo emocional).40
Declaración 3: capacidad de curar
3A. Herida curable: Determinar si existe un riego sanguíneo adecuado para la cicatrización de la herida y si se dispone del tratamiento apropiado para tratar la causa o causas subyacentes
3B. Herida de mantenimiento: Ajustar la práctica si existe un aporte sanguíneo adecuado para la cicatrización de la herida, pero el paciente no puede seguir el plan de cuidados y/o el sistema sanitario no dispone de los recursos necesarios
3C. Herida no curable: Determinar tratamiento(s) alternativo(s) de la herida si el riego sanguíneo es inadecuado y/o no puede corregirse la causa subyacente
El proceso de determinación de la clasificación de cicatrización de una herida comienza con una anamnesis y una exploración física minuciosas del paciente. Es importante identificar la(s) causa(s) subyacente(s) de la herida. Abordar la(s) causa(s) subyacente(s) es el primer paso para desarrollar un plan de gestión factible.
En algunos casos, las heridas crónicas también pueden estancarse y no lograr el avance del borde de la herida en el tiempo establecido; éstas se conocen como heridas de difícil cicatrización. A menudo entran en la categoría de mantenimiento, pero con una evaluación adicional, pueden ser curables con una reevaluación del paciente, los antecedentes, las causas y el plan de tratamiento.3,42
Las preocupaciones y expectativas centradas en el paciente deben identificarse, compararse y alinearse con la disponibilidad de recursos institucionales/clínicos, las habilidades y las opciones de intervención inmediata disponibles.3,42 El plan de manejo se basa en la clasificación de curación asignada, que puede cambiar.
Proteger las heridas no curables contra la pérdida de tejido, la infección profunda y circundante de la herida y el deterioro general provocado por un entorno húmedo de la herida. Reducir la humedad es una prioridad. Las heridas de mantenimiento también necesitan protección frente a nuevas pérdidas de tejido, con un tratamiento del lecho de la herida seco y controles locales de la infección como pilar fundamental. La protección de los tejidos también puede ser una medida temporal hasta que se disponga de recursos y se controlen otros factores del paciente para lograr una optimización completa.
Las heridas estancadas pero curables (difícil cicatrización) necesitan una segunda oportunidad para lograr el avance del borde con urgencia en la reevaluación y la intervención del equipo interprofesional como máximas prioridades.3,42
Declaración 4: cuidado local de las heridas: examinar, medir y controlar
4A. Documentar la evolución de la herida desde el punto de partida para establecer trayectorias de cicatrización mensurables (en papel y/o mediante imágenes fotográficas, si se dispone de ellas).
4B. Limpiar las heridas con agua potable tibia (previamente hervida), suero fisiológico o agentes antisépticos de baja toxicidad. Considerar la posibilidad de realizar empapamientos e irrigaciones, y usar compresas cuando proceda.
4C. Reevaluar y documentar las heridas periódicamente a intervalos apropiados a lo largo del tiempo con los recursos disponibles. Documentar y mantener la confidencialidad de los datos.
La documentación de la evaluación de heridas es un componente integral de la práctica asistencial. Es fundamental para garantizar la prestación de cuidados de alta calidad a los pacientes, supervisar el estado de las heridas y orientar sobre cualquier cambio en las intervenciones. El registro exhaustivo y preciso de las evaluaciones de las heridas es esencial para garantizar la mejora de los resultados de los pacientes, la comunicación eficaz entre los profesionales sanitarios y el cumplimiento de la legislación y la normativa.43
Seguimiento de los progresos. La documentación de la evaluación de la herida sirve como registro histórico de la progresión de la herida a lo largo del tiempo. Al documentar periódicamente las características de la herida, como el tamaño, la profundidad, el color, el exudado, la infección, el tipo de tejido, etc., los profesionales sanitarios pueden hacer un seguimiento de los cambios, identificar posibles complicaciones y ajustar los planes de tratamiento. Si se utiliza documentación fotográfica, se debe obtener el consentimiento del paciente de acuerdo con la política de la organización, garantizar una técnica apropiada con una iluminación adecuada y a una distancia apropiada de la herida, e incluir una guía de medición en la foto.44 Esta evaluación continua es fundamental para evaluar la eficacia de las intervenciones y tomar decisiones informadas con respecto al tratamiento de heridas. Al medir la superficie o el volumen, es imprescindible utilizar una técnica coherente independientemente de la tecnología.
Comunicación. Una evaluación precisa de las heridas facilita la comunicación eficaz entre los profesionales sanitarios. Cuando todos los miembros del equipo tienen acceso a una documentación coherente y actualizada sobre las heridas, pueden trabajar juntos para elaborar y aplicar un plan de cuidados coordinado que garantice que los pacientes reciben el mejor tratamiento posible. Es fundamental utilizar una terminología coherente y común a todas las disciplinas. El sistema de clasificación médica de la Clasificación Internacional de Enfermedades es un ejemplo de norma de aplicación mundial.45
Cumplimiento legal y reglamentario. La evaluación y documentación adecuadas de las heridas son esenciales para cumplir los requisitos legales y reglamentarios. Los registros inexactos o incompletos pueden dar lugar a problemas legales y repercutir negativamente en la práctica de un profesional sanitario, incluso en entornos con recursos limitados.
Reembolso. En muchos sistemas sanitarios, la documentación adecuada de la evaluación de las heridas está vinculada a modelos de financiación basados en el reembolso. A menudo se necesitan registros precisos y detallados para justificar el uso de productos o procedimientos específicos para el cuidado de heridas y garantizar que las organizaciones reciban un reembolso adecuado por los servicios prestados.
Investigación y mejora de la calidad. Los datos de evaluación de las heridas son un recurso valioso para la investigación y las iniciativas de mejora de la calidad. Este proceso de aprendizaje continuo contribuye a mejorar el cuidado global de las heridas y los resultados de los pacientes.
Atención centrada en el paciente. La evaluación y documentación adecuadas de las heridas son un componente esencial de la atención centrada en el paciente. Garantiza que las afecciones de los pacientes se evalúen a fondo y que sus planes de tratamiento se adapten a sus necesidades específicas. Cuando los pacientes observan que su profesional sanitario se compromete a documentar y controlar sus heridas, puede aumentar la confianza y la satisfacción del paciente.
Para promover la coherencia lingüística y mejorar la claridad de los datos, cada vez más empresas están creando programas y aplicaciones informáticos de evaluación electrónica de heridas con el fin de reducir el tiempo necesario para una documentación exhaustiva.43 Estos programas y aplicaciones (algunos más asequibles que otros) pueden proporcionar al equipo sanitario un conjunto estructurado de parámetros para garantizar que se documentan todas las características clínicas, mejorando así la comunicación general.46 Aunque estas herramientas son una ventaja para los profesionales sanitarios, no están exentas de riesgos, como el copiado y pegado incorrectos de informes/notas de consulta anteriores o los riesgos para la seguridad de los datos de los pacientes. En las zonas donde no se disponga de estos programas y aplicaciones, la actualización el paciente y proporcionar planes de evaluación e intervención por escrito puede estar justificado.
Declaración 5: cuidado local de las heridas: desbridamiento
5A. Heridas curables/causa corregida: Considere la posibilidad de realizar un desbridamiento quirúrgico cortante activo hasta el tejido sangrante con un control adecuado del dolor sólo si está dentro de su ámbito de práctica. Esto se lleva a cabo únicamente con la orientación de expertos en el cuidado avanzado de heridas. Si no está disponible, considerar el desbridamiento conservador (cortante)
5B. Heridas de mantenimiento/heridas no curables: Considere el desbridamiento conservador (cortante) con un control adecuado del dolor sólo si está dentro de su ámbito de práctica. Retirar los desechos sueltos sólo cuando esté indicado y sin provocar hemorragias
5C. Determinar si existen modalidades alternativas de desbridamiento para las heridas curables (por ejemplo, opciones autolíticas, mecánicas, enzimáticas y biológicas con gusanos)
El desbridamiento es un proceso importante en el paradigma de la WBP para eliminar el tejido necrótico y otros biomateriales, incluida la biopelícula, en las heridas curables y prevenir el olor y la infección en las heridas de mantenimiento. Para todas las heridas situadas por debajo de la rodilla, comunicar los resultados de cualquier prueba vascular (p. ej., ABPI, forma de onda) a todos los miembros del equipo interprofesional, y documentar en consecuencia antes de intentar el desbridamiento, ya que muchos tipos pueden ser perjudiciales para el lecho de la herida con un aporte vascular reducido.
En el caso de las heridas curables, las intervenciones locales en el lecho de la herida se determinan mejor mediante el paradigma de la WBP, basándose en las características del paciente y de la herida. Considerar el desbridamiento quirúrgico (hasta el tejido sangrante) como intervención de primera línea. Sin embargo, en muchas regiones rurales y remotas puede no haber acceso a un profesional sanitario cualificado con la formación, los conocimientos y el juicio necesarios para este procedimiento.
El desbridamiento conservador (cortante) (sin provocar hemorragias) requiere conocimientos y habilidades avanzados y es más adecuado para entornos de atención no aguda o clínicas especializadas. Retire de la herida únicamente los restos sueltos que cuelguen o estén sueltos sin causar traumatismo en el lecho de la herida.
La terapia de desbridamiento clínico estéril con gusanos es una modalidad de tratamiento limitada en entornos con recursos restringidos, excepto en casos de exposición accidental. La infestación por gusanos suele descubrirse durante los cambios de apósito. El tratamiento accidental con gusanos puede dar buenos resultados de desbridamiento, sobre todo si las larvas proceden de la muy selectiva mosca de la botella Lucilia sericata/cuprina, ya que se centran en el tejido desvitalizado como fuente de alimento.47,48 Pueden darse resultados perjudiciales si la infestación procede de la mosca doméstica común (Musca domestica) o de otras especies invasoras, ya que estas larvas pueden destruir indiscriminadamente el tejido sano.47,48
Los profesionales sanitarios deben evaluar métodos alternativos de desbridamiento (p. ej., autolítico, enzimático, mecánico) para los sectores comunitarios, incluida la atención primaria, la atención domiciliaria y la atención a largo plazo. Dentro de los recursos disponibles, es vital tener en cuenta la seguridad del paciente, evaluar los factores ambientales e identificar las barreras para la cicatrización de las heridas antes de iniciar el desbridamiento.
Los protocolos de desbridamiento adecuados para las heridas de mantenimiento y no curables difieren significativamente de los de las heridas curables. Aunque la cicatrización húmeda proporciona un entorno óptimo para la curación de las heridas, es una forma de desbridamiento (autolítica) que puede ser perjudicial para las heridas no curables y de mantenimiento. Por lo general, el desbridamiento no es una intervención adecuada para las heridas estables de mantenimiento o no curables, ya que el objetivo es mantenerlas secas y libres de infección.49 Considere el desbridamiento sólo cuando una herida de mantenimiento o no curable se vuelva inestable para eliminar los restos infectados o necróticos de la herida de la forma más atraumática posible.
Entre los objetivos de los pacientes suelen figurar la mejora de la comodidad, la minimización del olor relacionado con la herida, la reducción del dolor y la mejora de las ADL. Mantener la herida seca permite la formación de una capa protectora, mientras que el desbridamiento conlleva el riesgo de eliminar esta capa protectora e introducir organismos patógenos.
Declaración 6: cuidado local de las heridas: infeccion e inflamación
6A. Tratar la infección local/superficial de la herida (tres o más criterios NERDS) con antimicrobianos tópicos
6B. Tratar la infección profunda y circundante de la herida (tres o más criterios STONEES) con antimicrobianos sistémicos y antisépticos tópicos concurrentes
6C. Considerar agentes antiinflamatorios en heridas con inflamación persistente en curso (apósitos tópicos o medicación sistémica)
Los criterios validados NERDS y STONEES pueden orientar la evaluación y el tratamiento de la infección y la inflamación en las heridas crónicas.50 Basar el diagnóstico de la infección en los signos y síntomas clínicos más que en frotis superficiales de la herida, que deben utilizarse únicamente para orientar la selección de antimicrobianos en caso de infección. Si se sospecha una infección profunda y del tejido circundante, identificar las especies bacterianas y su sensibilidad a los agentes antibacterianos de uso común para ayudar a guiar el uso de antimicrobianos sistémicos. Esto es especialmente cierto si una infección profunda y circundante no responde al tratamiento empírico.
Las mejores muestras de tejido para los hisopos de cultivo del lecho de la herida se obtienen tras limpiar la herida con agua potable o solución salina y tomar muestras de la base de la herida sin restos. Lo más probable es que un cultivo a partir de muestras de tejido mediante una cureta u otra técnica de biopsia represente los organismos presentes en el tejido de la herida. Alternativamente, una técnica semicuantitativa con hisopo utilizando el método de Levine puede correlacionarse con las biopsias de tejido.51 El hisopo se coloca sobre el tejido de granulación y se presiona lo suficiente para extraer el exudado de la herida y, a continuación, se gira 360° para cubrir todas las superficies del hisopo.. Colocar el hisopo en el medio de transporte para prehumedecerlo antes de colocarlo sobre la piel puede aumentar el rendimiento bacteriano en pacientes con heridas poco exudadas.52
Las bacterias patógenas pueden infiltrarse en el hueso y causar osteomielitis, lo que descarrila el potencial de curación y es difícil de curar. La biopsia ósea es el criterio estándar para diagnosticar la sospecha de osteomielitis, ya que los cultivos superficiales no acceden al tejido óseo profundo y el diagnóstico por imagen está limitado por una especificidad variable.53 Sin embargo, la biopsia ósea puede resultar incómoda, depende de clínicos expertos y puede prolongar el daño tisular. Por estas razones, a menudo no es una opción viable, más aún si los recursos son escasos.
Cuando se confirma la infección profunda de la herida, los apósitos antimicrobianos son apropiados para apoyar localmente la terapia antibiótica sistémica y prevenir la propagación al compartimento profundo y circundante de las bacterias superficiales. Las cinco opciones más comunes de apósitos antimicrobianos son la plata, la biguanida de polihexametileno, el yodo, el azul de metileno/violeta de cristal y la miel. De ellos, la plata y la miel tienen propiedades antiinflamatorias adicionales.54
En algunas heridas, se aplican antisépticos de amplio espectro para reducir rápidamente la carga bacteriana a corto plazo como apoyo a los antibióticos sistémicos. Cuando el riesgo de infección es mayor que las propiedades citotóxicas, una gasa humedecida con povidona yodada de bajo coste que se cambie a diario sobre el hueso expuesto puede reducir las bacterias superficiales. Se trata de una estrategia a corto plazo acompañada de una evaluación clínica de los niveles séricos de la función tiroidea, especialmente cuando la superficie de la herida es grande. Sin embargo, con los nuevos antisépticos de baja toxicidad, ahora se dispone de otras opciones menos agresivas, pero igualmente eficaces.
En general, las heridas en pacientes inmunocompetentes que se presentan durante menos de 1 mes se tratan con agentes para la cobertura de grampositivos. Las infecciones polimicrobianas (típicamente observadas en las PWD) o las heridas de más de 1 mes de duración requieren agentes de amplio espectro con cobertura para grampositivos, gramnegativos y anaerobios, ya que estos pacientes suelen estar también inmunodeprimidos.55
Los agentes citotóxicos pueden ser apropiados para heridas no curables si la necesidad de acción antimicrobiana tópica es mayor que la toxicidad tisular. En general, se prefieren los antisépticos a los antibióticos tópicos como parte de la administración de antibióticos debido a un menor riesgo de resistencia bacteriana sistémica y a los efectos adversos asociados con la dermatitis irritante de contacto o alérgica de contacto.54
6D. Limpiar suavemente la herida con soluciones de baja toxicidad (agua, solución salina, agentes antisépticos no citotóxicos).
La solución de limpieza utilizada depende de las características de la herida y de la disponibilidad en la práctica. Existe poco consenso en la literatura sobre las recomendaciones de limpieza de heridas. Una revisión Cochrane actualizada de 2021 sobre las soluciones de limpieza de las úlceras venosas de la pierna concluyó que faltan pruebas de ensayos controlados aleatorios "para orientar la toma de decisiones sobre la eficacia de la limpieza de heridas en comparación con la no limpieza y los enfoques óptimos para la limpieza de las úlceras venosas de la pierna".56 Sin embargo, los principios generales del cuidado de heridas implican soluciones de baja toxicidad que incluyan agua potable o prehervida, suero fisiológico y otros agentes antisépticos inocuos para las heridas.57 Esto evita los efectos citotóxicos y el daño al tejido de granulación sano en las heridas curables.
El ácido acético diluido entre el 0,5% y el 1,0% o el ácido hipocloroso también pueden utilizarse en algunos casos en los que se prefiere un entorno ácido (p. ej., para el tratamiento tópico de Pseudomonas aeruginosa).58 En función de la clasificación de la curación de la herida, pueden utilizarse agentes antisépticos con cierta citotoxicidad tisular tras una evaluación positiva de la relación riesgo-beneficio. Esto incluye agentes como la clorhexidina de baja concentración o su derivado, la polihexametilenbiguanida y la povidona yodada. Esto puede ser beneficioso en casos de heridas de mantenimiento y no curables que tienen un alto potencial de infección. Además, estos agentes pueden utilizarse para controlar el olor y el exudado, así como la carga biológica. En entornos con recursos limitados, hay que tener en cuenta las medidas de higiene de las heridas y cómo se preparan, almacenan y distribuyen las soluciones a los pacientes para evitar la contaminación cruzada.
Existe un interés emergente en el uso de tensioactivos para eliminar biopelículas que a menudo existen entre los restos de heridas y tienen dos superficies de diferente viscosidad (Tabla suplementaria 2, http://links.lww.com/NSW/A177). La irrigación de heridas sigue siendo un tema controvertido para su uso en heridas crónicas. Sin embargo, la opinión de los expertos es no irrigar las heridas si la base de la herida no es visible para evitar la acumulación de la solución de irrigación en espacios cerrados y el agrandamiento accidental de la herida.57 Irrigar las heridas con un volumen de solución adecuado (50-100 mL por centímetro de longitud de la herida).59
Declaración 7: cuidado local de las heridas: control de la humedad
7A. Mantener el equilibrio de la humedad en heridas curables con hidrogeles, películas, hidrocoloides, hidrofibras, alginatos y espumas
7B. Instituir la reducción de la humedad con mecanismos de bloqueo de fluidos en heridas curables mediante superabsorbentes para alejar la humedad de la superficie (tecnología de pañales)
7C. Determinar si es necesario el taponamiento de heridas curables. Puede ser húmedo (dona humedad) o seco (absorbe humedad)
7D. Establecer un protocolo específico de reducción de la humedad en heridas de mantenimiento y no curables para reducir la proliferación bacteriana
Mantener el equilibrio de la humedad es complejo y depende del tipo de herida y de la clasificación de la cicatrización. A la hora de seleccionar los apósitos, hay que tener en cuenta el equilibrio de la humedad, el control de infecciones y la educación del paciente.60 La incorporación y adaptación de estrategias de control de la humedad al tipo específico de herida y a los recursos disponibles puede optimizar los resultados para el paciente y minimizar las complicaciones (tabla 6).3,54 La investigación y los estudios clínicos adicionales deben seguir perfeccionando nuestros conocimientos sobre el control de la humedad de las heridas para mejorar las prácticas de cuidado de heridas en el futuro.3,54
Tabla 6. Objetivos de la gestión de la humedad basados en la capacidad de curación de las heridas3,42,54
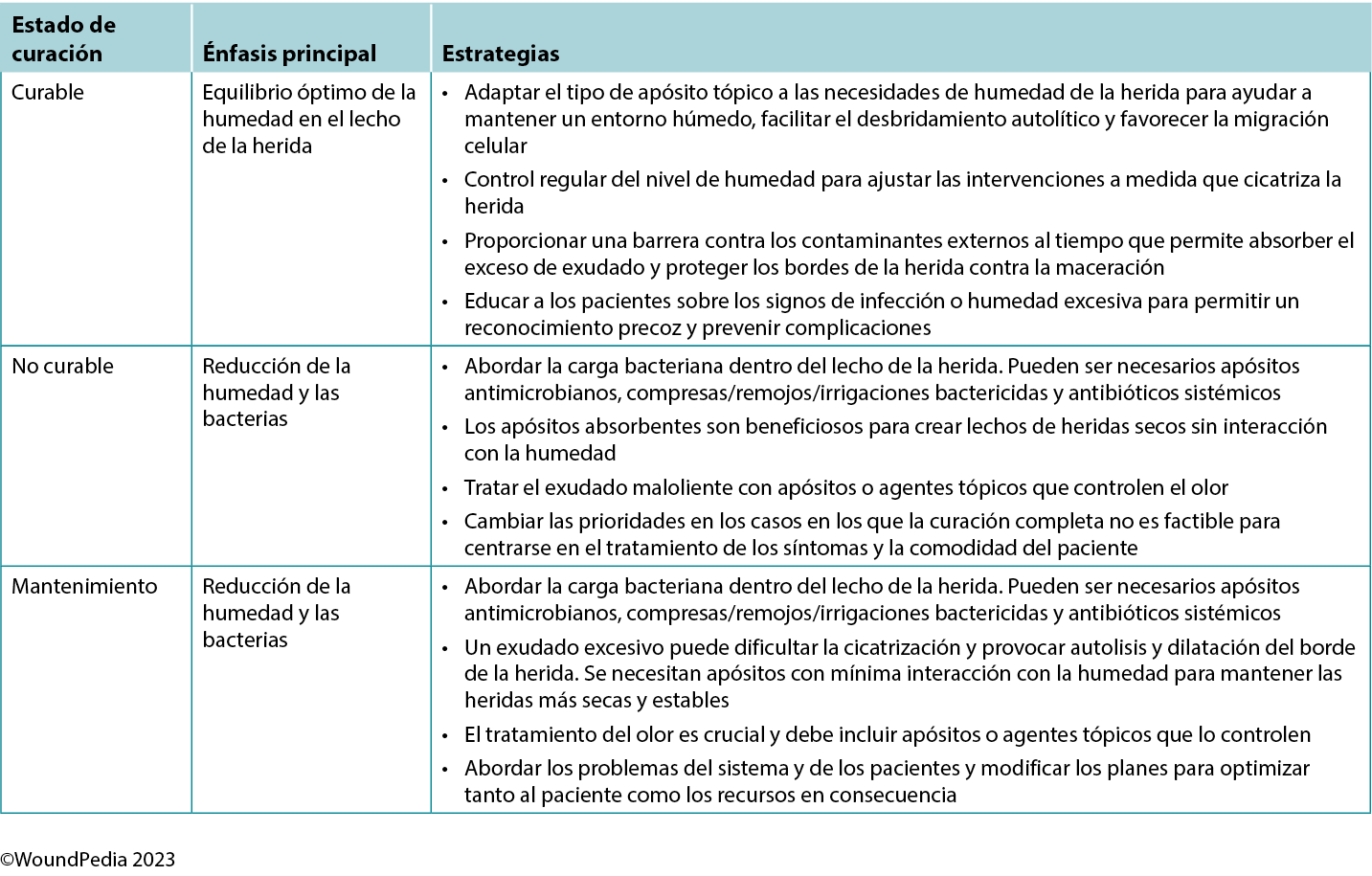
En general, a medida que aumenta el nivel de exudado, también debería hacerlo la capacidad de absorción o transferencia de humedad del apósito.3 Las opciones de apósitos con equilibrio de humedad pueden combinarse con propiedades antibacterianas y antiinflamatorias para satisfacer aún más las necesidades de la herida.
La elección del apósito para el mantenimiento y las heridas no curables debe dar prioridad a la comodidad, evitando al mismo tiempo la donación de líquido al lecho de la herida y la maceración de los bordes de la herida. Estas heridas requieren una reevaluación periódica para detectar cualquier progreso o deterioro y deben tratarse para reducir la carga bacteriana. Dependiendo de la evolución de la herida y de sus características a lo largo del tiempo, puede ser necesario adaptar los apósitos.
Declaración 8: trayectoria de curacion
8A. Considere que las heridas curables deben ser al menos entre un 20% y un 40% más pequeñas en la semana 4 para que cicatricen en la semana 12. Si existen factores que afectan al tiempo de cicatrización (mal control glucémico, por ejemplo), puede ser necesario un tiempo de cicatrización adicional
8B. Asignar tiempo adicional a la cicatrización más allá de las 12 semanas en heridas curables si los recursos disponibles son limitados, y continuar con cuidados constantes
8C. Dar prioridad a la derivación a centros especializados (cuando estén disponibles) para la realización de pruebas diagnósticas y/o una biopsia cutánea, especialmente cuando se enfrenten a graves restricciones de recursos
Las trayectorias de cicatrización de heridas son útiles y necesarias para evaluar el tiempo necesario para la cicatrización, especialmente utilizando datos clínicos (mediciones) tanto para heridas agudas como crónicas. La trayectoria de curación se basa en mediciones precisas y coherentes de la herida que determinan el cierre de la superficie de la herida a lo largo del tiempo. Esto ayuda a distinguir la progresión de la herida, las heridas estancadas y el empeoramiento del estado de la herida.
Las heridas agudas curables deben cerrarse completamente en un plazo de 30 días. Se espera que las heridas crónicas curables tengan un avance del borde de entre el 20% y el 40% a los 30 días (4 semanas) y que se cierren en 12 semanas.3,42,61,62 Las heridas no curables no tienen un tiempo definido asignado para cerrarse, no se espera ningún avance del borde y todas las medidas iniciadas son para prevenir un mayor deterioro. No se espera que las heridas de mantenimiento cicatricen ni se deterioren, y la cicatrización de la herida puede progresar lentamente sin una expectativa de tiempo fija, a menos que se logre la optimización del paciente/institución/sistema.
Reevaluar periódicamente las heridas de difícil cicatrización en busca de diagnósticos alternativos. En estos casos, considere la posibilidad de realizar una biopsia de la herida, una investigación adicional y/o la derivación a un equipo de evaluación interprofesional. Puede evaluarse una trayectoria de curación en las primeras 4 a 8 semanas para predecir si es probable que una herida se cure en la semana 12, siempre que no haya nuevos factores de complicación.63 Los cambios en la herida, el individuo o el entorno pueden hacer necesaria la reclasificación de una herida a la categoría de mantenimiento o no curable.
Declaración 9: avance del borde
9A. Considerar las modalidades activas construidas localmente según el mecanismo de acción requerido y las indicaciones específicas para iniciar una terapia complementaria que favorezca la cicatrización de las heridas
9B. Decidir las terapias complementarias mediante un enfoque de equipo interprofesional e incluir un análisis previo de la relación riesgo-beneficio
Seleccionar terapias complementarias en función de la capacidad de curación. Iniciarlos lo antes posible tras la lesión en personas con traumatismos importantes para prevenir secuelas de larga cronicidad. Seleccionar modalidades utilizando un enfoque de equipo interprofesional basado en lo que está disponible y en el mecanismo físico requerido (garantizando al mismo tiempo la capacidad de curación del tejido traumatizado). En las heridas de difícil cicatrización, la herida puede necesitar una segunda oportunidad para cicatrizar después de una nueva evaluación.42 Asegurarse de que el consentimiento informado forma parte de las decisiones terapéuticas complementarias.
Un análisis de la relación riesgo-beneficio y coste-eficacia es útil y contribuirá a la sostenibilidad del sistema. La clave para tomar decisiones eficaces sobre la modalidad complementaria se basa en el riesgo que supone iniciar la terapia (molestias físicas, dificultades económicas, adherencia del paciente) frente al beneficio que proporcionará (oxigenación tisular, contracción de la herida, reducción del edema, reactivación celular).42,64 Las mejores decisiones sobre la relación riesgo-beneficio se toman en el seno de un equipo interprofesional que incluye al paciente, lo que garantiza el compromiso del grupo y la finalización del tratamiento con un uso óptimo de los recursos.
La optimización de los recursos, o una ligera reasignación de los mismos, puede dar lugar a estrategias creativas en manos de equipos interprofesionales para elaborar soluciones a medida que garanticen que todos los pacientes reciben un tratamiento óptimo a pesar de las restricciones de recursos.
Cirugía. Incluso en los entornos más restringidos, se trata de la modalidad más disponible dentro de una zona de captación médica, a menudo en entornos de atención terciaria con derivaciones recibidas de clínicas de atención primaria para realizar desbridamientos, cirugía general con cierre de intención primaria/terciaria, injertos cutáneos y/o amputaciones.
Los injertos cutáneos pueden estar disponibles en entornos con recursos limitados como modalidad avanzada para lograr el cierre tisular con el fin de reducir los tiempos de cicatrización y prevenir las infecciones recurrentes de las heridas profundas. El procedimiento puede minimizar el uso extensivo de materiales para apósitos durante un periodo prolongado y reducir la carga de trabajo de la atención primaria en heridas crónicas. Las decisiones sobre injertos cutáneos suelen tomarse para preservar la funcionalidad corporal y promover el cierre precoz de la herida por encima de los resultados estéticos.65 Sin embargo, evite los injertos cutáneos en las heridas isquémicas y en la mayoría de las úlceras por estasis venosa; considérelos sólo en las heridas en las que pueda esperarse un resultado favorable.66,67
Estimulación eléctrica. La cicatrización de las heridas puede acelerarse potenciando la corriente eléctrica natural presente en la piel lesionada. En entornos con recursos limitados, esta modalidad debería investigarse para la cicatrización de heridas debido a su base de pruebas de alto nivel y a la disponibilidad de dispositivos de esta naturaleza (corriente continua, corriente alterna, corriente continua de baja intensidad, campos electromagnéticos pulsados, corriente pulsada de alto voltaje y dispositivos de estimulación nerviosa eléctrica transcutánea). Las pruebas apoyan el aumento de la proliferación celular y de la perfusión microcapilar, así como la reducción de la carga bacteriana y de las infecciones en los lechos de las heridas tratadas.68
Terapia de heridas con presión negativa montada en la pared. Este puede ofrecer al profesional sanitario control sobre la gestión del exudado y precisión en la reposición de líquidos para pacientes hospitalizados con gran exudado y grandes defectos tisulares. Comience con la presión más baja posible (menos 50-80 mm Hg). El paciente debe guardar cama para mantener la modalidad, y la capa de base (a menudo gasas o apósitos impregnados de vaselina) debe sustituirse al menos a diario. Esto, junto con comenzar con el ajuste de presión negativa más bajo posible, evitará traumatismos mecánicos en el lecho de la herida por adherencia tisular y la retirada traumática del apósito en los casos en que no se disponga de capas de base no adherentes.69 En la actualidad existen dispositivos desechables de tratamiento de heridas con presión negativa diseñados para su uso en la comunidad, así como opciones de hacerlo uno mismo que pueden ofrecer resultados clínicos aceptables.70,71
Respirar oxígeno de alto flujo y alta concentración. A menudo se pasa por alto que el oxígeno es una modalidad legítima de curación de heridas.72 Irónicamente, rara vez se utiliza, aunque casi todos los entornos sanitarios formales disponen de cantidades abundantes de oxígeno, incluso en entornos con recursos relativamente escasos. La disponibilidad de concentradores de oxígeno también ha aumentado debido a la pandemia de COVID-19, por lo que la administración de oxígeno también es una posibilidad ambulatoria en entornos domiciliarios.73 Aunque la oxigenación hiperbárica es el medio más eficaz para aumentar la concentración plasmática de oxígeno y la administración de oxígeno tisular, esta modalidad no siempre está fácilmente disponible. Sin embargo, la oxigenación normobárica (en sala) produce un aumento de 7,5 veces en el oxígeno plasmático (es decir, de 0,3 ml/dL a 2,3 ml/dL; Tabla 7).74 Además, la inhalación intermitente de oxígeno al 100% en pacientes sin trastorno pulmonar obstructivo crónico (p. ej., 6 horas sí/2 horas no con mascarilla no respiratoria) durante 3 ó 4 días no es perjudicial para los pulmones y puede proporcionar un sustrato de oxígeno adicional significativo, mientras que el aumento y la disminución intermitentes del aporte de oxígeno activan la expresión del factor inducible por hipoxia (un fuerte estímulo para la angiogénesis).75 Esto sugeriría que, en lugar de la oxigenoterapia hiperbárica, el oxígeno normobárico está justificado para mitigar afecciones de la lista de indicaciones aprobadas por la FDA para el oxígeno hiperbárico (Tabla 7).76 Esto puede incluir lesiones por reperfusión tisular (p. ej., lesiones por aplastamiento, síndromes compartimentales antes y después de la liberación quirúrgica); inhibición de toxinas bacterianas (p. ej., mionecrosis infecciosa u otras infecciones anaeróbicas); o defectos de tejidos grandes (después del desbridamiento para mantener la respuesta inflamatoria reactivada durante un máximo de 48 horas). El oxígeno normobárico proporciona el 50% de la Po2 de la oxigenoterapia hiperbárica típica (a 2 atmósferas); sin embargo, muchos de los efectos farmacológicos del oxígeno sólo se consiguen con dosis hiperbáricas.77,78
Tabla 7. Mecanismos y sistemas de administración de oxigenoterapia normobárica
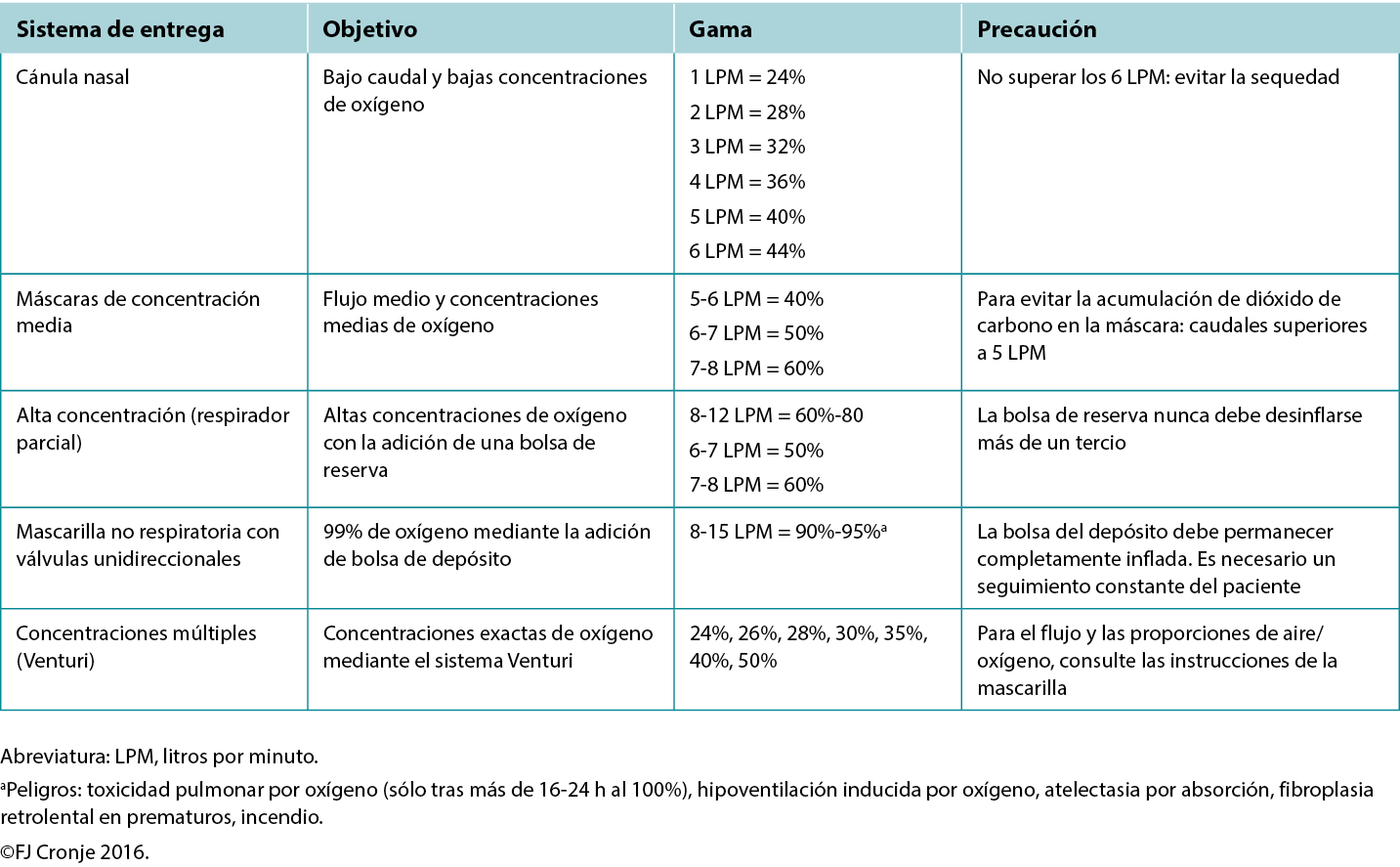
Obsérvese que la administración de oxígeno tópico directamente a una herida no tiene los mismos efectos fisiológicos atribuidos a la administración de oxígeno sistémico.79 Los sistemas de administración de oxígeno tópico siguen siendo objeto de investigación en curso para determinar sus acciones beneficiosas más allá de la mejora de la epitelización y posiblemente un efecto antiséptico leve.64 Este último efecto también se ha atribuido a la ozonoterapia.80 Una revisión sistemática finalizada en 2018 indicó que estas terapias podrían provocar potencialmente un estrés oxidativo leve o desinfección, pero que el riesgo de toxicidad debido a especies reactivas del oxígeno no controladas es elevado.81 En un entorno de recursos limitados, es probable que estos dispositivos y su uso no estén controlados.
Declaración 10: cambio del sistema sanitario
10A. Facilitar una atención basada en pruebas, culturalmente competente y equitativa para todos los pacientes
10B. Mejorar las competencias de los proveedores en el tratamiento de heridas para mejorar los resultados de los pacientes
10C. Establecer una comunicación oportuna y eficaz que incluya al paciente y a todos los miembros del equipo interprofesional de cuidado de heridas para mejorar los resultados del sistema sanitario en relación con las heridas
En todo el mundo, el tratamiento de heridas crónicas consume una parte importante de los recursos sanitarios; la atención preventiva representa la estrategia más rentable para reducir los gastos del sistema sanitario. Existen numerosos enfoques para integrar la atención preventiva en la práctica. Por ejemplo, las DFU son conocidas por provocar altas tasas de amputación y morbilidad en todo el mundo, a pesar de que muchas DFU son evitables. Aunque inicialmente se creía que la diabetes era más prevalente en los países desarrollados, cabe destacar que el 80% de las muertes relacionadas con la diabetes se producen en países con recursos limitados.82 Una herramienta de detección validada, un equipo interprofesional formado y disponible, y la aplicación de algoritmos de prevención pueden utilizarse en países independientemente de la disponibilidad de recursos.83-85 Otras estrategias organizativas que podrían aplicarse son las siguientes.
Navegación del paciente. La gestión de una DFU requiere el apoyo continuo de un círculo asistencial que incluya a familiares y profesionales sanitarios (incluidos los de asistencia domiciliaria y cuidado de heridas) que trabajen en equipo. El acceso oportuno a los servicios sanitarios y sociales suele ser necesario para prevenir y curar las DFU. Los servicios de diabetes regionalizados, integrados en la comunidad y vinculados a clínicas interprofesionales para el cuidado de heridas están demostrando ser los más exitosos.86
Una forma eficaz de garantizar una atención óptima y oportuna es la navegación del paciente. Este concepto es adaptable a todos los sectores sanitarios y puede mejorar el diagnóstico y el tratamiento oportunos de las infecciones de heridas, optimizar el tratamiento del dolor y aumentar el acceso a la atención especializada, acelerando así las tasas de cierre de heridas.87 La navegación del paciente se está convirtiendo en un componente vital de la atención integrada, facilitando una transición fluida entre sectores y unos mejores resultados clínicos. Además, va acompañada de un aumento de la moral tanto del paciente como del profesional sanitario, una disminución de los ingresos o reingresos hospitalarios no agudos, una mejora de la calidad de vida del paciente y un mayor cumplimiento de los protocolos de tratamiento. Todos estos factores combinados generan un importante ahorro de costes para los sistemas sanitarios.87,88
Un elemento crítico para el éxito de los programas de navegación de pacientes es la inclusión de un enfoque exhaustivo y sistemático para guiar a los profesionales sanitarios en la evaluación y prestación de cuidados a cada paciente individual (p. ej., el marco WBP). Estas vías no tienen por qué ser complicadas ni requerir mucho tiempo, pero deben garantizar el cumplimiento de criterios específicos, como el cuidado regular de los pies de las personas con alto riesgo de amputación, el control glucémico hasta una HbA1c inferior al 9% y una PA inferior a 130/90 mm Hg.23,89
Intervenciones políticas. Las políticas organizativas que detallan y orientan sobre las intervenciones y vías de buenas prácticas son cruciales para una aplicación satisfactoria y sostenible de los protocolos de cuidado de heridas. Basar estas políticas en las directrices actuales publicadas para cada tipo específico de herida y trasladarlas al entorno al que deben servir. La institución necesita aceptarlas como normas de práctica y ser aprobadas como tales para que sirvan como atención basada en la evidencia en entornos en los que otras directrices pueden no adoptarse con éxito debido a problemas culturales o de traducción lingüística. Además, estas políticas deben describir claramente el proceso de introducción y utilización de los datos, ya que las iniciativas de mejora continua de la calidad se basan en los datos para mejorar y mantener procesos asistenciales eficaces.
Cuidados adaptados de las heridas. Aunque la prestación de asistencia debe adaptarse a las necesidades propias de cada sector sanitario, algunos conceptos deben ser estándar, sobre todo los que mejoran la comunicación eficaz tanto dentro de los sectores como entre ellos. La creciente adopción de la tecnología digital agiliza las evaluaciones, mejora el acceso a la atención especializada y optimiza la asignación de recursos limitados.90 Cuando las adaptaciones se implementan como procesos de atención, estas prácticas deben estar bien documentadas como normas de atención y ser fácilmente accesibles para garantizar la coherencia y la continuidad de la atención dentro de las respectivas instituciones.
Puntos destacados del consenso delphi
Algunos comentarios importantes del grupo:
- La capacidad de curación es una modalidad cambiante y no debe considerarse una clasificación estática, ya que el estado, las circunstancias y las elecciones del paciente determinan el proceso de asignación de la clasificación (3A).
- El ajuste de la práctica necesario en las heridas de mantenimiento incorpora el establecimiento de un enfoque conservador del lecho de la herida, con atención a las concesiones que el paciente está dispuesto a hacer dentro de sus opciones vitales para garantizar lentamente la optimización del paciente y aumentar posteriormente la competencia del huésped (3B).
- Cuando el método de documentación del paciente se acuerda dentro de una institución, debe utilizarse de manera uniforme para evitar lagunas de comunicación entre los proveedores que puedan causar inadvertidamente un impacto negativo en los resultados de la atención al paciente (4A).
- Los colutorios antisépticos aptos para mucosas suelen ser también adecuados para su uso en el lecho de una herida (4B). Esto puede considerarse un uso no indicado en la etiqueta.
- La elección para el control tópico de la carga bacteriana debe recaer en los antisépticos tópicos (de baja) toxicidad (los cinco más importantes), en función de la capacidad de cicatrización y de las prioridades de carga bacteriana que deban abordarse. Abstenerse de utilizar preparados antibióticos tópicos, pomadas y cremas en las heridas crónicas, ya que dichos preparados suelen centrarse únicamente en los organismos Gram positivos y permitirían que los organismos Gram negativos y anaerobios del lecho de la herida se multiplicaran libremente. Además, los preparados antibióticos tópicos sólo necesitan una mutación para crear resistencia sistémica al organismo objetivo. Los antibióticos tópicos suelen estar en un medio portador que se asocia a dermatitis irritante o alérgica de contacto (6A y 6B).
- Cuando una herida curable tiene una carga de humedad significativa y sigue necesitando apósitos superabsorbentes para controlar el equilibrio de humedad del lecho de la herida, ésta necesita una reevaluación exhaustiva para asegurarse de que se han corregido todas las causas subyacentes (7B).
- Al establecer un equipo interprofesional, hay que utilizar cualquier medio de comunicación para crear y mantener dicho equipo, ya que ello podría optimizar significativamente la capacidad local a pesar de las distancias entre proveedores y especialistas para aumentar los resultados clínicos a pesar de las limitaciones locales (9B).
Conclusiones
Optimizar el cuidado de heridas crónicas en entornos con recursos limitados iniciando pequeñas adaptaciones e intervenciones creativas sin comprometer los principios básicos de los cuidados requeridos. Los equipos interprofesionales de cuidado de heridas pueden servir de recurso virtual a comunidades aisladas y remotas para mejorar los resultados clínicos. Todos los elementos críticos para el tratamiento y el cuidado del pie (diabético) pueden incorporarse fácilmente en entornos diversos aumentando la capacidad local y proporcionando formación clínica y capacitación culturalmente adecuada al paciente.
Perlas de la practica
- El cuidado holístico de las PWD incluye la optimización de los niveles de HbA1c, la PA, los niveles de colesterol y los fármacos con propiedades cardioprotectoras y renales.
- La señal de pulso Doppler de 8 MHz audible a mano es una prueba de cabecera adecuada para el riego sanguíneo arterial de las extremidades inferiores. Puede realizarse como una modificación del ABPI tradicional, y los sonidos del pulso son fácilmente verificables por miembros del equipo de expertos a distancia mediante grabaciones en MP3 o MP4 desde un teléfono móvil.
- Las mnemotecnias NERDS y STONEES pueden orientar el diagnóstico y el tratamiento de la infección local/profunda y circundante, incluida una indicación de antibiótico oral para la osteomielitis.
- La redistribución de la presión plantar puede llevarse a cabo desde alternativas innovadoras y menos costosas, como las plantillas simples de fieltro blando, hasta la escayola de contacto total y el andador de escayola desmontable, que se convierten en inamovibles si estos últimos no están disponibles o no se adaptan a las preferencias del paciente o a sus ADV.
- Los equipos integrados de atención coordinada pueden conectar con la experiencia virtual dotando a los profesionales sanitarios de competencias en navegación del paciente.
- Los kits de herramientas que contienen facilitadores para la práctica junto con Dopplers de 8 MHz y termómetros de infrarrojos pueden facilitar la atención en entornos con recursos limitados.
Conflicto de intereses
Los autores declaran no tener conflictos de intereses.
Financiación
Los autores no recibieron financiación por este estudio.
Author(s)
Hiske Smart*
MA RN PG Dip (UK)
Clinical Nurse Specialist: Wound Specialist Services King Hamad American Mission Hospital, A’Ali, Kingdom of Bahrain
R Gary Sibbald
MD Med FRCPC (Med Derm) FAAD MAPWCA JM
Professor of Medicine and Public Health, Dalla Lana School of Public Health, University of Toronto, Ontario, Canada
Laurie Goodman
MHScN RN Advanced Practice Nurse
WoundPedia, Mississauga, Ontario, Canada
Elizabeth A Ayello
PhD RN CWON ETN MAWPCA FAAN
President, Ayello Harris & Associates, Inc, Copake, New York, USA
Reneeka Jaimangal
MD MDcCH IIWCC
Project Manager, Project ECHO Ontario Skin and Wound Care, WoundPedia, Mississauga, Ontario, Canada
John H Gregory
BEng
President, Opencity Inc, Kitchener, Ontario, Canada
Sadanori Akita
MD PhD
Professor, Fukushima Medical University, Fukuoka, Japan
Afsaneh Alavi
MD FRCPC
Professor of Dermatology, Mayo Clinic, Rochester, Minnesota, USA
David G Armstrong
DPM MD PhD
Professor of Surgery, Keck School of Medicine, University of Southern California, Los Angeles, California, USA
Helen Arputhanathan
MSc RN NSWOC WOCC(C)
Manager, Patient Services & Clinical Wound Care, Home and Community Care Support Services, Hamilton Niagara Haldimand Brant, Waterloo, Ontario, Canada
Febe Bruwer
PhD (UFS) MSocSci MSc
Advanced Nurse Specialist and Unit Manager of the Wound Clinic, Life Roseacres Hospital, Germiston, South Africa
Jeremy Caul
MClSc-WH RN WOCC(c)
Nurse Advisor, Home and Community Care, Ontario Region for Indigenous Services Canada/First Nations and Inuit Health Branch, Ontario, Canada
Beverley Chan
MD MSc,FRCSC
Vascular Surgeon and Division Lead, Halton Healthcare, Oakville, Ontario, Canada
Frans Cronje
MBChB MSc
Aerospace Medicine, PGDOccMed, Fellow EHM (Duke), Aviation and Aerospace Medical Specialist, Head of Department Baromedicine, King Hamad American Mission Hospital, A’ali, Kingdom of Bahrain
Belen Dofitas
MD PhD
Associate Professor, Department of Dermatology, College of Medicine & Philippine General Hospital, University of the Philippines, Manila
Jassin Hamed
MD
Consultant Internal Medicine, COO Global Care Hospital, Abu Dhabi, United Arab Emirates
Catherine Harley
eMBA RN
Chief Executive Officer, Nurses Specialized in Wound, Ostomy and Continence Canada, Ottawa, Ontario, Canada
Jolene Heil
MclSc-WH RN NSWOC
Advanced Practice Nurse and Clinical Nurse Specialist—Wound Care, Providence Care, Kingston, Ontario, Canada
Mary Hill
MN BScN RN NSWOC WOCC(C)
NSWOC Educator/Consultant CAT Team, Integrated Home Care—Calgary Zone, Alberta, Canada
Devon Jahnke
DCh MCISc-WH
Chiropodist, Complex Centre for Diabetes Care, Health Sciences North, Sudbury Outpatient Centre, Ontario, Canada
Dale Kalina
MD MBA FRCPC (ID)
Chief Medical Information Officer, Brant Community Healthcare System, Brantford, Ontario, Canada
Chaitanya Kodange
MBBS DMM DHA MD (Psy) IIWCC-UAE
Consultant Diving, Hyperbaric and Wound Care & Psychiatrist, King Hamad University Hospital, Kingdom of Bahrain
Bharat Kotru
PhD MSc DPM
Podiatrist and Wound Care Specialist, Advance Foot & Wound Care Centre, Amandeep Group of Hospitals, Amritsar, Punjab, India
Laura Lee Kozody
DCh
Chiropodist, Toronto Regional Wound Healing Clinic, Mississauga, Ontario, Canada
Stephan Landis
MD FRCPC
Consultant, Guelph General Hospital Ambulatory Wound Clinic, Guelph, Ontario, Canada
Kimberly LeBlanc
PhD RN NSWOC WOCC(C) FCAN
Academic Chair, Nurses Specializing in Wound, Ostomy and Continence Canada, Ottawa, Ontario, Canada
Mary MacDonald
MD PhD FRCSC
Assistant Professor, School of Medicine, NOSM University, and Vascular Surgeon, Thunder Bay Regional Health Sciences Centre, Thunder Bay, Ontario, Canada
Tobi Mark
BSc DCh
Associate Professor of Chiropody, The Michener Institute of Education at UHN, Toronto, Ontario, Canada
Carlos Martin
DM PG-Dip MBBS
Consultant, Vascular Surgery, Georgetown Public Hospital Corporation, Guyana
Dieter Mayer
MD FAPWCA Consultant, Institute for Advanced Wound Care & Education, Hausen am Albis, Switzerland
Christine Murphy
PhD MClSc-WH RN NSWOC WOCC(C)
Advanced Practice Nurse, The Ottawa Hospital, Ontario, Canada
Harikrishna Nair
MD PhD FRCPI FRCPE FCWCS
Head and Senior Wound Care Physician, Wound Care Unit, Department of Internal Medicine, Kuala Lumpur Hospital, and Professor, Faculty of Medicine, Lincoln University College, Malaysia
Cesar Orellana
MD FRCPC FACP
Infectious Diseases Consultant, Grand River Hospital and St Mary’s General Hospital, Kitchener, Ontario, Canada
Brian Ostrow
MD BSc FRCS(C)
Adjunct Assistant Professor (retired), Department of Surgery, University of Toronto, Ontario, Canada
Douglas Queen
PhD MBA
Chief Executive Officer, Medicalhelplines.com Inc, Toronto, Ontario, Canada
Patrick Rainville
DCh,
Owner, Rainville Foot Health, Timmins, Ontario, Canada
Erin Rajhathy
MclSc-WH RN NSWOC WOCC(C)
Doctoral Student, Swedish Centre for Skin and Wound Research, Nursing Science Unit, School of Health Sciences, Faculty of Medicine and Health, Örebro University, Örebro, Sweden
Gregory Schultz
PhD
Professor Emeritus, University of Florida, Gainesville, Florida, USA
Ranjani Somayaji
MD MPH FRCPC
Associate Professor, University of Calgary, Calgary, Canada
Michael C Stacey
DS MBBS FRACS
Vascular Surgeon and Professor of Surgery, McMaster University, Hamilton, Ontario, Canada
Gulnaz Tariq
MSc (UK) RN PG Dip (PAK)
Director of Wound Care & Education, Global Care Hospital, Abu Dhabi, United Arab Emirates
Gregory Weir
MBChB Mmed (Ch)
Vascular Surgeon, Life Eugene Marais Hospital, Pretoria, South Africa
Catharine Whiteside
MD PhD CM FRCPC
Professor Emerita and Former Dean of Medicine, University of Toronto, Ontario, Canada
Helen Yifter
MD
Associate Professor of Medicine, University of Rwanda, Kigali, Rwanda
Ramesh Zacharias
MD FRCS(C)
Assistant Clinical Professor, Anesthesia, Faculty of Health Sciences, McMaster University, Hamilton, Ontario, Canada
* Corresponding author
References
- Sibbald RG, Williamson D, Orsted HL, et al. Preparing the wound bed—debridement, bacterial balance and moisture balance. Ostomy Wound Manage 2000;46(11):14-35.
- Fitridge R, Chuter V, Mills J, et al. The intersocietal IWGDF, ESVS, SVS guidelines on peripheral artery disease in people with diabetes mellitus and a foot ulcer. J Vasc Surg 2023;78(5):1101-31.
- Sibbald RG, Elliott JA, Persaud-Jaimangal R, et al. Wound Bed Preparation 2021. Adv Skin Wound Care 2021;34(4):183-95.
- Alavi A, Sibbald RG, Nabavizadeh R, Valaei F, Coutts P, Mayer D. Audible handheld Doppler ultrasound determines reliable and inexpensive exclusion of significant peripheral arterial disease. Vascular 2015;23(6):622-9.
- Dworak M, Andraska EA, Gharacholou SM, Myers M, Chapman SC. Fluorescent angiography used as a tool to guide angiosome-directed endovascular therapy for diabetic foot ulcers. J Vasc Surg Cases Innov Tech 2021;7(1):159-63.
- Sassaki VS, Fukaya E. Varicose veins: approach, assessment, and management to the patient with chronic venous disease. Med Clin North Am 2023;107(5):895-909.
- Armstrong DG, Boulton AJM, Sicco AB. Diabetic foot ulcers and their recurrence. N Engl J Med 2017;376(24):2367-75.
- Eikelboom JW, Connolly SJ, Bosch J, et al. Rivaroxaban with or without aspirin in stable cardiovascular disease. N Engl J Med 2017;377(14):1319-30.
- Levin ME. An overview of the diabetic foot: pathogenesis, management and prevention of lesions. Int J Diab Dev Countries 1994;14:39-47.
- Bekele F, Chelkeba L, Fekadu G, Bekele K. Risk factors and outcomes of diabetic foot ulcer among diabetes mellitus patients admitted to Nekemte referral hospital, Western Ethiopia: prospective observational study. Ann Med Surg (Lond) 2020;51:17-23.
- Govindasamy K, Darlong J, Watson SI, Gill P. Prevalence of plantar ulcer and its risk factors in leprosy: a systematic review and meta-analysis. J Foot Ankle Res 2023;16(1):77.
- Sibbald RG, Ayello EA, Alavi A, et al. Screening for the high-risk diabetic foot: a 60-Second Tool. Adv Skin Wound Care 2012;25(10):465-76.
- Sibbald RG, Mufti A, Armstrong DG. Infrared skin thermometry: an underutilized cost-effective tool for routine wound care practice and patient high-risk diabetic foot self-monitoring. Adv Skin Wound Care 2015;28(1):37-44.
- Amemiya A, Noguchi H, Oe M, et al. Factors associated with callus formation in the plantar region through gait measurement in patients with diabetic neuropathy: an observational case-control study. Sensors 2020;20:4863.
- Armstrong DG, Swerdlow MA, Armstrong AA, Conte MS, Padula WV, Bus SA. Five year mortality and direct costs of care for people with diabetic foot complications are comparable to cancer. J Foot Ankle Res 2020;13(1):16.
- Diabetes Canada Clinical Practice Guidelines Expert Committee. Diabetes Canada 2018 clinical practice guidelines for the prevention and management of diabetes in Canada. Can J Diabetes 2018;42(Suppl 1):S1-325.
- Zhang X, Yang X, Sun B, et al. Perspectives of glycemic variability in diabetic neuropathy: a comprehensive review. Commun Biol 2021;4:1366.
- Bril V, Breiner A, Perkins BA, Zochodne D. Diabetes Canada 2018 clinical practice guidelines for the prevention and management of diabetes in Canada. Neuropathy. Can J Diabetes 2018;42:S217-21.
- Soyoye DO, Abiodun OO, Ikem RT, Kolawole BA, Akintomide AO. Diabetes and peripheral artery disease: a review. World J Diabetes 2021;12(6):827-38.
- Song P, Rudan D, Zhu Y, et al. Global, regional, and national prevalence and risk factors for peripheral artery disease in 2015: an updated systematic review and analysis. Lancet Glob Health 2019;7:e1020-30.
- Williams B, Mancia G. Ten commandments of the 2018 ESC/ESH HTN guidelines on hypertension in adults. Eur Heart J 2018;39:3007-8.
- Dagenais GR. Vascular protection: telmisartan in the ONTARGET trial programme. Eur Heart J Suppl 2009;11(suppl_F):F47-53.
- Gerstein HC. Diabetes and the HOPE study: implications for macrovascular and microvascular disease. Int J Clin Pract Suppl 2001;(117):8-12.
- Fonseca-Correa JI, Correa-Rotter R. Sodium-glucose cotransporter 2 inhibitors mechanisms of action: a review. Front Med 2021;8:777861.
- Rasmussen BSB, Yderstraede KB, Carstensen B, et al. Substantial reduction in the number of amputations among patients with diabetes: a cohort study over 16 years. Diabetologia 2016;59:121-9.
- de Mestral C, Hussain MA, Austin PC, et al. Regional health care services and rates of lower extremity amputation related to diabetes and peripheral artery disease: an ecological study. CMAJ Open 2020;8(4):E659-66.
- Baird R, Cosh L, Bruser G, Rowe R, Walker J. Indigenous Diabetes Health Circle: Foot Care Evaluation Program. April 2022. https://idhc.life/wp-content/uploads/2023/02/IDHC_Foot-Care-Research-Report.pdf. Last accessed January 3, 2024.
- Bus SA, Armstrong DG, Crews RT, et al. Guidelines on offloading foot ulcers in persons with diabetes (IWGDF 2023 update). Diabetes Metab Res Rev 2023:e3647.
- Withers RV, Perrin BM, Landorf KB, et al. Offloading effects of a removable cast walker with and without modification for diabetes-related foot ulceration: a plantar pressure study. J Foot Ankle Res 2023;16:27.
- Moffatt CJ, Franks PJ, Hollinworth H. Understanding wound pain and trauma: an international perspective. In: Pain at Wound Dressing Changes: A Position Document. European Wound Management Association; 2002:2-7.
- Queen D, Woo K, Shulz VN, Sibbald RG. Chronic wound pain and palliative cancer care. Ostomy Wound Manage 2003;49(10):16-8.
- Reddy M, Kohr R, Queen D, Keast D, Sibbald RG. Practical treatment of wound pain and trauma: a patient-centered approach. An overview. Ostomy Wound Manage 2003;49(4A):2-15.
- Boonstra AM, Stewart RE, Köke AJ, et al. Cut-off points for mild, moderate, and severe pain on the numeric rating scale for pain in patients with chronic musculoskeletal pain: variability and influence of sex and catastrophizing. Front Psychol 2016;7:1466.
- Byma EA, Wheeler H. The experience of new graduate registered nurses as managers of pain. Pain Manage Nurs 2021;22(3):429-35.
- D’Souza RS, Barman R, Joseph A, Abd-Elsayed A. Evidence-based treatment of painful diabetic neuropathy: a systematic review. Curr Pain Headache Rep 2022;26(8):583-94.
- Sibbald RG, Hastings-Truelove A, DeJong P, Ayello EA. Reconciliation and diversity for educators: the medicine wheel, Bloom’s taxonomy, and CanMEDS competencies. Adv Skin Wound Care 2023;36(2):64-6.
- Murphy A, McGowan C, McKee M, et al. Coping with healthcare costs for chronic illness in low-income and middle-income countries: a systematic literature review. BMJ Global Health 2019;4:e001475.
- Okediji PT, Ojo AO, Ojo AI, Ojo AS, Ojo OE, Abioye-Kuteyi EA. The economic impacts of chronic illness on households of patients in Ile-Ife, South-western Nigeria. Cureus 2017;9(10):e1756.
- Adelman RD, Tmanova LL, Delgado D, Dion S, Lachs MS. Caregiver burden: a clinical review. JAMA 2014;311(10):1052-60.
- Kodange C. Screening for depression in patients with chronic wounds. Adv Skin Wound Care 2021;34(9):502-3.
- Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care 2022;45(11):2753-86.
- Boersema GC, Smart H, Giaquinto-Cilliers MGC, et al. Management of nonhealable and maintenance wounds: a systematic integrative review and referral pathway. Adv Skin Wound Care 2021;34(1):11-22.
- Ebbers T, Kool RB, Smeele LE, et al. The impact of structured and standardized documentation on documentation quality; a multicenter, retrospective study. J Med Syst 2022;46(7):46.
- Onuh OC, Brydges HT, Nasr H, Savage E, Gorenstein S, Chiu E. Capturing essentials in wound photography past, present, and future: a proposed algorithm for standardization. Adv Skin Wound Care 2022;35:483-92.
- World Health Organization. International Statistical Classification of Diseases and Related Health Problems (ICD). 2023. www.who.int/standards/classifications/classification-of-diseases. Last accessed January 3, 2024.
- Wurster F, Fütterer G, Beckmann M, et al. The analyzation of change in documentation due to the introduction of electronic patient records in hospitals—a systematic review. J Med Syst 2022;46(8):54.
- Nair HK, Ahmad NW, Ismail AA, et al. Maggot debridement therapy to treat hard-to-heal diabetic foot ulcers: a single-centre study. J Wound Care 2021;30(Sup12):S30-6.
- Williams KA, Cronje FJ, Avenant L, Villet MH. Identifying flies used for maggot debridement therapy. S Afr Med J 2008;98(3):196-9.
- Tran DL, Huang RW, Chiu ES, et al. Debridement: technical considerations and treatment options for the interprofessional team. Adv Skin Wound Care 2023;36(4):180-7.
- Woo KY, Sibbald RG. A cross-sectional validation study of using NERDS and STONEES to assess bacterial burden. Ostomy Wound Manage 2009;55(8):40.
- Angel DE, Lloyd P, Carville K, Santamaria N. The clinical efficacy of two semi‐quantitative wound‐swabbing techniques in identifying the causative organism(s) in infected cutaneous wounds. Int Wound J 2011;8(2):176-85.
- Rawlinson S, Ciric L, Cloutman-Green E. How to carry out microbiological sampling of healthcare environment surfaces? A review of current evidence. J Hosp Infect 2019;103(4):363-74.
- Hatzenbuehler J, Pulling TJ. Diagnosis and management of osteomyelitis. Am Fam Physician 2011;84(9):1027-33.
- Sibbald RG, Elliott JA, Ayello EA, Somayaji R. Optimizing the moisture management tightrope with Wound Bed Preparation 2015©. Adv Skin Wound Care 2015;28(10):466-76.
- Joshi N, Caputo GM, Weitekamp MR, Karchmer AW. Infections in patients with diabetes mellitus. N Engl J Med 1999;341(25):1906-12.
- McLain NE, Moore ZE, Avsar P. Wound cleansing for treating venous leg ulcers. Cochrane Database Syst Rev 2021;3(3):CD011675.
- Sibbald RG, Goodman L, Woo KY, et al. Special considerations in Wound Bed Preparation 2011: an update©. Adv Skin Wound Care 2011;24(9): 415-36.
- Block MS, Rowan BG. Hypochlorous acid: a review. J Oral Maxillofacial Surg 2020;78(9):1461-6.
- International Wound Infection Institute. Wound infection in clinical practice: principles of best practice. 3rd ed. Wounds Int 2022:1-60.
- Giaquinto-Cilliers MGC. Classification of dressings: a framework adapted to the Wound Bed Preparation Paradigm. Wound Heal South Afr 2023;16(2):31-3.
- Berezo M, Budman J, Deutscher D, Hess CT, Smith K, Hayes D. Predicting chronic wound healing time using machine learning. Adv Wound Care 2022;11(6):281-96.
- Pavlovčič U, Diaci J, Možina J, et al. Wound perimeter, area, and volume measurement based on laser 3D and color acquisition. Biomed Eng Online 2015;14(39).
- Laporte M, Keller HH, Payette H, et al. Validity and reliability of the new Canadian Nutrition Screening Tool in the ‘real-world’ hospital setting. Eur J Clin Nutr 2015;69(5):558-64.
- Feldmeier JJ, Hopf HW, Warriner R3, Fife CE, Gesell LB, Bennett M. UHMS position statement: topical oxygen for chronic wounds. Undersea Hyperb Med 2005;32(3):157-68.
- Guzman KJ, Gemo N, Martins DB, et al. Current challenges of plastic surgical care in sub-Saharan Africa (Maputo, Mozambique). Plast Reconstr Surg Glob Open 2018;6(8):e1893.
- Jones JE, Nelson EA. Skin grafting for venous leg ulcers. Cochrane Database Syst Rev 2007;(2):CD001737.
- Kirketerp-Møller K, Doerfler P, Schoefmann N, et al. Biomarkers of skin graft healing in venous leg ulcers. Acta Derm Venereol 2022;102:adv00749.
- Thakral G, Lafontaine J, Najafi B, Talal TK, Kim P, Lavery LA. Electrical stimulation to accelerate wound healing. Diabetes Foot Ankle 2013;4.
- Chaput B, Garrido I, Eburdery H, Grolleau JL, Chavoin JP. Low-cost negative-pressure wound therapy using wall vacuum: a 15 dollars by day alternative. Plast Reconstr Surg Glob Open 2015;3(6):e418.
- Estillore KM, Quevedo GL, Bonifacio LR. Improvised suction apparatus for closure of large soft tissue deficit. Malaysian Orthop J 2013;7(2):29.
- Farré R, Rodríguez-Lázaro MA, Gonzalez-Martin J, et al. Device for negative pressure wound therapy in low-resource regions: open-source description and bench test evaluation. J Clin Med 2022;11(18):5417.
- Rose S, Sardar S, Sasi S, Al Mohanadi DH, Al-Mohammed AA, Zahid M. Time for change in practice of in-patient oxygen therapy: a period-limited, multidimensional approach to improve oxygen prescription compliance: quality improvement project at Hamad General Hospital, Qatar. BMJ Open Qual 2021;10(4):e001574.
- McAllister S, Thorn L, Boladuadua S, et al. Cost analysis and critical success factors of the use of oxygen concentrators versus cylinders in sub-divisional hospitals in Fiji. BMC Health Serv Res 2021;21(1):1-7.
- Jain KK. Physical, physiological, and biochemical aspects of hyperbaric oxygenation. In: Jain KK, ed. Textbook of Hyperbaric Medicine. 6th ed. Springer; 2017:11-22.
- Chang AJ, Bargmann CI. Hypoxia and the HIF-1 transcriptional pathway reorganize a neuronal circuit for oxygen-dependent behavior in Caenorhabditis elegans. Proc Natl Acad Sci USA 2008;105(20):7321-6.
- Moon RE. Hyperbaric Oxygen Therapy Indications. North Palm Beach, FL: Best Publishing Company; 2019.
- Chazalviel L, Blatteau JE, Vallée N, Risso JJ, Besnard S, Abraini JH. Effects of normobaric versus hyperbaric oxygen on cell injury induced by oxygen and glucose deprivation in acute brain slices. Med Gas Res 2016;6(3):169-73.
- Velej V, Cankar K, Vidmar J. The effects of normobaric and hyperbaric oxygenation on MRI signal intensities in T1 -weighted, T2 -weighted and FLAIR images in human brain. Radiol Oncol 2023;57(3):317-24.
- UHMS position statement: topical oxygen for chronic wounds. Undersea Hyperb Med 2018;45(3):379-80.
- Rapone B, Ferrara E, Santacroce L, et al. The gaseous ozone therapy as a promising antiseptic adjuvant of periodontal treatment: a randomized controlled clinical trial. Int J Environ Res Public Health 2022;19(2):985.
- Fitzpatrick E, Holland OJ, Vanderlelie JJ. Ozone therapy for the treatment of chronic wounds: a systematic review. Int Wound J 2018;15(4):633-44.
- Woodbury M, Sibbald RG, Ostrow B, Persaud R, Lowe J. Tool for rapid & easy identification of high-risk diabetic foot: validation & clinical pilot of the simplified 60 second diabetic foot screening tool. PLoS One 2015;10(6):1-3.
- Abbas ZG, Lutale JK, Bakker K, Baker N, Archibald LK. The ‘step by step’ diabetic foot project in Tanzania: a model for improving patient outcomes in less-developed countries. Int Wound J 2011;8:169-75.
- Abbas ZG. Reducing diabetic limb amputations in developing countries. Expert Rev Endocrinol Metab 2015;10:425-34.
- Ousey K, Chadwick P, Jawien A, et al. Identifying and treating foot ulcers in patients with diabetes: saving feet, legs and lives. J Wound Care 2018;27(5 Suppl 5b).
- Heerschap C, Nicholas A, Whitehead M. Wound management: investigating the interprofessional decision-making process. Int Wound J 2019;16(1):233-42.
- Arputhanathan H, Hyde J, Atiloa T, Queen D, Elliott J, Sibbald RG. A patient navigation model to improve complex wound care outcomes. Adv Skin Wound Care 2022;35(9):499-508.
- Doucet S, Luke A, Anthonisen G, et al. Hospital-based patient navigation programmes for patients who experience injury-related trauma and their caregivers: a scoping review protocol. BMJ Open 2022;12:e055750.
- Narayan KMV, Zhang P, Kanaya AM, et al. Diabetes: the pandemic and potential solutions. In: Jamison DT, Breman JG, Measham AR, et al, eds. Disease Control Priorities in Developing Countries. 2nd ed. Washington, DC: World Bank; 2006:591-603.
- Kostovich CT, Etinggen B, Wirth M, et al. Outcomes of telehealth for wound care: a scoping review. Adv Skin Wound Care 2022;35(7):394-403.
Supplemental Table 1. Delphi consensus achieved among 41 contributors on 32 wound bed preparation (wbp) 2024 statements
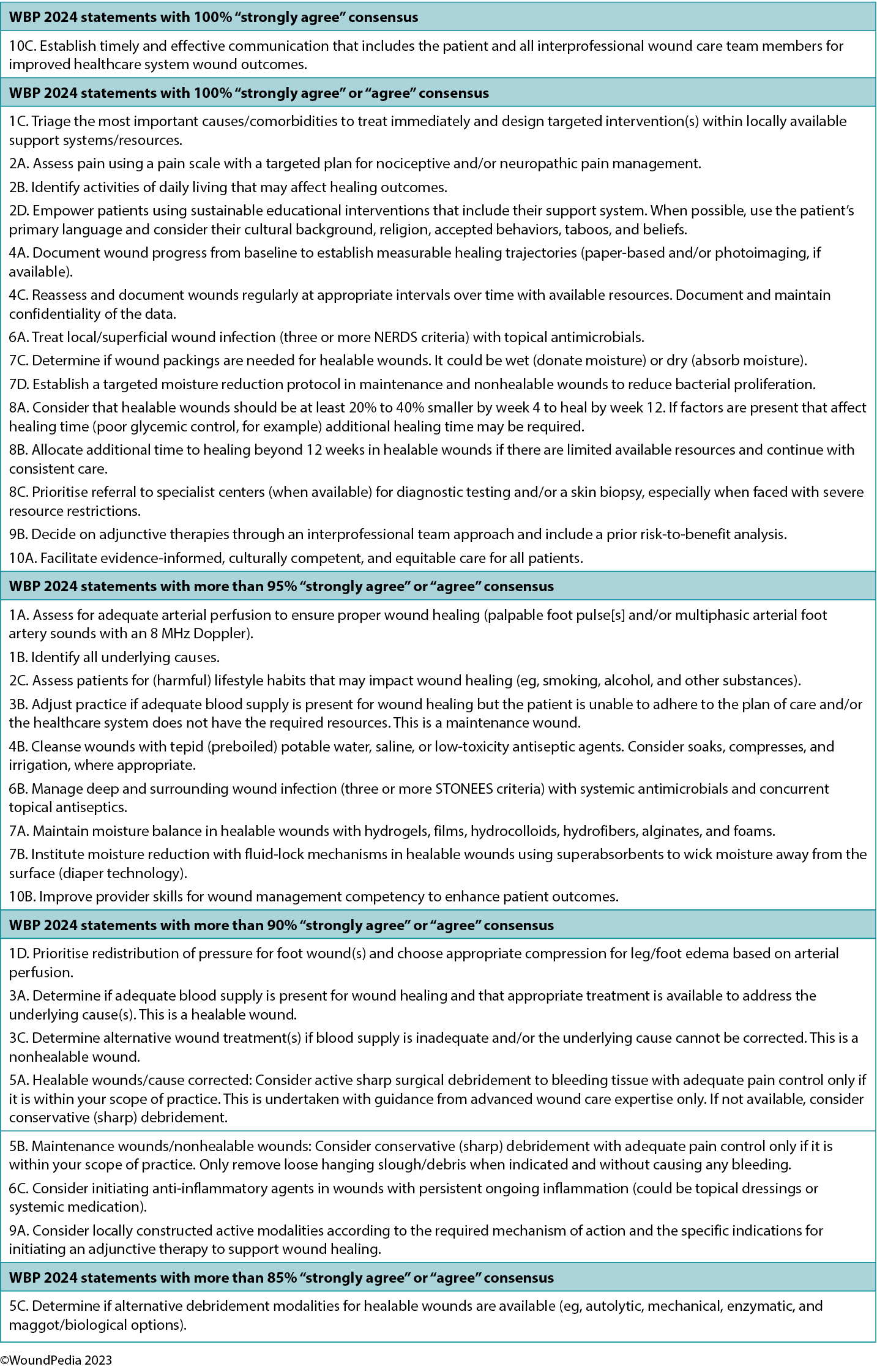
Supplement Table 2. Common antiseptic agents for nonhealable wounds
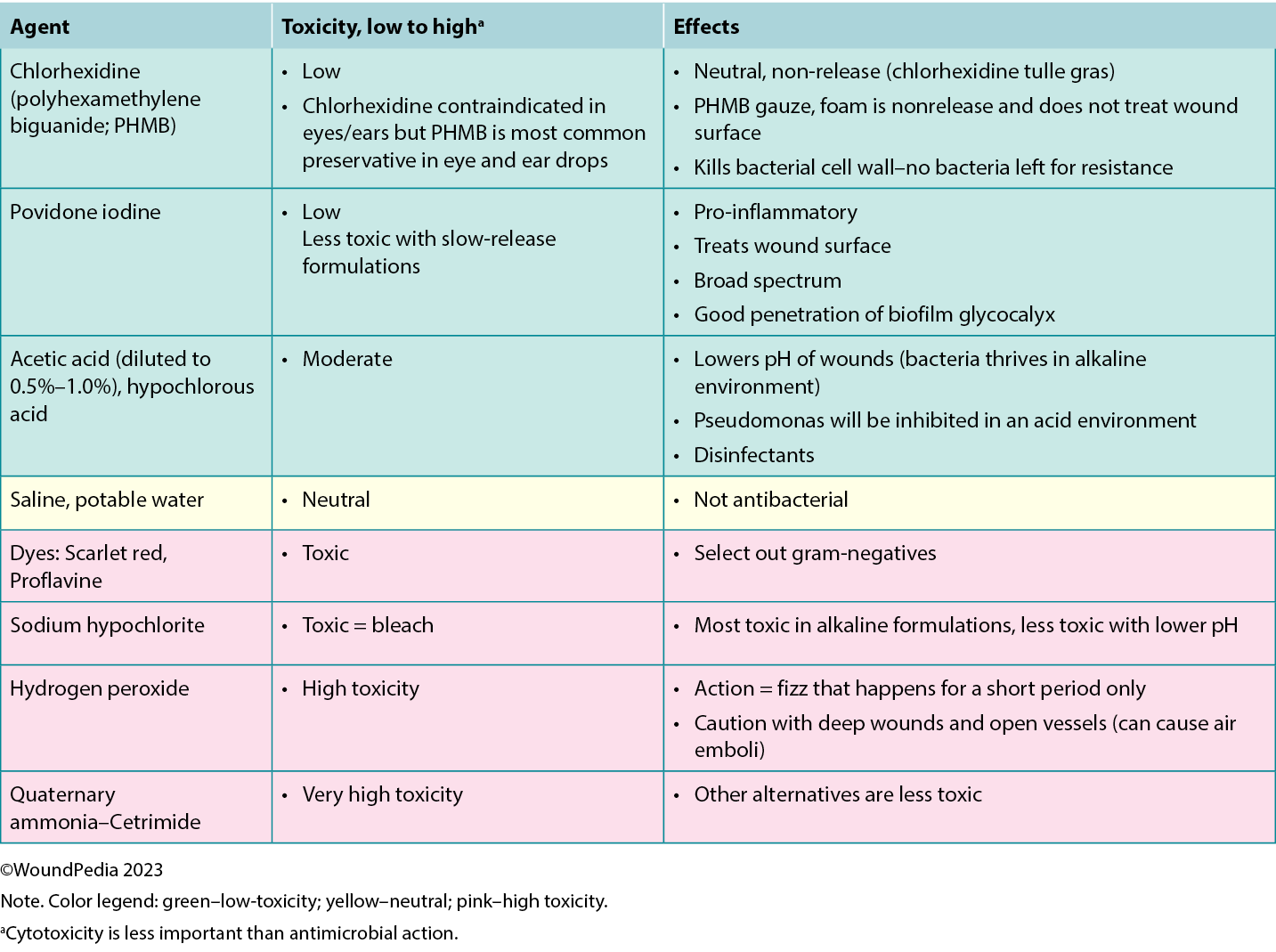
Tabla suplementaria 1. Consenso Delphi alcanzado entre 41 colaboradores sobre 32 declaraciones relativas a la preparación del lecho de la herida (WBP) 2024

Tabla suplementaria 2. Agentes antisépticos comunes para heridas no curables