Volume 43 Number 2
Healing peristomal wounds around retracted stomas with negative-pressure wound therapy: a case series
Jarosław Cwaliński, Jacek Hermann, Tomasz Banasiewicz
Keywords ostomy, Wound care, Negative-pressure wound therapy, hydrofiber dressing, peristomal infection, peristomal leak, retraction
For referencing Cwaliński J, Hermann J & Banasiewicz T. Healing peristomal wounds around retracted stomas with negative-pressure wound therapy: a case series. WCET® Journal 2023;43(2):29-34
DOI
https://doi.org/10.33235/wcet.43.2.29-34
Submitted 16 February 2022
Accepted 29 April 2022
Abstract
One method for treating a retracted stoma is a vacuum dressing that cleans the wound and protects against intestinal leakage. This case series describes the use of an integrated, single-use negative-pressure wound therapy (NPWT) dressing to treat retracted stomas as an alternative to other noninvasive remedies. The report includes seven patients who were hospitalized in the authors’ surgical department from 2019 to 2020. All patients developed severe peristomal infection that failed to respond to local treatment with proper ostomy appliances or specialist dressings. After cleaning each wound and removing necrotic lesions, the authors applied a single-use hydrofiber NPWT dressing to each patient. The dressing was changed every 2 to 5 days, depending on the effects of the therapy. The stoma orifice was covered with a bag with two-piece ostomy systems. The peristomal wound healed in all cases and leakage was eliminated. The mean time of treatment was 14 days (range, 10-21 days), and the vacuum dressings were changed an average of four times (range, 3-7). None of the patients required a stoma translocation or other additional surgery. Three patients received systemic IV antibiotic therapy to treat general infection. Single-use NPWT dressings protect peristomal wounds from bowel leakage and do not hinder the application of stoma bags. This system, similar to standard NPWT devices, effectively protects infected stomas from retraction.
Introduction
An ostomy is a communication between the lumen of a bowel loop and the abdominal wall; stoma creation is one of the most basic procedures of colorectal surgery. It is performed on the large or small bowel to treat malignant, inflammatory, or vascular diseases and following bowel injuries. Colorectal cancer is the most common indication, comprising up to 75% of cases.1,2 Ostomies are performed for almost 100,000 patients per year in the US, and the procedure reduces major morbidity and mortality.3
However, there is a relatively high rate of ostomy-related morbidity. The early complications, such as peristomal infection, skin irritation, ischemia, and retraction continue to challenge surgeons.2 Ostomy retraction causes continuous leakage of bowel contents into the subcutaneous tissue; this can be followed by severe necrosis and infection of the tissues surrounding the ostomy, with ostomy detachment occurring in some cases.4,5 Although most of the aforementioned complications are treated with proper ostomy appliances and specialist dressings, severe complications can require advanced modalities such as negative-pressure wound therapy (NPWT), which offers effective, continuous evacuation of infectious effusion and pus. However, although ostomy salvage using standard NPWT devices has been described, to the authors’ knowledge there are no extant reports about single-use NPWT systems. Accordingly, this case series described the treatment of peristomal wounds and stoma retraction prevention with integrated single-use vacuum dressings.
Methods
A preliminary and prospective study was carried out from 2019 to 2020 on a group of seven patients with early retracted ostomy and peristomal wounds. The series included four men and three women whose characteristics are presented in Table 1.
Table 1. Patient characteristics (N = 7)
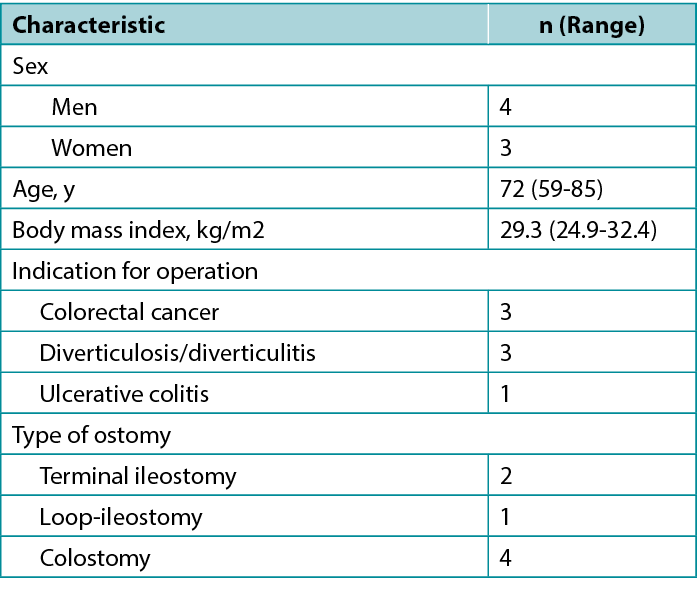
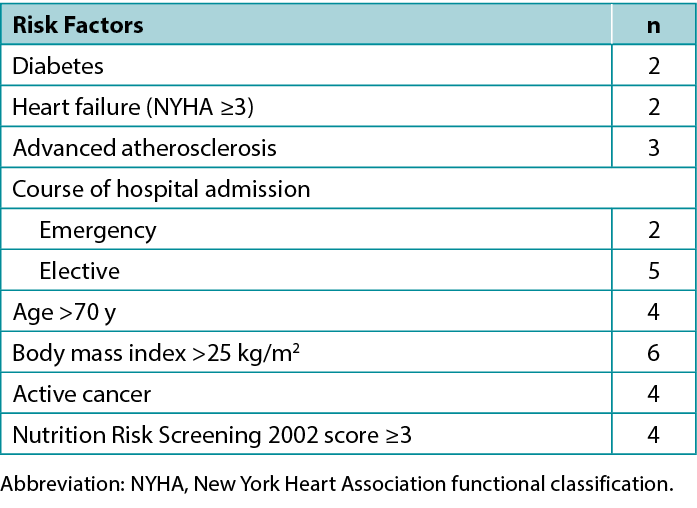
All of the patients had a moderate or severe peristomal infection that failed to respond to local treatment with proper ostomy appliances and specialist dressings. In addition, preoperative risk factors for healing dysfunction were observed in the study group, including emergency surgery, malnutrition, steroid use, active inflammatory bowel disease, and other comorbidities (Table 2). All patients received oral immunomodulatory nutrition beginning the second day after surgery, and four of the patients were also fed intravenously during the four postoperative days. Further, three patients required systemic antibiotic therapy due to septic complications.
Table 2. Preoperative risk factors for surgical site infection
Ethics and Consent
Negative-pressure wound therapy is widely approved for medical therapy and the aim of the study was to adapt this method to the treatment of stoma-related complications. Therefore, the ethics committee of the author’s institution concluded that there was no need to issue a separate consent for this study. However, due to this atypical application of single-use NPWT, the authors obtained informed consent for the therapy from each patient, as well as written approval to publish images and case details.
Surgical Technique
First, the authors debrided the infected wound surrounding the retracted ostomy and, if necessary, placed a drain derived from a separate cut given any persistent leakage of the bowel contents into the surgical site (Figure 1). Next, they washed the wound and surrounding skin with disinfectant and applied a carboxymethylated cellulose fiber dressing measuring 15 × 10 cm or 10 × 10 cm (Avelle NPWT System, ConvaTec; or PICO NPWT System, Smith & Nephew; Figure 2). A hole was cut in the dressing to fit the ostomy as well as the wound. The adherence and tightness of the dressings were enhanced with adhesive foil strips placed on the margins (Figure 2). In the next step, a hydrocolloid stoma paste was applied to increase adhesion of the ostomy bag or plate edges (Figure 3). The stoma paste also used to improve the system seal and create a barrier between the stoma contents and the hydrofiber filling of the NPWT dressing. In addition, deep peristomal wound recesses with residual necrosis were filled with silver alginate dressing or silicone open-weave gauze (Figure 4).
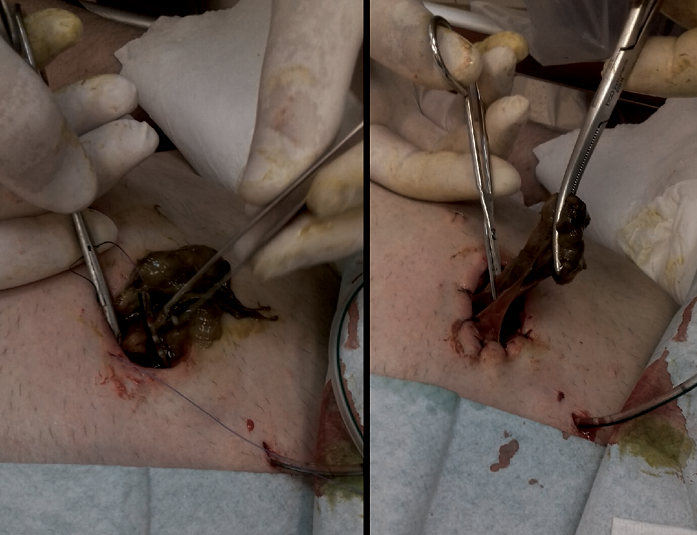
Figure 1. Stabilization of retracted ostomy with necrectomy and bowel-to-skin sutures
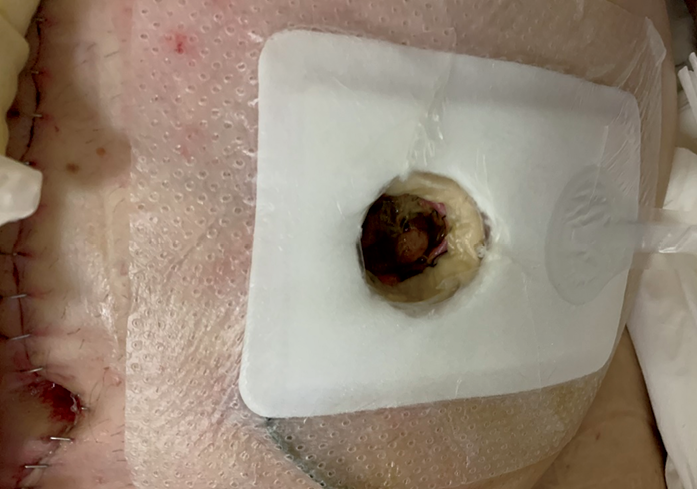
Figure 2. Peristomal wound after single-use negative pressure wound therapy dressing application

Figure 3. Ostomy bag application during the treatment of a retracted stoma with a negative-pressure wound therapy dressing
Stoma paste fills the space between the edge of the tissues and the dressing (left) ensuring better adhesion of the pouch and protecting against leakage (right)
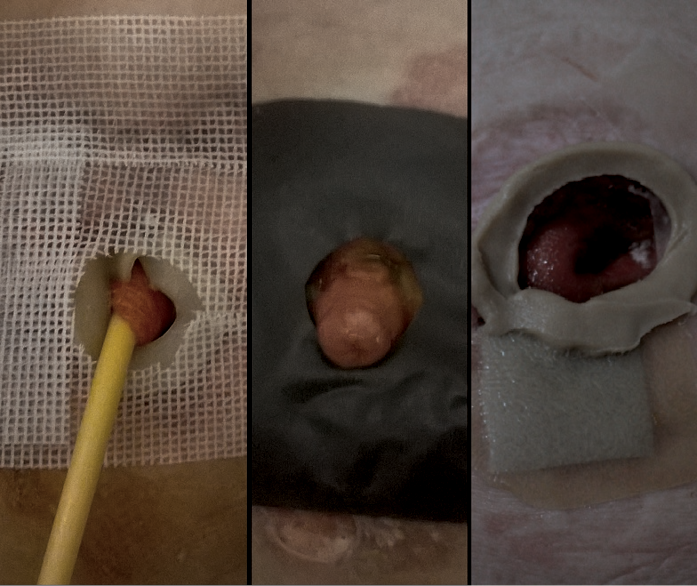
Figure 4.Peristomal wound with silver alginate dressing or silicone open-weave gauze
Finally, the port of a negative-pressure generator was attached to the dressing and a stable negative pressure of 80 mm Hg was maintained during the therapy. At each dressing change, any bowel leakage into the wound was controlled and eliminated as needed (Figure 5). The dressings were changed at the beginning of every second day with the use of a one-piece stoma bag. Subsequently, dressings were left in place for 3 to 5 days using two-piece ostomy systems (Figure 6). A summary diagram of the procedure is presented in the Table 3.
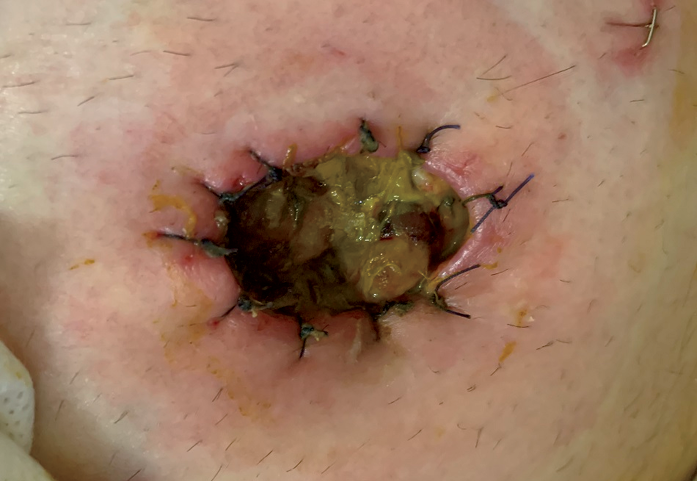
Figure 5. Ostomy on day 4 of treatment after second change of vacuum drainage with no bowel contents leakage
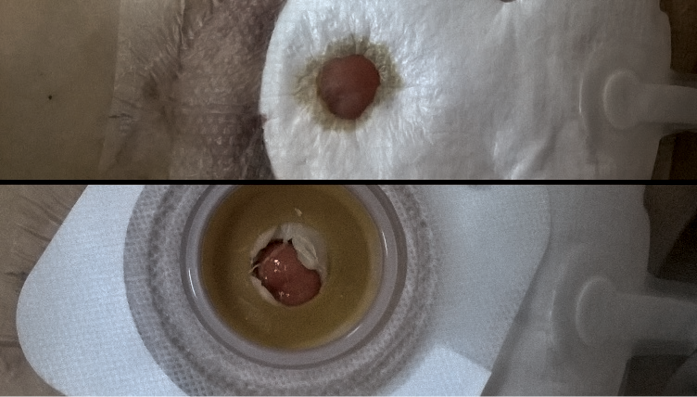
Figure 6. One-piece bag applied to ostomy
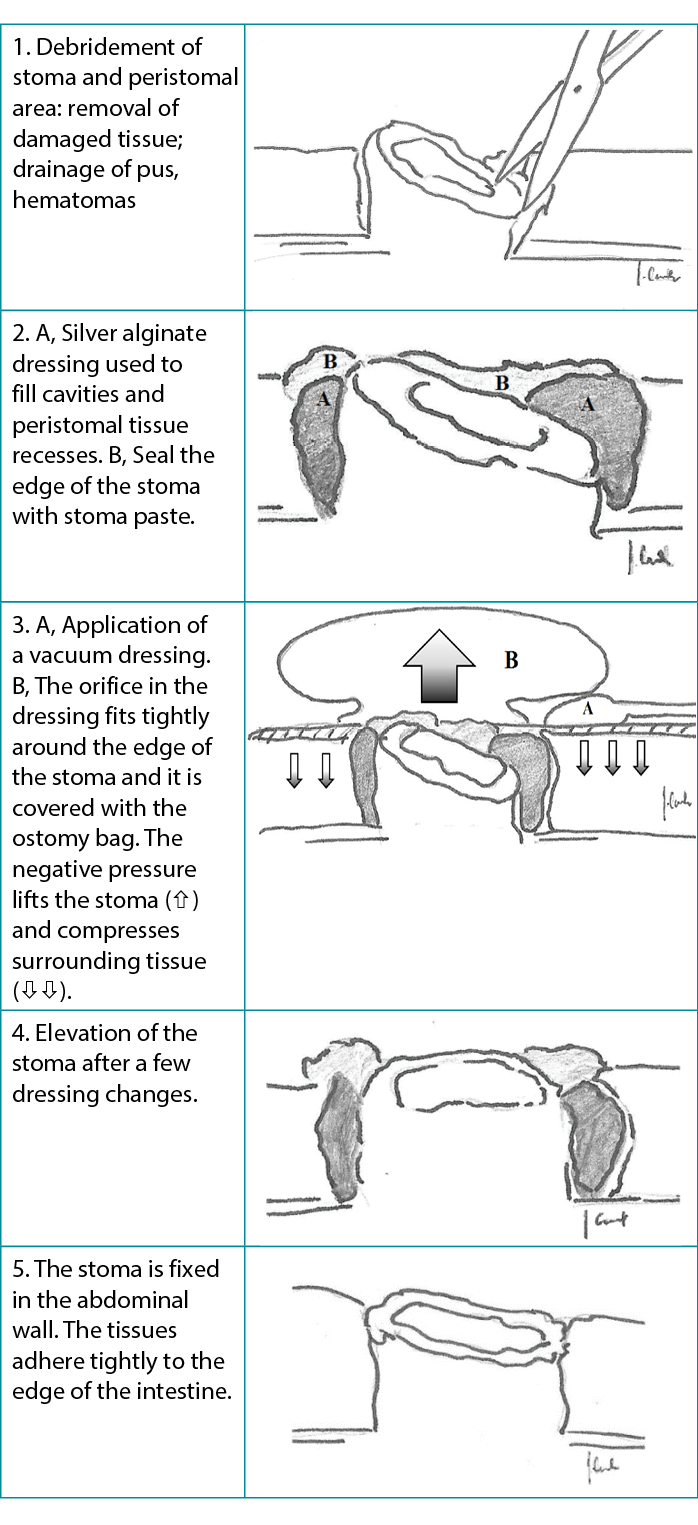
Table 3. Stoma healing: single-use negative-pressure wound therapy dressing removes necrotic tissue and prevents stoma erosion
Results
Patients’ deep, infected peristomal wounds healed and the ostomies were retained in their primary locations. None of the patients required secondary operations. The mean time of treatment was 14 days (range, 10-21 days), and the NPWT was changed an average of four times (range, 3-7). Figure 7 shows a representative treatment effect after four dressing changes. Regular ostomy appliances were used in six patients with terminal ostomy; additional sealing rings were necessary in one patient with loop ostomy. Two patients, one with colostomy and one with ileostomy, received appropriate systemic antibiotic therapy because of elevated inflammatory markers in the serum.
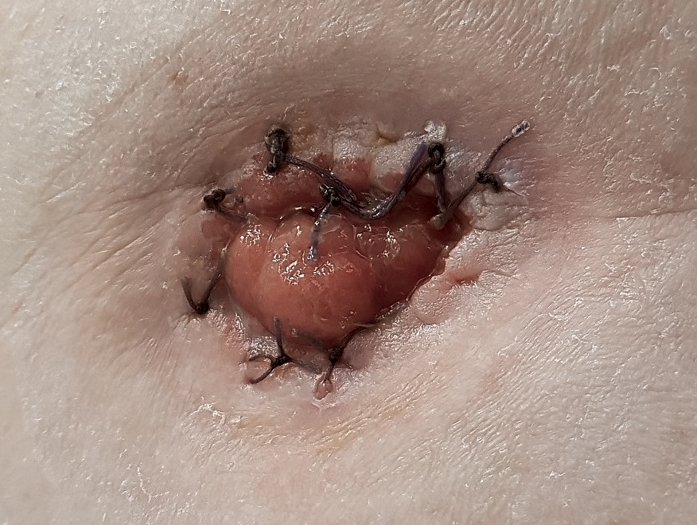
Figure 7. Effect on day 10 of treatment and after four dressing changes
Discussion
The incidence of overall stoma-related complications is reported to be between 10% and 70%.6,7 Hematoma formation, bleeding, ostomy edema, skin irritation with erosion or ulceration, ischemia with necrosis, and early ostomy retraction are the most common complications to occur within 30 days of any procedure, with frequencies ranging from 25% to 34%.1 Although most of these complications resolve spontaneously within a few days or require only conservative medical treatment, patients who develop major complications such as ischemia with necrosis or ostomy retraction usually require secondary surgery because of the threat of severe infection and gastrointestinal tract dysfunction.1,8 Proper surgical technique—displacing the bowel with no tension to the skin surface and suturing it to the pre-planned place—is the most effective way to prevent patients from experiencing complications.
Before elective procedures, a stoma nurse should prepare the location of the stoma, assessing the location of skin folds and scars and considering the patient’s lifestyle and occupation. Typically, the stoma site is designated in standing, lying, and sitting positions. The stoma nurse should also mark an alternative site in case of intraoperative difficulties.9
According to the surgical technique, the stoma should be positioned through the rectus abdominis muscle leaving sufficient gut margin above the skin surface. For an end ostomy, it should be 5 cm for the small intestine and 2 cm for the colon, which allows the stoma to contract to about 2 cm and 0.5 cm after a few months.10 Lack of proper pre-operative preparation may occur in emergency operations, where the rate of morbidity is increasing.11,12
A refractory ostomy may be cause for reoperation, which, in some cases, then increases the risk of additional complications. Avoiding reoperation is extremely important for some patient populations in particular, such as those with cachexia and/or cancer, for whom surgical site infections or other complications may prolong the length of stay and affect chemotherapy. In addition, avoiding reoperation enables the patient to maintain oral nutrition which improves nutrient absorption and the condition of the gut microbiome.12,13
Preventing the continuous leakage of bowel contents into peristomal subcutaneous tissue and enabling the unhindered outflow of bowel contents through the ostomy are the basic therapeutic targets in cases with ostomy complications.11,14 Those targets are met initially with modified stoma appliances in the form of rings, washers, and feet with a concave profile, the aims of which are shape adaptation and leveling the height of the ostomy.15 Vacuum-assisted therapy is recommended as an effective method to treat patients with severely retracted ostomy. Vacuum-assisted dressings consist of a polyurethane foam covered with adhesive foil. A stationary or portable electrical suction pump is attached to the dressing and a stable negative pressure of 50 to 200 mm Hg is maintained during therapy. The objectives of vacuum treatment are to remove tissue exudate, divert bowel contents, reduce edema, and improve blood supply.16,17 The polyurethane foam also removes devitalized and infected tissues and improves lymphatic drainage. Thus, after a few dressing changes, the wound contracts and it is covered with fresh granulation tissue.16,18 The antibacterial mode of action, mostly against Gram-negative bacteria, relies on direct elimination of bacterial cells, followed by local regulation of pharmacodynamic and pharmacokinetic conditions, the effect of which is better antibiotic tissue penetration.19,20
Proper application of vacuum dressings on peristomal wounds with a retracted bowel remnant is challenging because bowel contents can be suctioned into a stoma bag through badly adherent layers of the dressing. It is a priority to isolate the stoma from the wound without secondary tissue damage caused by the vacuum dressing. Therefore, it is absolutely necessary to place an insulating layer between the intestine and the polyurethane foam and use an under pressure between 75 mm Hg and 125 mm Hg.21,22 Close vicinity of the suction port and stoma bag is another drawback of the application. Finally, a patient’s daily life activities may be limited by needing to carry a stationary or portable negative pressure electrical suction pump.23,24 Another important issue remains the long-term outpatient and home-based care with properly selected equipment and qualified personnel. Nurses caring for wounds can successfully carry out vacuum therapy after a few weeks of practical training.25
Applying single-use NPWT dressings can help avoid the aforementioned obstacles. Because single-use NPWT dressings are much thinner than regular polyurethane foam and all the layers (separating, absorbent, and insulating) are integrated into one pack, the dressing thoroughly fills the wound and properly adheres to the ostomy margins. Moreover, this type of vacuum therapy may be left in the wound for up to 7 days, on the condition that it retains its full capacity to absorb exudates. Typically, a portable pump included in the set generates a stable pressure of approximately 80 mm Hg as the surface of a wound decreases and the retracted ostomy is elevated.27,28 Because this system is lightweight, has a silent pump, and requires simple battery changes, it is accepted by patients in both ambulatory settings and at home. In the authors’ experience, telemedicine (eg, iWound; Polmedi) improves the safety of NPWT use in patients’ continued treatment at home.
Conclusions
The use of single-use NPWT dressings combined with properly balanced nutrition and antibiotic therapy is an effective method of treatment for patients with early stoma complications. Single-use NPWT systems are “skin-friendly,” because they do not damage the skin surrounding the ostomy and simultaneously heal the area affected by inflammation or infection. They are inexpensive and easy to use, even in home settings. The authors recommend this treatment method for the management of an early phase retracted ostomy with concomitant peristomal infection.
Conflict of Interest
The authors declare no conflicts of interest.
Funding
The authors received no funding for this study.
Cicatrisation des plaies péristomiales autour des stomies rétractées par traitement des plaies par pression négative : une série de cas
Jarosław Cwaliński, Jacek Hermann, Tomasz Banasiewicz
DOI: https://doi.org/10.33235/wcet.43.2.29-34
Résumé
L'une des méthodes de traitement d'une stomie rétractée consiste à utiliser un pansement sous vide qui nettoie la plaie et la protège contre les fuites intestinales. Cette série de cas décrit l'utilisation d'un pansement de traitement des plaies par pression négative (TPN) intégré à usage unique afin de traiter les stomies rétractées comme alternative à d'autres remèdes non invasifs. Le compte-rendu inclut sept patients qui ont été hospitalisés dans le service de chirurgie des auteurs entre 2019 et 2020. Tous les patients ont développé une infection péristomiale sévère qui n'a pas répondu au traitement local avec des appareillages de stomie appropriés ou des pansements spécialisés. Après avoir nettoyé chaque plaie et retiré les lésions nécrotiques, les auteurs ont appliqué un pansement TPN hydrofibre à usage unique à chaque patient. Le pansement a été changé tous les 2 à 5 jours, en fonction des effets du traitement. L'orifice de la stomie a été recouvert d'une poche avec des systèmes de stomie à deux pièces. La plaie péristomiale a cicatrisé dans tous les cas et les fuites ont été éliminées. La durée moyenne du traitement était de 14 jours (intervalle, 10-21 jours), et les pansements sous vide ont été changés en moyenne quatre fois (intervalle, 3-7). Aucun des patients n'a eu besoin d'une translocation de stomie ou d'une autre intervention chirurgicale supplémentaire. Trois patients ont reçu une antibiothérapie systémique IV pour traiter une infection générale. Les pansements TPN à usage unique protègent les plaies péristomiales des fuites intestinales et n'entravent pas l'application des poches de stomie. Ce système, similaire aux dispositifs TPN standard, protège efficacement les stomies infectées contre la rétraction.
Introduction
Une stomie est une communication entre la lumière d'une anse intestinale et la paroi abdominale ; la création d'une stomie est l'une des procédures les plus fondamentales de la chirurgie colorectale. Elle est pratiquée sur le gros ou le petit intestin pour traiter des maladies malignes, inflammatoires ou vasculaires et à la suite de lésions intestinales. Le cancer colorectal est l'indication la plus courante, représentant jusqu'à 75 % des cas.1,2 Les stomies sont pratiquées sur près de 100 000 patients par an aux États-Unis, et la procédure réduit la morbidité et la mortalité majeures.3
Cependant, le taux de morbidité lié aux stomies est relativement élevé. Les complications précoces, telles que l'infection péristomiale, l'irritation cutanée, l'ischémie et la rétraction continuent de poser un défi aux chirurgiens.2 La rétraction de la stomie provoque une fuite continue du contenu intestinal dans le tissu sous-cutané ; elle peut être suivie d'une nécrose et d'une infection sévères des tissus entourant la stomie, avec un détachement de la stomie dans certains cas.4,5 Bien que la plupart des complications susmentionnées soient traitées avec des appareillages de stomie appropriés et des pansements spécialisés, les complications sévères peuvent nécessiter des modalités avancées telles que le traitement de la plaie par pression négative (TPN), qui offre une évacuation efficace et continue de l'épanchement infectieux et du pus. Cependant, bien que le sauvetage des stomies à l'aide de dispositifs TPN standard ait été décrit, à la connaissance des auteurs, il n'existe aucun compte-rendu sur les systèmes de TPN à usage unique. Par conséquent, cette série de cas décrit le traitement des plaies péristomiales et la prévention de la rétraction de la stomie à l'aide de pansements sous vide intégrés à usage unique.
Méthodes
Une étude préliminaire et prospective a été menée de 2019 à 2020 sur un groupe de sept patients présentant une stomie rétractée précoce et des plaies péristomiales. La série comprenait quatre hommes et trois femmes dont les caractéristiques sont présentées dans le tableau 1.
Tableau 1. Caractéristiques du patient (N=7)
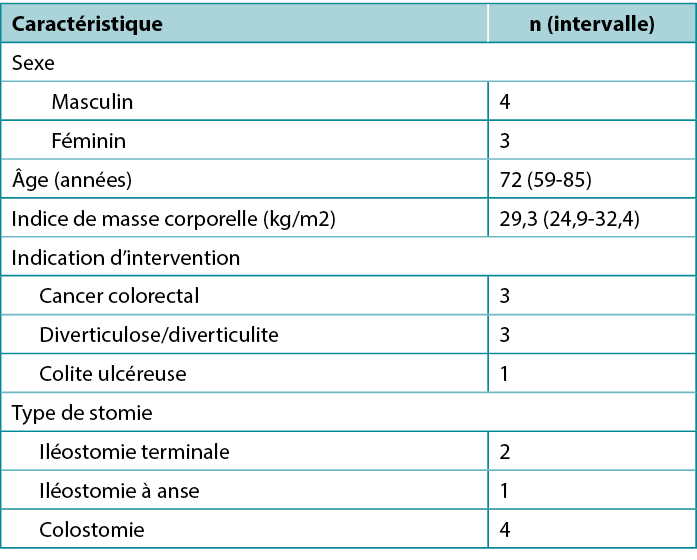
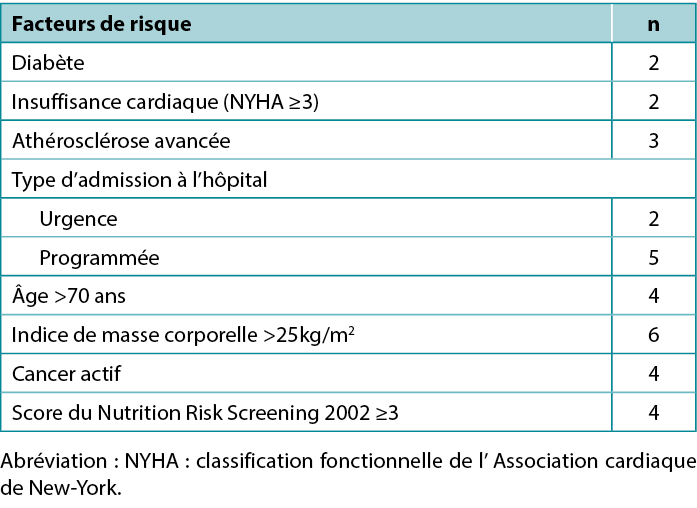
Tous les patients présentaient une infection péristomiale modérée ou sévère qui ne répondait pas au traitement local avec des appareillages de stomie appropriés et des pansements spécialisés. En outre, des facteurs de risque préopératoires de dysfonctionnement de la cicatrisation ont été observés dans le groupe d'étude, notamment la chirurgie d'urgence, la malnutrition, l'utilisation de stéroïdes, les maladies inflammatoires actives de l'intestin et d'autres comorbidités (tableau 2). Tous les patients ont reçu une alimentation immunomodulatrice par voie orale à partir du deuxième jour après l'opération, et quatre d'entre eux ont également été nourris par voie intraveineuse pendant les quatre jours postopératoires. En outre, trois patients ont dû recevoir une antibiothérapie systémique en raison de complications septiques.
Tableau 2. Facteurs de risque préopératoires d'infection du site opératoire
Éthique et consentement
Le traitement des plaies par pression négative est largement approuvé comme traitement médical et l'objectif de l'étude était d'adapter cette méthode au traitement des complications liées aux stomies. Par conséquent, le comité d'éthique de l'institution des auteurs a conclu qu'il n'était pas nécessaire de délivrer un consentement séparé pour cette étude. Cependant, en raison de cette application atypique du TPN à usage unique, les auteurs ont obtenu le consentement éclairé de chaque patient pour le traitement, ainsi que l'autorisation écrite de publier les images et les détails du cas.
Technique chirurgicale
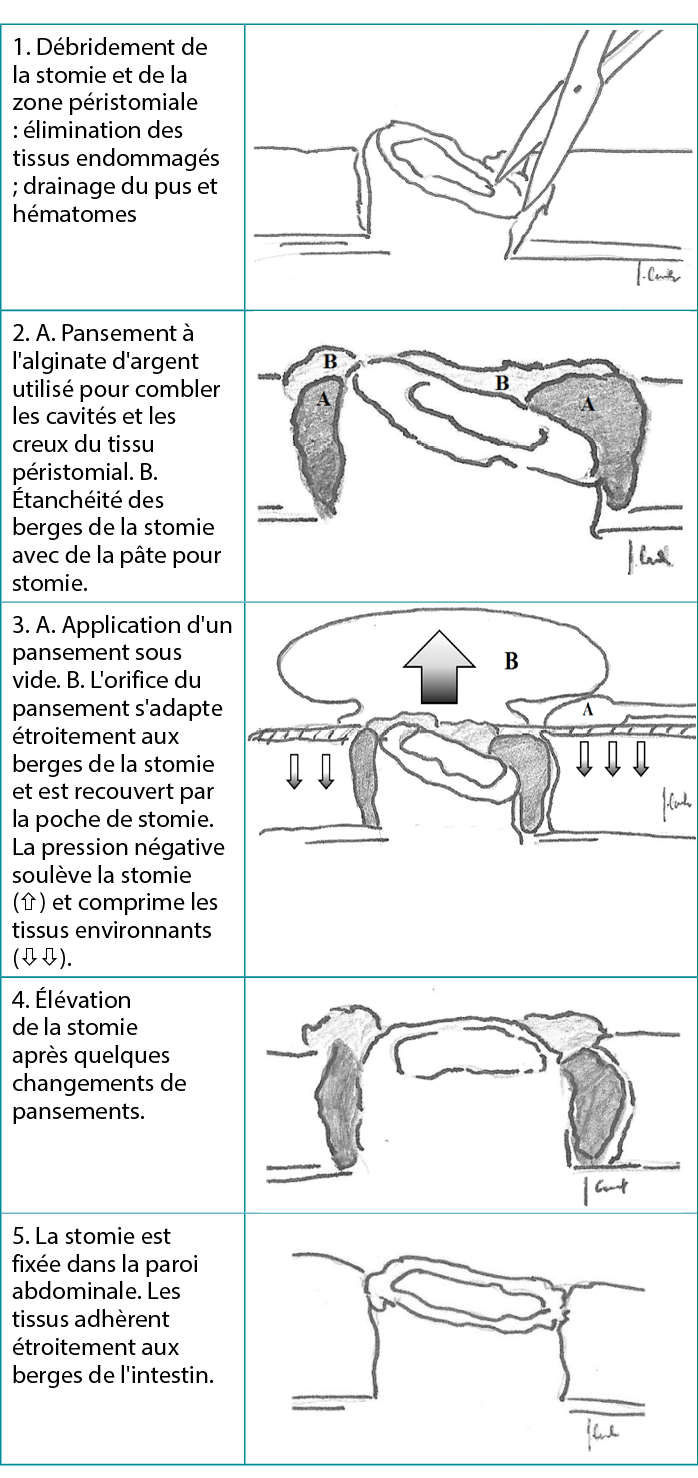
Tout d'abord, les auteurs ont débridé la plaie infectée entourant la stomie rétractée et, si nécessaire, ont placé un drain dérivé d'une coupe séparée en cas de fuite persistante du contenu intestinal dans le site chirurgical (figure 1). Ensuite, ils ont lavé la plaie et la peau environnante avec un désinfectant et ont appliqué un pansement en fibre de cellulose carboxyméthylée mesurant 15 × 10 cm ou 10 × 10 cm (Avelle NPWT System, ConvaTec ; ou PICO NPWT System, Smith & Nephew ; figure 2). Un trou a été pratiqué dans le pansement pour s’adapter à la stomie ainsi qu'à la plaie. L'adhérence et l'étanchéité des pansements ont été renforcées par des bandes de film adhésif placées sur les bords (figure 2). Lors de l'étape suivante, une pâte hydrocolloïde pour stomie a été appliquée pour augmenter l'adhérence des bords de la poche de stomie ou de la plaque (figure 3). La pâte pour stomie est également utilisée pour améliorer l'étanchéité du système et créer une barrière entre le contenu de la stomie et l'hydrofibre du pansement TPN. En outre, les cavités profondes de la plaie péristomiale présentant une nécrose résiduelle ont été comblées avec un pansement d'alginate d'argent ou une gaze de silicone à mailles ouvertes (figure 4).

Figure 1. Stabilisation d'une stomie rétractée par nécrectomie et sutures de l'intestin à la peau

Figure 2. Plaie péristomiale après application d'un pansement de traitement des plaies par pression négative à usage unique

Figure 3. Application d'une poche de stomie pendant le traitement d'une stomie rétractée à l'aide d'un pansement de traitement des plaies par pression négative
La pâte pour stomie remplit l'espace entre le bord des tissus et le pansement (à gauche), assurant une meilleure adhérence de la poche et la protégeant contre les fuites (à droite)

Figure 4 : Plaie péristomiale avec pansement d'alginate d'argent ou gaze de silicone à mailles ouvertes
Enfin, le port d'un générateur de pression négative a été fixé au pansement et une pression négative stable de 80 mm Hg a été maintenue pendant le traitement. A chaque changement de pansement, toute fuite intestinale dans la plaie a été contrôlée et éliminée si nécessaire (figure 5). Les pansements ont été changés au un jour sur deux à l'aide d'une poche de stomie en seule pièce. Par la suite, les pansements ont été laissés en place pendant 3 à 5 jours à l'aide de systèmes de stomie à deux pièces (figure 6). Un schéma récapitulatif de la procédure est présenté dans le tableau 3.

Figure 5. Stomie au quatrième jour de traitement après le deuxième changement du système de drainage par le vide, sans fuite du contenu intestinal

Figure 6. Poche en une seule pièce appliquée à la stomie
Tableau 3. Cicatrisation de la stomie : le pansement de traitement des plaies par pression négative à usage unique élimine les tissus nécrosés et prévient l'érosion de la stomie
Résultats
Les plaies péristomiales profondes et infectées des patients ont cicatrisé et les stomies ont été maintenues à leur emplacement initial. Aucun des patients n'a dû subir d'opération secondaire. La durée moyenne du traitement était de 14 jours (intervalle, 10-21 jours), et le TPN a été changé en moyenne quatre fois (intervalle, 3-7). La figure 7 montre un effet représentatif du traitement après quatre changements de pansements. Des appareillages de stomie ordinaires ont été utilisés chez six patients ayant une stomie terminale ; des anneaux d'étanchéité supplémentaires ont été nécessaires chez un patient ayant une stomie à anse. Deux patients, l'un ayant subi une colostomie et l'autre une iléostomie, ont reçu une antibiothérapie systémique appropriée en raison de la présence de marqueurs inflammatoires élevés dans le sérum.

Figure 7. Effet au jour 10 de traitement et après quatre changements de pansements
Discussion
L'incidence de l'ensemble des complications liées à la stomie se situe entre 10 et 70 %.6,7 La formation d'hématomes, les saignements, l'œdème stomial, l'irritation cutanée avec érosion ou ulcération, l'ischémie avec nécrose et la rétraction précoce de la stomie sont les complications les plus courantes qui surviennent dans les 30 jours suivant toute intervention, avec des fréquences allant de 25 à 34 %.1 Bien que la plupart de ces complications se résolvent spontanément en quelques jours ou ne nécessitent qu'un traitement médical conservateur, les patients qui développent des complications majeures telles que l'ischémie avec nécrose ou la rétraction de la stomie nécessitent généralement une chirurgie secondaire en raison de la menace d'infection sévère et de dysfonctionnement du tractus gastro-intestinal.1,8 Une technique chirurgicale appropriée - déplacer l'intestin sans tension vers la surface cutanée et le suturer à l'endroit prévu - est le moyen le plus efficace de prévenir les complications chez les patients.
Avant les interventions programmées, l'infirmière ou l’infirmier stomathérapeute doit préparer la localisation de la stomie, en évaluant l'emplacement des plis cutanés et des cicatrices et en tenant compte du mode de vie et de l'activité professionnelle du patient. En règle générale, le site de la stomie est défini en position debout, couchée et assise. L'infirmière ou l’infirmier stomathérapeute doit également marquer un site alternatif en cas de difficultés peropératoires.9
Selon la technique chirurgicale, la stomie doit être positionnée à travers le muscle grand droit de l'abdomen en laissant une marge intestinale suffisante au-dessus de la surface cutanée. Pour une stomie terminale, elle doit être de 5 cm pour l'intestin grêle et de 2 cm pour le côlon, ce qui permet à la stomie de se contracter à environ 2 cm et 0,5 cm après quelques mois.10 L'absence de préparation préopératoire adéquate peut se produire lors d'interventions en urgence, pour lesquelles le taux de morbidité augmente.11,12
Une stomie réfractaire peut être un motif de réintervention, ce qui, dans certains cas, augmente le risque de complications supplémentaires. Il est extrêmement important d'éviter les réinterventions pour certaines populations de patients en particulier, comme les personnes souffrant de cachexie et/ou de cancer, pour lesquelles les infections du site chirurgical ou d'autres complications peuvent prolonger la durée du séjour et affecter la chimiothérapie. En outre, le fait d'éviter une réintervention permet au patient de maintenir une alimentation orale, ce qui améliore l'absorption des nutriments et l'état du microbiome intestinal.12,13
Empêcher la fuite continue du contenu intestinal dans le tissu sous-cutané péristomial et permettre l'écoulement sans entrave du contenu intestinal à travers la stomie sont les objectifs thérapeutiques de base dans les cas de complications liées à la stomie.11,14 Ces objectifs sont d'abord atteints avec des appareillages de stomie modifiés sous forme d'anneaux, de rondelles et de pieds à profil concave, dont les objectifs sont l'adaptation de la forme et le nivellement de la hauteur de la stomie.15 Le traitement assisté par le vide est recommandée comme méthode efficace pour traiter les patients dont la stomie est sévèrement rétractée. Les pansements assistés par le vide sont constitués d'une mousse de polyuréthane recouverte d'une feuille adhésive. Une pompe d'aspiration électrique fixe ou portable est fixée au pansement et une pression négative stable de 50 à 200 mm Hg est maintenue pendant le traitement. Les objectifs du traitement par aspiration sont d'éliminer l'exsudat des tissus, de dévier le contenu des intestins, de réduire l'œdème et d'améliorer l'apport sanguin.16,17 La mousse de polyuréthane élimine également les tissus dévitalisés et infectés et améliore le drainage lymphatique. Ainsi, après quelques changements de pansements, la plaie se contracte et se recouvre d'un tissu de granulation neuf. 16,18 Le mode d'action antibactérien, principalement contre les bactéries à Gram négatif, repose sur l'élimination directe des cellules bactériennes, suivie d'une régulation locale de l’état pharmacodynamique et pharmacocinétique, dont l'effet est une meilleure pénétration de l'antibiotique dans les tissus.19,20
L'application correcte de pansements sous vide sur des plaies péristomiales avec un reste d'intestin rétracté est un défi car le contenu de l'intestin peut être aspiré dans une poche de stomie à travers les couches mal adhérentes du pansement. Il est prioritaire d'isoler la stomie de la plaie sans provoquer de lésions tissulaires secondaires causées par le pansement sous vide. Il est donc absolument nécessaire de placer une couche isolante entre l'intestin et la mousse de polyuréthane et d'utiliser une sous-pression comprise entre 75 mm Hg et 125 mm Hg.21,22 La proximité de l'orifice d'aspiration et de la poche de stomie est un autre inconvénient de l'application. Enfin, les activités quotidiennes du patient peuvent être limitées par la nécessité de transporter une pompe d'aspiration électrique à pression négative fixe ou portable.23,24 Une autre question importante reste celle des soins ambulatoires et à domicile à long terme avec un équipement correctement sélectionné et un personnel qualifié. Les infirmières et infirmiers qui prennent en charge les plaies peuvent appliquer avec succès un traitement par le vide après quelques semaines de formation pratique.25
L'utilisation de pansements TPN à usage unique permet d'éviter les obstacles susmentionnés. Comme les pansements TPN à usage unique sont beaucoup plus fins que la mousse de polyuréthane ordinaire et que toutes les couches (séparatrice, absorbante et isolante) sont intégrées dans un seul élément, le pansement remplit complètement la plaie et adhère correctement aux bords de la stomie. En outre, ce type de traitement par le vide peut être laissé dans la plaie jusqu'à 7 jours, à condition qu'il conserve sa pleine capacité d'absorption des exsudats. Généralement, une pompe portable incluse dans le kit génère une pression stable d'environ 80 mm Hg lorsque la surface d'une plaie diminue et que la stomie rétractée est surélevée.27,28 Parce que ce système est léger, qu'il est doté d'une pompe silencieuse et qu'il nécessite de simples changements de piles, il est accepté par les patients en établissements ambulatoire et à domicile. D'après l'expérience des auteurs, la télémédecine (par exemple, iWound ; Polmedi) améliore la sécurité de l'utilisation du TPN dans le cadre du suivi du traitement des patients à domicile.
Conclusions
L'utilisation de pansements TPN à usage unique combinée à une alimentation équilibrée et à une antibiothérapie est une méthode de traitement efficace pour les patients souffrant de complications précoces liées à leur stomie. Les systèmes TPN à usage unique sont "respectueux de la peau", car ils n'endommagent pas la peau entourant la stomie et soignent simultanément la zone affectée par l'inflammation ou l'infection. Ils sont peu coûteux et faciles à utiliser, même à domicile. Les auteurs recommandent cette méthode de traitement pour la prise en charge d'une stomie rétractée en phase précoce avec une infection péristomiale concomitante.
Conflit d'intérêt
Les auteurs ne déclarent aucun conflit d'intérêt.
Financement
Les auteurs n'ont reçu aucun financement pour cette étude.
Author(s)
Jarosław Cwaliński*
MD, PhD
Jacek Hermann
MD, PhD
Tomasz Banasiewicz
MD, PhD
* Corresponding author
In the Department of General, Endocrinological Surgery and Gastroenterological Oncology, Poznan University of Medical Sciences, Poland, Jaroslaw Cwalinski, MD, PhD and Jacek Hermann, MD, PhD are Senior Assistants and Tomasz Banasiewicz, MD, PhD, is Professor and Head of Clinic.
References
- Ambe PC, Kurz NR, Nitschke C, Odeh SF, Möslein G, Zirngibl H. Intestinal ostomy. Dtsch Arztebl Int 2018; 16;115(11):182-7.
- Malik T, Lee MJ, Harikrishnan AB. The incidence of stoma related morbidity - a systematic review of randomised controlled trials. Ann R Coll Surg Engl 2018;100(7):501-8.
- Goldberg M, Aukett LK, Carmel J, et al. Management of the patient with a fecal ostomy: best practice guideline for clinicians. J Wound Ostomy Continence Nurs 2010;37:596–8.
- Kann BR. Early stomal complications. Clin Colon Rectal Surg 2008;21(1):23-30.
- Duchesne JC, Wang Y, Weintraub SL, Boyle M, Hunt JP. Stoma complications: a multivariate analysis. Am Surg 2002;68:961–6.
- Robertson I, Leung E, Hughes D, et al. Prospective analysis of stoma-related complications. Colorectal Dis 2005;7(3):279-85.
- Sheetz KH, Waits SA, Krell RW, et al. Complication rates of ostomy surgery are high and vary significantly between hospitals. Dis Colon Rectum 2014;57(5):632-7.
- Beraldo S, Titley G, Allan A. Use of w-plasty in stenotic stoma: a new solution for an old problem. Colorectal Dis 2006;8:715–6.
- Whitehead A, Cataldo PA. Technical considerations in stoma creation. Clin Colon Rectal Surg 2017;30(3):162-71.
- WOCN Society, AUA, and ASCRS Position Statement on Preoperative Stoma Site Marking for Patients Undergoing Ostomy Surgery. J Wound Ostomy Continence Nurs 2021;48(6):533-6.
- Bass EM, Del Pino A, Tan A, Pearl RK, Orsay CP, Abcarian H. Does preoperative stoma marking and education by the enterostomal therapist affect outcome? Dis Colon Rectum 1997;40:440–2.
- Park JJ, Del Pino A, Orsay CP, et al. Stoma complications: the Cook County Hospital experience. Dis Colon Rectum 1999;42(12):1575-80.
- Shellito PC. Complications of abdominal stoma surgery. Dis Colon Rectum 1998; 41(12):1562-72.
- Kwiatt M, Kawata M. Avoidance and management of stomal complications. Clin Colon Rectal Surg 2013;26(2):112-21.
- LeBlanc K, Whiteley I, McNichol L, Salvadalena G, Gray M. Peristomal medical adhesive-related skin injury: results of an international consensus meeting. J Wound Ostomy Continence Nurs 2019;46(2):125-136.
- Cwaliński J, Paszkowski J, Banasiewicz T. New perspectives in the treatment of hard-to-heal wounds. NPWTJ 2018;5(4):10-2.
- Banasiewicz T, Borejsza-Wysocki M, Meissner W, et al. Vacuum-assisted closure therapy in patients with large postoperative wounds complicated by multiple fistulas. Wideochir Inne Tech Maloinwazyjne 2011;6(3):155–63.
- Hasan MY, Teo R, Nather A. Negative-pressure wound therapy for management of diabetic foot wounds: a review of the mechanism of action, clinical applications, and recent developments. Diabet Foot Ankle 2015;1,6:27618.
- Li T, Zhang L, Han LI, et al. Early application of negative pressure wound therapy to acute wounds contaminated with Staphylococcus aureus: an effective approach to preventing biofilm formation. Exp Ther Med 2016;11(3):769–76.
- Omar A, Wright JB, Schultz G, at al. Microbial biofilms and chronic wounds. Microorganisms 2017;5(1):9.
- Herrero Valiente L, García-Alcalá DG, Serrano Paz P, Rowan S. The challenges of managing a complex stoma with NPWT. J Wound Care 2012;21(3):120-3.
- Wright H, Kearney S, Zhou K, Woo K. Topical management of enterocutaneous and enteroatmospheric fistulas: a systematic review. Wound Manag Prev 2020;66(4):26-37.
- Herrero Valiente L, García-Alcalá DG, Serrano Paz P, Rowan S. The challenges of managing a complex stoma with NPWT. J Wound Care. 2012 Mar;21(3):120-3.
- Sun X, Wu S, Xie T, Zhang J. Combing a novel device and negative pressure wound therapy for managing the wound around a colostomy in the open abdomen: a case report. Medicine (Baltimore) 2017;96(52):e9370.
- Mohamed E, Elmoniem AE, Elmowafi HM, Shebl AM. Effect of training program on performance of nurses caring for patient with negative pressure wound therapy. IOSR-JNHS 2019;8(1):31-5.
- Malmsjö M, Huddleston E, Martin R. Biological effects of a disposable, canisterless negative pressure wound therapy system. Eplasty 2014;2,14:e15.
- Ozkan B, Markal Ertas N, Bali U, Uysal CA. Clinical Experiences with Closed Incisional Negative Pressure Wound Treatment on Various Anatomic Locations. Cureus. 2020, 26;12(6):e8849.
