Volume 44 Number 1
Wound bed preparation 2024: Delphi consensus on foot ulcer management in resource-limited settings
Hiske Smart, R Gary Sibbald, Laurie Goodman, Elizabeth A Ayello, Reneeka Jaimangal, John H Gregory, Sadanori Akita, Afsaneh Alavi, David G Armstrong, Helen Arputhanathan, Febe Bruwer, Jeremy Caul, Beverley Chan, Frans Cronje, Belen Dofitas, Jassin Hamed, Catherine Harley, Jolene Heil, Mary Hill, Devon Jahnke, Dale Kalina, Chaitanya Kodange, Bharat Kotru, Laura Lee Kozody, Stephan Landis, Kimberly LeBlanc, Mary MacDonald, Tobi Mark, Carlos Martin, Dieter Mayer, Christine Murphy, Harikrishna Nair, Cesar Orellana, Brian Ostrow, Douglas Queen, Patrick Rainville, Erin Rajhathy, Gregory Schultz, Ranjani Somayaji, Michael C Stacey, Gulnaz Tariq, Gregory Weir, Catharine Whiteside, Helen Yifter, Ramesh Zacharias
Keywords Diabetes, wound bed preparation, low-resource settings, foot ulcer, rural, delphi consensus, low- and middle-income countries, innovation
For referencing Smart H et al. Wound bed preparation 2024: Delphi consensus on foot ulcer management in resource-limited settings. WCET® Journal 2024;44(1):13-35.
DOI 10.33235/wcet.44.1.13-35
Abstract
Background Chronic wound management in low-resource settings deserves special attention. Rural or underresourced settings (ie, those with limited basic needs/healthcare supplies and inconsistent availability of interprofessional team members) may not be able to apply or duplicate best practices from urban or abundantly resourced settings.
Objective The authors linked world expertise to develop a practical and scientifically sound application of the wound bed preparation model for communities without ideal resources.
Methods A group of 41 wound experts from 15 countries reached a consensus on wound bed preparation in resource-limited settings.
Results Each statement of 10 key concepts (32 substatements) reached more than 88% consensus.
Conclusions The consensus statements and rationales can guide clinical practice and research for practitioners in low-resource settings. These concepts should prompt ongoing innovation to improve patient outcomes and healthcare system efficiency for all persons with foot ulcers, especially persons with diabetes.
General purpose
To review a practical and scientifically sound application of the wound bed preparation model for communities without ideal resources.
Target audience
This continuing education activity is intended for physicians, physician assistants, nurse practitioners, and nurses with an interest in skin and wound care.
Learning objectives/putcomes
After participating in this educational activity, the participant will:
- Summarise issues related to wound assessment.
- Identify a class of drugs for the treatment of type II diabetes mellitus that has been shown to improve glycemia, nephroprotection, and cardiovascular outcomes.
- Synthesise strategies for wound management, including treatment in resource-limited settings.
- Specify the target time for edge advancement in chronic, healable wounds.
Introduction
A framework for wound bed preparation (WBP) was introduced in 2000 to emphasise treating the whole person as a foundation of optimal local wound care.1 As this has evolved into an international framework, it became clear that not all wounds are healable. These concepts of maintenance and nonhealable wounds led to revisions of local wound care principles and WBP expansion. The importance of integrated coordinated care with nurses, doctors, and allied healthcare professionals working together to optimise patient care outcomes and healthcare system utilisation was paramount in further WBP developments.
This article focuses on applying the WBP framework to manage foot-related wounds, particularly in persons with diabetes (PWDs), leprosy-related neuropathic foot ulcers, and other complications that include neuropathy and vascular disease. Several parameters are critical to PWDs, including poor glycemic control, BP changes, high cholesterol, inadequate plantar pressure redistribution, infections, and lack of exercise. The effects of smoking are also particularly detrimental to saving limbs and lives of PWDs.
Critical for this article is a set definition for resource-restricted settings, including low resource availability; lacking or restricted funding; remote, isolated, or rural settings; and Indigenous populations. These terms all relate to healthcare settings that may have challenges accessing supplies, equipment, specialists, and advanced wound care competencies and skills. Low-resource settings can be present anywhere in the world and are not limited to lower-income or developing countries.
The Delphi process underpinning this work expanded and developed the WBP framework in its current format. Forty-one authors drawn from 15 countries took part in the Delphi process, which occurred over two rounds using a four-part Likert-type scale (1, strongly agree; 2, agree; 3, disagree; 4, strongly disagree). The first round consisted of 29 statements. Although all statements exceeded the desired 80% consensus level, there were 299 comments considered by the lead group of authors. A professional editor was employed to improve the comprehension and grammatical accuracy of the statements before a Delphi round 2 was deployed with 32 constructed statements. All statements exceeded 88% consensus level.
In round 2, 14 statements achieved 100% consensus. One statement stood out and was rated as “strongly agree” by all Delphi panel members: 10C. Establish timely and effective communication that includes the patient and all interprofessional wound care team members for improved healthcare system wound outcomes. In parallel, each of the international wound experts worked in groups to develop the manuscript content. Refer to Supplemental Table 1 (http://links.lww.com/NSW/A176) for the consensus statements.
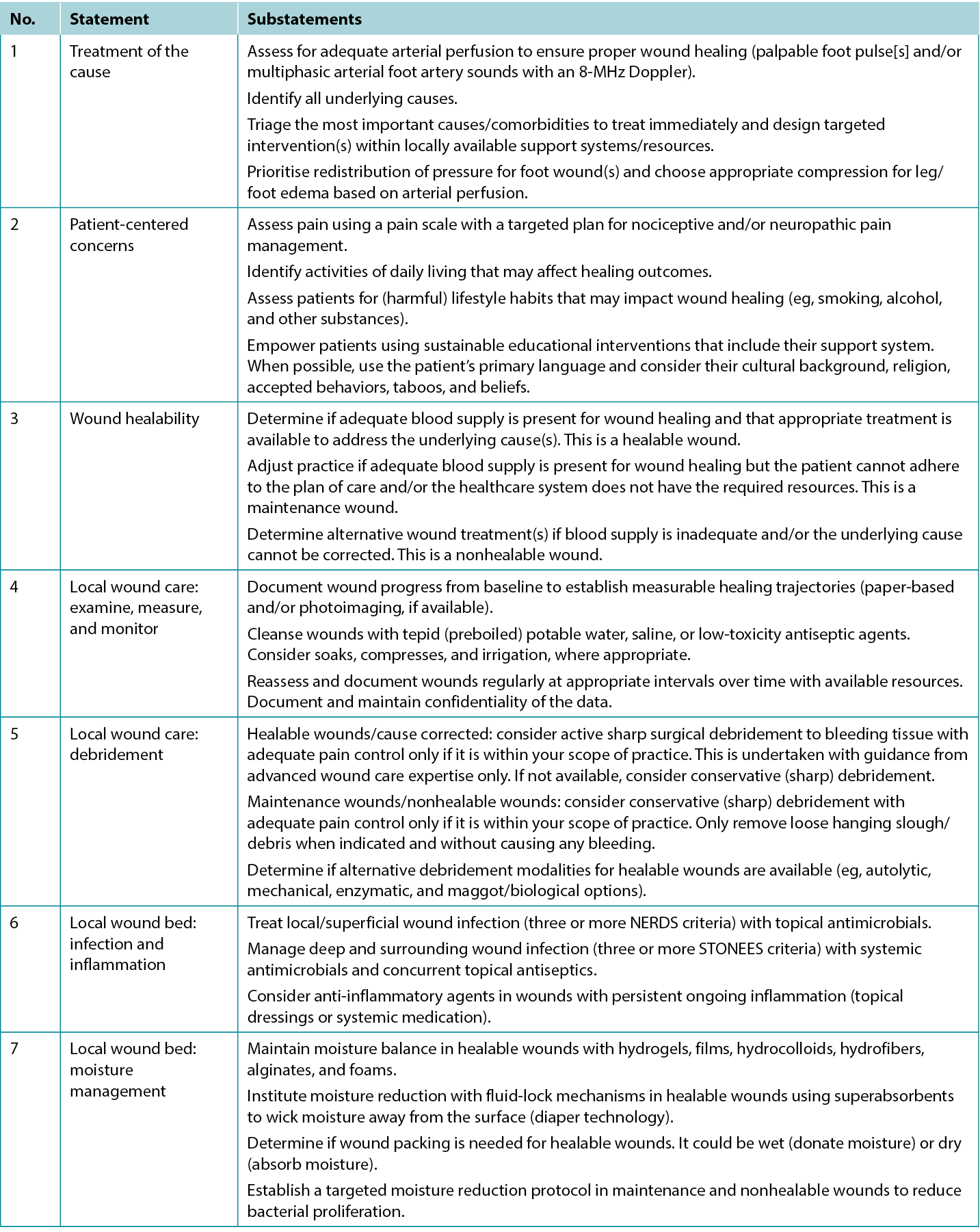
The consensus aimed to set a scientifically based minimal standard of care that could be optimised for available resources. Refer to Table 1 for the 10 key steps and 32 substatements for wounds in limited-resource environments. This consensus process updated the framework for WBP to be applicable regardless of resource availability. In addition, it also includes the concepts of healing trajectories and healthcare system change for the first time (Figure 1).
The remainder of this report will highlight the 10 consensus statements and discuss the rationale for each statement.
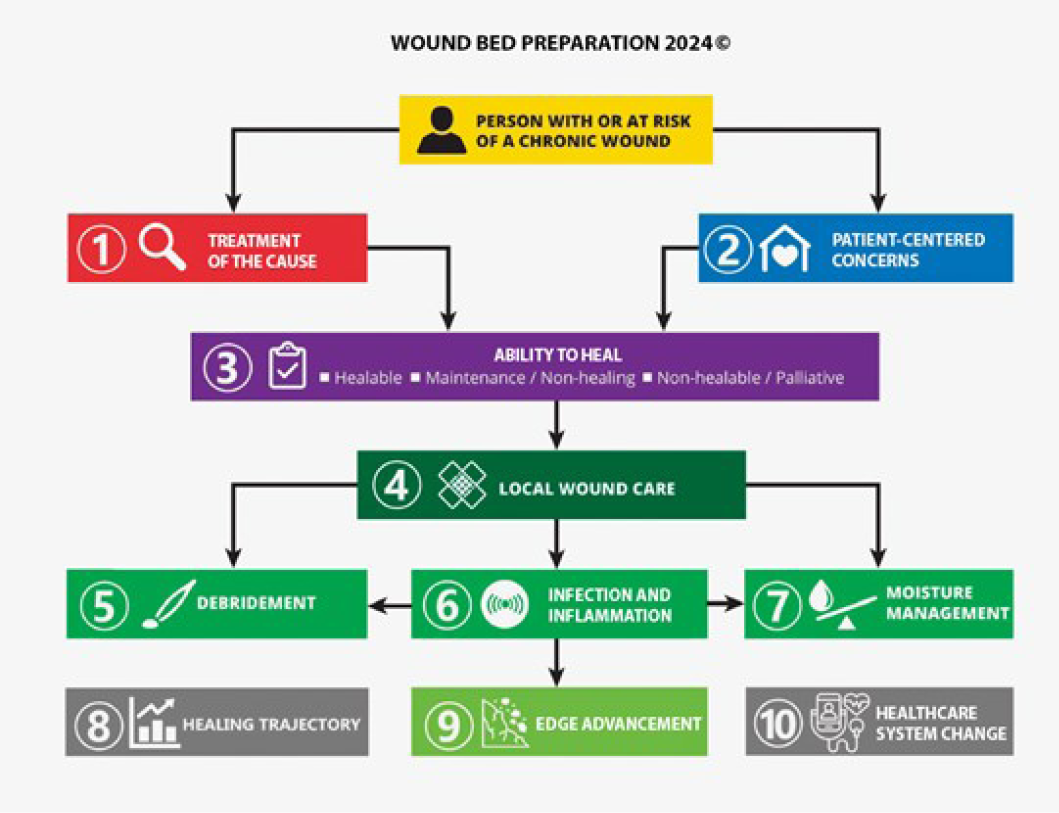
Figure 1. Wound bed preparation 2024. ©WoundPedia 2023
Table 1. Wound bed preparation for wounds below the knee in environments with limited resource availability

Statement 1: treatment of the cause
1A. Assess for adequate arterial perfusion to ensure proper wound healing (palpable foot pulse[s] and/or multiphasic arterial foot artery sounds with an 8-MHz Doppler)
To determine lower-limb blood flow, find a palpable foot pulse(s) as a vital first action. Start with the dorsalis pedis and/or the posterior tibial pulses. If an 8-MHz handheld Doppler is available, confirm multiphasic flow patterns (biphasic/triphasic). Refer to vascular specialists when a monophasic or absent Doppler sound is observed or foot pulses are not palpable. Other signs of inadequate arterial perfusion are lower limb pain at rest and ischemic limb changes (cold extremity with dependent rubor that blanches on elevation).
Persons with diabetes are susceptible to microvascular issues (peripheral neuropathy, Charcot foot changes) and macrovascular complications including peripheral arterial disease (PAD). These conditions contribute to calluses, foot ulcers, and mixed tissue loss. Because up to 50% of susceptible populations experience both diabetes and PAD,2 timely identification of PAD is critical (using physical examination and vascular tests) because it is a major risk factor for poor ulcer healing and amputation. If detected, immediate revascularisation (angioplasty or vascular bypass) is vital to restore proper arterial flow to the foot. Additional assessment may include capillary refill time, a Buerger blanching test (pale on elevation, bright red rubor on dependency), and claudication with walking.
Vascular examination. In cases of arterial insufficiency, the extremity is often cool to the touch because of insufficient nutrient and oxygen supply (Table 2). Severe cases may manifest tissue necrosis presenting as ulcers, macerated toe webs (often with secondary infection), fissures, or gangrene. Other severe case indicators include pallor upon leg elevation, exercise-induced claudication that resolves with rest, dependent cyanosis or rubor, and muscle atrophy. Notably, lower extremity edema is more indicative of venous rather than arterial issues. Arterial lesions are generally punched out, with a deep base that often contains tendons, whereas venous ulcers show irregular border morphology with a shallow granulation tissue base.3
Table 2. Vascular supply needed for tissue healing
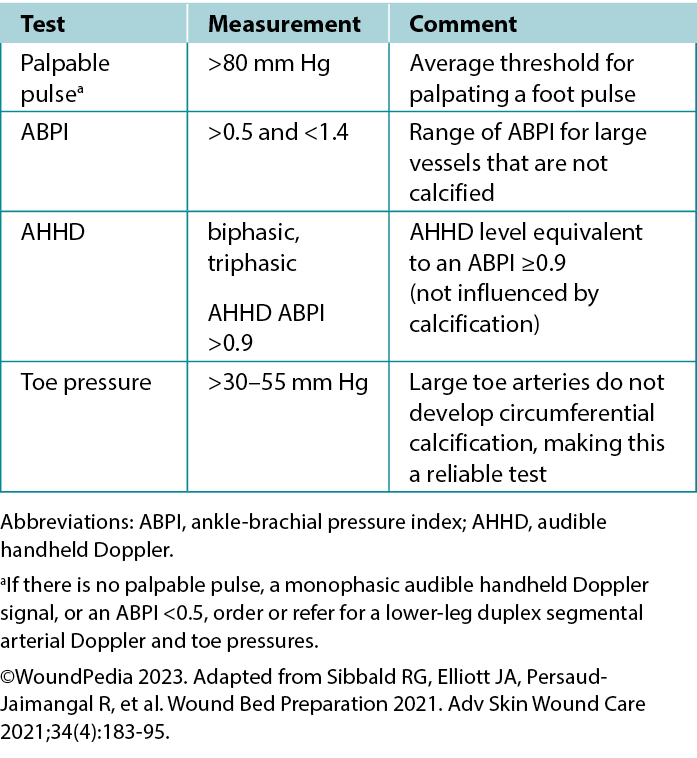
Ankle-brachial pressure index (ABPI) examination. The ABPI measures the ratio of ankle systolic BP divided by the brachial systolic BP using an 8-MHz Doppler. The procedure involves using a BP cuff and recording systolic BP when arterial sounds reappear after cuff inflation. However, factors such as edema, inflammation, and arterial calcification can affect its accuracy. If an 8-MHz Doppler cannot be afforded/obtained, early referral to a tertiary assessment center becomes the priority in cases where the absent foot pulses are present. In certain healthcare settings, an ABPI is still required as vital quantification assessment before beginning any lower limb intervention.
Audible handheld Doppler (AHHD) examination. An AHHD can easily be added as an additional parameter in certain settings, should providers choose a simpler and faster test (not influenced by calcification, no need to squeeze a painful calf, and no need to be recumbent for 20 minutes). The AHHD assessment also can provide accurate results in case of large toe amputation and be recorded as an MP3 or MP4 file and transferred for remote verification of the signal interpretation.
Healthcare professionals should apply gel on the appropriate foot pulse sites with an 8-MHz Doppler probe positioned at a 45° angle to the skin on the dorsalis pedis, posterior tibial, and peroneal arteries. The acquired Doppler signals/waveforms can then be analysed (either by audible sound or visual tracings): A comprehensive tutorial on the AHHD procedure is available online at https://journals.lww.com/aswcjournal/Pages/videogallery.aspx?videoId=20. Optimise signal quality with careful repositioning of the probe to obtain the loudest or most multiphasic signal.
A monophasic or absent waveform warrants a comprehensive vascular assessment, including a Duplex segmental lower leg arterial Doppler in the vascular laboratory. A multiphasic waveform typically indicates the absence of peripheral vascular disease.4 In PWDs, interpret the ABPI ratio with caution (due to arteriosclerosis or arterial calcification); AHHD multiphasic findings are a preferable choice to confirm adequate blood supply for wound healing. A multiphasic waveform (biphasic, triphasic) suggests an AHHD value equivalent to a normal ABPI ≥0.9.
Although AHHD is effective in excluding arterial disease, it may not identify existing segmental perfusion deficits—islands of ischemia or angiosome defects.5 Therefore, physical examination of the foot and lower limb is vital for a conclusive diagnosis. Healthcare professionals can record AHHD signals and transmit them to specialists, facilitating either synchronous or asynchronous assessments remotely. Synchronous assessments enable real-time patient involvement and prompt decision-making.
Chronic venous insufficiency. Chronic venous insufficiency may coexist in PWDs and those with foot ulcers. It mainly affects the lower limbs and impairs the return of deoxygenated blood to the heart and lungs. This condition often arises from venous valve dysfunction that can be triggered by factors including pregnancy or weight gain. Symptoms commonly include varicose veins, edema, skin discoloration from hemosiderin, lipodermatosclerosis, and venous ulcers.6 These ulcers can be any size (from small to circumferential) and form quickly over areas of venous pooling, usually on the medial aspects of the lower limbs.
The cornerstone of treatment for venous ulcers is compression therapy. This compensates for valve dysfunction by enhancing the peristaltic action of the calf muscle pump. Additional measures include leg elevation and walking. Venous ablative procedures may be considered when ulcers are attributed to superficial veins. Untreated venous edema can delay foot ulcer healing.7
For the medical optimisation of PAD, key strategies include optimal BP control, initiating cholesterol medication, and, often, starting statin therapy. Recent studies also recommend treating patients with PAD and concurrent coronary artery disease or carotid disease using a combination of low-dose aspirin (91-100 mg PO daily) and low-dose rivaroxaban (2.5 mg PO BID).8 Additional modifiable factors are smoking cessation and walking or exercise programs. For patients with a foot ulcer (especially in PWDs), appropriate plantar pressure redistribution or offloading is essential.
1B. Identify all underlying causes
Foot complications are of great concern to PWDs and represent a significant burden of disease to healthcare systems. A holistic approach is represented by the mnemonic AIM (assessment, identification, management) and focuses on treating or mitigating the underlying cause of diabetic foot issues, especially neuropathy. The application of a focused assessment approach as a baseline standard of care (VIPS: vascular, infection, pressure, surgical debridement) is crucial in preventing severe complications, including foot ulcerations, lower limb amputations, and an increased incidence of early/preventable death. Some critical foot-related elements in resource-challenged settings include late presentations to formal care, delayed diagnosis,9 barefoot walking, neglected wounds, and the absence of preventive foot care. A hospital-based observational analysis conducted in Ethiopia identified several factors contributing to diabetic foot complications;10 these included high humidity, foot deformity, neuropathy, unidentified active ulcers, inadequate or ill-fitting footwear, poor foot hygiene (eg, foot and toenail fungus), and lack of foot care awareness. A systematic review on plantar ulcers among patients with leprosy (n = 7 studies) identified the following risk factors for developing ulcers: inability to feel a 10 g monofilament on sensory testing, severe foot deformities or hyperpronation, lower education, and unemployment.11 Addressing these challenges in any resource-challenged environment requires a multipronged approach that may include patient and healthcare professional education, early detection, access to care, footwear programs, and community engagement.
Regular and thorough foot assessments include detecting neuropathy (loss of protective sensation), vascular issues (poor or absent lower limb blood circulation), signs of infection, areas of high pressure (callus formation), and friction (blisters, often with hemorrhagic components) to facilitate timely interventions. The simplified 60-second screening tool may be a valuable means to quickly assess, stratify, and follow up patients based on their risk levels without significant cost.12 Patients with a history of ulceration, amputation, peripheral vascular surgery, or Charcot neuroarthropathy are at the highest risk for skin breakdown and should receive additional attention to prevent ulceration and further complications.
To detect infection, the NERDS (superficial wound infection: nonhealing, exudate, red friable granulation tissue, debris, smell) or STONEES (deep and surrounding wound infection: size increased, 3 °F temperature warmer, os [probe to bone], new areas of breakdown, erythema >2, exudate, smell) criteria along with using noncontact infrared thermometry can be helpful.13 Elevated temperatures of 3 °F compared with the opposite limb may signal inflammation and a foot at a higher risk of ulceration.13 A comparative change of 1.67 °C is difficult to measure clinically. This same finding in a person with a lower leg or foot ulcer is eight times more likely to signify deep and surrounding infection when accompanied by two or more additional STONEES criteria.13
Patients with neuropathy without an ulcer and presenting with a hot swollen foot could have acute Charcot neuroarthropathy. Infrared thermometry is a valuable assessment tool in these cases: acute Charcot feet may be 8 to 15 °F warmer than the mirror image on the opposite foot. These patients require a comprehensive medical history, physical examination, and radiographic images to facilitate early detection. Further actions include the application of a total contact cast for stabilisation and complete plantar pressure offloading with a wheelchair to prevent further bone deterioration and prevent lower limb amputation (Table 3).
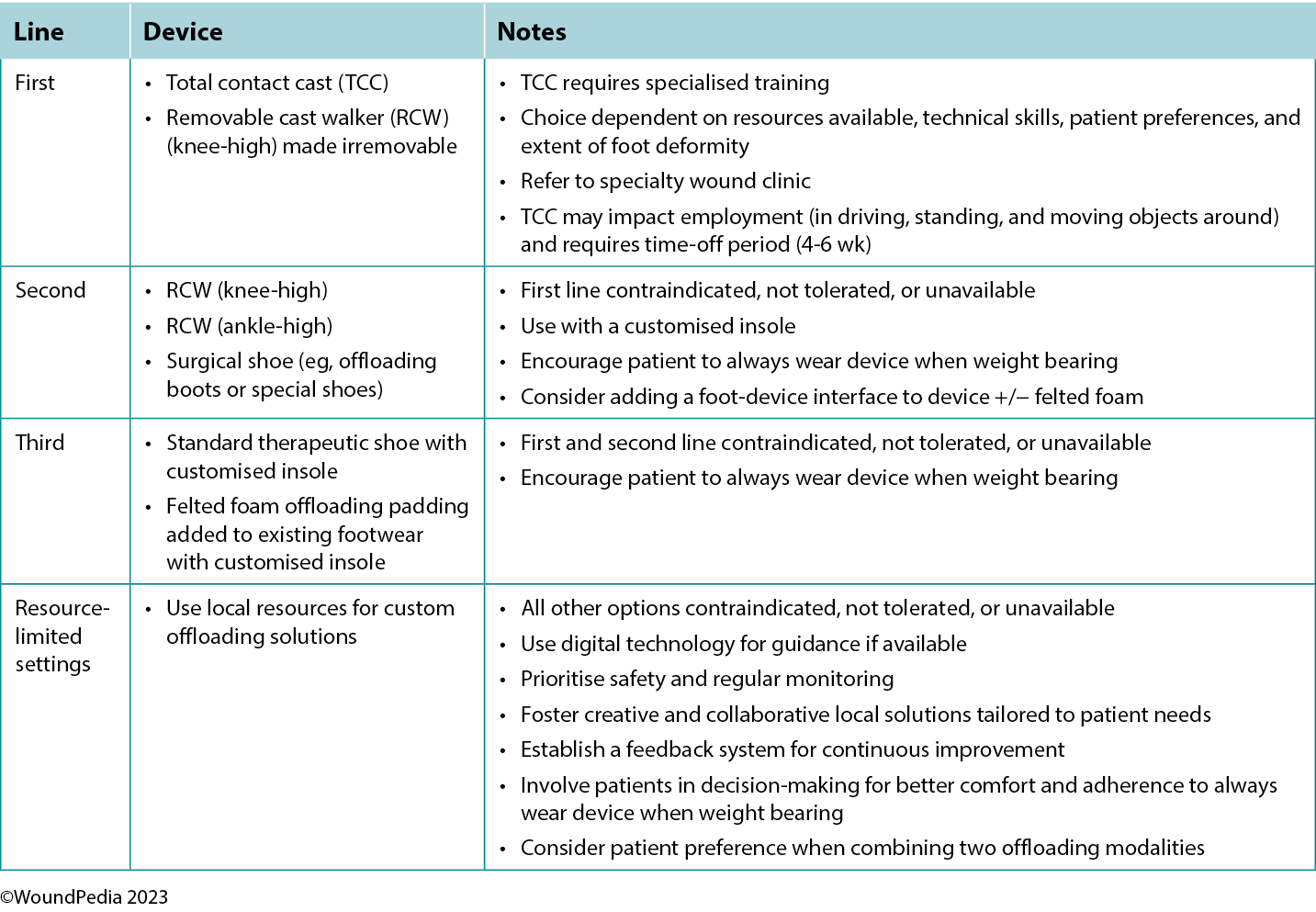
Table 3. Offloading interventions for a plantar diabetic/neuropathic foot wound28
Callus formation in PWDs is positively correlated with pressure and shear stress. In individuals with diabetic neuropathy, various factors including foot deformities, limited joint mobility, repetitive stress during walking, and poorly fitting shoes can increase the risk of callus formation.14 Moreover, the presence of calluses can pose a significant risk because repetitive trauma may lead to subcutaneous hemorrhage and eventually progress to ulceration. Provide tailor-made pressure redistribution devices (soft insoles, cobbler interventions to adapt shoes, and reduced barefoot walking) to prevent subsequent callous-to-ulcer progression.
Different etiologic causes may lead to foot ulcers in PWDs: neuropathic because of peripheral neuropathy, ischemic associated with PAD, or a combination of both—neuroischemic foot complications. The presence of diabetic neuropathy is established from medical history; physical examination (5.07/10 g monofilament test); altered sensation distributed symmetrically in both limbs (stocking and glove distribution); and burning, stinging, shooting, or stabbing pain.
1C. Triage the most important causes/comorbidities to treat immediately and design targeted intervention(s) within locally available support systems/resources
A diabetic foot ulcer (DFU) occurs in 25% to 34% of PWDs and is one of the most feared complications, potentially leading to lower limb amputation, severe disability, and reduced life expectancy.15 Multifactorial in origin, diabetes-related peripheral neuropathy and PAD leave feet highly vulnerable to traumatic injury. Access to timely diagnosis and intervention are determinant factors in effective management and limb preservation.
Chronic hyperglycemia measured by elevated hemoglobin A1c (HbA1c) is a major risk factor for sensory, motor, and autonomic neuropathy. Both PAD and dry skin increase foot vulnerability to infection and delayed healing, all contributing to poor outcomes. Chronic kidney disease adds to the risk.16 Recent studies of continuous glucose monitoring report that high glucose variability (reduced time to target range levels) may additionally contribute to long-term complications.17
Up to 50% of PWDs will develop neuropathy with no known cure. Management includes proper daily foot inspections for evidence of trauma or infection, foot care, and effective glucose control.18 In addition to neuropathy, PAD contributes equally to DFUs; PAD is largely asymptomatic and may remain underdiagnosed and untreated for a prolonged period. Individuals with diabetes have more than a twofold increased prevalence of PAD compared with those without.19 A systematic review of community-based studies for global prevalence and risk factors for PAD ranked diabetes highest next to smoking.20
The European Society of Hypertension recommends providers and patients target a systolic BP less than 130 mm Hg and diastolic BP less than 80 mm Hg. In PWDs, systolic BP should not fall less than 120 mm Hg to prevent reduced blood flow to vital organs and lower limbs.21 Although diuretics, calcium-channel blockers, angiotensin-converting enzyme inhibitors, angiotensin receptor blockers, and β-blockers can all be used, angiotensin-converting enzyme inhibitors and angiotensin receptor blockers reduce cardiovascular events.22,23 Recently, SGLT2 inhibitors have shown excellent results in improving glycemia, nephroprotection, and cardiovascular outcomes.24 In addition, DFU incidence is reduced by early detection of PAD with lifestyle modifications.17
The complexity of managing a DFU requires an interprofessional team approach to identify biological, social, geographic, and cultural determinants of health. In Denmark, PWDs are registered by region with access to specialised clinics with interprofessional wound care teams. Lower limb amputation rates have declined significantly due to improved diabetes care, regular foot inspection, better self-care, and timely treatment.25 In more geographically dispersed diverse populations (eg, Ontario, Canada), significant disparities in amputation rates exist, highest in rural regions where timely prevention such as revascularisation surgery and foot care specialists are underserviced or absent.
The most vulnerable persons for diabetic foot-related amputations in Canada are Indigenous people, immigrants, and persons living in rural and northern regions.26 The Indigenous Diabetes Health Circle provides a culturally sensitive approach to local Ontario First Nations communities with education and knowledge about diabetes, wellness, and self-management. Its holistic foot care program supports a continuum of services that connects community members to Indigenous agency partners and local healthcare professionals and is proven to reduce DFU incidence and prevent amputations.27
1D. Prioritise redistribution of pressure for foot wound(s) and choose appropriate compression for leg/foot edema based on arterial perfusion
The criterion standard for plantar pressure redistribution devices is the total contact cast or the removable cast walker made irremovable.28 Even in healthcare systems in which these offloading modalities are readily available, less than 10% of eligible patients are fitted for and adherent to the use of these devices.29
Offloading is paramount to healing foot ulcers (Table 3). The aim is to select the best device for the patient incorporating patient-centered concerns, the goals of care, and best practice evidence. Consider creative solutions to repurpose local materials such as soft felted inserts for offloading in resource-limited settings. It is important to establish an early surveillance program between the patient and healthcare professional to monitor and ensure the desired offloading outcomes. Healthcare professionals need to evaluate the effectiveness of the devices and continually make modifications as needed through established follow-up. In regions lacking specialised practitioners, empowering healthcare workers with competencies in basic offloading can bridge this gap.
Statement 2: patient-centred concerns
2A. Assess pain using a pain scale with a targeted plan for nociceptive and/or neuropathic pain management
The perception of pain involves a stimulus that may be physical or chemical. There are two main types of pain: nociceptive and neuropathic (Table 4). Wound-related pain is an important component of patient-centered concerns that is often undervalued by healthcare professionals. By the late 1990s, wound pain was a focus for healthcare professionals with the launch of a pivotal position document focused on wound pain.30 The document recognised and focused on the distress of chronic wound pain and its influence on patients’ health-related quality of life. The management of wound pain was then integrated into the WBP framework.1,31
Table 4. Pain types and responses30
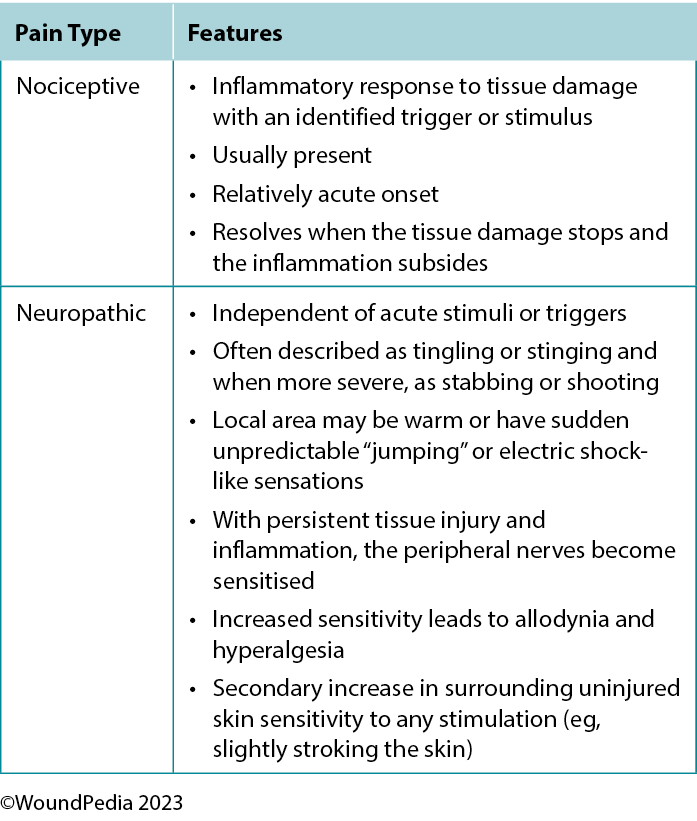
Pain can play a significant role in the total management of persons with wounds and their ultimate healing success.32 Pain signals associated with injury play an important function in patient wellness and as such must be acknowledged through adequate assessment and management. For example, pain or any change in pain is a key predictor of wound infection and one of the four cardinal signs of inflammation.1 Unresolved pain is often associated with delayed wound closure.
Assessment. A pain history is essential to wound pain management.32 Assessment must include the nature, onset, duration, and exacerbating and relieving factors. This will help determine the cause of the pain and direct its management. Pain intensity can be reliably measured using validated pain scales. A verbally administered 0- to 10-point numerical rating scale is a good first choice for measuring pain numerical intensity. Most patients can function with a pain level of 3 to 4 out of 10.33
Patients with persistent pain should be reassessed regularly for improvement, deterioration, and adherence to medication regimens. The use of a pain diary with entries regarding pain intensity, medications used, mood, and response to treatment may be a good management strategy. For individuals with communication limitations, the pain scale should incorporate pictures for easy recognition.
Management. The management of wound pain can be integrated into the WBP framework: treat the cause and address local wound factors and patient-centered concerns.3 Treating the cause should determine the correct diagnosis and initiate treatment of the wound pain. Patient-centered concerns must focus on what the patient sees as the primary reasons and resolutions for the pain. Patient anticipatory pain and suffering can be just as disruptive to quality of life as the actual experience of pain.
Multiple pain management strategies exist and are not always pharmaceutical (Table 5). Consider total patient management, including all aspects of WBP, in choosing a management strategy. Remember: pain is what the patient says it is.34
Table 5. Pain management strategies
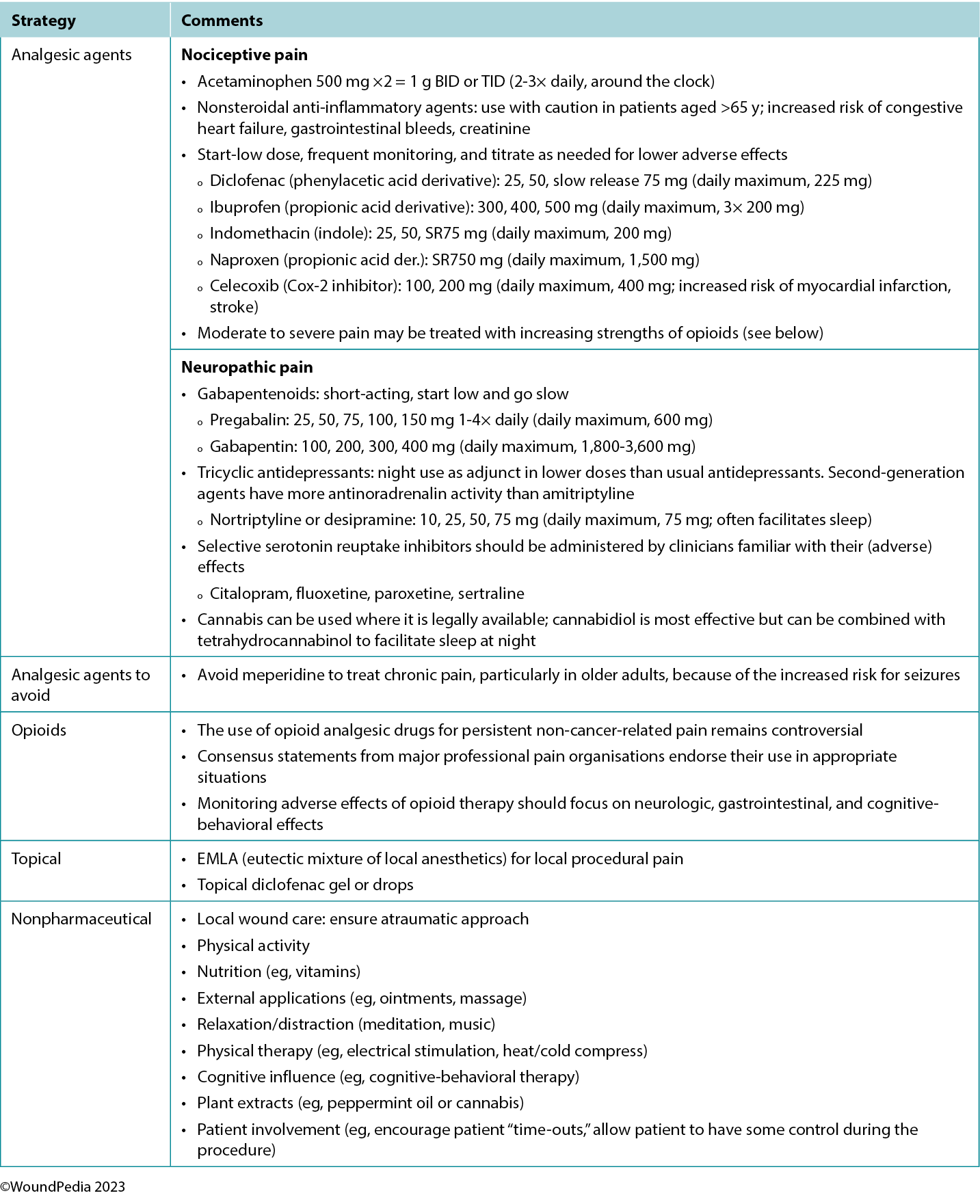
Assessment and management given limited resources. In regions with limited resources, assessment remains possible because it requires no costly tools. Most pain scales are freely available despite some initial cost relative to education and training of practitioners.31 Treatment options for pain in resource-restricted environments may be more practical if driven with nonpharmacologic methods (Table 5). Some of these options may also be more socially acceptable or already practiced culturally (eg, meditation, plant-based treatments) and particularly applicable in nociceptive pain management. Implementing such strategies can then preserve pharmaceutical management for those with pain that cannot be managed by nonpharmacologic means (eg, neuropathic pain).35
2B. Identify activities of daily living that may affect healing outcomes
2C. Assess patients for (harmful) lifestyle habits that may impact wound healing (eg, smoking, alcohol, and other substances)
2D. Empower patients using sustainable educational interventions that include their support system. When possible, use the patient’s primary language and consider their cultural background, religion, accepted behaviors, taboos, and beliefs
In resource-limited environments, patient-centered concerns and barriers to clinical outcomes are crucial for providers to understand and address within the context of cultural, spiritual, and religious beliefs of the respective community.
Wound healing disparities exist among Indigenous populations across the globe. These disparities are often rooted in historical and ongoing socioeconomic, cultural, and healthcare-related factors. Cultural diversity and societal pressure also often dictate formal resource allocation processes to certain health sectors. Some key barriers to wound healing among Indigenous populations include historical trauma, socioeconomic disparities, limited access to healthcare, cultural barriers, chronic health conditions, cultural healing practices, geographic isolation, and healthcare system bias.36 Many cultures have an honor system in managing their sick, older adult, and chronically ill members. These principles are easier upheld if sufficient resources are available to maintain them.
Many studies have identified a major medical illness as one of the core reasons a family can incur large debts.37,38 Even in government-run clinics, additional dressing materials or medicines may be charged to the family. Patients and family members may therefore resort to alternative treatment methods (nonallopathic medicine) from local/Indigenous/traditional healers. Although often less costly, these healers may not have the necessary skills or expertise in managing chronic wounds, leading to deterioration.
Loss of independent mobility because of wound chronicity is another major factor that impacts attendance and regular follow-up. Transport availability varies in resource-restricted environments, and walking may be the only way to access a public transport pick-up point. Secluded rural environments are often affected the most and require traveling significant distances to reach a formal healthcare facility.
The social health of the family environment and willingness to incorporate a person with healthcare needs can drive the quality of care/self-care rendered as well as patient safety within a home environment. Because of the social structure and milieu in various countries, family support and social support may differ by culture. Often, as time passes, the financial burden increases; patient independence and activities of daily living (ADLs) achievement deteriorates; dressing changes become more challenging; and caregivers become stressed, fatigued, and exhausted.39 Late referrals and critical/terminal patient conditions when eventually presenting to formal care are additional aggravating social and behavioral factors that can compound poor wound healing outcomes.
Individuals with wounds treated at home need a designated space to themselves. Wound odor, persistent pain, and a different routine are the main stressors on both the patient and family in settings where space is at a premium. The mere presence of a major skin wound already negatively impacts the patient’s own social interactions, relationships, sexuality, and self-confidence. This leads to progressive anxiety and depression that may bring about pessimism regarding perceived treatment benefits. Subsequently, patients have lowered self-efficacy that is often associated with further wound deterioration including eventual lower-extremity amputations.40
The real challenge occurs when lifestyle modifications are needed. This often requires additional resources or tailor-made education to construct self-care plans.40,41 The need for health education and lifestyle modification interventions to have clear rationales cannot be overemphasised. Lifestyle interventions may become a financial, social, and logistical challenge, first to acquire and then to maintain within any restricted living domain. Further, it is a vital step to ensure that any financial help received is correctly allocated to the family member with a wound.
A biopsychosocial approach is necessary in managing wound care for patients in resource-restricted environments. The wound care team, beyond managing the wound, must address the social stressors/factors affecting the patient. Each patient will need a unique, mutually agreed-upon management plan that fits their constraints (medical, financial, family, social, and emotional support).40
Statement 3: ability to heal
3A. Healable wound: Determine if adequate blood supply is present for wound healing and that appropriate treatment is available to address the underlying cause(s)
3B. Maintenance wound: Adjust practice if adequate blood supply is present for wound healing but the patient cannot adhere to the plan of care and/or the healthcare system does not have the required resources
3C. Nonhealable wound: Determine alternative wound treatment(s) if blood supply is inadequate and/or the underlying cause cannot be corrected
The process of determining the healing classification of a wound begins with a thorough patient history and physical examination. Identifying the underlying cause(s) of the wound is important. Addressing the underlying cause(s) is the first step to developing an achievable management plan.
In some cases, chronic wounds may also become stalled and fail to achieve the wound edge advancement over the set time; these are known as hard-to-heal wounds. They often fall into the maintenance category but, with additional assessment, may be healable with a re-evaluation of the patient, history, causes, and treatment plan.3,42
Patient-centered concerns and expectations need to be identified, compared with, and aligned with institutional/clinician resource availability, skills, and immediate intervention options that are available.3,42 The management plan is based on the assigned healing classification, which may change.
Protect nonhealable wounds against tissue loss, deep and surrounding wound infection, and general deterioration from a wet wound environment. Decreasing moisture is a priority. Maintenance wounds also need protection against further tissue losses with dry wound bed management and local infection controls as the mainstay. Tissue protection may also be a temporary measure until resources become available and additional patient factors are controlled to achieve full optimisation.
Stalled but healable wounds (hard-to-heal) need a second chance to achieve edge advancement with urgency in reassessment and interprofessional team intervention as the highest priorities.3,42
Statement 4: local wound care: examine, measure and monitor
4A. Document wound progress from baseline to establish measurable healing trajectories (paper-based and/or photoimaging, if available).
4B. Cleanse wounds with tepid (preboiled) potable water, saline, or low-toxicity antiseptic agents. Consider soaks, compresses, and irrigation, where appropriate.
4C. Reassess and document wounds regularly at appropriate intervals over time with available resources. Document and maintain confidentiality of the data.
Wound assessment documentation is an integral component of healthcare practice. It is instrumental in ensuring the delivery of high-quality patient care, monitoring wound status, and providing direction for any changes in wound interventions. The comprehensive and accurate recording of wound assessments is essential to ensure improved patient outcomes, effective communication among healthcare professionals, and legal and regulatory compliance.43
Monitoring progress. Wound assessment documentation serves as a historical record of the wound’s progression over time. By regularly documenting wound characteristics, including size, depth, color, exudate, infection, tissue type, and so on, healthcare professionals can track changes, identify potential complications, and adjust treatment plans. If photo documentation is used, obtain patient consent according to organisational policy, ensure appropriate technique with adequate lighting and appropriate distance from the wound, and include a measuring guide in the photo.44 This ongoing evaluation is critical for evaluating the effectiveness of interventions and making informed decisions regarding wound management. When measuring surface area or volume, it is imperative to use a consistent technique regardless of technology.
Communication. Accurate wound assessments facilitate effective communication among healthcare professionals. When all team members have access to consistent and up-to-date wound documentation, they can work together to develop and implement a coordinated care plan, ensuring patients receive the best possible treatment. It is vital to use consistent terminology that is common to all disciplines. The International Classification of Diseases medical classification system is an example of a globally applicable standard.45
Legal and regulatory compliance. Proper wound assessment and documentation are essential to meet legal and regulatory requirements. Inaccurate or incomplete records can lead to legal issues and negatively impact a healthcare professional’s practice, even in resource-limited environments.
Reimbursement. In many healthcare systems, proper wound assessment documentation is tied to reimbursement-based funding models. Accurate and detailed records are often necessary to justify the use of specific wound care products or procedures and ensure organisations receive adequate reimbursement for services rendered.
Research and quality improvement. Wound assessment data are a valuable resource for research and quality improvement initiatives. This continuous learning process helps improve global wound care and patient outcomes.
Patient-centered care. Proper wound assessment and documentation are an essential component of patient-centered care. It ensures that patients’ conditions are thoroughly evaluated and their treatment plans are tailored to their specific needs. When patients observe that their healthcare provider is committed to documenting and monitoring their wounds, it can enhance trust and patient satisfaction.
To promote language consistency and enhance data clarity, an increasing number of enterprises are creating electronic wound assessment software and applications to reduce the time required for thorough documentation.43 These programs and applications (some more affordable than others) can provide the healthcare team with a structured set of parameters to ensure all clinical features are documented, thereby enhancing overall communication.46 Although these tools are an asset to healthcare professionals, they are not without risk, such as incorrect copying and pasting from previous reports/consult notes or patient data security risks. In areas where such programs and applications are not available, updating
the patient and providing written assessment and intervention plans may be warranted.
Statement 5: local wound care: debridement
5A. Healable wounds/cause corrected: Consider active sharp surgical debridement to bleeding tissue with adequate pain control only if it is within your scope of practice. This is undertaken with guidance from advanced wound care expertise only. If not available, consider conservative (sharp) debridement
5B. Maintenance wounds/nonhealable wounds: Consider conservative (sharp) debridement with adequate pain control only if it is within your scope of practice. Only remove loose hanging slough/debris when indicated and without causing any bleeding
5C. Determine if alternative debridement modalities for healable wounds are available (eg, autolytic, mechanical, enzymatic, and maggot biological options)
Debridement is an important process in the WBP paradigm to remove necrotic tissue and other biomaterials, including biofilm, in healable wounds and prevent odor and infection in maintenance wounds. For all wounds located below the knee, communicate the outcomes of any vascular testing (eg, ABPI, waveform) to all members of the interprofessional team, and document accordingly before attempting debridement because many types may be deleterious to the wound bed with reduced vascular supply.
For healable wounds, local wound bed interventions are best determined via the WBP paradigm based on the patient and wound characteristics. Consider surgical debridement (to bleeding tissue) as a first-line intervention. However, in many rural and remote regions, access to a skilled healthcare professional with the necessary education, knowledge, and judgment for this procedure may not exist.
Conservative (sharp) debridement (without causing bleeding) requires advanced knowledge and skills and is more suitable for nonacute care or specialty clinic settings. Only remove loose hanging or unattached debris from the wound without causing trauma to the wound bed.
Clinical sterile maggot debridement therapy is a limited treatment modality in resource-restricted environments, except in cases of accidental exposure. Maggot infestation is often discovered during dressing changes. Good debridement outcomes may result from accidental maggot therapy, particularly if the larvae are from the highly selective Lucilia sericata/cuprina bottlefly source, as they focus on devitalised tissue as their food source.47,48 Detrimental outcomes may present if the infestation is from the ordinary housefly (Musca domestica) or other invader species, as those larvae may indiscriminately destroy healthy tissue.47,48
Healthcare professionals should assess alternative methods of debridement (eg, autolytic, enzymatic, mechanical) for community sectors, including primary care, home care, and long-term care. Within available resources it is vital to consider patient safety, assess environmental factors, and identify barriers to wound healing before initiating debridement.
Appropriate debridement protocols for maintenance and nonhealable wounds differ significantly from those for healable wounds. Although moist wound healing provides an optimal environment for wound healing, it is a form of debridement (autolytic) that may be detrimental to nonhealable and maintenance wounds. Debridement is generally not a suitable intervention for stable maintenance or nonhealable wounds, because the goal is to keep those dry and free of infection.49 Consider debridement only when a maintenance or nonhealable wound becomes unstable to remove infected or necrotic wound debris in the most atraumatic manner possible.
Patient goals typically include enhancing comfort, minimising wound-related odor, reducing pain, and improving ADLs. Keeping the wound dry enables the formation of a protective layer, whereas debridement carries the risk of removing this protective layer and introducing pathogenic organisms.
Statement 6: local wound care: infection and inflammation
6A. Treat local/superficial wound infection (three or more NERDS criteria) with topical antimicrobials
6B. Manage deep and surrounding wound infection (three or more STONEES criteria) with systemic antimicrobials and concurrent topical antiseptics
6C. Consider anti-inflammatory agents in wounds with persistent ongoing inflammation (topical dressings or systemic medication)
The validated NERDS and STONEES criteria can guide the assessment and treatment of infection and inflammation in chronic wounds.50 Base the diagnosis of infection on clinical signs and symptoms rather than superficial wound swabs, which should be used only to guide antimicrobial selection in the event of an infection. If deep and surrounding tissue infection is suspected, identify the bacterial species and their sensitivity to commonly used antibacterial agents to help guide systemic antimicrobial use. This is especially true if a deep and surrounding infection is not responding to the empiric treatment.
The best tissue samples for wound bed culture swabs are obtained after cleaning the wound with potable water or saline and sampling the wound base without debris. A culture from tissue samples using a curette or other biopsy technique is most likely to represent the organisms in the wound tissue. Alternately, a semiquantitative swab technique using the Levine method can correlate to tissue biopsies.51 The swab is placed on granulation tissue and pressed enough to extract wound exudate and then rotated 360° to cover all surfaces of the swab. Placing the swab in the transport media to premoisten it prior to placing the swab on the skin may increase the bacterial yield for patients with low-exudate wounds.52
Pathogenic bacteria may infiltrate to the bone and cause osteomyelitis, which derails healing potential and is challenging to cure. A bone biopsy is the criterion standard to diagnose suspected osteomyelitis, because superficial cultures do not access the deep bone tissue, and imaging is limited by variable specificity.53 However, a bone biopsy may be uncomfortable, is dependent on skilled clinicians, and may extend the tissue damage. For these reasons, it frequently is not a feasible option, even more so if resources are scarce.
When deep wound infection is confirmed, antimicrobial dressings are appropriate to locally support systemic antibiotic therapy and prevent spread to the deep and surrounding compartment from surface bacteria. The five most common choices of antimicrobial dressings are silver, polyhexamethylene biguanide, iodine, methylene blue/crystal violet, and honey. Of these, silver and honey have additional anti-inflammatory properties.54
In some wounds, broad-spectrum antiseptics are applied for short-term rapid bacterial burden reduction to support systemic antibiotics. When the risk of infection outweighs the cytotoxic properties, low-cost povidone-iodine-moistened gauze changed daily over exposed bone can reduce surface bacteria. This is a short-term strategy accompanied by clinical evaluation for serum thyroid function levels especially when wound surfaces are large. However, with the newer low-toxicity antiseptics, other options are now available that are less aggressive but equally effective.
In general, wounds in immunocompetent patients that present for less than 1 month are treated with agents for Gram-positive coverage. Polymicrobial infections (typically seen in PWDs) or wounds longer than 1 month in duration call for broad-spectrum agents with Gram-positive, Gram-negative, and anaerobic coverage because these patients are often also immunocompromised.55
Cytotoxic agents may be appropriate for nonhealable wounds if the need for topical antimicrobial action is greater than the tissue toxicity. Antiseptics are generally preferred over topical antibiotics as part of antibiotic stewardship because of a lower risk of systemic bacterial resistance and adverse effects associated with contact irritant or contact allergic dermatitis.54
6D. Gently cleanse the wound with low-toxicity solutions (water, saline, noncytotoxic antiseptic agents).
The cleansing solution used depends on the characteristics of the wound and availability in practice. There is poor consensus in the literature on wound cleansing recommendations. An updated 2021 Cochrane review on cleansing solutions of venous leg ulcers concluded that there is a lack of randomised controlled trial evidence “to guide decision-making about the effectiveness of wound cleansing compared with no cleansing and the optimal approaches to cleansing of venous leg ulcers.”56 However, general wound care principles involve low-toxicity solutions including potable or preboiled water, saline, and other wound-friendly antiseptic agents.57 This avoids cytotoxic effects and damage to healthy granulation tissue in healable wounds.
Acetic acid diluted to 0.5% to 1.0% or hypochlorous acid can also be used in some cases in which an acidic environment is preferred (eg, for topical treatment of Pseudomonas aeruginosa).58 Based on the healability classification of the wound, antiseptic agents with some tissue cytotoxicity may be used after a positive risk-benefit assessment. This includes agents such as low-concentration chlorhexidine or its derivative polyhexamethylene biguanide and povidone-iodine. This may be beneficial in cases of maintenance and nonhealable wounds that have a high potential for infection. Further, these agents can be used to manage odor and exudate in addition to controlling bioburden. In resource-limited environments, consider wound hygiene measures and how solutions are prepared, stored, and distributed to patients to prevent cross-contamination.
There is emerging interest in the use of surfactants to remove biofilms that often exist within wound debris and have two surfaces of different viscosity (Supplemental Table 2, http://links.lww.com/NSW/A177). Wound irrigation remains a controversial topic for use in chronic wounds. However, expert opinion is not to irrigate wounds if the base of the wound is not visible to avoid accumulation of the irrigation solution in closed spaces and accidental enlargement of the wound.57 Irrigate wounds with an adequate solution volume (50-100 mL per centimeter of wound length).59
Statement 7: local wound care: moisture management
7A. Maintain moisture balance in healable wounds with hydrogels, films, hydrocolloids, hydrofibers, alginates, and foams
7B. Institute moisture reduction with fluid-lock mechanisms in healable wounds using superabsorbents to wick moisture away from the surface (diaper technology)
7C. Determine if wound packing is needed for healable wounds. It could be wet (donate moisture) or dry (absorb moisture)
7D. Establish a targeted moisture reduction protocol in maintenance and nonhealable wounds to reduce bacterial proliferation
Maintaining moisture balance is complex and depends on the wound type and healing classification. Consider moisture balance, infection control, and patient education in selection of dressing materials.60 Incorporating and tailoring moisture management strategies to the specific wound type and the resources available can optimise patient outcomes and minimise complications (Table 6).3,54 Further research and clinical studies should continue to refine our understanding of wound moisture management to enhance wound care practices in the future.3,54
Table 6. Goals of moisture management based on wound healability3,42,54
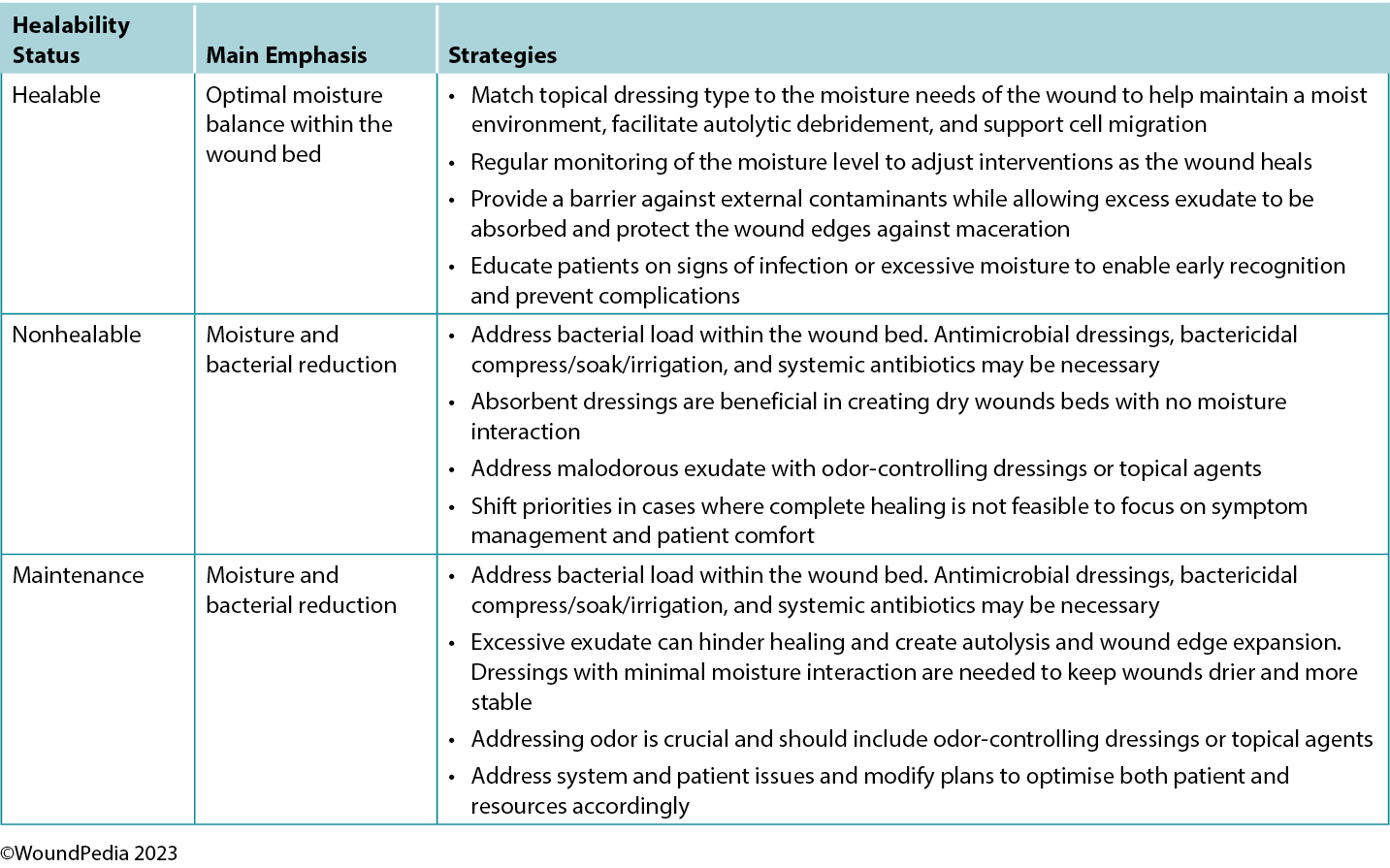
In general, as the level of exudate increases, so should the moisture absorbency or transferring capability of the dressing.3 Moisture-balance dressing options can be combined with antibacterial and anti-inflammatory properties to further meet the wound needs.
The choice of dressing for maintenance and nonhealable wounds should prioritise comfort while avoiding fluid donation to the wound bed and maceration of the wound edges. These wounds require regular reassessment for any progress or deterioration and should be managed to reduce bacterial load. Depending on wound evolution and characteristics over time, dressings may need to be adapted.
Statement 8: Healing trajectory
8A. Consider that healable wounds should be at least 20% to 40% smaller by week 4 to heal by week 12. If factors are present that affect healing time (poor glycemic control, for example), additional healing time may be required
8B. Allocate additional time to healing beyond 12 weeks in healable wounds if there are limited available resources, and continue with consistent care
8C. Prioritise referral to specialist centers (when available) for diagnostic testing and/or a skin biopsy, especially when faced with severe resource restrictions
Wound healing trajectories are useful and necessary for evaluating the needed time to heal, especially using clinical data (measurements) for both acute and chronic wounds. The healing trajectory is based on accurate and consistent wound measurements that determine the wound surface area closure over time. This helps to distinguish wound progression, stalled wounds, and worsening wound status.
Healable acute wounds should be completely closed within 30 days. Expect chronic healable wounds to have a 20% to 40% edge advancement at 30 days (4 weeks) and to close within 12 weeks.3,42,61,62 Nonhealable wounds have no defined time allocated to close, no edge advancement is expected, and all initiated steps are to prevent further deterioration. Maintenance wounds are not expected to heal nor deteriorate, and wound healing may progress slowly without a fixed time expectation unless patient/institution/system optimisation is achieved.
Re-evaluate hard-to-heal wounds periodically for alternate diagnoses. In these cases, consider wound biopsy, further investigation, and/or referral to an interprofessional assessment team. A healing trajectory can be assessed in the first 4 to 8 weeks to predict if a wound is likely to heal by week 12, provided there are no new complicating factors.63 Changes in the wound, the individual, or the environment may necessitate the reclassification of a wound to the maintenance or nonhealable category.
Statement 9: Edge advancement
9A. Consider locally constructed active modalities according to the required mechanism of action and the specific indications for initiating an adjunctive therapy to support wound healing
9B. Decide on adjunctive therapies through an interprofessional team approach and include a prior risk-to-benefit analysis
Select adjunctive therapies according to healability. Initiate these as soon as possible after injury in persons with major trauma to prevent sequelae of long chronicity. Select modalities using an interprofessional team approach based on what is available and the physical mechanism required (while ensuring trauma tissue healability). In hard-to-heal wounds, the wound may need a second chance to heal after reassessment.42 Ensure informed consent is a part of adjunctive therapy decisions.
A risk-to-benefit and cost-effectiveness analysis is helpful and will add in system sustainability. The key to effective adjunctive modality decisions is based on the risk it poses to initiate the therapy (physical discomfort, financial hardship, patient adherence) versus the benefit it will provide (tissue oxygenation, wound contraction, edema reduction, cellular reactivation).42,64 The best risk-benefit decisions are made within an interprofessional team including the patient, ensuring group commitment and treatment completion within optimal use of resources.
Optimising resources, or the slight repurposing thereof, may lead to creative strategies in the hands of interprofessional teams to tailor-make solutions to ensure all patients are optimally treated despite resource restrictions.
Surgery. Even in the most restricted environments, this is the one modality that is mostly available within a medical catchment area, often in tertiary care settings with referrals received from primary care clinics to provide debridement, general surgery with primary/tertiary intention closure, skin grafts, and/or amputations.
Skin grafts may be available in resource-restricted environments as an advanced modality to achieve tissue closure to reduce healing times and prevent recurrent deep wound infections. The procedure can minimise the extensive use of dressing materials over a prolonged period and reduce primary care chronic wound workload. Skin graft decisions are often made to preserve body functionality and promote early wound closure above aesthetic outcomes.65 However, avoid skin grafts for ischemic wounds and most venous stasis ulcers; consider them only in wounds where a favorable outcome could be expected.66,67
Electrical stimulation. Wound healing can be accelerated by enhancing the natural electrical current present in injured skin. In resource-limited environments, this modality should be investigated for wound healing because of its high-level evidence base and availability of devices of this nature (direct current, alternating current, low-intensity direct current, pulsed electromagnetic fields, high-voltage pulsed current, and transcutaneous electrical nerve stimulation devices). The evidence supports increased cellular proliferation and increased microcapillary perfusion, as well as a reduction in bacterial burden and infection on treated wound beds.68
Wall-mounted negative-pressure wound therapy. This can give the healthcare professional control over exudate management and accuracy in fluid replacement for inpatients with high exudate and large tissue defects. Start with the lowest possible pressure (minus 50-80 mm Hg). The patient becomes bedbound for the modality to be maintained, and the base layer (often gauze or petrolatum-impregnated dressings) needs to be replaced at least daily. This, together with starting on the lowest possible negative-pressure setting, will prevent mechanical trauma to the wound bed from tissue adherence and traumatic dressing removal in cases where nonadherent base layers are not available.69 There are now disposable negative-pressure wound therapy devices designed for use in the community as well as do-it-yourself options that can render acceptable clinical outcomes.70,71
Breathing high-flow, highly concentrated oxygen. Oxygen is often overlooked as a legitimate wound healing modality.72 Ironically, it is rarely used, although nearly all formal healthcare settings have copious amounts of oxygen available, even in relatively resource-poor environments. The availability of oxygen concentrators has also increased because of the COVID-19 pandemic, making oxygen administration also a possibility on an outpatient basis in home-based settings.73 Although hyperbaric oxygenation is the most effective means of increasing plasma oxygen concentration and tissue oxygen delivery, this modality is not always readily available. However, providing normobaric (ward) oxygenation still produces a 7.5-fold increase in plasma-borne oxygen (ie, from 0.3 mL/dL to 2.3 mL/dL; Table 7).74 Moreover, intermittent inhalation of 100% oxygen in patients without chronic obstructive pulmonary disorder (eg, 6 hours on/2 hours off by nonrebreather mask) over 3 to 4 days is not harmful to the lungs and may provide significant additional oxygen substrate, while the intermittent increase and decrease in oxygen delivery activate the expression of hypoxia-inducible factor (a strong stimulus for angiogenesis).75 This would suggest that in lieu of hyperbaric oxygen therapy, normobaric oxygen is justified for mitigating conditions on the FDA-approved list of indications for hyperbaric oxygen (Table 7).76 This may include tissue reperfusion injuries (eg, crush injuries, compartment syndromes before and after surgical release); bacterial toxin inhibition (ie, infective myonecrosis or other anaerobic infections); or large-tissue defects (after debridement to maintain the reactivated inflammatory response for up to 48 hours). Normobaric oxygen provides 50% of the Po2 of typical hyperbaric oxygen therapy (at 2 atmospheres); however, many of the pharmacologic effects of oxygen are achieved only under hyperbaric dosages.77,78
Table 7. Normobaric oxygen therapy mechanisms and delivery systems
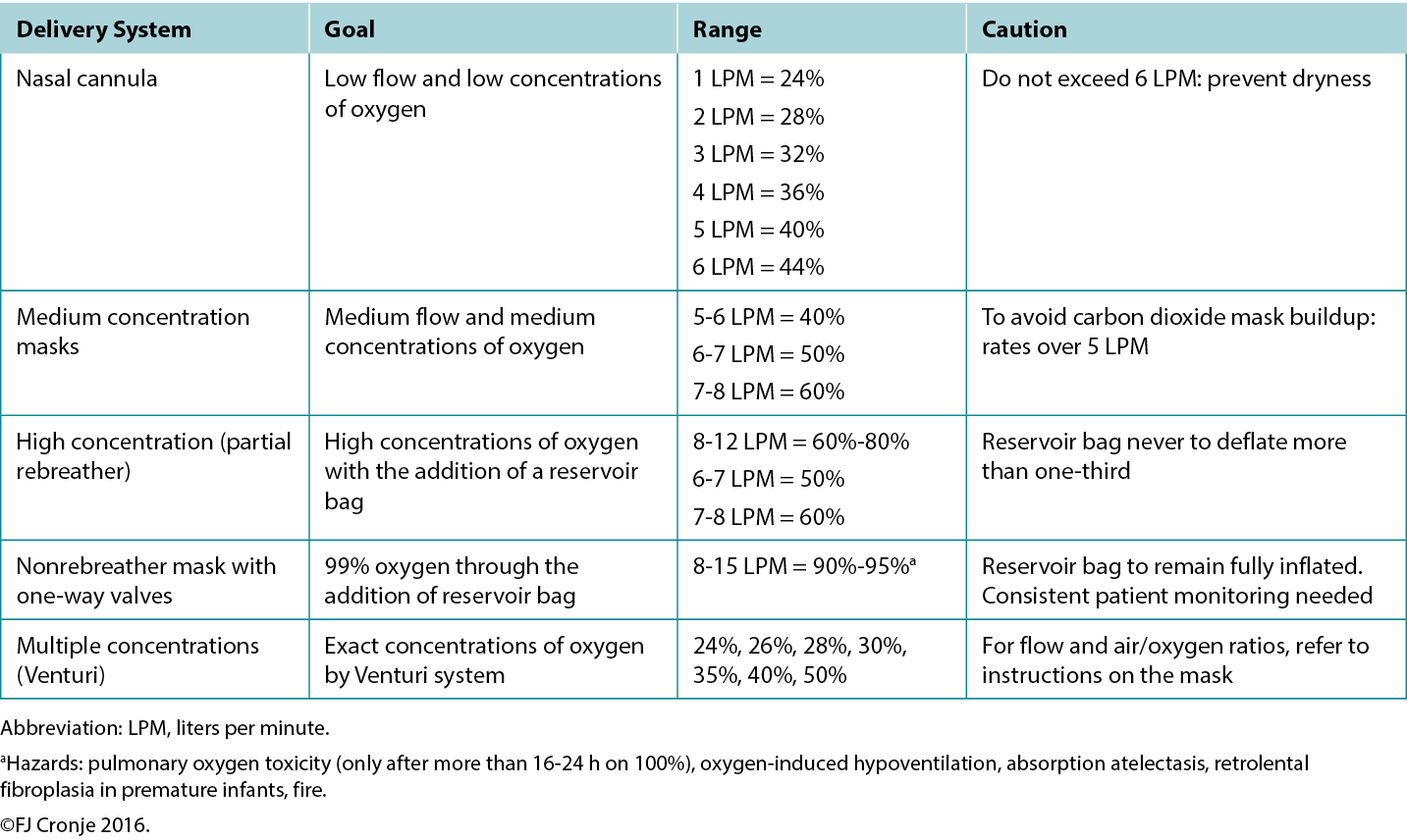
Note that topical oxygen administration directly to a wound does not have the same physiologic effects attributed to systemic oxygen delivery.79 Topical oxygen delivery systems remain subject to ongoing research to determine their beneficial actions beyond improved epithelialisation and possibly a mild antiseptic effect.64 The latter effect has also been attributed to ozone therapy.80 A systematic review completed in 2018 indicated that these therapies could potentially elicit mild oxidative stress or disinfection but that the risk of toxicity due to uncontrolled reactive oxygen species is high.81 Within the limited-resource environment, these devices and use thereof are likely uncontrolled.
Statement 10: Healthcare system change
10A. Facilitate evidence-informed, culturally competent, and equitable care for all patients
10B. Improve provider skills for wound management competency to enhance patient outcomes
10C. Establish timely and effective communication that includes the patient and all interprofessional wound care team members for improved healthcare system wound outcomes
Globally, chronic wound management consumes a significant portion of healthcare resources; preventive care represents the most cost-effective strategy for reducing healthcare system expenditures. There are numerous approaches to integrating preventive care into practice. For instance, DFUs are notorious for leading to high amputation rates and morbidity worldwide, even though many DFUs are preventable. Although diabetes was initially believed to be most prevalent in developed countries, it is noteworthy that 80% of diabetes-related deaths occur in countries with limited resources.82 A validated screening tool, an educated and available interprofessional team, and the implementation of prevention algorithms can be used in countries regardless of the availability of resources.83-85 Other organisational strategies that could be implemented include the following.
Patient navigation. Managing a DFU requires continual support from a circle of care that includes family members and healthcare professionals (including home care and wound care) working as a team. Timely access to both health and social services is often necessary to prevent and heal DFUs. Regionalised, community-based integrated diabetes services linked to interprofessional wound care clinics are proving to be most successful.86
One effective way to ensure optimal and timely care is patient navigation. This concept is adaptable to all healthcare sectors and can improve the timely diagnosis and treatment of wound infections, optimise pain management, and increase access to specialised care, thereby expediting wound closure rates.87 Patient navigation is becoming a vital component of integrated care, facilitating seamless transition between sectors and enhanced clinical outcomes. Further, it is accompanied by a boost in morale for both patient and healthcare professional, decreased nonacute hospital admissions or readmissions, enhanced patient quality of life, and improved adherence to treatment protocols. All these factors combined generate significant cost savings to healthcare systems.87,88
A critical element of successful patient navigation programs is the inclusion of a comprehensive and systematic approach to guide healthcare professionals in assessing and delivering care to each individual patient (eg, the WBP framework). These pathways do not need to be complicated or time consuming, but should ensure specific criteria are met, including regular foot care for those at high risk of amputation, glycemic control to an HbA1c less than 9%, and a BP less than 130/90 mm Hg.23,89
Policy interventions. Organisational policies that detail and provide guidance on best practice interventions and pathways are crucial for the successful and sustainable implementation of wound care protocols. Base these policies on current published guidelines for each specific wound type and translate them into the environment they need to serve. The institution needs to accept them as standards of practice and be approved as such to serve as evidence-based care in environments in which other guidelines may not be successfully adopted because of cultural or language translation challenges. Further, these policies must clearly outline the process for entering and using data, as ongoing quality improvement initiatives are based on data to improve and maintain effective care processes.
Adapted wound care. Although the delivery of care should be adapted to the unique needs of each healthcare sector, certain concepts should be standard, particularly those that enhance effective communication both within and across sectors. The increased adoption of digital technology expedites assessments, enhances access to specialised care, and optimises the allocation of limited resources.90 Where adaptations are implemented as care processes, these practices should be well documented as care standards and be easily accessible to ensure consistency and continuity of care within respective institutions.
Delphi consensus highlights
Some important comments from the panel:
- The ability to heal (healability) is a changeable modality and not to be seen as a static classification as patient condition, circumstances, and choices drive the classification allocation process (3A).
- The adjustment of practice as required in maintenance wounds incorporates the establishment of a conservative wound bed approach, with attention to the allowances the patient is willing to make within their life choices to slowly ensure patient optimisation and subsequently increase host competence (3B).
- When the method of patient documentation is agreed upon within an institution, it should be uniformly used to prevent communication gaps between providers that may inadvertently cause a negative impact on patient care outcomes (4A).
- Antiseptic mouth washes suitable for mucosa are often also friendly for use on a wound bed (4B). This may be considered off-label use.
- The choice for topical bacterial burden control should be on topical (low) toxicity antiseptics (the five most important ones), depending on the ability to heal and bacterial burden priorities to be addressed. Refrain from using topical antibiotic preparations, ointments, and creams on chronic wounds because those preparations are often focused only on Gram-positive organisms and would allow Gram-negative and anaerobic organisms on the wound bed to multiply freely. Further, topical antibiotic preparations need only one mutation to create systemic resistance to the targeted organism. Topical antibiotics are often in a carrier medium that is associated with contact irritant or contact allergic dermatitis (6A and 6B).
- When a healable wound has a significant moisture burden and remains in need of superabsorbent dressings to control the moisture balance of the wound bed, the wound needs thorough reassessment to ensure all underlying causes have been corrected for (7B).
- In establishing an interprofessional team, use any means of communication to build and maintain such a team as that could significantly optimise local capacity despite distances between providers and specialists to increase clinical outcomes despite local limitations (9B).
Conclusions
Optimise chronic wound care in resource-limited environments by initiating small adaptations and creative interventions without compromise to the core principles of care required. Interprofessional wound care teams can serve as a virtual resource to isolated and remote communities to improve clinical outcomes. All of the critical elements for (diabetic) foot management and care can easily be incorporated into diverse environments by increasing local capacity and providing clinician education and culturally appropriate patient empowerment.
Practice pearls
- The holistic care of PWDs includes the optimisation of HbA1c levels, BP, cholesterol levels, and drugs with cardiac- and renal-protective properties.
- The audible handheld 8-MHz Doppler pulse signal is a suitable bedside test for arterial blood supply to the lower limbs. It can be performed as a modification of the traditional ABPI, and the pulse sounds are easy verifiable by remote expert team members using MP3 or MP4 recordings from a cellphone.
- The NERDS and STONEES mnemonics can guide diagnosis and treatment of local/deep and surrounding infection, including an oral antibiotic indication for osteomyelitis.
- Plantar pressure redistribution can be accomplished from innovative, less costly alternatives such as soft felted simple inserts, to the total contact cast and removable cast walker made irremovable if the latter are unavailable or unsuitable for patient preferences or ADLs.
- Integrated coordinated care teams can connect with virtual expertise by equipping healthcare professionals with skills in patient navigation.
- Toolkits containing enablers for practice along with 8-MHz Dopplers and infrared thermometers can facilitate care in resource-limited settings.
Conflict of Interest
The authors declare no conflicts of interest.
Funding
The authors received no funding for this study.
Preparação do leito da ferida 2024: Consenso Delphi sobre o tratamento das úlceras do pé em contextos de recursos limitados
Hiske Smart, R Gary Sibbald, Laurie Goodman, Elizabeth A Ayello, Reneeka Jaimangal, John H Gregory, Sadanori Akita, Afsaneh Alavi, David G Armstrong, Helen Arputhanathan, Febe Bruwer, Jeremy Caul, Beverley Chan, Frans Cronje, Belen Dofitas, Jassin Hamed, Catherine Harley, Jolene Heil, Mary Hill, Devon Jahnke, Dale Kalina, Chaitanya Kodange, Bharat Kotru, Laura Lee Kozody, Stephan Landis, Kimberly LeBlanc, Mary MacDonald, Tobi Mark, Carlos Martin, Dieter Mayer, Christine Murphy, Harikrishna Nair, Cesar Orellana, Brian Ostrow, Douglas Queen, Patrick Rainville, Erin Rajhathy, Gregory Schultz, Ranjani Somayaji, Michael C Stacey, Gulnaz Tariq, Gregory Weir, Catharine Whiteside, Helen Yifter, Ramesh Zacharias
DOI: 10.33235/wcet.44.1.13-35
Resumo
Antecedentes O tratamento de feridas crónicas em locais com poucos recursos merece uma atenção especial. Os contextos rurais ou com poucos recursos (ou seja, os contextos com necessidades básicas/fornecimentos de cuidados de saúde limitados e disponibilidade inconsistente de membros de uma equipa interprofissional) podem não ser capazes de aplicar ou replicar as melhores práticas dos contextos urbanos ou com muitos recursos.
Objetivo Os autores associaram experiência mundial para o desenvolvimento de uma aplicação prática e cientificamente sólida do modelo de preparação do leito da ferida em comunidades sem recursos ideais.
Métodos Um grupo de 41 especialistas em feridas de 15 países chegou a um consenso sobre a preparação do leito da ferida em ambientes com recursos limitados.
Resultados Cada declaração de 10 conceitos-chave (32 subcategorias) obteve um consenso de mais de 88%.
Conclusões As declarações de consenso e os fundamentos podem orientar os profissionais na prática clínica e na investigação em locais com poucos recursos. Estes conceitos devem estimular a inovação contínua para a melhoria dos resultados dos doentes, assim como a eficiência do sistema de saúde para todas as pessoas com úlceras nos pés, especialmente em pessoas com diabetes.
Objectivo geral
Analisar uma aplicação prática e cientificamente sólida do modelo de preparação do leito da ferida em comunidades sem recursos ideais.
Público-alvo
Esta atividade de formação contínua destina-se a médicos, assistentes médicos, enfermeiros e enfermeiros com interesse no tratamento de pele e de feridas.
Objectivos de aprendizagem/resultados
Depois de participar nesta atividade educativa, o participante irá
1. Resumir as questões relacionadas com a avaliação de feridas.
2. Identificar uma classe de medicamentos para o tratamento da diabetes mellitus tipo II que tenha demonstrado conseguir melhorar a glicémia, a nefroprotecção e os resultados cardiovasculares.
3. Sintetizar estratégias para o tratamento de feridas, incluindo o tratamento em ambientes com recursos limitados.
4. Especificar o tempo previsto para o avanço do bordo em feridas crónicas e cicatrizáveis.
Introdução
Em 2000, foi introduzida uma estrutura para a preparação do leito da ferida (WBP), de forma a enfatizar o tratamento da pessoa como um todo como base do tratamento local ideal de feridas.1 À medida que esta estrutura evoluiu para uma estrutura internacional, tornou-se claro que nem todas as feridas são curáveis. Estes conceitos de manutenção e de feridas não cicatrizáveis levaram a revisões dos princípios locais de tratamento de feridas e à expansão do WBP. A importância de cuidados coordenados e integrados, com enfermeiros, médicos e profissionais de saúde afins a trabalharem conjuntamente para otimizar os resultados dos cuidados prestados aos doentes e a utilização do sistema de saúde, foi fundamental para o desenvolvimento do WBP.
Este artigo centra-se na aplicação da estrutura WBP para gerir feridas relacionadas com os pés, particularmente em pessoas com diabetes (PWDs), úlceras neuropáticas do pé relacionadas com a lepra e outras complicações que incluem a neuropatia e a doença vascular. Em pessoas com diabetes são críticos vários parâmetros, incluindo o mau controlo glicémico, as alterações da PA, o colesterol elevado, a redistribuição inadequada da pressão plantar, as infecções e a falta de exercício. Os efeitos do tabagismo são também particularmente prejudiciais para salvar os membros e as vidas das pessoas com diabetes.
É fundamental para este artigo estabelecer uma definição para os contextos com recursos limitados, incluindo a baixa disponibilidade de recursos, a falta ou restrição de financiamento, os contextos remotos, isolados ou rurais e as populações indígenas. Todos estes termos estão relacionados com contextos de cuidados de saúde em que podem existir dificuldades em aceder a materiais, equipamento, especialistas e a competências e aptidões avançadas no tratamento de feridas. Os locais com poucos recursos podem estar presentes em qualquer parte do mundo e não se limitam aos países com baixos rendimentos ou aos países em desenvolvimento.
O processo Delphi subjacente a este trabalho alargou e desenvolveu o quadro WBP no seu formato atual. Quarenta e um autores de 15 países participaram no processo Delphi, o qual decorreu em duas rondas, utilizando uma escala de tipo Likert de quatro partes (1, concordo totalmente; 2, concordo; 3, discordo; 4, discordo totalmente). A primeira ronda foi constituída por 29 afirmações. Embora todas as declarações tenham excedido o nível de consenso desejado de 80%, houve 299 comentários considerados pelo grupo principal de autores. Foi utilizado um editor profissional para melhorar a compreensão e a exatidão gramatical das afirmações, antes de se realizar a segunda ronda Delphi com 32 afirmações construídas. Todas as afirmações ultrapassaram um nível de consenso de 88%.
Na segunda ronda, 14 afirmações obtiveram 100% de consenso. Uma afirmação destacou-se e foi classificada como "concordo totalmente" por todos os membros do painel Delphi: 10C. Estabelecer uma comunicação atempada e eficaz que inclua o doente e todos os membros da equipa interprofissional de tratamento de feridas, de forma a melhorar os resultados do sistema de cuidados de saúde. Paralelamente, cada um dos peritos internacionais em feridas trabalhou em grupos para o desenvolvimento do conteúdo do manuscrito. Consultar o Tabela Suplementar 1 (http://links.lww.com/NSW/A176) para as declarações de consenso.
O consenso visava estabelecer um padrão mínimo de cuidados, com base científica, que pudesse ser optimizado em função dos recursos disponíveis. Consulte a Tabela 1 para visualizar as 10 etapas principais e 32 subtópicos para feridas em ambientes de recursos limitados. Este processo de consenso actualizou o quadro de forma que o WBP seja aplicável independentemente da disponibilidade de recursos. Além disso, inclui também pela primeira vez os conceitos de trajectórias de cura e de mudança do sistema de saúde (Figura 1).
O resto do presente relatório destacará as 10 declarações de consenso e discutirá a fundamentação de cada declaração.

Figura 1. Preparação do leito da ferida 2024. ©WoundPedia 2023
Tabela 1. Preparação do leito da ferida para feridas abaixo do joelho em ambientes com disponibilidade limitada de recursos
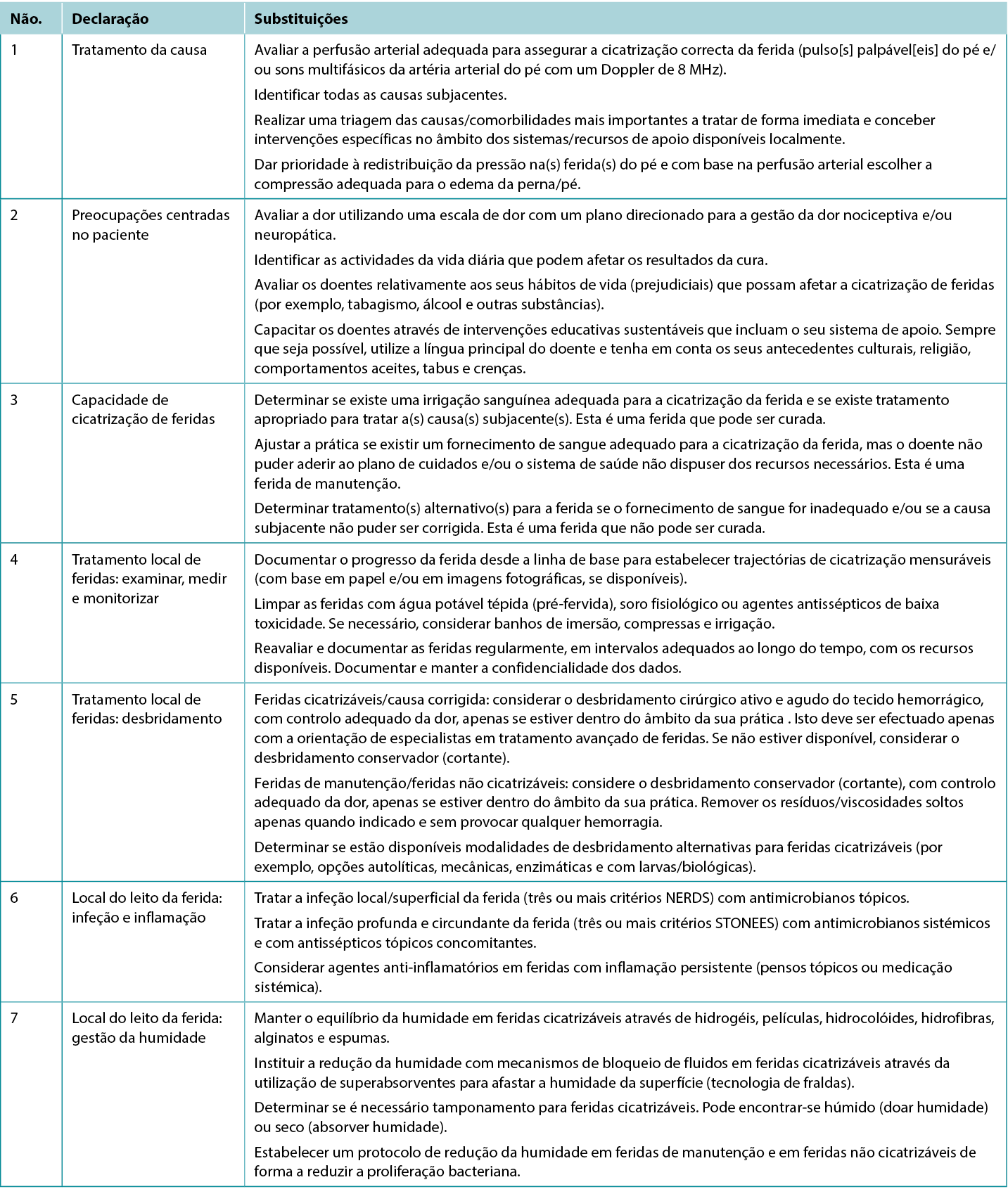

Declaração 1: tratamento da causa
1A. Avaliar a perfusão arterial adequada para garantir a cicatrização correcta da ferida (pulso(s) palpável(eis) do pé e/ou sons multifásicos da artéria arterial do pé com um Doppler de 8 MHz)
Para poder determinar o fluxo sanguíneo nos membros inferiores, a primeira ação vital é encontrar um pulso palpável no pé. Iniciar com os pulsos dorsalis pedis e/ou tibial posterior. Se estiver disponível um Doppler portátil de 8 MHz, confirmar os padrões de fluxo multifásico (bifásico/trifásico). Referenciar para especialistas vasculares quando se observar um som Doppler monofásico ou ausente ou quando os pulsos do pé não são palpáveis. Outros sinais de perfusão arterial inadequada são a dor nos membros inferiores em repouso e as alterações isquémicas dos membros (extremidade fria com rubor dependente que branqueia com a elevação).
As pessoas com diabetes são susceptíveis a terem problemas microvasculares (neuropatia periférica, alterações do pé de Charcot) e a complicações macrovasculares, incluindo a doença arterial periférica (DAP). Estas condições contribuem para a formação de calosidades, úlceras nos pés e perda de tecido misto. Uma vez que até 50% das populações susceptíveis têm diabetes e DAP,2 a identificação atempada da DAP é fundamental (através de exame físico e de testes vasculares), pois é um fator de risco importante para a má cicatrização de úlceras e para amputação. Se detectada, a revascularização imediata (angioplastia ou bypass vascular) é vital para restaurar o fluxo arterial adequado ao pé. A avaliação adicional pode incluir o tempo de enchimento capilar, um teste de branqueamento de Buerger (pálido na elevação, rubor vermelho vivo na dependência) e claudicação ao caminhar.
Exame vascular. Nos casos de insuficiência arterial, a extremidade é frequentemente fria ao toque devido ao fornecimento insuficiente de nutrientes e de oxigénio (Tabela 2). Os casos graves podem manifestar necrose tecidular, a qual se apresenta sob a forma de úlceras, teias maceradas dos dedos dos pés (frequentemente com infeção secundária), fissuras ou gangrena. Outros indicadores de casos graves incluem a palidez à elevação da perna, claudicação induzida pelo exercício que se resolve com o repouso, cianose ou rubor dependente e a atrofia muscular. Em particular, o edema dos membros inferiores é mais indicativo de problemas venosos do que arteriais. As lesões arteriais são geralmente perfuradas, com uma base profunda que contém frequentemente tendões, enquanto as úlceras venosas apresentam uma morfologia irregular dos bordos com uma base de tecido de granulação pouco profunda.3
Tabela 2. Fornecimento vascular necessário para a cicatrização dos tecidos
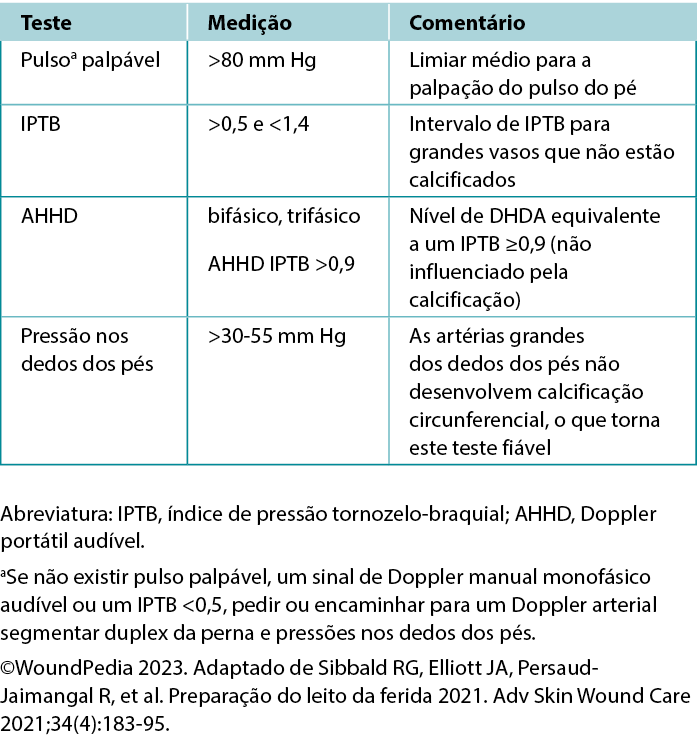
Exame do índice de pressão tornozelo-braquial (IPTB). O IPTB mede o rácio da PA sistólica do tornozelo, dividido pela PA sistólica braquial utilizando um Doppler de 8 MHz. O procedimento envolve a utilização de uma braçadeira de PA e o registo da PA sistólica quando os sons arteriais reaparecem após a insuflação da braçadeira. No entanto, factores como o edema, a inflamação e a calcificação arterial podem afetar a sua precisão. Se um Doppler de 8 MHz não puder ser comprado/obtido, o encaminhamento precoce para um centro de avaliação terciário torna-se prioritário nos casos em que se verifica a ausência dos pulsos do pé. Em certos contextos de cuidados de saúde, continua a ser necessário efetuar um IPTB como avaliação de quantificação vital antes de se iniciar qualquer intervenção nos membros inferiores.
Exame Doppler manual audível (AHHD). Em determinados contextos, um AHHD pode ser facilmente adicionado como parâmetro adicional, caso os prestadores de cuidados de saúde optem por um teste mais simples e mais rápido (não influenciado pela calcificação, sem necessidade de apertar uma barriga da perna dolorosa e sem necessidade de estar deitado durante 20 minutos). A avaliação AHHD também pode fornecer resultados precisos em caso de amputação de dedos grandes do pé e ser gravada como um ficheiro MP3 ou MP4 e transferida para verificação remota da interpretação do sinal.
Os profissionais de saúde devem aplicar o gel nos locais apropriados de pulsação do pé, com uma sonda Doppler de 8 MHz posicionada num ângulo de 45°em relação à pele nas artérias dorsal do pé, tibial posterior e peroneal. Os sinais/formas de onda Doppler adquiridos podem então ser analisados (através de um som audível ou de traçados visuais): Um tutorial completo sobre o procedimento AHHD está disponível online em https://journals.lww.com/aswcjournal/Pages/videogallery.aspx?videoId=20. Otimizar a qualidade do sinal com o reposicionamento cuidadoso da sonda para obter um sinal mais alto ou mais multifásico.
Uma forma de onda monofásica ou ausente justifica uma avaliação vascular completa, incluindo um Doppler arterial segmentar duplex da perna em laboratório vascular. Uma forma de onda multifásica indica tipicamente a ausência de doença vascular periférica.4 Em diabéticos, interpretar o rácio IPTB com precaução (devido a arteriosclerose ou a calcificação arterial); os resultados multifásicos da AHHD são uma escolha preferível para se confirmar o fornecimento adequado de sangue para a cicatrização da ferida. Uma forma de onda multifásica (bifásica, trifásica) sugere um valor de AHHD equivalente a um IPTB normal ≥0,9.
Embora a AHHD seja eficaz na exclusão de doença arterial, pode não identificar os défices de perfusão segmentar existentes - ilhas de isquemia ou defeitos nos angiossomas.5 Por conseguinte, o exame físico do pé e do membro inferior é vital para se conseguir um diagnóstico conclusivo. Os profissionais de saúde podem registar os sinais AHHD e transmiti-los a especialistas, facilitando avaliações síncronas ou assíncronas à distância. As avaliações síncronas permitem o envolvimento do doente em tempo real e a tomada rápida de decisões.
Insuficiência venosa crónica. A insuficiência venosa crónica pode coexistir em pessoas com diabetes e com úlceras nos pés. Afecta principalmente os membros inferiores e prejudica o retorno do sangue desoxigenado ao coração e aos pulmões. Esta doença resulta frequentemente de uma disfunção da válvula venosa, a qual pode ser desencadeada por factores como a gravidez ou o aumento de peso. Os sintomas incluem habitualmente varizes, edema, descoloração da pele devido à hemossiderina, lipodermatosclerose e úlceras venosas.6 Estas úlceras podem ser de qualquer tamanho (desde pequenas a circunferenciais) e formam-se rapidamente sobre áreas de acumulação venosa, normalmente na face medial dos membros inferiores.
A pedra angular do tratamento das úlceras venosas é a terapia de compressão. Isto compensa a disfunção da válvula, permitindo aumentar a ação peristáltica da bomba muscular da barriga da perna. Outras medidas incluem a elevação das pernas e a caminhada. Os procedimentos ablativos venosos podem ser considerados quando as úlceras são atribuídas a veias superficiais. O edema venoso não tratado pode atrasar a cicatrização da úlcera do pé.7
Para a otimização médica da DAP, as principais estratégias incluem o controlo ideal da PA, o início de medicação para o colesterol e, frequentemente, o início de terapêutica com estatinas. Estudos recentes também recomendam o tratamento de doentes com DAP e doença arterial coronária ou doença carotídea concomitante utilizando uma combinação de aspirina em dose baixa (91-100 mg PO diariamente) e de rivaroxabano em dose baixa (2,5 mg PO BID).8 Outros factores modificáveis são a cessação do tabagismo e programas de caminhada ou exercício. Para os doentes com uma úlcera no pé (especialmente nas pessoas com diabetes), é essencial uma redistribuição ou descarga adequada da pressão plantar.
1B. Identificar todas as causas subjacentes
As complicações do pé são motivo de grande preocupação para as pessoas com diabetes e representam um peso significativo para os sistemas de saúde. Uma abordagem holística é representada pela mnemónica AIG (avaliação, identificação, gestão) e centra-se no tratamento ou na mitigação da causa subjacente dos problemas do pé diabético, especialmente a neuropatia. A aplicação de uma abordagem de avaliação focalizada como norma de base dos cuidados (VIPS: vascular, infeção, pressão, desbridamento cirúrgico) é crucial para a prevenção de complicações graves, incluindo ulcerações nos pés, amputações dos membros inferiores e um aumento da incidência de morte precoce/prevenível. Alguns elementos críticos relacionados com os pés em locais com poucos recursos incluem apresentações tardias aos cuidados formais, diagnóstico tardio,9 andar descalço, feridas negligenciadas e a ausência de cuidados preventivos com os pés. Uma análise observacional de base hospitalar realizada na Etiópia identificou vários factores que contribuem para as complicações do pé diabético,10 incluindo humidade elevada, deformidade do pé, neuropatia, úlceras activas não identificadas, calçado inadequado ou mal ajustado, má higiene dos pés (por exemplo, fungos nos pés e nas unhas dos pés) e falta de sensibilização para os cuidados com os pés. Uma revisão sistemática sobre úlceras plantares entre pacientes com hanseníase (n = 7 estudos) identificou os seguintes fatores de risco para o desenvolvimento de úlceras: incapacidade de sentir um monofilamento de 10 g no teste sensorial, deformidades graves do pé ou hiperpronação, baixa escolaridade e desemprego.11 Enfrentar esses desafios em qualquer ambiente com recursos limitados requer uma abordagem multifacetada, a qual pode incluir a educação do paciente e dos profissionais de saúde, deteção precoce, acesso a cuidados, programas de calçados e envolvimento da comunidade.
As avaliações regulares e completas dos pés incluem a deteção de neuropatia (perda da sensação de proteção), problemas vasculares (circulação sanguínea deficiente ou ausente nos membros inferiores), sinais de infeção, áreas de pressão elevada (formação de calos) e fricção (bolhas, muitas vezes com componentes hemorrágicos) para assim facilitar intervenções atempadas. A ferramenta de rastreio simplificada de 60 segundos pode ser um meio valioso para avaliar, estratificar e acompanhar rapidamente os doentes com base nos seus níveis de risco e sem custos significativos.12 Os doentes com antecedentes de ulceração, amputação, cirurgia vascular periférica ou neuroartropatia de Charcot correm o maior risco de rutura da pele, pelo que devem receber atenção adicional para evitar ulcerações e outras complicações.
Para poder detetar a infeção, podem ser úteis os critérios NERDS (infeção superficial da ferida: não cicatrização, exsudado, tecido de granulação vermelho e friável, detritos, odor) ou STONEES (infeção profunda e circundante da ferida: tamanho aumentado, temperatura 3 °F mais quente, os [sonda no osso], novas áreas de rutura, eritema >2, exsudado, odor), juntamente com a utilização de termometria de infravermelhos sem contacto.13 Temperaturas elevadas de 3 °F em comparação com o membro oposto podem indicar inflamação e um pé com maior risco de ulceração.13 Uma alteração comparativa de 1,67 °C é clinicamente difícil de medir. Este mesmo resultado numa pessoa com uma úlcera na perna ou no pé tem oito vezes mais probabilidades de significar uma infeção profunda e circundante quando é acompanhado de dois ou mais critérios STONEES adicionais.13
Os doentes com neuropatia sem úlcera e que apresentam um pé quente e inchado podem apresentar neuroartropatia de Charcot aguda. A termometria de infravermelhos é uma ferramenta de avaliação valiosa nestes casos: o pé de Charcot agudo pode ser 8 a 15 °F mais quente do que a imagem no espelho do pé oposto. Estes doentes necessitam de um historial clínico completo, de um exame físico e de imagens radiográficas para facilitar a deteção precoce. Outras acções incluem a aplicação de um gesso de contacto total para estabilização e descarga completa da pressão plantar, com uma cadeira de rodas para evitar uma maior deterioração óssea e prevenir a amputação do membro inferior (Tabela 3).
Tabela 3. Intervenções de descarga para uma ferida plantar do pé diabético/neuropático28
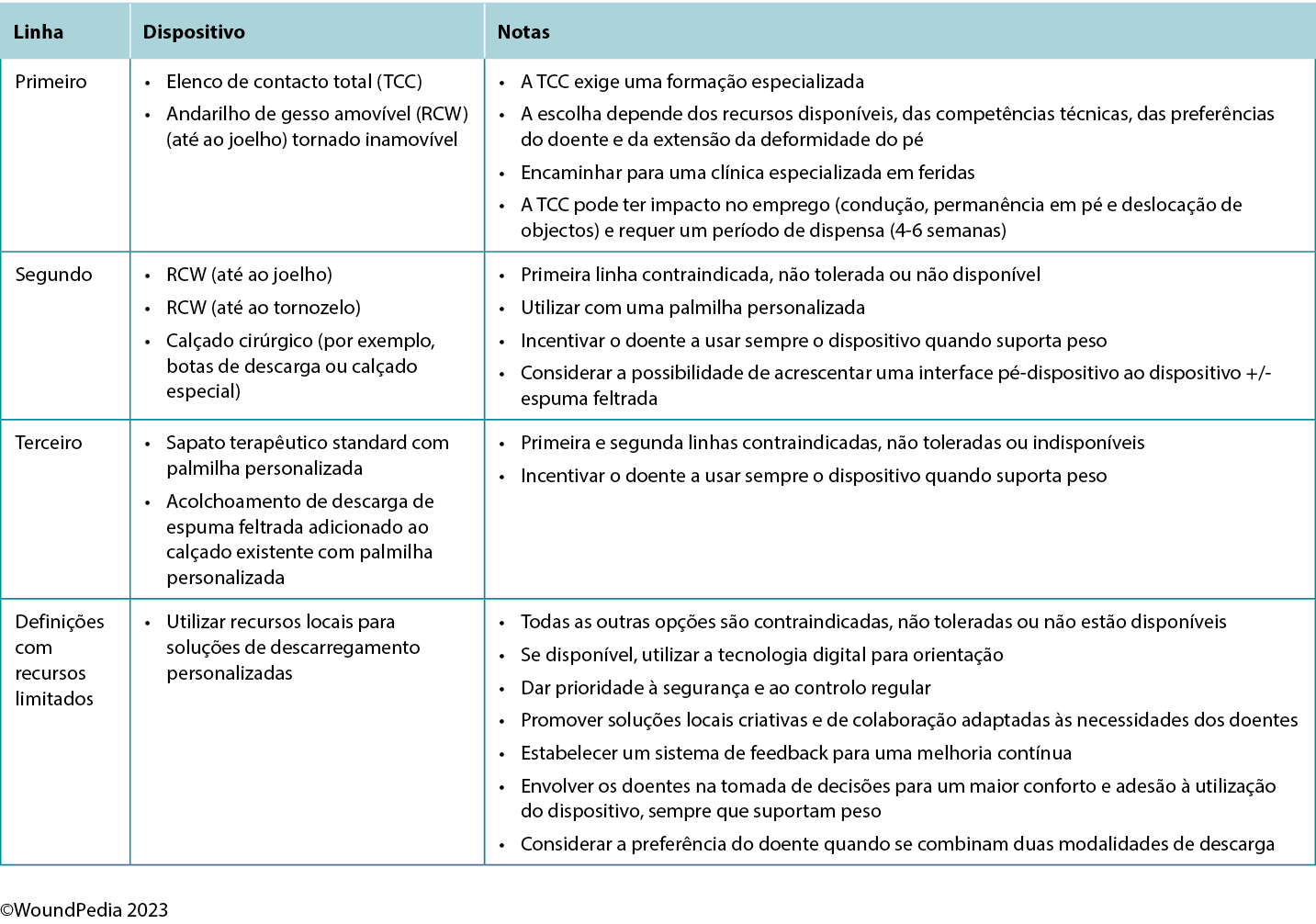
A formação de calos em diabéticos está positivamente correlacionada com a pressão e com a tensão de cisalhamento. Em indivíduos com neuropatia diabética, vários factores, incluindo deformações do pé, mobilidade articular limitada, stress repetitivo durante a caminhada e calçado mal ajustado, podem aumentar o risco de formação de calos.14 Além disso, a presença de calosidades pode representar um risco significativo, porque o trauma repetitivo pode levar a hemorragia subcutânea e eventualmente progredir para ulceração. Fornecer dispositivos de redistribuição da pressão feitos à medida (palmilhas macias, intervenções de sapateiro para adaptar o calçado e redução do andar descalço) para conseguir evitar a progressão subsequente de calosidades para úlceras.
Diferentes causas etiológicas podem originar úlceras nos pés de pessoas com diabetes: neuropáticas devido a neuropatia periférica, isquémicas associadas a DAP ou uma combinação de ambas - complicações neuro-isquémicas do pé. A presença de neuropatia diabética é estabelecida a partir do historial clínico, do exame físico (teste do monofilamento de 5,07/10 g), da alteração da sensibilidade distribuída simetricamente em ambos os membros (distribuição em meias e luvas) e de dor de tipo ardor, picada, pontada ou facada.
1C. Realizar uma triagem das causas/comorbilidades mais importantes a tratar imediatamente e conceber intervenções específicas no âmbito dos sistemas/recursos de apoio disponíveis localmente
A úlcera do pé diabético (DFU) ocorre em 25% a 34% das pessoas com diabetes e é uma das complicações mais temidas, podendo levar à amputação do membro inferior, incapacidade grave e à redução da esperança de vida.15 De origem multifatorial, a neuropatia periférica relacionada com a diabetes e com a DAP deixam os pés altamente vulneráveis a lesões traumáticas. O acesso a um diagnóstico e a uma intervenção atempados são factores determinantes para uma gestão eficaz e para a preservação dos membros.
A hiperglicémia crónica medida pela elevação da hemoglobina A1c (HbA1c) constitui um importante fator de risco para a neuropatia sensorial, motora e autonómica. Tanto a DAP como a pele seca aumentam a vulnerabilidade do pé à infeção e atrasam a cicatrização, contribuindo para resultados fracos. A doença renal crónica aumenta o risco.16 Estudos recentes sobre a monitorização contínua da glicose referem que a elevada variabilidade da glicose (tempo reduzido para atingir os níveis da gama-alvo) pode adicionalmente contribuir para complicações a longo prazo.17
Até 50% das pessoas com diabetes desenvolverão neuropatia, não havendo cura conhecida. A gestão inclui inspecções diárias adequadas dos pés para a deteção de traumatismos ou infecções, cuidados com os pés e um controlo eficaz da glicose.18 Para além da neuropatia, a DAP contribui igualmente para as DFU; a DAP é em grande parte assintomática e pode permanecer subdiagnosticada sem ser tratada durante um período prolongado. Os indivíduos com diabetes têm uma prevalência de DAP mais de duas vezes superior à dos indivíduos sem diabetes.19 Uma revisão sistemática de estudos baseados na comunidade relativamente à prevalência global e aos factores de risco para a DAP classificou a diabetes em primeiro lugar, a seguir ao tabagismo.20
A Sociedade Europeia de Hipertensão recomenda que os prestadores de cuidados de saúde e os doentes tenham como objetivo uma PA sistólica inferior a 130 mm Hg e uma PA diastólica inferior a 80 mm Hg. Nas pessoas com DAP, a PA sistólica não deve ser inferior a 120 mm Hg para evitar a redução do fluxo sanguíneo para os órgãos vitais e para os membros inferiores.21 Embora possam ser utilizados diuréticos, bloqueadores dos canais de cálcio, inibidores da enzima de conversão da angiotensina, bloqueadores dos receptores da angiotensina e β-bloqueadores, os inibidores da enzima de conversão da angiotensina e os bloqueadores dos receptores da angiotensina reduzem os eventos cardiovasculares.22,23 Recentemente, os inibidores do SGLT2 demonstraram excelentes resultados na melhoria da glicémia, da nefroprotecção e dos resultados cardiovasculares.24 Além disso, a incidência de DFU é reduzida pela deteção precoce da DAP, conjuntamente com modificações do estilo de vida.17
A complexidade da gestão de uma DFU exige uma abordagem de equipa interprofissional para poder identificar os determinantes biológicos, sociais, geográficos e culturais da saúde. Na Dinamarca, as pessoas com diabetes estão registadas por região e têm acesso a clínicas especializadas com equipas interprofissionais de tratamento de feridas. As taxas de amputação dos membros inferiores diminuíram significativamente devido à melhoria dos cuidados com a diabetes, à inspeção regular dos pés, à melhoria dos cuidados pessoais e ao tratamento atempado.25 Em populações mais diversificadas e geograficamente dispersas (por exemplo, Ontário, Canadá), existem disparidades significativas nas taxas de amputação, mais elevadas nas regiões rurais onde a prevenção atempada, como a cirurgia de revascularização e os especialistas em cuidados com os pés, apresenta carências ou está ausente.
No Canadá, as pessoas mais vulneráveis às amputações relacionadas com o pé diabético são os povos indígenas, os imigrantes e as pessoas que vivem nas regiões rurais e setentrionais.26 O Círculo de Saúde Indígena para a Diabetes proporciona uma abordagem culturalmente sensível às comunidades locais das Primeiras Nações do Ontário, com educação e conhecimentos sobre a diabetes, o bem-estar e a auto-gestão. O seu programa holístico de cuidados com os pés apoia um conjunto contínuo de serviços que liga os membros da comunidade a parceiros de agências indígenas e a profissionais de saúde locais e está provado que reduz a incidência de DFU, evitando amputações.27
1D. Dar prioridade à redistribuição da pressão na(s) ferida(s) do pé e com base na perfusão arterial escolher a compressão adequada para o edema da perna/pé
O critério padrão para os dispositivos de redistribuição da pressão plantar é o gesso de contacto total ou o andarilho de gesso amovível tornado irremovível.28 Mesmo nos sistemas de saúde em que estas modalidades de descarga estão imediatamente disponíveis, menos de 10% dos doentes elegíveis são adaptados e aderem à utilização destes dispositivos.29
A descarga é fundamental para curar as úlceras do pé (Tabela 3). O objetivo é o de selecionar o melhor dispositivo para o doente, incorporando preocupações centradas no doente, os objectivos dos cuidados e as provas das melhores práticas. Em ambientes com recursos limitados considere soluções criativas para reutilizar materiais locais, tais como inserções de feltro macio para descarregar. É importante estabelecer um programa de vigilância precoce entre o doente e o profissional de saúde para monitorizar e poder garantir os resultados de descarga desejados. Os profissionais de saúde devem avaliar a eficácia dos dispositivos e efetuar continuamente as modificações necessárias através de um acompanhamento definido. Nas regiões onde não existem profissionais especializados, a capacitação dos profissionais de saúde com competências em descarregamento básico pode conseguir colmatar esta lacuna.
Declaração 2: preocupações centradas no paciente
2A. Avaliar a dor utilizando uma escala de dor com um plano orientado para a gestão da dor nociceptiva e/ou neuropática
A perceção da dor implica um estímulo que pode ser físico ou químico. Existem dois tipos principais de dor: nociceptiva e neuropática (Tabela 4). A dor relacionada com a ferida é uma componente importante das preocupações centradas no doente que é frequentemente subvalorizada pelos profissionais de saúde. No final da década de 1990, a dor provocada por feridas era um tema central para os profissionais de saúde, com o lançamento de um documento de posição central focalizado na dor provocada por feridas.30 O documento reconhecia e centrava-se no sofrimento da dor crónica provocada por feridas e na sua influência na qualidade de vida relacionada com a saúde dos doentes. A gestão da dor da ferida foi então integrada na estrutura do WBP.1,31
Tabela 4. Tipos de dor e respostas30
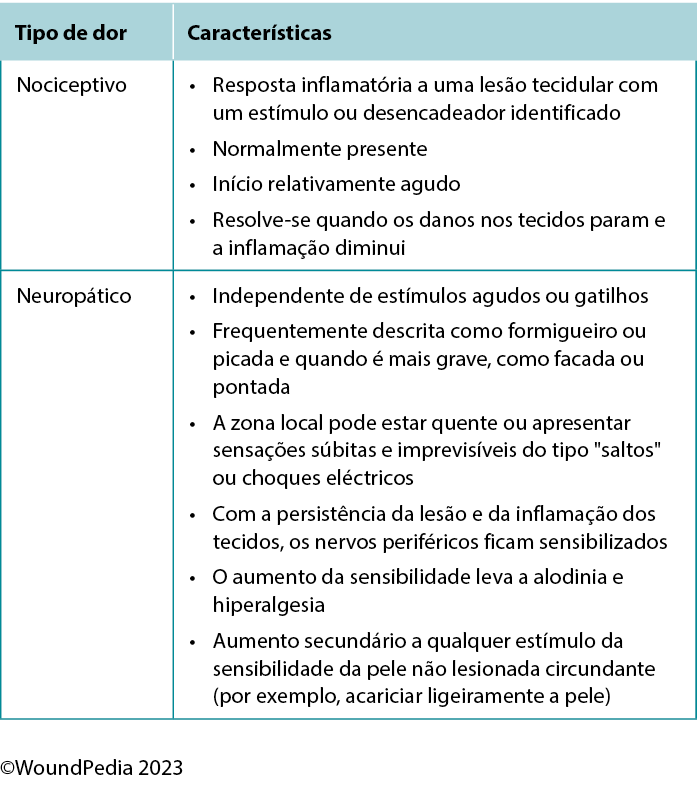
A dor pode desempenhar um papel significativo na gestão total das pessoas com feridas e no sucesso final da sua cicatrização.32 Os sinais de dor associados à lesão desempenham uma função importante no bem-estar do doente e, como tal, devem ser reconhecidos através de uma avaliação e de gestão adequadas. Por exemplo, a dor ou qualquer alteração na dor é um indicador chave de infeção da ferida e um dos quatro sinais cardinais de inflamação.1 A dor não resolvida está frequentemente associada a um atraso no encerramento da ferida.
Avaliação. Um historial de dor é essencial para a gestão da dor na ferida.32 A avaliação deve incluir a natureza, o início, a duração e os factores de exacerbação e de alívio. Isto ajudará a determinar a causa da dor e a orientar o seu tratamento. A intensidade da dor pode ser medida de forma fiável através da utilização de escalas de dor validadas. Uma escala de classificação numérica de 0 a 10 pontos, administrada verbalmente, é uma boa primeira escolha para medir a intensidade numérica da dor. A maioria dos doentes consegue funcionar com um nível de dor de 3 a 4 em 10.33
Os doentes com dor persistente devem ser reavaliados regularmente para verificar a sua melhoria, a deterioração e a adesão aos regimes de medicação. A utilização de um diário da dor com registos relativos à intensidade da dor, medicamentos utilizados, humor e resposta ao tratamento pode constituir uma boa estratégia de gestão. Para os indivíduos com limitações de comunicação, a escala de dor deve incluir imagens para facilitar o reconhecimento.
Gestão. A gestão da dor da ferida pode ser integrada na estrutura WBP: tratar a causa e tratar os factores locais da ferida e as preocupações centradas no doente.3 O tratamento da causa deve determinar o diagnóstico correto e iniciar o tratamento da dor da ferida. As preocupações centradas no doente devem focalizar-se naquilo que o doente considera serem as principais razões e as resoluções para a dor. A dor e o sofrimento antecipados pelo doente podem ser tão prejudiciais para a qualidade de vida como a real experiência da dor.
Existem várias estratégias de controlo da dor que nem sempre são farmacêuticas (Tabela 5). Ao escolher uma estratégia de gestão considerar a gestão total do doente, incluindo todos os aspectos do WBP. Lembre-se: a dor é aquilo que o doente diz que é.34
Avaliação e gestão com recursos limitados. Em regiões com recursos limitados, a avaliação continua a ser possível porque não necessita de ferramentas dispendiosas. A maioria das escalas de dor está disponível gratuitamente, apesar de algum custo inicial relativo à educação e formação dos profissionais.31 As opções de tratamento da dor em ambientes com recursos limitados podem ser mais práticas se forem orientadas por métodos não farmacológicos (Tabela 5). Algumas destas opções podem também ser socialmente mais aceitáveis ou serem já praticadas culturalmente (por exemplo, meditação, tratamentos à base de plantas) e particularmente aplicáveis no tratamento da dor nociceptiva. A implementação de tais estratégias pode então reservar a gestão farmacêutica para as pessoas com dor que não pode ser gerida por meios não farmacológicos (por exemplo, dor neuropática).35
Tabela 5. Estratégias de gestão da dor
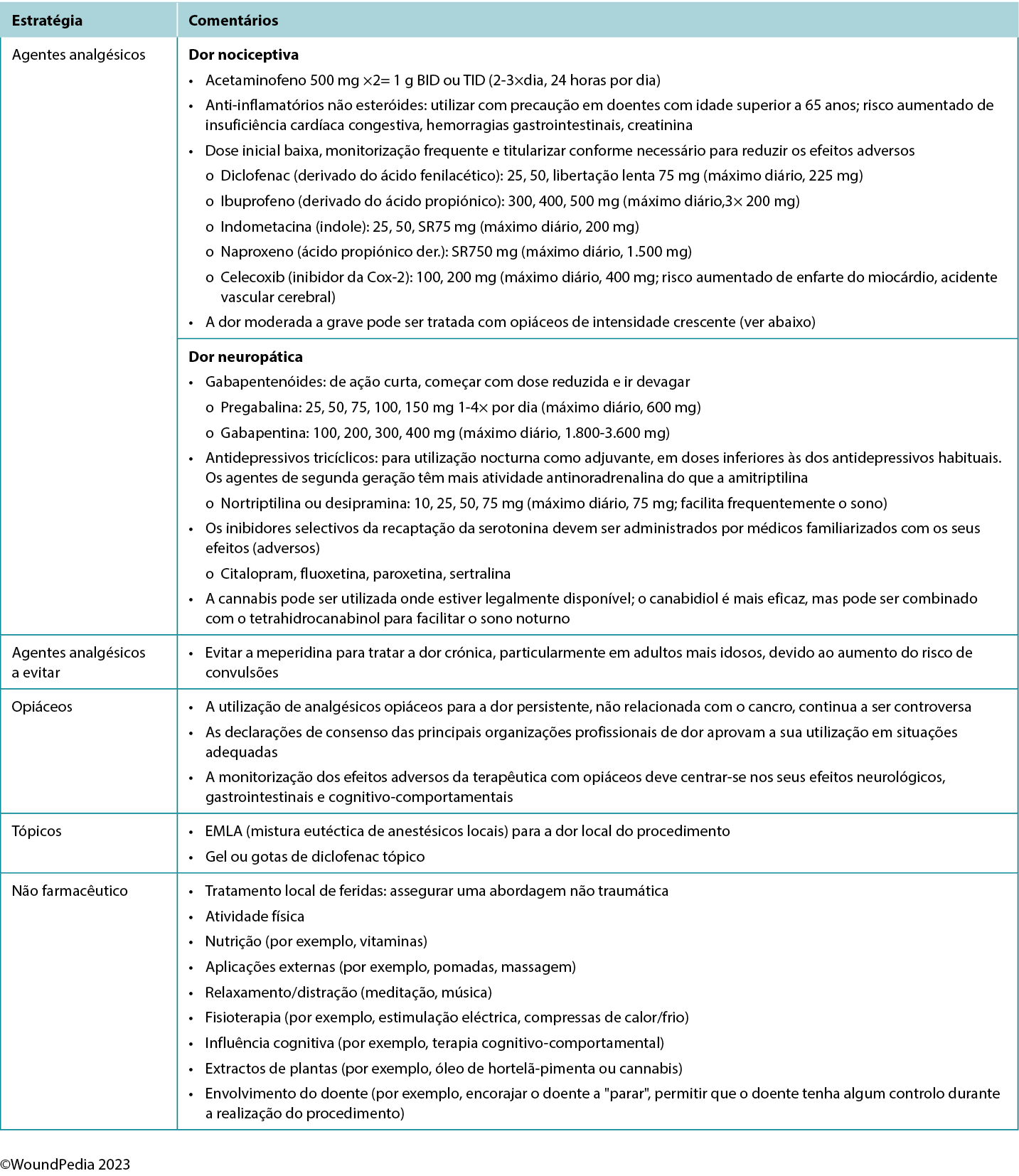
2B. Identificar as atividades da vida diária que podem afetar os resultados da cura
2C. Avaliar os doentes relativamente aos seus hábitos de vida (prejudiciais) que possam afetar a cicatrização de feridas (por exemplo, tabagismo, álcool e outras substâncias)
2D. Capacitar os doentes através de intervenções educativas sustentáveis que incluam o seu sistema de apoio. Sempre que seja possível, utilize a língua principal do doente e tenha em conta os seus antecedentes culturais, religião, comportamentos aceites, tabus e crenças
Em ambientes com recursos limitados, as preocupações centradas no doente e os obstáculos aos resultados clínicos são cruciais para que os prestadores de cuidados de saúde possam compreender e tratar no contexto das crenças culturais, espirituais e religiosas da respectiva comunidade.
Entre as populações indígenas de todo o mundo existem disparidades na cicatrização de feridas. Estas disparidades estão frequentemente enraizadas em questões históricas e atuais de natureza socioeconómica, cultural e em factores relacionados com os cuidados de saúde. A diversidade cultural e a pressão social frequentemente ditam também processos formais de atribuição de recursos a determinados sectores da saúde. Algumas das principais barreiras à cicatrização de feridas, entre as populações indígenas, incluem traumas históricos, disparidades socioeconómicas, acesso limitado aos cuidados de saúde, barreiras culturais, condições de saúde crónicas, práticas culturais de cicatrização, isolamento geográfico e preconceitos do sistema de cuidados de saúde.36 Muitas culturas têm um sistema de honra na gestão dos seus membros doentes, adultos mais velhos e doentes crónicos. Estes princípios são mais facilmente respeitados se estiverem disponíveis os recursos suficientes para os manter.
Muitos estudos identificaram uma doença médica grave como uma das principais razões pelas quais uma família pode contrair grandes dívidas.37,38 Mesmo em clínicas geridas pelo governo, podem ser cobrados à família materiais de penso ou medicamentos adicionais. Por conseguinte, os doentes e os membros da família podem recorrer a métodos de tratamento alternativos (medicina não alopática) junto de curandeiros locais/indígenas/tradicionais. Embora muitas vezes menos dispendiosos, estes curandeiros podem não ter as competências ou os conhecimentos necessários para tratar as feridas crónicas, o que leva à sua deterioração.
A perda de mobilidade independente devido à cronicidade da ferida é outro fator importante que tem impacto na assiduidade e no acompanhamento regular. A disponibilidade de transportes varia em ambientes com recursos limitados e caminhar pode ser a única forma de aceder a um ponto de recolha de transportes públicos. Os ambientes rurais isolados são muitas vezes os mais afectados, sendo necessário percorrer distâncias significativas para chegar a uma unidade de saúde formal.
A saúde social do ambiente familiar e a vontade de incorporar uma pessoa com necessidades de cuidados de saúde podem determinar a qualidade dos cuidados/autocuidados prestados, assim como a segurança do doente num ambiente doméstico. Devido à estrutura social e ao meio em que se inserem os vários países, o apoio familiar e o apoio social podem diferir consoante a cultura. Frequentemente, à medida que o tempo passa, os encargos financeiros aumentam; a independência do doente e a realização das atividades da vida diária (AVDs) deterioram-se; as mudanças de penso tornam-se mais difíceis; e os prestadores de cuidados ficam stressados, fatigados e exaustos.39 As consultas tardias e as condições críticas/terminais dos doentes quando se apresentam aos cuidados formais são factores sociais e comportamentais agravantes adicionais que podem acentuar os maus resultados na cicatrização de feridas.
As pessoas com feridas que são tratadas em casa precisam de um espaço reservado para si. O odor da ferida, a dor persistente e uma rotina diferente são os principais factores de stress para o doente e para a família em ambientes onde o espaço é escasso. A simples presença de uma ferida cutânea grave já tem um impacto negativo nas interacções sociais, nas relações, na sexualidade e na autoconfiança do doente. Isto leva a uma ansiedade e depressão progressivas, as quais podem provocar pessimismo relativamente aos benefícios do tratamento. Subsequentemente, os doentes apresentam uma diminuição da autoeficácia, a qual está frequentemente associada a uma maior deterioração da ferida, incluindo eventuais amputações das extremidades inferiores.40
O verdadeiro desafio ocorre quando são necessárias modificações no estilo de vida. Isto requer frequentemente recursos adicionais ou uma educação personalizada para permitir a elaboração de planos de autocuidado.40,41 Nunca é demais sublinhar a necessidade de que as intervenções de educação para a saúde e de modificação do estilo de vida tenham fundamentos claros. As intervenções no estilo de vida podem tornar-se um desafio financeiro, social e logístico, primeiro para adquirir e depois para poder manter em qualquer domínio de vida restrito. Além disso, é um passo vital para garantir que qualquer ajuda financeira recebida seja corretamente atribuída ao membro da família com uma ferida.
Em doentes em ambientes com recursos limitados é necessária uma abordagem biopsicossocial da gestão do tratamento de feridas. A equipa de tratamento de feridas, para além de tratar a ferida, deve abordar os factores de stress social que afectam o doente. Cada doente precisará de um plano de gestão único, mutuamente acordado e que se adapte às suas limitações (apoio médico, financeiro, familiar, social e emocional).40
Declaração 3: capacidade de curar
3A. Ferida curável: Determinar se existe uma irrigação sanguínea adequada para a cicatrização da ferida e se existe tratamento apropriado para tratar a(s) causa(s) subjacente(s)
3B. Ferida de manutenção: Ajustar a prática se existir um fornecimento de sangue adequado para a cicatrização da ferida, mas o doente não pode aderir ao plano de cuidados e/ou o sistema de saúde não dispõe dos recursos necessários
3C. Ferida não cicatrizável: Determinar tratamento(s) alternativo(s) para a ferida se o fornecimento de sangue for inadequado e/ou se a causa subjacente não puder ser corrigida
O processo de determinação da classificação da cicatrização de uma ferida inicia-se com um historial e um exame físico completos do doente. É importante identificar a(s) causa(s) subjacente(s) da ferida. Tratar a(s) causa(s) subjacente(s) é o primeiro passo para desenvolver um plano de gestão exequível.
Em alguns casos, as feridas crónicas também podem ficar estagnadas e não se conseguir alcançar o avanço do bordo da ferida durante o tempo definido; estas são conhecidas como feridas de difícil cicatrização. Frequentemente, enquadram-se na categoria de manutenção, mas com uma avaliação adicional, podem ser curáveis com uma reavaliação do doente, do historial, das causas e do plano de tratamento.3,42
As preocupações e as expectativas centradas no doente têm de ser identificadas, comparadas e alinhadas com a disponibilidade de recursos institucionais/clínicos, as competências e as opções de intervenção imediata disponíveis.3,42 O plano de gestão baseia-se na classificação de cura atribuída, a qual pode mudar.
Protege as feridas não cicatrizáveis contra a perda de tecido, infecções profundas e circundantes da ferida e deterioração geral do ambiente húmido da ferida. A redução da humidade é uma prioridade. As feridas de manutenção também necessitam de proteção contra mais perdas de tecido, sendo a base principal a gestão do leito seco da ferida e o controlo local das infecções. A proteção dos tecidos pode também ser uma medida temporária até que os recursos estejam disponíveis e os factores adicionais do doente sejam controlados, de form a conseguir-se uma otimização total.
As feridas estagnadas, mas cicatrizáveis (difíceis de cicatrizar), precisam de uma segunda oportunidade para alcançar o avanço do bordo, com urgência na reavaliação e na intervenção da equipa interprofissional como sendo as prioridades mais elevadas.3,42
Declaração 4: tratamento local de feridas: examinar, medir e controlar
4A. Documentar o progresso da ferida desde a linha de base para estabelecer trajectórias de cicatrização mensuráveis (com base em papel e/ou em imagens fotográficas, se disponíveis).
4B. Limpar as feridas com água potável tépida (pré-fervida), soro fisiológico ou agentes antissépticos de baixa toxicidade. Se necessário, considerar banhos de imersão, compressas e irrigação.
4C. Reavaliar e documentar as feridas regularmente, em intervalos adequados ao longo do tempo, com os recursos disponíveis. Documentar e manter a confidencialidade dos dados.
A documentação da avaliação de feridas é uma componente integral da prática dos cuidados de saúde. É fundamental para assegurar a prestação de cuidados de elevada qualidade aos doentes, monitorizar o estado da ferida e fornecer as orientações para quaisquer alterações nas intervenções relativas à ferida. O registo exaustivo e preciso das avaliações de feridas é essencial para se garantirem melhores resultados para os doentes, uma comunicação eficaz entre os profissionais de saúde, assim como a conformidade legal e regulamentar.43
Acompanhamento dos progressos. A documentação de avaliação da ferida serve como registo histórico da progressão da ferida ao longo do tempo. Ao documentar regularmente as características da ferida, incluindo o tamanho, a profundidade, a cor, o exsudado, a infeção, o tipo de tecido, etc., os profissionais de saúde podem acompanhar as alterações, identificar potenciais complicações e ajustar os planos de tratamento. Se for utilizada documentação fotográfica, deve-se obter o consentimento do doente de acordo com a política organizacional, assegurar uma técnica apropriada com iluminação adequada e uma distância apropriada da ferida e incluir um guia de medição na fotografia.44 Esta avaliação contínua é fundamental para se avaliar a eficácia das intervenções e poder tomar decisões informadas relativamente ao tratamento de feridas. Ao medir a área de superfície ou o volume, é imperativo utilizar uma técnica consistente, independentemente da tecnologia.
Comunicação. As avaliações exactas das feridas facilitam uma comunicação eficaz entre os profissionais de saúde. Quando todos os membros da equipa têm acesso a documentação consistente e actualizada sobre feridas, podem trabalhar em conjunto para desenvolver e implementar um plano de cuidados coordenado, dessa forma garantindo que os doentes recebem o melhor tratamento possível. É fundamental utilizar uma terminologia coerente, que seja comum a todas as disciplinas. O sistema de classificação médica da Classificação Internacional de Doenças constitui um exemplo de uma norma aplicável a nível mundial.45
Conformidade legal e regulamentar. A avaliação e a documentação correctas da ferida são essenciais para cumprir os requisitos legais e regulamentares. Mesmo em ambientes com recursos limitados, registos inexactos ou incompletos podem dar origem a problemas legais e ter um impacto negativo na prática de um profissional de saúde.
Reembolso. Em muitos sistemas de saúde, a documentação correcta da avaliação de feridas está associada a modelos de financiamento baseados em reembolsos. São frequentemente necessários registos exactos e detalhados para se justificar a utilização de produtos ou de procedimentos específicos de tratamento de feridas e garantir que as organizações recebem o reembolso adequado pelos serviços prestados.
Investigação e melhoria da qualidade. Os dados de avaliação de feridas são um recurso valioso para as iniciativas de investigação e de melhoria da qualidade. Este processo de aprendizagem contínua ajuda a melhorar o tratamento global de feridas e os resultados dos doentes.
Cuidados centrados no doente. A avaliação e a documentação correctas das feridas são uma componente essencial dos cuidados centrados no doente. Assegura que as condições dos pacientes são avaliadas minuciosamente e que os planos de tratamento são adaptados às suas necessidades específicas. Quando os doentes observam que o seu prestador de cuidados de saúde está empenhado em documentar e monitorizar as suas feridas, isso pode aumentar a confiança e a satisfação do doente.
Para promover a consistência da linguagem e melhorar a clareza dos dados, um número crescente de empresas está a criar software e aplicações electrónicas de avaliação de feridas de forma a reduzir o tempo necessário para uma documentação completa.43 Estes programas e aplicações (alguns mais acessíveis do que outros) podem fornecer à equipa de cuidados de saúde um conjunto estruturado de parâmetros para garantir que todas as características clínicas são documentadas, dessa forma melhorando a comunicação global.46 Embora estas ferramentas sejam uma mais-valia para os profissionais de saúde, não estão isentas de riscos, como o de copiar e colar incorretamente a partir de relatórios/notas de consulta anteriores ou riscos de segurança dos dados dos doentes. Nas zonas onde esses programas e aplicações não estão disponíveis, a atualização do paciente e o fornecimento de uma avaliação escrita e de planos de intervenção podem ser justificados.
Declaração 5: tratamento local de feridas: desbridamento
5A. Feridas cicatrizáveis/causa corrigida: Considerar o desbridamento cirúrgico ativo e agudo do tecido hemorrágico, com controlo adequado da dor, apenas se estiver dentro do âmbito da sua prática. Isto deve ser efectuado apenas com a orientação de especialistas em tratamento avançado de feridas. Se não estiver disponível, considerar o desbridamento conservador (cortante)
5B. Feridas de manutenção/feridas não cicatrizáveis: Considere o desbridamento conservador (cortante), com controlo adequado da dor, apenas se estiver dentro do âmbito da sua prática. Remover os resíduos/viscosidades soltas apenas quando indicado e sem provocar qualquer hemorragia
5C. Determinar se estão disponíveis modalidades de desbridamento alternativas para feridas cicatrizáveis (por exemplo, opções autolíticas, mecânicas, enzimáticas e biológicas com larvas)
O desbridamento é um processo importante no paradigma WBP para a remoção de tecido necrótico e outros biomateriais, incluindo biofilme, em feridas cicatrizáveis e prevenir o odor e a infeção em feridas de manutenção. Para todas as feridas localizadas abaixo do joelho, comunicar os resultados de quaisquer testes vasculares (por exemplo, IPTB, forma de onda) a todos os membros da equipa interprofissional e documentar em conformidade antes de tentar o desbridamento, uma vez que muitos tipos podem ser prejudiciais para o leito de uma ferida com fornecimento vascular reduzido.
Para feridas cicatrizáveis, as intervenções locais no leito da ferida são melhor determinadas através do paradigma WBP, com base nas características do doente e da ferida. Considerar o desbridamento cirúrgico (até ao tecido hemorrágico) como uma intervenção de primeira linha. No entanto, em muitas regiões rurais e remotas, pode não existir acesso a um profissional de saúde qualificado com a formação, os conhecimentos e o discernimento necessários para este procedimento.
O desbridamento conservador (cortante) (sem causar hemorragia) requer conhecimentos e competências avançados e é mais adequado para cuidados não agudos ou para clínicas especializadas. Remover apenas detritos soltos ou não fixados na ferida sem causar trauma no leito da ferida.
A terapia clínica de desbridamento com larvas estéreis é uma modalidade de tratamento limitada em ambientes com recursos limitados, exceto em casos de exposição acidental. A infestação por larvas é frequentemente descoberta durante a mudança de pensos. Podem obter-se bons resultados de desbridamento com a terapia acidental com larvas, particularmente se as larvas em causa forem da altamente selectiva Lucilia sericata/cuprina, uma vez que estas se concentram no tecido desvitalizado como fonte de alimento.47,48 Podem obter-se resultados prejudiciais se a infestação for da vulgar mosca doméstica (Musca domestica) ou de outras espécies invasoras, uma vez que essas larvas podem destruir indiscriminadamente tecido saudável.47,48
Os profissionais de saúde devem avaliar métodos alternativos de desbridamento (por exemplo, autolítico, enzimático, mecânico) para os sectores comunitários, incluindo os cuidados primários, os cuidados domiciliários e os cuidados prolongados. Antes de iniciar o desbridamento e dentro dos recursos disponíveis, é vital considerar a segurança do doente, avaliar os factores ambientais e identificar as barreiras à cicatrização da ferida.
Os protocolos de desbridamento adequados para feridas de manutenção e para feridas não cicatrizáveis diferem significativamente dos protocolos para feridas cicatrizáveis. Embora a cicatrização de feridas húmidas proporcione um ambiente ótimo para a cicatrização de feridas, é uma forma de desbridamento (autolítico) que pode ser prejudicial para feridas não cicatrizáveis e de manutenção. Geralmente, o desbridamento não é uma intervenção adequada para feridas de manutenção estáveis ou para feridas não cicatrizáveis, porque o objetivo é mantê-las secas e sem infecções.49 Considerar o desbridamento apenas quando uma ferida de manutenção ou não cicatrizável se torna instável, para remover resíduos infectados ou necróticos da ferida da forma o menos traumática possível.
Os objectivos dos doentes incluem, normalmente, o aumento do conforto, a minimização do odor relacionado com a ferida, a redução da dor e a melhoria das atividades do dia a dia. Manter a ferida seca permite a formação de uma camada protetora, ao passo que o desbridamento acarreta o risco de remover esta camada protetora e de se introduzirem organismos patogénicos.
Declaração 6: tratamento local de feridas: infecção e inflamação
6A. Tratar a infeção local/superficial da ferida (três ou mais critérios NERDS) com antimicrobianos tópicos
6B. Gerir a infeção profunda e circundante da ferida (três ou mais critérios STONEES) com antimicrobianos sistémicos e com antissépticos tópicos concomitantes
6C. Considerar agentes anti-inflamatórios em feridas com inflamação persistente (pensos tópicos ou medicação sistémica)
Os critérios validados NERDS e STONEES podem orientar a avaliação e o tratamento da infeção e inflamação em feridas crónicas.50 Basear o diagnóstico de infeção em sinais e em sintomas clínicos e não em esfregaços superficiais da ferida, os quais devem ser utilizados apenas para orientar a seleção de antimicrobianos em caso de infeção. Se houver suspeita de uma infeção dos tecidos profundos e circundantes, identificar as espécies bacterianas e a sua sensibilidade aos agentes antibacterianos normalmente utilizados para auxiliar a orientar a utilização de antimicrobianos sistémicos. Isto é especialmente verdadeiro se uma infeção profunda e circundante não estiver a responder ao tratamento empírico.
As melhores amostras de tecido para zaragatoas de cultura do leito da ferida são as obtidas após a limpeza da ferida com água potável ou com soro fisiológico, realizando-se a recolha de amostras da base da ferida sem detritos. É mais provável que uma cultura de amostras de tecido utilizando uma cureta ou outra técnica de biópsia represente os organismos no tecido da ferida. Em alternativa, uma técnica de esfregaço semiquantitativa, utilizando o método de Levine, pode correlacionar-se com biópsias de tecido.51 O esfregaço é colocado no tecido de granulação e pressionado o suficiente para extrair o exsudado da ferida, sendo depois rodado 360° para cobrir todas as superfícies do esfregaço. Colocar a zaragatoa no meio de transporte para a humedecer previamente antes de a colocar na pele, pode aumentar a produção bacteriana em doentes com feridas com pouco exsudado.52
As bactérias patogénicas podem infiltrar-se no osso e causar osteomielite, o que prejudica o potencial de cura e é difícil de curar. A biópsia óssea é o critério padrão para se diagnosticar a suspeita de osteomielite, uma vez que as culturas superficiais não acedem ao tecido ósseo profundo e a imagiologia é limitada por uma especificidade variável.53 No entanto, a biópsia óssea pode ser desconfortável, depende de clínicos qualificados e pode prolongar o dano tecidular. Por estas razões, frequentemente não se apresenta como uma opção viável, ainda mais se os recursos forem escassos.
Quando a infeção profunda da ferida é confirmada, os pensos antimicrobianos são os adequados para apoiar localmente a terapia antibiótica sistémica e assim evitar a propagação das bactérias da superfície para o compartimento profundo e circundante. As cinco opções mais comuns de pensos antimicrobianos são a prata, a polihexametileno biguanida, o iodo, o azul de metileno/violeta de cristal e o mel. Destes, a prata e o mel apresentam propriedades anti-inflamatórias adicionais.54
Em algumas feridas, são aplicados antissépticos de largo espetro para uma redução rápida da carga bacteriana a curto prazo, de forma a apoiar os antibióticos sistémicos. Quando o risco de infeção ultrapassa as propriedades citotóxicas, uma gaze humedecida com iodopovidona de baixo custo, mudada diariamente sobre o osso exposto, pode reduzir as bactérias da superfície. Esta é uma estratégia de curto prazo, acompanhada de uma avaliação clínica dos níveis séricos da função tiroideia, especialmente quando as superfícies das feridas são grandes. No entanto, com os novos antissépticos de baixa toxicidade, estão agora disponíveis outras opções menos agressivas, mas igualmente eficazes.
Em geral, as feridas em doentes imunocompetentes que se apresentam há menos de 1 mês são tratadas com agentes para cobertura Gram-positivos. As infecções polimicrobianas (normalmente observadas em pessoas com diabetes) ou feridas com mais de 1 mês de duração, requerem agentes de largo espetro com cobertura de Gram-positivos, Gram-negativos e anaeróbios, uma vez que estes doentes também estão frequentemente imunocomprometidos.55
Os agentes citotóxicos podem ser adequados para feridas não cicatrizáveis, se a necessidade de ação antimicrobiana tópica for superior à toxicidade tecidular. Os antissépticos são geralmente os preferidos em relação aos antibióticos tópicos como parte da gestão de antibióticos devido ao seu menor risco de resistência bacteriana sistémica e aos efeitos adversos associados à dermatite de contacto irritante ou alérgica.54
6D. Limpar suavemente a ferida com soluções de baixa toxicidade (água, soro fisiológico, agentes antissépticos não citotóxicos).
A solução de limpeza utilizada depende das características da ferida e da sua disponibilidade na prática. Existe um fraco consenso na literatura sobre as recomendações de limpeza de feridas. Uma revisão Cochrane actualizada em 2021 sobre soluções de limpeza de úlceras venosas de perna, concluiu que faltam provas de ensaios aleatórios controlados "para orientar a tomada de decisões sobre a eficácia da limpeza de feridas em comparação com a ausência de limpeza e as abordagens ideais para a limpeza de úlceras venosas de perna."56 No entanto, os princípios gerais de tratamento de feridas envolvem soluções de baixa toxicidade, incluindo água potável ou pré-fervida, soro fisiológico e outros agentes antissépticos não agressivos para as feridas.57 Isto evita efeitos citotóxicos e danos no tecido de granulação saudável em feridas cicatrizáveis.
O ácido acético diluído de 0,5% a 1,0% ou o ácido hipocloroso também podem ser utilizados em alguns casos em que é preferível um ambiente ácido (por exemplo, para tratamento tópico de Pseudomonas aeruginosa).58 Com base na classificação de cicatrização da ferida e após uma avaliação positiva do risco-benefício, podem ser utilizados agentes anti-sépticos com alguma citotoxicidade tecidular. Isto inclui agentes como a clorexidina de baixa concentração ou o seu derivado polihexametileno biguanida e a iodopovidona. Isto pode ser benéfico em casos de manutenção e de feridas não cicatrizáveis que apresentem um elevado potencial de infeção. Além disso, estes agentes podem ser utilizados para gerir o odor e o exsudado, para além de controlar a carga biológica. Em ambientes com recursos limitados e para evitar a contaminação cruzada, considerar as medidas de higiene das feridas e a forma como as soluções são preparadas, armazenadas e distribuídas aos doentes.
Há um interesse emergente na utilização de tensioactivos para remover biofilmes que existem frequentemente nos resíduos da ferida e que apresentam duas superfícies de viscosidade diferente (Tabela suplementar 2, http://links.lww.com/NSW/A177). A irrigação de feridas continua a ser um tópico controverso para utilização em feridas crónicas. No entanto, a opinião dos especialistas é a de não irrigar as feridas se a base da ferida não estiver visível, para evitar a acumulação da solução de irrigação em espaços fechados e o aumento acidental da ferida.57 Irrigar as feridas com um volume de solução adequado (50-100 ml por centímetro de comprimento da ferida).59
Declaração 7: tratamento local de feridas: gestão da humidade
7A. Manter o equilíbrio da humidade em feridas cicatrizáveis através de hidrogéis, películas, hidrocolóides, hidrofibras, alginatos e espumas
7B. Instituir a redução da humidade com mecanismos de bloqueio de fluidos em feridas cicatrizáveis através da utilização de superabsorventes para afastar a humidade da superfície (tecnologia de fraldas)
7C. Determinar se é necessário tamponamento para feridas cicatrizáveis. Pode encontrar-se húmido (doar humidade) ou seco (absorver humidade)
7D. Estabelecer um protocolo de redução da humidade em feridas de manutenção e em feridas não cicatrizáveis de forma a reduzir a proliferação bacteriana
A manutenção do equilíbrio da humidade é complexa e depende do tipo de ferida e da classificação da cicatrização. Considerar o equilíbrio da humidade, o controlo de infecções e a educação do doente na seleção dos materiais de penso.60 A incorporação e a adaptação das estratégias de gestão da humidade ao tipo de ferida específico e aos recursos disponíveis pode otimizar os resultados dos doentes e minimizar as complicações (Tabela 6).3,54 A investigação e os estudos clínicos adicionais devem continuar a aperfeiçoar a nossa compreensão da gestão da humidade das feridas para, no futuro, melhorar as práticas de tratamento de feridas.3,54
Tabela 6. Objectivos da gestão da humidade com base na capacidade de cicatrização da ferida3,42,54
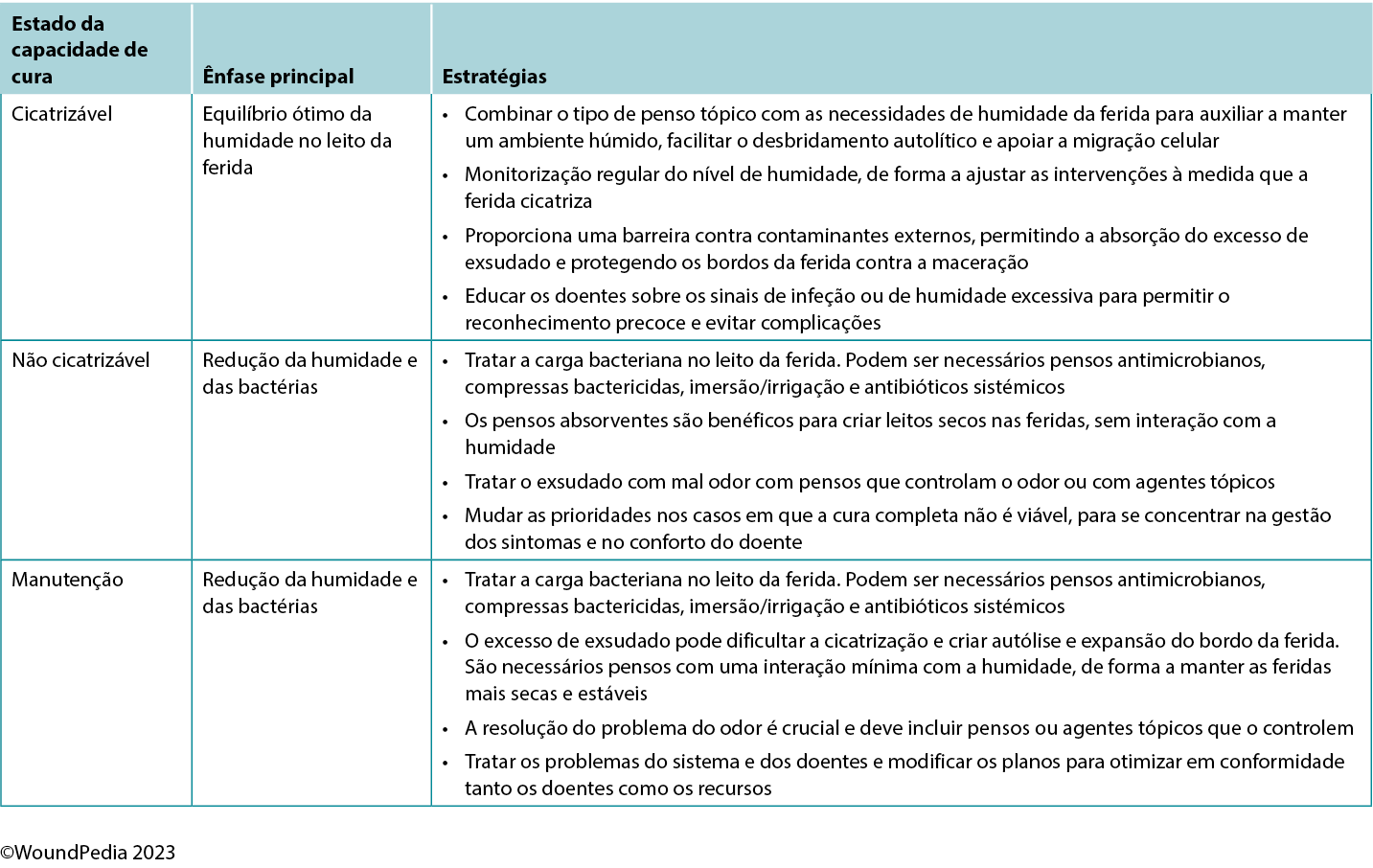
Em geral, à medida que o nível de exsudado aumenta, o mesmo acontece com a capacidade de absorção ou de transferência de humidade do penso.3 As opções de pensos com equilíbrio de humidade podem ser combinadas com propriedades antibacterianas e anti-inflamatórias para assim satisfazer ainda mais as necessidades da ferida.
A escolha do penso para feridas de manutenção e para feridas não cicatrizáveis deve dar prioridade ao conforto, evitando a doação de fluidos para o leito da ferida e a maceração dos bordos da ferida. Estas feridas requerem uma reavaliação regular para detetar qualquer progresso ou deterioração e devem ser tratadas de forma a reduzir a carga bacteriana. Dependendo da evolução e das características da ferida ao longo do tempo, os pensos podem vir a ter de ser adaptados.
Declaração 8: trajectória de cura
8A. Considere que as feridas cicatrizáveis devem ser pelo menos 20% a 40% mais pequenas na 4ª semana, para cicatrizarem na 12 semana. Se existirem factores que afectem o tempo de cicatrização (por exemplo, um mau controlo glicémico), poderá ser necessário um tempo de cicatrização adicional
8B. Atribuir um tempo adicional para a cicatrização para além das 12 semanas em feridas cicatrizáveis, se os recursos disponíveis forem limitados, continuando com cuidados consistentes
8C. Dar prioridade ao encaminhamento para centros especializados (quando disponíveis) para testes de diagnóstico e/ou biópsia cutânea, especialmente quando se estão confrontados com graves restrições de recursos
As trajectórias de cicatrização de feridas são úteis e necessárias para avaliar o tempo necessário para a cicatrização, especialmente se se utilizam dados clínicos (medições) para feridas agudas e crónicas. A trajetória de cicatrização baseia-se em medições precisas e consistentes da ferida, que determinam o fecho da área de superfície da ferida ao longo do tempo. Isto ajuda a identificar a progressão da ferida, as feridas paradas e o agravamento do estado da ferida.
As feridas agudas curáveis devem ser completamente fechadas no prazo de 30 dias. Espera-se que as feridas crónicas cicatrizáveis apresentem um avanço do bordo de 20% a 40% aos 30 dias (4 semanas) e que fechem no prazo de 12 semanas.3,42,61,62 As feridas não cicatrizáveis não têm um tempo definido para fechar, não se espera um avanço do bordo e todos os passos iniciados são destinados a evitar uma maior deterioração. Não se espera que as feridas de manutenção cicatrizem ou se deteriorem e a cicatrização da ferida pode progredir lentamente sem uma expetativa de tempo fixo, a menos que se consiga uma otimização do doente/instituição/sistema.
Para obter diagnósticos alternativos reavaliar periodicamente as feridas de difícil cicatrização. Nestes casos, considerar a biópsia da ferida, uma investigação adicional e/ou encaminhamento para uma equipa de avaliação interprofissional. Uma trajetória de cicatrização pode ser avaliada nas primeiras 4 a 8 semanas para prever se uma ferida tem probabilidade de cicatrizar até à 12 semana, desde que não existam novos factores de complicação.63 As alterações na ferida, no indivíduo ou no ambiente podem exigir a reclassificação de uma ferida para a categoria de manutenção ou para não cicatrizável.
Declaração 9: avanço do bordo
9A. Considerar modalidades activas, construídas localmente de acordo com o mecanismo de ação necessário, assim como as indicações específicas para se iniciar uma terapia adjuvante para apoiar a cicatrização da ferida
9B. Decidir sobre terapias adjuvantes através de uma abordagem de equipa interprofissional e incluir uma análise prévia do risco-benefício
Selecionar as terapias adjuvantes de acordo com a possibilidade de cura. Iniciá-los o mais rapidamente possível após a lesão em pessoas com traumatismos graves, de forma a evitar sequelas de longa duração. Selecionar modalidades utilizando uma abordagem de equipa interprofissional com base no que está disponível e no mecanismo físico necessário (assegurando, ao mesmo tempo, a possibilidade de cicatrização dos tecidos traumatizados). Em feridas de difícil cicatrização e após a reavaliação, a ferida pode necessitar de uma segunda oportunidade para cicatrizar.42 Assegurar que o consentimento informado faz parte das decisões de terapia adjuvante.
Uma análise do risco-benefício e da relação custo-eficácia é útil e contribuirá para a sustentabilidade do sistema. A chave para decisões eficazes sobre modalidades adjuvantes baseia-se no risco que representa iniciar a terapêutica (desconforto físico, dificuldades financeiras, adesão do doente), versus o benefício que irá proporcionar (oxigenação dos tecidos, contração da ferida, redução do edema, reativação celular).42,64 As melhores decisões em termos de risco-benefício são tomadas no seio de uma equipa interprofissional, a qual inclui o doente, assegurando o empenho do grupo e a conclusão do tratamento com uma utilização óptima dos recursos.
A otimização dos recursos, ou a sua ligeira reorientação, pode conduzir a estratégias criativas nas mãos de equipas interprofissionais, de modo a criar soluções à medida que garantam que todos os doentes são tratados da melhor forma, apesar das restrições de recursos.
Cirurgia. Mesmo nos ambientes mais restritos, esta é a única modalidade que está maioritariamente disponível numa área de influência médica, muitas vezes em contextos de cuidados terciários com referências recebidas de clínicas de cuidados primários para fornecer desbridamento, cirurgia geral com intenção de encerramento primário/terciário, enxertos de pele e/ou amputações.
Os enxertos de pele podem estar disponíveis em ambientes com recursos limitados como uma modalidade avançada para conseguir o encerramento dos tecidos, a fim de reduzir o tempo de cicatrização e dessa forma evitar infecções recorrentes de feridas profundas. O procedimento pode minimizar a utilização extensiva de materiais de penso durante um período prolongado e assim reduzir a carga de trabalho dos cuidados primários com feridas crónicas. As decisões sobre enxertos de pele são muitas vezes tomadas para preservar a funcionalidade do corpo e dessa forma promover o encerramento precoce da ferida, acima dos resultados estéticos.65 No entanto, evite enxertos de pele em feridas isquémicas e na maioria das úlceras de estase venosa; considere-os apenas para feridas em que se possa esperar um resultado favorável.66,67
Estimulação eléctrica. A cicatrização da ferida pode ser acelerada através do aumento da corrente eléctrica natural que está presente na pele ferida. Em ambientes com recursos limitados, esta modalidade deve ser investigada para a cicatrização de feridas devido à sua base de evidência de elevado nível e à disponibilidade de dispositivos desta natureza (corrente contínua, corrente alternada, corrente contínua de baixa intensidade, campos electromagnéticos pulsados, corrente pulsada de alta tensão e dispositivos de estimulação eléctrica nervosa transcutânea). As provas apoiam o aumento da proliferação celular e o aumento da perfusão microcapilar, assim como uma redução da carga bacteriana e da infeção nos leitos das feridas tratadas.68
Terapia de feridas com pressão negativa montada na parede. Esta pode dar ao profissional de saúde controlo sobre a gestão do exsudado e precisão na reposição de fluidos em doentes internados com exsudado elevado e grandes defeitos nos tecidos. Comece com a pressão mais baixa possível (menos 50-80 mm Hg). O doente fica acamado para que a modalidade seja mantida e a camada de base (frequentemente gaze ou pensos impregnados de petrolato) tem que ser substituída pelo menos diariamente. Isto, conjuntamente com o facto de se começar com a definição de pressão negativa o mais baixa possível, evitará o trauma mecânico no leito da ferida devido à aderência dos tecidos e à remoção traumática do penso nos casos em que não estejam disponíveis camadas de base não aderentes.69 Existem atualmente dispositivos descartáveis de terapia de feridas com pressão negativa concebidos para utilização na comunidade, bem como opções de bricolage que podem proporcionar resultados clínicos aceitáveis.70,71
Respirar oxigénio de alto fluxo e altamente concentrado. O oxigénio é frequentemente ignorado como uma modalidade legítima de cicatrização de feridas.72 Ironicamente, é raramente utilizado, apesar de quase todos os ambientes de cuidados de saúde formais terem quantidades abundantes de oxigénio disponíveis, mesmo em ambientes relativamente pobres em recursos. A disponibilidade de concentradores de oxigénio também aumentou devido à pandemia de COVID-19, tornando a administração de oxigénio também uma possibilidade em regime de ambulatório, em casa.73 Embora a oxigenação hiperbárica seja o meio mais eficaz de aumentar a concentração de oxigénio no plasma e de administrar oxigénio nos tecidos, esta modalidade nem sempre está facilmente disponível. No entanto, o fornecimento de oxigenação normobárica (em enfermaria) ainda produz um aumento de 7,5 vezes no oxigénio transportado pelo plasma (ou seja, de 0,3 ml/dL para 2,3 ml/dL; Tabela 7).74 Além disso, a inalação intermitente de oxigénio a 100% em doentes sem doença pulmonar obstrutiva crónica (por exemplo, 6 horas de utilização/2 horas de desativação através de uma máscara sem respirador), ao longo de 3 a 4 dias, não é prejudicial para os pulmões e pode fornecer um substrato de oxigénio adicional bastante significativo, enquanto que o aumento e a diminuição intermitentes do fornecimento de oxigénio activam a expressão do fator indutor de hipóxia (um forte estímulo para a angiogénese).75 Isto sugeriria que, em vez da oxigenoterapia hiperbárica, o oxigénio normobárico se pode justificar para atenuar as condições na lista de indicações aprovadas pela FDA para o oxigénio hiperbárico (Tabela 7).76 Isto pode incluir lesões de reperfusão tecidular (por exemplo, lesões por esmagamento, síndromes de compartimento antes e depois da libertação cirúrgica); inibição de toxinas bacterianas (ou seja, mionecrose infecciosa ou outras infecções anaeróbias); ou defeitos em tecidos grandes (após desbridamento para manter a resposta inflamatória reactivada durante até 48 horas). O oxigénio normobárico fornece 50% da Po2 da oxigenoterapia hiperbárica típica (a 2 atmosferas); no entanto, muitos dos efeitos farmacológicos do oxigénio só são alcançados em doses hiperbáricas.77,78
Tabela 7. Mecanismos e sistemas de administração de oxigenoterapia normobárica
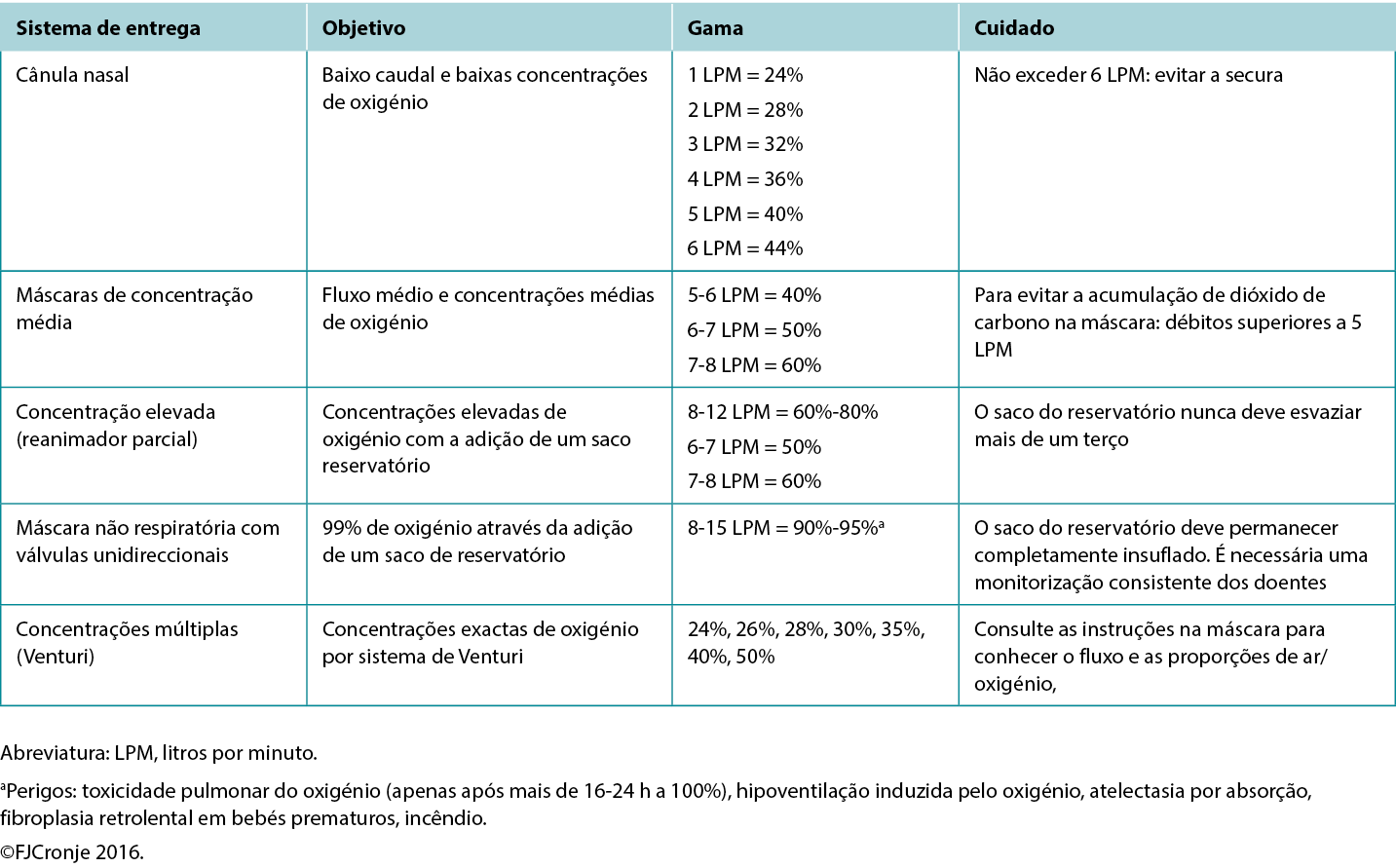
Note-se que a administração tópica de oxigénio diretamente a uma ferida não apresenta os mesmos efeitos fisiológicos que são atribuídos à administração sistémica de oxigénio.79 Os sistemas de administração tópica de oxigénio continuam a ser objeto de investigação contínua para poder determinar as suas acções benéficas para além da melhoria da epitelização e possivelmente, de um efeito antissético ligeiro.64 Este último efeito também foi atribuído à terapia com ozono.80 Uma revisão sistemática concluída em 2018 indicou que estas terapias poderiam potencialmente provocar um stress oxidativo ligeiro ou desinfeção, mas que o risco de toxicidade devido a espécies de oxigénio reactivas não controladas é elevado.81 Num ambiente de recursos limitados, estes dispositivos e a sua utilização provavelmente não são controlados.
Declaração 10: mudança do sistema de saúde
10A. Para todos os doentes facilitar cuidados informados com base em provas, culturalmente competentes e equitativos
10B. Reforçar as aptidões dos prestadores de cuidados de saúde em matéria de tratamento de feridas para melhorar os resultados para os doentes
10C. Estabelecer uma comunicação atempada e eficaz que inclua o doente e todos os membros da equipa interprofissional de tratamento de feridas, de forma a melhorar os resultados do sistema de cuidados de saúde
A nível mundial, o tratamento de feridas crónicas consome uma parte significativa dos recursos dos cuidados de saúde; em termos de custos, os cuidados preventivos representam a estratégia mais eficaz para conseguir reduzir as despesas do sistema de saúde. Existem numerosas abordagens para integrar os cuidados preventivos na prática. Por exemplo, as DFU são famosas por conduzirem a elevadas taxas de amputação e de morbilidade a nível mundial, apesar de muitas DFU serem evitáveis. Embora inicialmente se acreditasse que a diabetes fosse mais prevalente em países desenvolvidos, é de salientar que 80% das mortes relacionadas com a diabetes ocorrem em países com recursos limitados.82 Uma ferramenta de rastreio validada, uma equipa interprofissional instruída e disponível e a implementação de algoritmos de prevenção podem ser utilizados em países, independentemente da disponibilidade de recursos.83-85 Outras estratégias organizacionais que podem ser implementadas incluem as seguintes.
Navegação do doente. A gestão de uma DFU requer o apoio contínuo de um círculo de cuidados, o qual inclui membros da família e profissionais de saúde (incluindo cuidados domiciliários e tratamento de feridas) e que trabalham em equipa. O acesso atempado aos serviços de saúde e sociais é frequentemente necessário para prevenir e curar as DFUs. Os serviços integrados de diabetes, regionalizados e baseados na comunidade, ligados a clínicas interprofissionais de tratamento de feridas, estão a revelar-se mais bem sucedidos.86
Uma forma eficaz de garantir cuidados óptimos e atempados é a navegação do doente. Este conceito é adaptável a todos os sectores dos cuidados de saúde e pode melhorar o diagnóstico e o tratamento atempado das infecções das feridas, otimizar a gestão da dor e aumentar o acesso a cuidados especializados, acelerando dessa forma as taxas de encerramento das feridas.87 A navegação do doente está a tornar-se uma componente vital dos cuidados integrados, facilitando a transição sem problemas entre sectores e melhorando os resultados clínicos. Além disso, é acompanhada por um aumento da moral do doente e do profissional de saúde, pela diminuição dos internamentos hospitalares não agudos ou das readmissões, pelo aumento da qualidade de vida do doente e pela melhor adesão aos protocolos de tratamento. Todos estes factores combinados geram poupanças de custos significativas para os sistemas de saúde.87,88
Um elemento crítico dos programas de navegação de pacientes bem-sucedidos está na inclusão de uma abordagem abrangente e sistemática para orientar os profissionais de saúde na avaliação e prestação de cuidados a cada paciente de forma individual (por exemplo, a estrutura WBP). Estes percursos não têm de ser complicados ou demorados, mas devem assegurar o cumprimento de critérios específicos, incluindo cuidados regulares com os pés em pessoas com elevado risco de amputação, controlo glicémico para uma HbA1c inferior a 9% e uma PA inferior a 130/90 mm Hg.23,89
Política de intervenções. As políticas organizacionais que detalham e fornecem orientações sobre intervenções e percursos das melhores práticas são cruciais para a implementação bem-sucedida e sustentável de protocolos de tratamento de feridas. Basear estas políticas nas directrizes atualmente publicadas para cada tipo específico de ferida e traduzi-las para o ambiente em que devem servir. A instituição tem que as aceitar como normas de prática e serem aprovadas como tal, de forma a servir como cuidados baseados na evidência em ambientes em que outras orientações podem não ser adoptadas com êxito devido a desafios culturais ou de tradução linguística. Além disso, estas políticas devem definir claramente o processo de introdução e de utilização de dados, uma vez que as iniciativas de melhoria contínua da qualidade se baseiam em dados para aperfeiçoar e manter processos de cuidados eficazes.
Tratamento adaptado de feridas. Embora a prestação de cuidados de saúde deva de ser adaptada às necessidades específicas de cada sector de cuidados de saúde, certos conceitos devem ser uniformes, em especial os que melhoram a comunicação eficaz dentro e entre sectores. A adoção crescente da tecnologia digital acelera as avaliações, melhora o acesso a cuidados especializados e optimiza a afetação de recursos limitados.90 Quando as adaptações são implementadas como processos de cuidados, estas práticas devem de estar bem documentadas como normas de cuidados e ser facilmente acessíveis, de forma a garantir a coerência e a continuidade dos cuidados nas respectivas instituições.
Destaques do consenso delphi
Alguns comentários importantes do painel:
- A capacidade de curar (curabilidade) é uma modalidade mutável e não deve ser vista como uma classificação estática, uma vez que o estado do doente, as circunstâncias e as escolhas vão determinar o processo de atribuição da classificação (3A).
- O ajuste da prática, conforme necessário nas feridas de manutenção, incorpora o estabelecimento de uma abordagem conservadora do leito da ferida, com atenção às concessões que o doente está disposto a aceitar no âmbito das suas escolhas de vida, para assegurar lentamente a otimização do doente e, subsequentemente, aumentar a competência da instituição (3B).
- Quando o método de documentação do doente é acordado dentro de uma instituição, deve ser utilizado uniformemente de modo a evitar falhas de comunicação entre os prestadores de cuidados de saúde que possam inadvertidamente vir a causar um impacto negativo nos resultados dos cuidados de saúde do doente (4A).
- Os colutórios antissépticos que são adequados para a mucosa também podem ser utilizados no leito da ferida (4B). Esta pode ser considerada uma utilização não autorizada.
- A escolha para o controlo da carga bacteriana tópica deve recair sobre antissépticos tópicos de (baixa) toxicidade (os cinco mais importantes), dependendo da capacidade de cicatrização e das prioridades da carga bacteriana a tratar. Evitar a utilização de preparações antibióticas tópicas, de pomadas e de cremes em feridas crónicas, uma vez que estas preparações se concentram frequentemente apenas em organismos Gram-positivos e permitem que os organismos Gram-negativos e anaeróbios se multipliquem livremente no leito da ferida. Além disso, as preparações antibióticas tópicas necessitam apenas de uma mutação para criar resistência sistémica ao organismo visado. Os antibióticos tópicos encontram-se frequentemente num meio de transporte que está associado à dermatite de contacto irritante ou alérgica (6A e 6B).
- Quando uma ferida cicatrizável tem uma carga de humidade significativa e continua a necessitar de pensos superabsorventes para controlar o equilíbrio de humidade do leito da ferida, esta necessita de uma reavaliação completa para se garantir que todas as causas subjacentes foram corrigidas (7B).
- Ao estabelecer uma equipa interprofissional, utilizar todos os meios de comunicação para criar e manter essa equipa, uma vez que isso poderá otimizar significativamente a capacidade local, apesar das distâncias entre os prestadores e os especialistas, para melhorar os resultados clínicos, apesar das limitações locais (9B).
Conclusões
Otimizar o tratamento de feridas crónicas em ambientes com recursos limitados, iniciando pequenas adaptações e intervenções criativas, sem comprometer os princípios fundamentais dos cuidados necessários. As equipas interprofissionais de tratamento de feridas podem servir como um recurso virtual em comunidades isoladas e remotas, de forma a melhorar os resultados clínicos. Todos os elementos críticos para a gestão e cuidados com o pé (diabético) podem ser facilmente incorporados em ambientes diversos, aumentando a capacidade local e fornecendo aos doentes educação clínica e capacitação culturalmente adequada.
Lições práticas
- Os cuidados holísticos das pessoas com diabetes incluem a otimização dos níveis de HbA1c, de PA, dos níveis de colesterol e de medicamentos com propriedades protectoras a nível cardíaco e renal.
- O sinal de pulso Doppler portátil audível de 8 MHz é um teste de cabeceira adequado relativamente ao fornecimento de sangue arterial aos membros inferiores. Pode ser realizado como uma modificação do IPTB tradicional, sendo que os sons de pulso são facilmente verificáveis por membros remotos da equipa de peritos, utilizando gravações MP3 ou MP4 de um telemóvel.
- As mnemónicas NERDS e STONEES podem orientar o diagnóstico e o tratamento da infeção local/profunda e circundante, incluindo uma indicação para o antibiótico oral para a osteomielite.
- A redistribuição da pressão plantar pode ser conseguida a partir de alternativas inovadoras e menos dispendiosas, tais como inserções simples de feltro macio, até ao gesso de contacto total e ao andarilho com gesso amovível, tornado inamovível se este último não estiver disponível ou não for adequado às preferências do doente ou às suas atividades do dia a dia.
- As equipas de cuidados coordenados integrados podem ligar-se a uma especialização virtual, equipando os profissionais de saúde com competências em navegação de doentes.
- Em locais com recursos limitados, os kits de ferramentas que contêm elementos facilitadores para a prática, juntamente com Dopplers de 8 MHz e termómetros de infravermelhos, podem facilitar os cuidados.
Conflito de interesses
Os autores declaram não existirem conflitos de interesse.
Financiamento
Os autores não receberam financiamento para este estudo.
Author(s)
Hiske Smart*
MA RN PG Dip (UK)
Clinical Nurse Specialist: Wound Specialist Services King Hamad American Mission Hospital, A’Ali, Kingdom of Bahrain
R Gary Sibbald
MD Med FRCPC (Med Derm) FAAD MAPWCA JM
Professor of Medicine and Public Health, Dalla Lana School of Public Health, University of Toronto, Ontario, Canada
Laurie Goodman
MHScN RN Advanced Practice Nurse
WoundPedia, Mississauga, Ontario, Canada
Elizabeth A Ayello
PhD RN CWON ETN MAWPCA FAAN
President, Ayello Harris & Associates, Inc, Copake, New York, USA
Reneeka Jaimangal
MD MDcCH IIWCC
Project Manager, Project ECHO Ontario Skin and Wound Care, WoundPedia, Mississauga, Ontario, Canada
John H Gregory
BEng
President, Opencity Inc, Kitchener, Ontario, Canada
Sadanori Akita
MD PhD
Professor, Fukushima Medical University, Fukuoka, Japan
Afsaneh Alavi
MD FRCPC
Professor of Dermatology, Mayo Clinic, Rochester, Minnesota, USA
David G Armstrong
DPM MD PhD
Professor of Surgery, Keck School of Medicine, University of Southern California, Los Angeles, California, USA
Helen Arputhanathan
MSc RN NSWOC WOCC(C)
Manager, Patient Services & Clinical Wound Care, Home and Community Care Support Services, Hamilton Niagara Haldimand Brant, Waterloo, Ontario, Canada
Febe Bruwer
PhD (UFS) MSocSci MSc
Advanced Nurse Specialist and Unit Manager of the Wound Clinic, Life Roseacres Hospital, Germiston, South Africa
Jeremy Caul
MClSc-WH RN WOCC(c)
Nurse Advisor, Home and Community Care, Ontario Region for Indigenous Services Canada/First Nations and Inuit Health Branch, Ontario, Canada
Beverley Chan
MD MSc,FRCSC
Vascular Surgeon and Division Lead, Halton Healthcare, Oakville, Ontario, Canada
Frans Cronje
MBChB MSc
Aerospace Medicine, PGDOccMed, Fellow EHM (Duke), Aviation and Aerospace Medical Specialist, Head of Department Baromedicine, King Hamad American Mission Hospital, A’ali, Kingdom of Bahrain
Belen Dofitas
MD PhD
Associate Professor, Department of Dermatology, College of Medicine & Philippine General Hospital, University of the Philippines, Manila
Jassin Hamed
MD
Consultant Internal Medicine, COO Global Care Hospital, Abu Dhabi, United Arab Emirates
Catherine Harley
eMBA RN
Chief Executive Officer, Nurses Specialized in Wound, Ostomy and Continence Canada, Ottawa, Ontario, Canada
Jolene Heil
MclSc-WH RN NSWOC
Advanced Practice Nurse and Clinical Nurse Specialist—Wound Care, Providence Care, Kingston, Ontario, Canada
Mary Hill
MN BScN RN NSWOC WOCC(C)
NSWOC Educator/Consultant CAT Team, Integrated Home Care—Calgary Zone, Alberta, Canada
Devon Jahnke
DCh MCISc-WH
Chiropodist, Complex Centre for Diabetes Care, Health Sciences North, Sudbury Outpatient Centre, Ontario, Canada
Dale Kalina
MD MBA FRCPC (ID)
Chief Medical Information Officer, Brant Community Healthcare System, Brantford, Ontario, Canada
Chaitanya Kodange
MBBS DMM DHA MD (Psy) IIWCC-UAE
Consultant Diving, Hyperbaric and Wound Care & Psychiatrist, King Hamad University Hospital, Kingdom of Bahrain
Bharat Kotru
PhD MSc DPM
Podiatrist and Wound Care Specialist, Advance Foot & Wound Care Centre, Amandeep Group of Hospitals, Amritsar, Punjab, India
Laura Lee Kozody
DCh
Chiropodist, Toronto Regional Wound Healing Clinic, Mississauga, Ontario, Canada
Stephan Landis
MD FRCPC
Consultant, Guelph General Hospital Ambulatory Wound Clinic, Guelph, Ontario, Canada
Kimberly LeBlanc
PhD RN NSWOC WOCC(C) FCAN
Academic Chair, Nurses Specializing in Wound, Ostomy and Continence Canada, Ottawa, Ontario, Canada
Mary MacDonald
MD PhD FRCSC
Assistant Professor, School of Medicine, NOSM University, and Vascular Surgeon, Thunder Bay Regional Health Sciences Centre, Thunder Bay, Ontario, Canada
Tobi Mark
BSc DCh
Associate Professor of Chiropody, The Michener Institute of Education at UHN, Toronto, Ontario, Canada
Carlos Martin
DM PG-Dip MBBS
Consultant, Vascular Surgery, Georgetown Public Hospital Corporation, Guyana
Dieter Mayer
MD FAPWCA Consultant, Institute for Advanced Wound Care & Education, Hausen am Albis, Switzerland
Christine Murphy
PhD MClSc-WH RN NSWOC WOCC(C)
Advanced Practice Nurse, The Ottawa Hospital, Ontario, Canada
Harikrishna Nair
MD PhD FRCPI FRCPE FCWCS
Head and Senior Wound Care Physician, Wound Care Unit, Department of Internal Medicine, Kuala Lumpur Hospital, and Professor, Faculty of Medicine, Lincoln University College, Malaysia
Cesar Orellana
MD FRCPC FACP
Infectious Diseases Consultant, Grand River Hospital and St Mary’s General Hospital, Kitchener, Ontario, Canada
Brian Ostrow
MD BSc FRCS(C)
Adjunct Assistant Professor (retired), Department of Surgery, University of Toronto, Ontario, Canada
Douglas Queen
PhD MBA
Chief Executive Officer, Medicalhelplines.com Inc, Toronto, Ontario, Canada
Patrick Rainville
DCh,
Owner, Rainville Foot Health, Timmins, Ontario, Canada
Erin Rajhathy
MclSc-WH RN NSWOC WOCC(C)
Doctoral Student, Swedish Centre for Skin and Wound Research, Nursing Science Unit, School of Health Sciences, Faculty of Medicine and Health, Örebro University, Örebro, Sweden
Gregory Schultz
PhD
Professor Emeritus, University of Florida, Gainesville, Florida, USA
Ranjani Somayaji
MD MPH FRCPC
Associate Professor, University of Calgary, Calgary, Canada
Michael C Stacey
DS MBBS FRACS
Vascular Surgeon and Professor of Surgery, McMaster University, Hamilton, Ontario, Canada
Gulnaz Tariq
MSc (UK) RN PG Dip (PAK)
Director of Wound Care & Education, Global Care Hospital, Abu Dhabi, United Arab Emirates
Gregory Weir
MBChB Mmed (Ch)
Vascular Surgeon, Life Eugene Marais Hospital, Pretoria, South Africa
Catharine Whiteside
MD PhD CM FRCPC
Professor Emerita and Former Dean of Medicine, University of Toronto, Ontario, Canada
Helen Yifter
MD
Associate Professor of Medicine, University of Rwanda, Kigali, Rwanda
Ramesh Zacharias
MD FRCS(C)
Assistant Clinical Professor, Anesthesia, Faculty of Health Sciences, McMaster University, Hamilton, Ontario, Canada
* Corresponding author
References
- Sibbald RG, Williamson D, Orsted HL, et al. Preparing the wound bed—debridement, bacterial balance and moisture balance. Ostomy Wound Manage 2000;46(11):14-35.
- Fitridge R, Chuter V, Mills J, et al. The intersocietal IWGDF, ESVS, SVS guidelines on peripheral artery disease in people with diabetes mellitus and a foot ulcer. J Vasc Surg 2023;78(5):1101-31.
- Sibbald RG, Elliott JA, Persaud-Jaimangal R, et al. Wound Bed Preparation 2021. Adv Skin Wound Care 2021;34(4):183-95.
- Alavi A, Sibbald RG, Nabavizadeh R, Valaei F, Coutts P, Mayer D. Audible handheld Doppler ultrasound determines reliable and inexpensive exclusion of significant peripheral arterial disease. Vascular 2015;23(6):622-9.
- Dworak M, Andraska EA, Gharacholou SM, Myers M, Chapman SC. Fluorescent angiography used as a tool to guide angiosome-directed endovascular therapy for diabetic foot ulcers. J Vasc Surg Cases Innov Tech 2021;7(1):159-63.
- Sassaki VS, Fukaya E. Varicose veins: approach, assessment, and management to the patient with chronic venous disease. Med Clin North Am 2023;107(5):895-909.
- Armstrong DG, Boulton AJM, Sicco AB. Diabetic foot ulcers and their recurrence. N Engl J Med 2017;376(24):2367-75.
- Eikelboom JW, Connolly SJ, Bosch J, et al. Rivaroxaban with or without aspirin in stable cardiovascular disease. N Engl J Med 2017;377(14):1319-30.
- Levin ME. An overview of the diabetic foot: pathogenesis, management and prevention of lesions. Int J Diab Dev Countries 1994;14:39-47.
- Bekele F, Chelkeba L, Fekadu G, Bekele K. Risk factors and outcomes of diabetic foot ulcer among diabetes mellitus patients admitted to Nekemte referral hospital, Western Ethiopia: prospective observational study. Ann Med Surg (Lond) 2020;51:17-23.
- Govindasamy K, Darlong J, Watson SI, Gill P. Prevalence of plantar ulcer and its risk factors in leprosy: a systematic review and meta-analysis. J Foot Ankle Res 2023;16(1):77.
- Sibbald RG, Ayello EA, Alavi A, et al. Screening for the high-risk diabetic foot: a 60-Second Tool. Adv Skin Wound Care 2012;25(10):465-76.
- Sibbald RG, Mufti A, Armstrong DG. Infrared skin thermometry: an underutilized cost-effective tool for routine wound care practice and patient high-risk diabetic foot self-monitoring. Adv Skin Wound Care 2015;28(1):37-44.
- Amemiya A, Noguchi H, Oe M, et al. Factors associated with callus formation in the plantar region through gait measurement in patients with diabetic neuropathy: an observational case-control study. Sensors 2020;20:4863.
- Armstrong DG, Swerdlow MA, Armstrong AA, Conte MS, Padula WV, Bus SA. Five year mortality and direct costs of care for people with diabetic foot complications are comparable to cancer. J Foot Ankle Res 2020;13(1):16.
- Diabetes Canada Clinical Practice Guidelines Expert Committee. Diabetes Canada 2018 clinical practice guidelines for the prevention and management of diabetes in Canada. Can J Diabetes 2018;42(Suppl 1):S1-325.
- Zhang X, Yang X, Sun B, et al. Perspectives of glycemic variability in diabetic neuropathy: a comprehensive review. Commun Biol 2021;4:1366.
- Bril V, Breiner A, Perkins BA, Zochodne D. Diabetes Canada 2018 clinical practice guidelines for the prevention and management of diabetes in Canada. Neuropathy. Can J Diabetes 2018;42:S217-21.
- Soyoye DO, Abiodun OO, Ikem RT, Kolawole BA, Akintomide AO. Diabetes and peripheral artery disease: a review. World J Diabetes 2021;12(6):827-38.
- Song P, Rudan D, Zhu Y, et al. Global, regional, and national prevalence and risk factors for peripheral artery disease in 2015: an updated systematic review and analysis. Lancet Glob Health 2019;7:e1020-30.
- Williams B, Mancia G. Ten commandments of the 2018 ESC/ESH HTN guidelines on hypertension in adults. Eur Heart J 2018;39:3007-8.
- Dagenais GR. Vascular protection: telmisartan in the ONTARGET trial programme. Eur Heart J Suppl 2009;11(suppl_F):F47-53.
- Gerstein HC. Diabetes and the HOPE study: implications for macrovascular and microvascular disease. Int J Clin Pract Suppl 2001;(117):8-12.
- Fonseca-Correa JI, Correa-Rotter R. Sodium-glucose cotransporter 2 inhibitors mechanisms of action: a review. Front Med 2021;8:777861.
- Rasmussen BSB, Yderstraede KB, Carstensen B, et al. Substantial reduction in the number of amputations among patients with diabetes: a cohort study over 16 years. Diabetologia 2016;59:121-9.
- de Mestral C, Hussain MA, Austin PC, et al. Regional health care services and rates of lower extremity amputation related to diabetes and peripheral artery disease: an ecological study. CMAJ Open 2020;8(4):E659-66.
- Baird R, Cosh L, Bruser G, Rowe R, Walker J. Indigenous Diabetes Health Circle: Foot Care Evaluation Program. April 2022. https://idhc.life/wp-content/uploads/2023/02/IDHC_Foot-Care-Research-Report.pdf. Last accessed January 3, 2024.
- Bus SA, Armstrong DG, Crews RT, et al. Guidelines on offloading foot ulcers in persons with diabetes (IWGDF 2023 update). Diabetes Metab Res Rev 2023:e3647.
- Withers RV, Perrin BM, Landorf KB, et al. Offloading effects of a removable cast walker with and without modification for diabetes-related foot ulceration: a plantar pressure study. J Foot Ankle Res 2023;16:27.
- Moffatt CJ, Franks PJ, Hollinworth H. Understanding wound pain and trauma: an international perspective. In: Pain at Wound Dressing Changes: A Position Document. European Wound Management Association; 2002:2-7.
- Queen D, Woo K, Shulz VN, Sibbald RG. Chronic wound pain and palliative cancer care. Ostomy Wound Manage 2003;49(10):16-8.
- Reddy M, Kohr R, Queen D, Keast D, Sibbald RG. Practical treatment of wound pain and trauma: a patient-centered approach. An overview. Ostomy Wound Manage 2003;49(4A):2-15.
- Boonstra AM, Stewart RE, Köke AJ, et al. Cut-off points for mild, moderate, and severe pain on the numeric rating scale for pain in patients with chronic musculoskeletal pain: variability and influence of sex and catastrophizing. Front Psychol 2016;7:1466.
- Byma EA, Wheeler H. The experience of new graduate registered nurses as managers of pain. Pain Manage Nurs 2021;22(3):429-35.
- D’Souza RS, Barman R, Joseph A, Abd-Elsayed A. Evidence-based treatment of painful diabetic neuropathy: a systematic review. Curr Pain Headache Rep 2022;26(8):583-94.
- Sibbald RG, Hastings-Truelove A, DeJong P, Ayello EA. Reconciliation and diversity for educators: the medicine wheel, Bloom’s taxonomy, and CanMEDS competencies. Adv Skin Wound Care 2023;36(2):64-6.
- Murphy A, McGowan C, McKee M, et al. Coping with healthcare costs for chronic illness in low-income and middle-income countries: a systematic literature review. BMJ Global Health 2019;4:e001475.
- Okediji PT, Ojo AO, Ojo AI, Ojo AS, Ojo OE, Abioye-Kuteyi EA. The economic impacts of chronic illness on households of patients in Ile-Ife, South-western Nigeria. Cureus 2017;9(10):e1756.
- Adelman RD, Tmanova LL, Delgado D, Dion S, Lachs MS. Caregiver burden: a clinical review. JAMA 2014;311(10):1052-60.
- Kodange C. Screening for depression in patients with chronic wounds. Adv Skin Wound Care 2021;34(9):502-3.
- Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care 2022;45(11):2753-86.
- Boersema GC, Smart H, Giaquinto-Cilliers MGC, et al. Management of nonhealable and maintenance wounds: a systematic integrative review and referral pathway. Adv Skin Wound Care 2021;34(1):11-22.
- Ebbers T, Kool RB, Smeele LE, et al. The impact of structured and standardized documentation on documentation quality; a multicenter, retrospective study. J Med Syst 2022;46(7):46.
- Onuh OC, Brydges HT, Nasr H, Savage E, Gorenstein S, Chiu E. Capturing essentials in wound photography past, present, and future: a proposed algorithm for standardization. Adv Skin Wound Care 2022;35:483-92.
- World Health Organization. International Statistical Classification of Diseases and Related Health Problems (ICD). 2023. www.who.int/standards/classifications/classification-of-diseases. Last accessed January 3, 2024.
- Wurster F, Fütterer G, Beckmann M, et al. The analyzation of change in documentation due to the introduction of electronic patient records in hospitals—a systematic review. J Med Syst 2022;46(8):54.
- Nair HK, Ahmad NW, Ismail AA, et al. Maggot debridement therapy to treat hard-to-heal diabetic foot ulcers: a single-centre study. J Wound Care 2021;30(Sup12):S30-6.
- Williams KA, Cronje FJ, Avenant L, Villet MH. Identifying flies used for maggot debridement therapy. S Afr Med J 2008;98(3):196-9.
- Tran DL, Huang RW, Chiu ES, et al. Debridement: technical considerations and treatment options for the interprofessional team. Adv Skin Wound Care 2023;36(4):180-7.
- Woo KY, Sibbald RG. A cross-sectional validation study of using NERDS and STONEES to assess bacterial burden. Ostomy Wound Manage 2009;55(8):40.
- Angel DE, Lloyd P, Carville K, Santamaria N. The clinical efficacy of two semi‐quantitative wound‐swabbing techniques in identifying the causative organism(s) in infected cutaneous wounds. Int Wound J 2011;8(2):176-85.
- Rawlinson S, Ciric L, Cloutman-Green E. How to carry out microbiological sampling of healthcare environment surfaces? A review of current evidence. J Hosp Infect 2019;103(4):363-74.
- Hatzenbuehler J, Pulling TJ. Diagnosis and management of osteomyelitis. Am Fam Physician 2011;84(9):1027-33.
- Sibbald RG, Elliott JA, Ayello EA, Somayaji R. Optimizing the moisture management tightrope with Wound Bed Preparation 2015©. Adv Skin Wound Care 2015;28(10):466-76.
- Joshi N, Caputo GM, Weitekamp MR, Karchmer AW. Infections in patients with diabetes mellitus. N Engl J Med 1999;341(25):1906-12.
- McLain NE, Moore ZE, Avsar P. Wound cleansing for treating venous leg ulcers. Cochrane Database Syst Rev 2021;3(3):CD011675.
- Sibbald RG, Goodman L, Woo KY, et al. Special considerations in Wound Bed Preparation 2011: an update©. Adv Skin Wound Care 2011;24(9): 415-36.
- Block MS, Rowan BG. Hypochlorous acid: a review. J Oral Maxillofacial Surg 2020;78(9):1461-6.
- International Wound Infection Institute. Wound infection in clinical practice: principles of best practice. 3rd ed. Wounds Int 2022:1-60.
- Giaquinto-Cilliers MGC. Classification of dressings: a framework adapted to the Wound Bed Preparation Paradigm. Wound Heal South Afr 2023;16(2):31-3.
- Berezo M, Budman J, Deutscher D, Hess CT, Smith K, Hayes D. Predicting chronic wound healing time using machine learning. Adv Wound Care 2022;11(6):281-96.
- Pavlovčič U, Diaci J, Možina J, et al. Wound perimeter, area, and volume measurement based on laser 3D and color acquisition. Biomed Eng Online 2015;14(39).
- Laporte M, Keller HH, Payette H, et al. Validity and reliability of the new Canadian Nutrition Screening Tool in the ‘real-world’ hospital setting. Eur J Clin Nutr 2015;69(5):558-64.
- Feldmeier JJ, Hopf HW, Warriner R3, Fife CE, Gesell LB, Bennett M. UHMS position statement: topical oxygen for chronic wounds. Undersea Hyperb Med 2005;32(3):157-68.
- Guzman KJ, Gemo N, Martins DB, et al. Current challenges of plastic surgical care in sub-Saharan Africa (Maputo, Mozambique). Plast Reconstr Surg Glob Open 2018;6(8):e1893.
- Jones JE, Nelson EA. Skin grafting for venous leg ulcers. Cochrane Database Syst Rev 2007;(2):CD001737.
- Kirketerp-Møller K, Doerfler P, Schoefmann N, et al. Biomarkers of skin graft healing in venous leg ulcers. Acta Derm Venereol 2022;102:adv00749.
- Thakral G, Lafontaine J, Najafi B, Talal TK, Kim P, Lavery LA. Electrical stimulation to accelerate wound healing. Diabetes Foot Ankle 2013;4.
- Chaput B, Garrido I, Eburdery H, Grolleau JL, Chavoin JP. Low-cost negative-pressure wound therapy using wall vacuum: a 15 dollars by day alternative. Plast Reconstr Surg Glob Open 2015;3(6):e418.
- Estillore KM, Quevedo GL, Bonifacio LR. Improvised suction apparatus for closure of large soft tissue deficit. Malaysian Orthop J 2013;7(2):29.
- Farré R, Rodríguez-Lázaro MA, Gonzalez-Martin J, et al. Device for negative pressure wound therapy in low-resource regions: open-source description and bench test evaluation. J Clin Med 2022;11(18):5417.
- Rose S, Sardar S, Sasi S, Al Mohanadi DH, Al-Mohammed AA, Zahid M. Time for change in practice of in-patient oxygen therapy: a period-limited, multidimensional approach to improve oxygen prescription compliance: quality improvement project at Hamad General Hospital, Qatar. BMJ Open Qual 2021;10(4):e001574.
- McAllister S, Thorn L, Boladuadua S, et al. Cost analysis and critical success factors of the use of oxygen concentrators versus cylinders in sub-divisional hospitals in Fiji. BMC Health Serv Res 2021;21(1):1-7.
- Jain KK. Physical, physiological, and biochemical aspects of hyperbaric oxygenation. In: Jain KK, ed. Textbook of Hyperbaric Medicine. 6th ed. Springer; 2017:11-22.
- Chang AJ, Bargmann CI. Hypoxia and the HIF-1 transcriptional pathway reorganize a neuronal circuit for oxygen-dependent behavior in Caenorhabditis elegans. Proc Natl Acad Sci USA 2008;105(20):7321-6.
- Moon RE. Hyperbaric Oxygen Therapy Indications. North Palm Beach, FL: Best Publishing Company; 2019.
- Chazalviel L, Blatteau JE, Vallée N, Risso JJ, Besnard S, Abraini JH. Effects of normobaric versus hyperbaric oxygen on cell injury induced by oxygen and glucose deprivation in acute brain slices. Med Gas Res 2016;6(3):169-73.
- Velej V, Cankar K, Vidmar J. The effects of normobaric and hyperbaric oxygenation on MRI signal intensities in T1 -weighted, T2 -weighted and FLAIR images in human brain. Radiol Oncol 2023;57(3):317-24.
- UHMS position statement: topical oxygen for chronic wounds. Undersea Hyperb Med 2018;45(3):379-80.
- Rapone B, Ferrara E, Santacroce L, et al. The gaseous ozone therapy as a promising antiseptic adjuvant of periodontal treatment: a randomized controlled clinical trial. Int J Environ Res Public Health 2022;19(2):985.
- Fitzpatrick E, Holland OJ, Vanderlelie JJ. Ozone therapy for the treatment of chronic wounds: a systematic review. Int Wound J 2018;15(4):633-44.
- Woodbury M, Sibbald RG, Ostrow B, Persaud R, Lowe J. Tool for rapid & easy identification of high-risk diabetic foot: validation & clinical pilot of the simplified 60 second diabetic foot screening tool. PLoS One 2015;10(6):1-3.
- Abbas ZG, Lutale JK, Bakker K, Baker N, Archibald LK. The ‘step by step’ diabetic foot project in Tanzania: a model for improving patient outcomes in less-developed countries. Int Wound J 2011;8:169-75.
- Abbas ZG. Reducing diabetic limb amputations in developing countries. Expert Rev Endocrinol Metab 2015;10:425-34.
- Ousey K, Chadwick P, Jawien A, et al. Identifying and treating foot ulcers in patients with diabetes: saving feet, legs and lives. J Wound Care 2018;27(5 Suppl 5b).
- Heerschap C, Nicholas A, Whitehead M. Wound management: investigating the interprofessional decision-making process. Int Wound J 2019;16(1):233-42.
- Arputhanathan H, Hyde J, Atiloa T, Queen D, Elliott J, Sibbald RG. A patient navigation model to improve complex wound care outcomes. Adv Skin Wound Care 2022;35(9):499-508.
- Doucet S, Luke A, Anthonisen G, et al. Hospital-based patient navigation programmes for patients who experience injury-related trauma and their caregivers: a scoping review protocol. BMJ Open 2022;12:e055750.
- Narayan KMV, Zhang P, Kanaya AM, et al. Diabetes: the pandemic and potential solutions. In: Jamison DT, Breman JG, Measham AR, et al, eds. Disease Control Priorities in Developing Countries. 2nd ed. Washington, DC: World Bank; 2006:591-603.
- Kostovich CT, Etinggen B, Wirth M, et al. Outcomes of telehealth for wound care: a scoping review. Adv Skin Wound Care 2022;35(7):394-403.
Supplemental Table 1. Delphi consensus achieved among 41 contributors on 32 wound bed preparation (wbp) 2024 statements
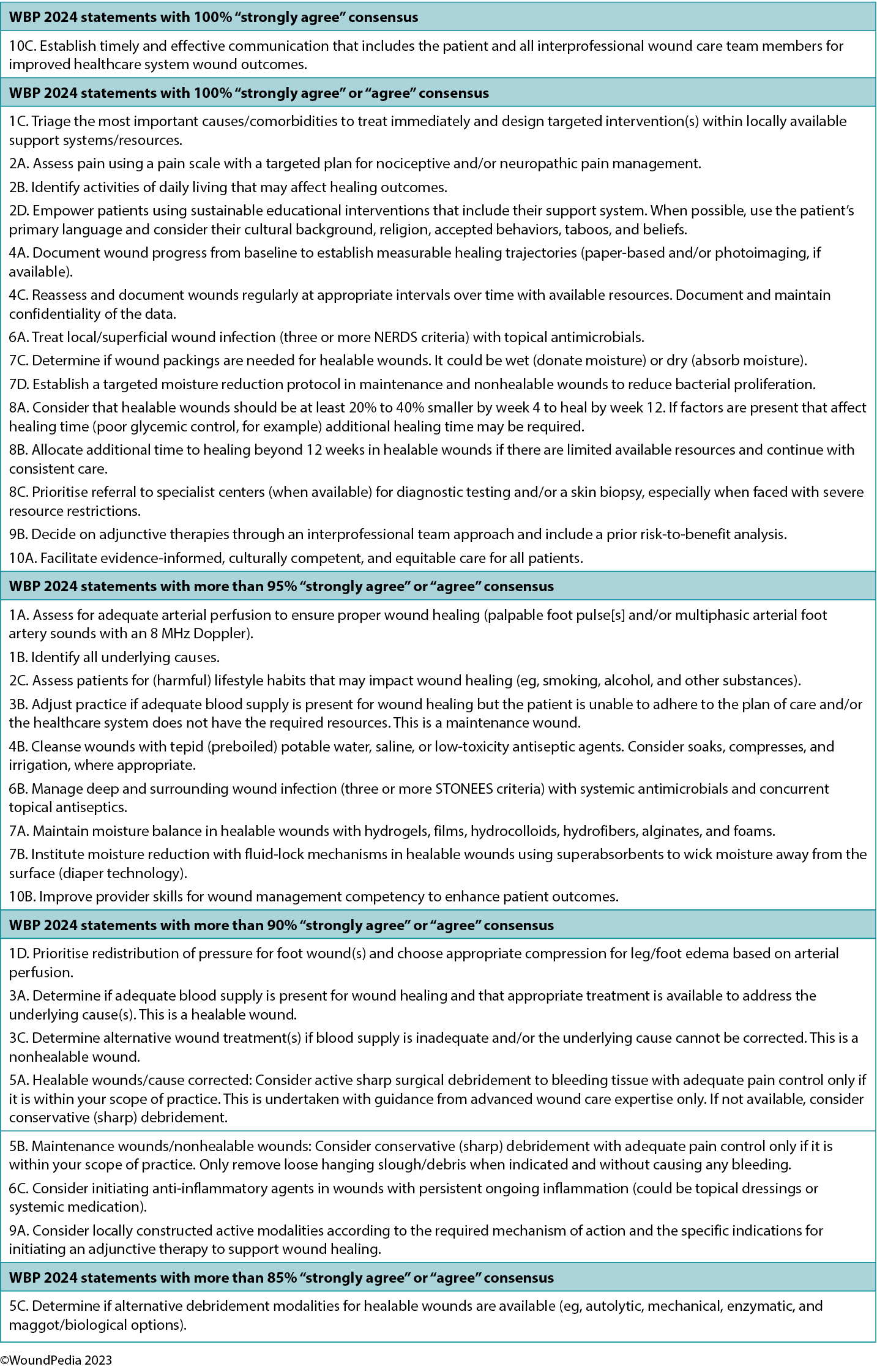
Supplement Table 2. Common antiseptic agents for nonhealable wounds
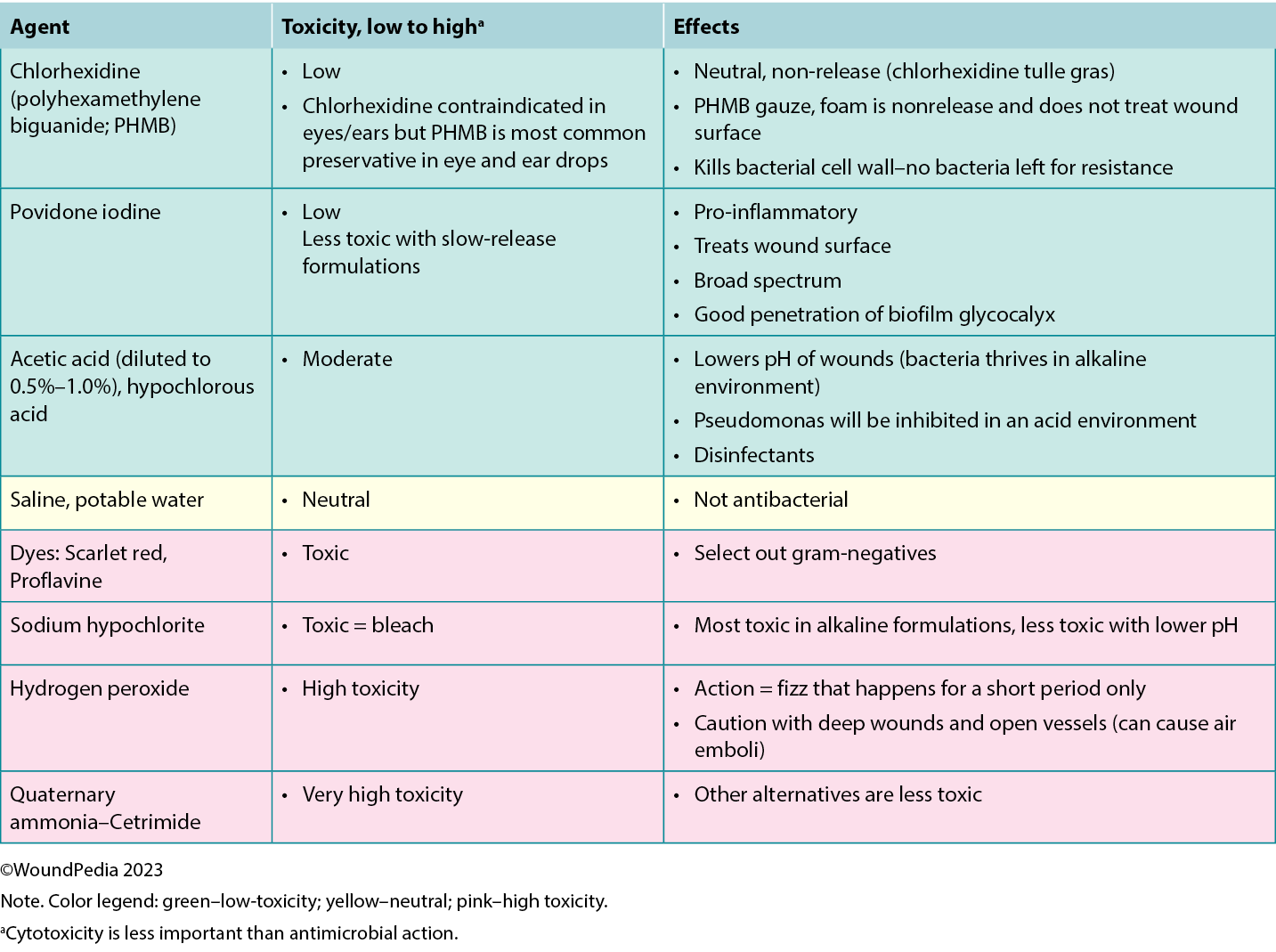
Tabela supplementar 1. Consenso Delphi alcançado entre 41 colaboradores sobre 32 declarações de preparação do leito da ferida(WBP) 2024
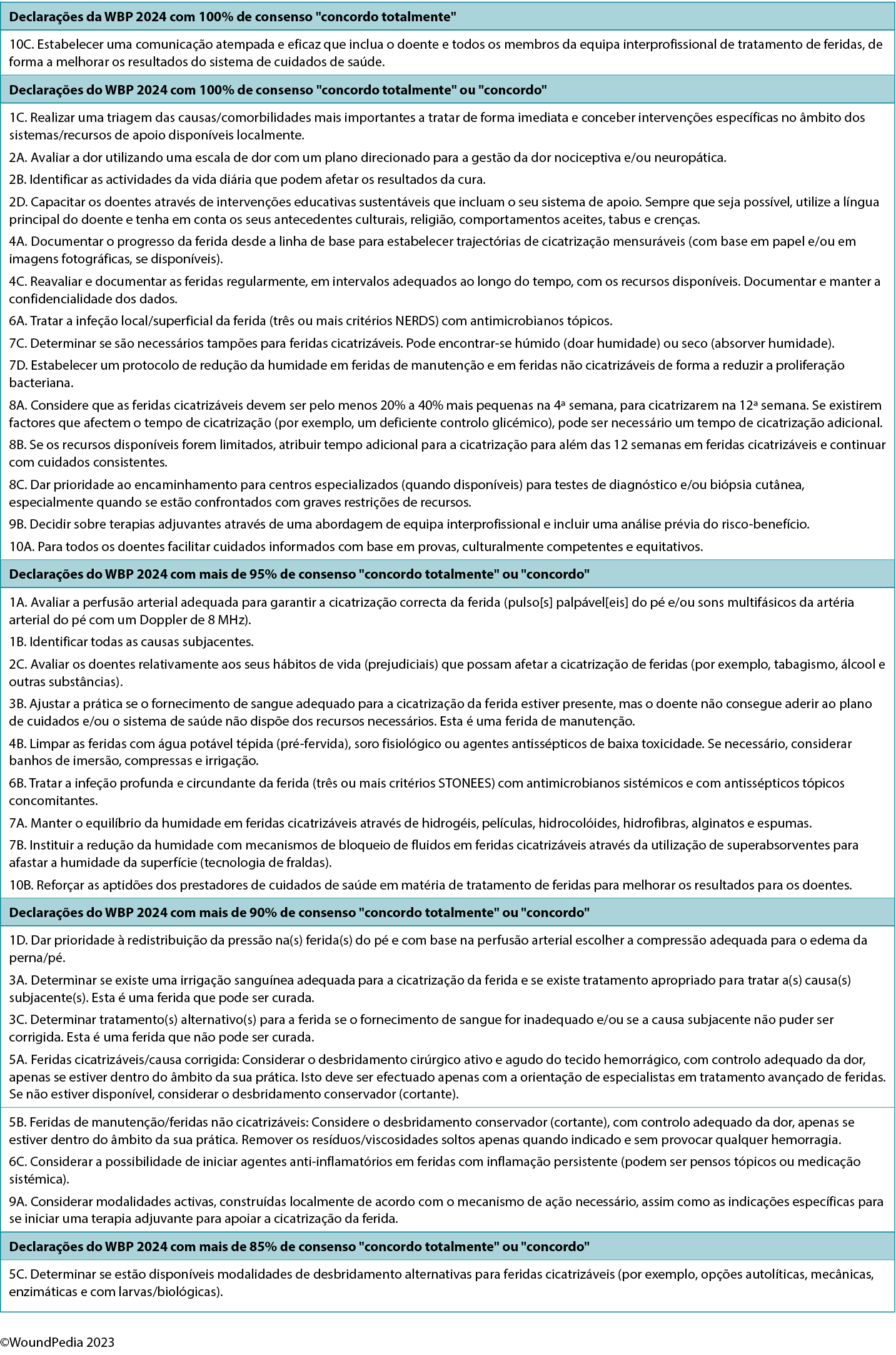
Tabela supplementar 2. Agentes antissépticos comuns para feridas não cicatrizáveis