Volume 41 Number 2
Budget impact of ceramide-infused skin barriers versus standard of care skin barriers for new ostomates: a six-country analysis
Ariel Berger, Gary Inglese, George Skountrianos, Davide Croce and Mustafa Oguz
Keywords ostomy, models, ceramides, economic evaluation, costs and cost analysis
For referencing Berger A et al. Budget impact of ceramide-infused skin barriers versus standard of care skin barriers for new ostomates: a six-country analysis. WCET® Journal 2021;41(2):22-31
DOI https://doi.org/10.33235/wcet.41.2.22-31
Abstract
Introduction In a randomised controlled study, the use of ceramide-infused skin barriers (CIB) resulted in lower costs of care over 12 weeks versus using a standard of care (SoC) skin barrier. However, the degree to which this information may influence prescribing patterns of ostomy products, and its corresponding impact on payers’ budgets, has not been examined.
Purpose To examine expected budget impact of CIB among recent ostomates in the United States (US), the United Kingdom (UK), Sweden, Australia, Italy and Norway.
Design A decision-analytic budget impact model.
Methods Total ostomy-related costs (i.e., skin barriers, ostomy accessories, care of peristomal skin complications [PSC]) were forecasted over 1 year for hypothetical cohorts of recent ostomates in each country of interest. Costs were assessed under two alternative scenarios – one in which all patients were assumed to use barriers other than CIB (the SoC scenario), and one in which 20% of patients were assumed to use CIB in lieu of SoC (the CIB scenario). The budget impact was assumed equal to the difference in these two scenarios.
Findings The use of CIB was expected to result in annual savings of US$6.6m in the US, £0.4m in the UK, SEK1.8m in Sweden, A$0.4m in Australia, €0.2m in Italy and NOK1.5m in Norway. Findings were consistent in sensitivity analyses.
Conclusions The use of CIB versus other barriers results in expected lower costs to the payers in each evaluated country. Further research is needed to better understand the complete clinical and economic benefits associated with the use of CIB.
Introduction
Faecal ostomy surgery is performed to treat both acute (e.g., trauma) and chronic (e.g., colorectal cancer, Crohn’s disease, ulcerative colitis) conditions. While effective for the underlying issue(s), an ostomy also has its own risk of complications, including peristomal skin complications (PSC) such as: mechanical, e.g., stripping or abraded skin; irritant dermatitis, typically caused by leakage that exposes the skin to ileostomy output; and infectious dermatitis. PSC are among the most commonly reported complications among ostomates, and may occur at any time following stoma creation1–3. Between 33.5% and 78.7% of ostomates report PSC4–11; one study estimated that 40% of consultations to ostomy clinics were for PSC12,. In 2011, the mean costs of care for PSC were estimated to range per ostomy from €32.45 for mild cases to €147.17 for severe cases, and the mean total costs of care (including ostomy pouching systems, accessories, visits to healthcare providers, hospitalisation and medications) over 7 weeks were shown to be approximately 22% greater among patients who experienced PSC versus those who did not5. PSC are also associated with deleterious impacts to quality of life, with a “loss” of approximately 11 quality-adjusted life-days (QALDs)/month for patients with severe PSC (versus no PSC)13.
CeraPlusTM is a novel skin barrier with Remois technology (Alcare Co Ltd, Sumida-ku, Tokyo, Japan) currently marketed by Hollister Inc. (Libertyville, Illinois, US). It is a ceramide-infused barrier (CIB) designed to support healthy peristomal skin. Ceramides are naturally occurring lipids that are essential to the barrier function of the skin and lipid bilayer of the stratum corneum14,15, and play an important role in the prevention of transepidermal water loss (TEWL) by fusing with corneocytes in the stratum corneum to help form a protective layer16,17.
In the ADVOCATE trial15 (a study determining variances in ostomy skin conditions and the economic impact: NCT02401412), 153 adults with healthy peristomal skin who had recently undergone ostomy surgery were randomly assigned to use CIB (n=79) or an alternative barrier (New Image FlexWear or New Image Flextend [Hollister Inc.]) (n=74). Over a maximum follow-up of 12 weeks (patients were assessed over 8 weeks, with those who experienced PSC observed for an additional 4-week “resolution period”), the mean costs of care among patients randomised to CIB were US$36.36 less than those randomised to control barrier (US$223.73 vs. US$260.19; p=0.017); they also were nominally less likely to experience PSC during follow-up15. A subsequent cost-effectiveness analysis indicated that the use of CIB among a hypothetical cohort of 100 Australian patients was expected, over 1 year, to result in 16 fewer PSC, an additional 35 QALDs, and a reduction in healthcare costs of A$13,700 (all versus standard of care [SoC]); the resulting net monetary benefit was A$17,400, indicating that CIB was a cost-effective alternative to SoC18.
Study/publication purpose
While CIB has been found to be cost-effective versus other barriers in both ADVOCATE and subsequent economic modelling, healthcare payers must also consider the overall expected impact to budgets (i.e., affordability) associated with the adoption of new technologies. Practitioners play an important role in the care of new ostomates, and are often asked to balance patients’ needs with cost-containment pressures imposed upon them by payers. Accordingly, findings presented herein are likely of great interest to nurse clinicians and other providers of care for this vulnerable population as it uses published information on patient-level efficacy and on the safety of CIB to estimate their expected value to payers.
To examine this and related questions, we developed a decision-analytic model that could estimate the budget impact associated with the use of CIB in lieu of other skin barriers. This model was estimated for the United States (US), the United Kingdom (UK), Sweden, Australia, Italy and Norway, based on information from ADVOCATE and supplemented with other sources where appropriate.
Methods and Procedures
Model overview
All patients were assumed to begin the model within 12 weeks of faecal stoma surgery outside hospital settings using either a CIB pouching system or a SoC system. The distribution of patients by ostomy type was assumed to be consistent with that reported by ADVOCATE and to be similar between patients who would use CIB versus SoC – 39%, 52% and 9% of subjects randomised to CIB in ADVOCATE had undergone ileostomy, colostomy and urostomy, respectively; corresponding values for subjects randomised to SoC were 36%, 54% and 10%, respectively; p=0.9715. We did not differentiate between type of ostomy as there was no statistically significant difference in the distribution of ostomy type at baseline in the ADVOCATE trial.
The model calculated the expected total 1-year ostomy-related medical costs under two alternative scenarios – one in which all patients were assumed to use barriers other than CIB (the SoC scenario), and one in which a percentage of patients were assumed to use CIB in lieu of SoC (the CIB scenario). We assumed that the SoC scenario represented any number of barriers from multiple manufacturers. Ostomy-related costs include ostomy pouching systems, ostomy accessories and PSC management, such as: specialist and nurse visits; facility fees (for US and Australia); topical steroids and antibiotics; and additional use of barriers, pouches and accessories due to increased frequency of barrier change. Budget impact was estimated by subtracting the total expected ostomy-related costs under the SoC scenario from those under the CIB scenario. The time horizon for the model was 1 year (i.e., 12 30-day months). Model programming was consistent with recommendations on budget impact analyses19. A schematic of the model is presented in Figure 1; key modelling assumptions are presented in Table 1.
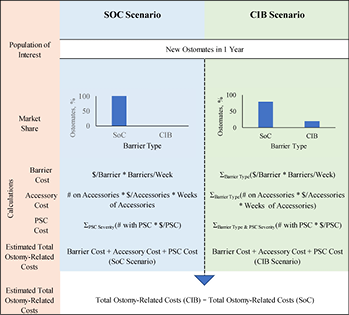
Figure 1. Model schematic
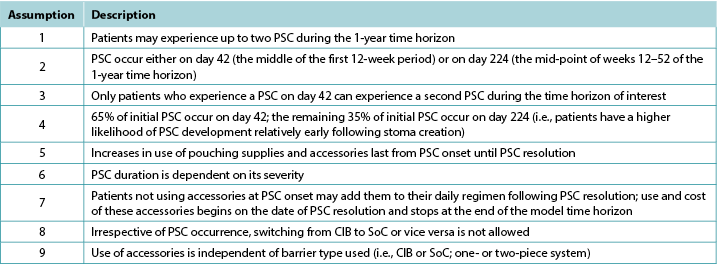
Table 1. Key modelling assumptions
Ostomy pouching systems and accessories
The use of ostomy pouching systems was based on country-specific information, as were the costs of healthcare services, including the 2018 Medicare schedule (US), the 2017–18 National Schedule of Reference Costs, NHS Trust and NHS Foundation Trusts (UK), the 2018 Regionala Priser Och Ersättningar för Södra Sjukvårdsregionen (Sweden), the 2019 (June) Stoma Appliance Scheme Schedule (Australia)20, the Sistema Socio Sanitario – Regione Lombardia (ATS Milano Città Metropolitana) (Italy), and the 2019 (January) Produkt-og Prisliste Refusjonsberettiget etter §5–14 Medisinsk Forbruksmateriell ved Stomi (Norway). Except for the UK, costs of CIB pouching systems were assumed equivalent to those of SoC systems. Values for all relevant parameters are provided in Appendix A.
The use of ostomy accessories (e.g., flat rings, ostomy belts, adhesive remover spray) was based on information from ADVOCATE unless more relevant country-specific data were available (Table 2). Accessory use was captured by means of an ‘average accessory use profile’ based on percentages of patients assumed to use each accessory, and the corresponding number of units and cost. Accessory use was assumed dependent on weekly frequency of change of pouching system.
Table 2. Accessory use, by country
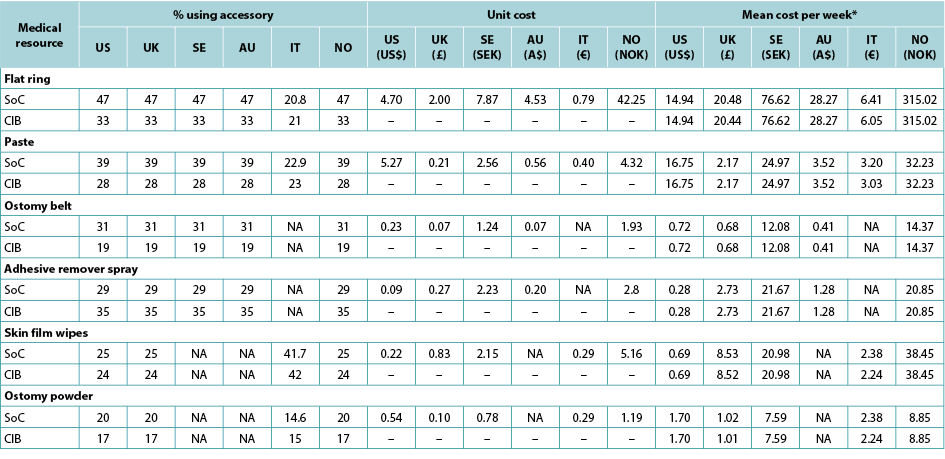
* Calculated using the average of the number of ostomy system changes per week, weighted by the proportions receiving one- and two-piece systems respectively.
PSC incidence
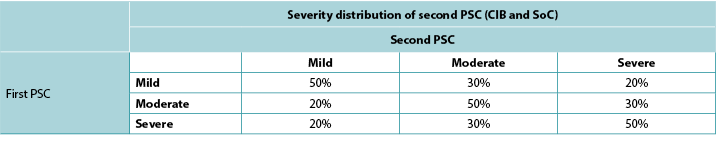
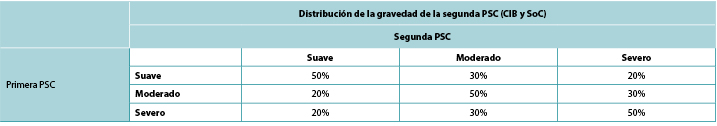
Consistent with ADVOCATE, we assumed that 55% of SoC patients and 41% of CIB patients would experience PSC; PSC severity distributions were taken from ADVOCATE (Figure 2). Given its relatively short follow-up, ADVOCATE was not used to estimate probability of a second PSC. Accordingly, we arbitrarily assumed that 10% of CIB patients would experience a second PSC, that the 5% risk difference observed in ADVOCATE was constant, and therefore that 15% of SoC patients would experience a second PSC. We also assumed that addition of accessories following the initial PSC would reduce the risk of subsequent PSC by 50% (i.e., 7.5% for SoC; 5% for CIB). The severity of the second PSC was dependent on that of the first (Table 3).
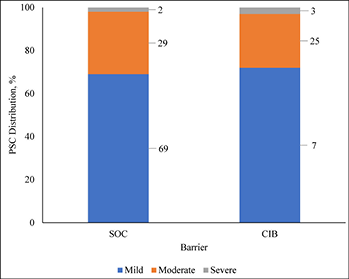
Figure 2. Distribution of PSC severity by barrier received
Table 3. Severity distribution of second PSC based on severity of first PSC
As per ADVOCATE, the time to PSC resolution was assumed to be 18 days for mild cases (defined in ADVOCATE as a Discoloration, Erosion, Tissue overgrowth [DET] score <4), and 33 days for moderate cases (4≤ DET <7) and severe cases (DET ≥7). Time to resolution was assumed invariant to barrier choice. Patterns of use of various healthcare services during PSC were based on information from ADVOCATE; while one-piece pouching systems were not evaluated, we assumed that these barriers would perform similarly to their two-piece counterparts. As per ADVOCATE, we assumed that the use of pouching supplies among CIB patients would increase by 29% for mild PSC, by 83% for moderate PSC, and by 83% for severe PSC; corresponding increases among SoC patients were 64%, 49% and 49%, respectively. We also assumed PSC management was similar in each country (Table 4).
Table 4. Use and cost of healthcare services during PSC, by PSC severity, barrier received, and country
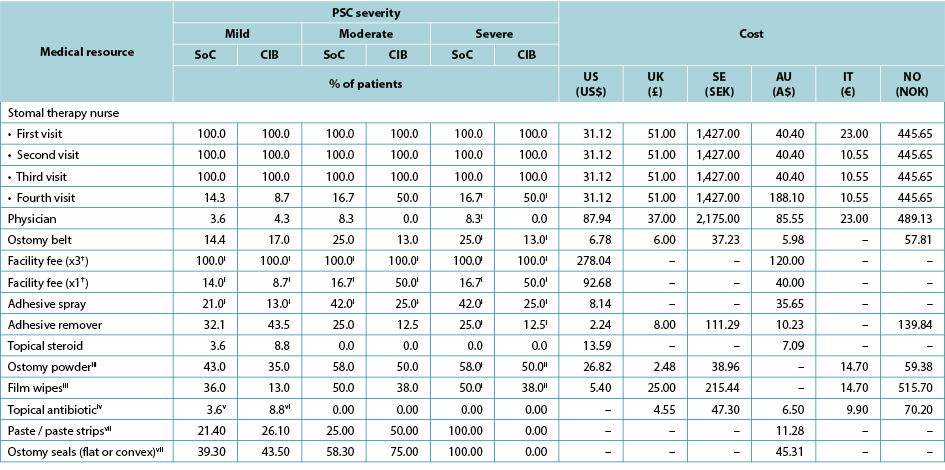
† Facility fee (x3) is the facility fee associated with the first three STN visits. Facility fee (x1) is the facility fee associated with the fourth STN visit.
i 0% for the UK, Sweden, Norway and Italy
ii 100% for the UK, Sweden, Norway and Italy
iii 0% in Australia
iv 0% in the US; values in the table are for the UK, Sweden, Norway and Italy
v 7.1 in Australia
vi 8.7 in Australia
vii Australia only
We assumed that there would be 149,000 ostomates in the US, 29,000 in the UK, 6,900 in Sweden, 9,000 in Australia, 17,000 in Italy and 3,700 in Norway. For the US, ostomates were assumed to be enrolled in a health plan comprised of 58,400,000 members; estimates of plan size were limited to the US as payers in the US tend to view estimates of budget impact in terms of costs per-member per-month (PMPM) which is estimated by dividing the expected cost by the total number of plan members and then dividing the resulting quotient by 12. Country-specific estimates of changes in population size (both plan members and number of ostomates) is presented in Table 5, as is the assumed annual inflation rate for medical costs.
Table 5. Country-specific estimates of changes in population size (both plan members and number of ostomates) and the assumed annual inflation rate for medical costs: assumptions for a 5-year analysis
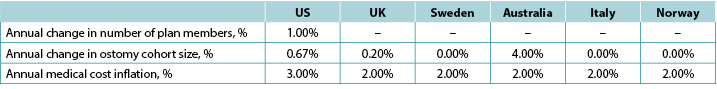
Note: Positive values denote expected increases; negative values expected decreases
Data Analysis
The model generated total expected numbers of expected PSC under both scenarios and corresponding expected ostomy-related costs, i.e., PSC-related care plus ostomy-related care. The 1-year budget impact was estimated by subtracting the total expected costs under the CIB scenario from those of the SoC scenario. We calculated the estimates of the budget impact alternatively, assuming uptake of CIB to be 5%, 10%, 15%, 20% and 25% (all versus 0% for the SoC scenario) (Table 6).
Table 6. 1-year budget impact results under different CIB scenarios
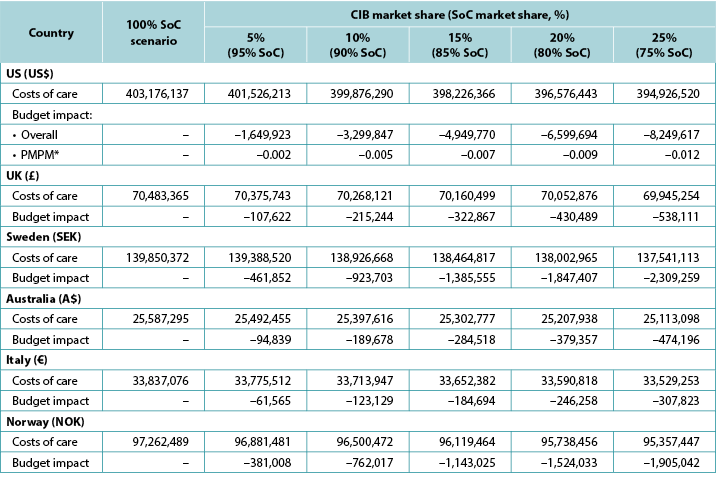
* Based on a plan with 58,400,000 members.
Note: Negative values denote expected savings.
We examined the 5-year expected budget impact of CIB, considering cost inflation and annual changes in ostomy cohort size; in addition, for the US, we estimated annual change in plan enrolment (Table 5). We also varied the uptake of CIB over time, assuming 5% would use these barriers in year 1 of the CIB scenario, 7.5% in year 2, 10.0% in year 3, 10.0% in year 4 and 10.0% in year 5 (all versus 0% for SoC) (Table 7).
Table 7. Expected annual budget impact of CIB over 5 years
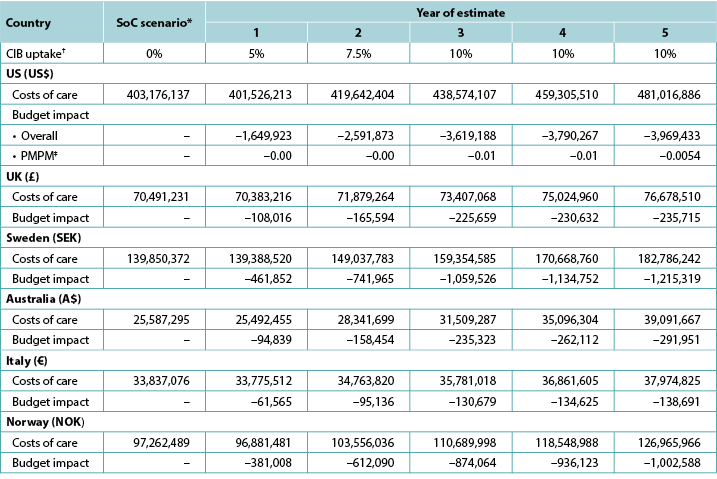
* Costs of care under the SoC scenario increase annually due to inflation and assumptions on cohort size.
† In each year of interest, all patients not assumed to use CIB were assumed to use SoC barriers.
‡ Based on a plan with 58,400,000 members.
Note: Negative values denote expected savings.
We conducted a sensitivity analysis in which the costs of PSC were changed to those reported in a retrospective study of ostomates identified in a US integrated healthcare system by Taneja and colleagues21; findings from their study indicated that patients who experienced PSC averaged US$8,031 more in all-cause medical-care costs over 120 days than those who did not (US$58,329 versus US$50,298; p=0.251)21. For this analysis, we used the model to estimate the incidence of PSC in both the SoC and CIB cohorts, and used these proportions to calculate average costs for a patient assumed to use SoC and CIB, respectively. We then multiplied these costs by the corresponding market shares for SoC and CIB, respectively, to calculate the expected budget impact of CIB. Due to the source of cost and utilisation estimates, this analysis was limited to the US.
We also conducted deterministic sensitivity analyses (DSA) to examine the sensitivity of model output to varying parameter values. In these analyses, each model parameter was varied to its lower and upper 95% confidence interval (CI) value, respectively.
Results
1-year model
Over 1 year, the total expected stoma-related costs for the SoC scenario were US$403.2m in the US, £70.5m in the UK, SEK139.9m in Sweden, A$25.6m in Australia, €33.8m in Italy, and NOK97.3m in Norway; corresponding values for the CIB scenario (20% of patients in each country assumed to use CIB in lieu of SoC; 80% used SoC) were US$396.6m, £70.1m, SEK138.0m, A$25.2m, €33.6m and NOK95.7m respectively. Resulting budget savings associated with CIB were therefore US$6.7m in the US, £0.4m in the UK, SEK1.8m in Sweden, A$0.4m in Australia, €0.2m in Italy, and NOK1.5m in Norway. As the use of CIB was expected to be cost-saving, the corresponding PMPM impact in the US was also expected to be cost-saving, although relatively small due to the large number of assumed plan members (Table 6).
5-year model
Five-year analyses yielded cost savings ranging from US$1.7m in year 1 to US$4.0m in year 5 in the US, from £0.1m in year 1 to £0.2m in year 5 in the UK, from SEK0.5m in year 1 to SEK1.2m in year 5 in Sweden, from A$0.09m in year 1 to A$0.3m in year 5 in Australia, from €0.06m in year 1 to €0.3m in year 5 in Italy, and from NOK0.4m in year 1 to NOK1.0m in year 5 in Norway (Table 7). Over the longer period, the use of CIB in a relatively limited population (i.e., a maximum of 10% of all eligible ostomates in any given year) resulted in expected cost savings of stoma-related care of US$15,620,684 in the US, £965,616 in the UK, SEK4,613,414 in Sweden, A$1,042,678 in Australia, €560,695 in Italy, and NOK3,805,873 in Norway.
Deterministic sensitivity analyses
The 20 variables for which budget impact results are most sensitive are presented for each country in Figures B1–B6 in Appendix B, i.e., one figure per country. Regardless of country, variables with the largest effect on budget impact were the percentage of patients using pouching supplies and accessories with relatively high unit costs, and the annual probability of PSC given the use of SoC barriers. In the US and Australia, CIB remained cost-saving across all DSAs conducted; in the other countries it was expected to be cost-saving in all sensitivity analyses except one ‘extreme’ scenario – the percentage of patients using more costly pouching supplies or accessories was set to the lower-bound 95% CI value of weekly costs for SoC and the higher-bound 95% CI value for CIB. In this extreme scenario, expected budget increases were <1% of annual costs of care expected under the SoC scenario (£207,042 in the UK, SEK116,916 in Sweden, €293,897 in Italy and NOK112,709 in Norway). In all countries evaluated, CIB was expected to be cost-saving when the probability of PSC with SoC was set to its lower-bound 95% CI value and the corresponding estimate for CIB was set to its higher-bound 95% CI value.
Scenario analysis
When we replaced cost inputs derived from ADVOCATE with those estimated using real-world US data over the 120-day period following ostomy surgery, resulting estimates of budget savings associated with an increased use of CIB were greater than those obtained in the base case (Table 8).
Table 8. Expected 1-year budget impact associated with the use of CIB and real-world healthcare costs in US patients
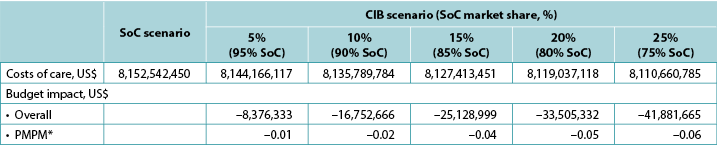
* Based on a plan with 58,400,000 members.
Discussion
Findings from our study suggests that the use of CIB in lieu of other skin barriers is expected to result in savings to payers within 1 year. The magnitude of expected savings is dependent on the percentage of ostomates who would use CIB instead of other skin barriers. Estimates of impact were greatest for the US (from US$1.7m at 5% CIB to US$8.3m at 25% CIB), and lowest for Norway (from NOK381,008 [US$43,321] at 5% CIB to NOK1,905,042 [US$216,603] at 25% CIB)22. Estimates for the US were substantially larger than those expected for other countries of interest, likely due to its relatively high costs of medical care (including accessories) versus the other countries included in this evaluation. CIB was expected to result in lower costs of care (i.e., savings) across all six countries assessed.
Results were fairly robust in sensitivity analyses. 5-year projections of budget impact were most heavily influenced by assumptions of market share of CIB, although additional payer savings were projected simply by increasing the number of ostomates and/or costs of medical care, respectively. Similarly, results of the scenario analysis that used real-world US costs of PSC as opposed to ADVOCATE (i.e., approximately US$8,000 versus US$36.46 over a 12-week period) also projected increased savings in all scenarios (versus SoC) relative to the base case, irrespective of assumed CIB uptake. However, this scenario included all-cause healthcare costs, not only those specific to ostomy care. Unsurprisingly, CIB was found to be cost-saving across nearly all DSA scenarios, with the model being most sensitive to the percentages of patients using relatively expensive pouching supplies and accessories and PSC incidence. In the one ‘extreme’ instance where the use of CIB was expected to increase total costs, the resulting budget impact represented a very modest increase in annual costs of care. Findings were consistent across all countries assessed.
While the economic value of pharmaceutical products (in terms of cost-effectiveness and budgetary impact) have been assessed for decades, comparatively less is typically done for medical devices. This is somewhat counter-intuitive, as the number of devices coming to market vastly exceed that of pharmaceuticals. In 2012, over 10,000 patent applications for medical devices were filed in Europe, which was approximately twice that for pharmaceuticals23. As opposed to cost-effectiveness analyses, which focus on the benefits of the assessed technology at the patient level, budget impact analyses examine affordability to the payer. In our opinion, this question of affordability is of equal importance. In fact, assessments of budget impact are “…an ‘essential’ part of comprehensive economic assessment of medical technology”24.
This issue is perhaps even more important in fields such as ostomy, in which nurse clinicians and other providers are often tasked with a dual, often competing, role to provide quality care while simultaneously containing costs. Accordingly, the use of economic models based on evidence obtained from randomised trials and other well-conducted studies is an important means by which healthcare professionals, payers and other interested parties can estimate the value of a given product based on its efficacy and safety. Results of such models can then be used to help align these parties on cost-effective, high-quality patient care.
We implemented principles of good practice for budget impact analyses, as set forth by the International Society for Pharmacoeconomics and Outcomes Research (ISPOR)19, including our reliance on ADVOCATE, a randomised clinical trial, for most input values used in the model, as well as the inclusion of sensitivity analyses to better understand the degree to which model output relied on inputs and assumptions. Results of our analyses are consistent with those of ADVOCATE15 and the published cost-effectiveness model18, and provide evidence that the value of CIB enjoyed by patients also manifests as cost savings to payers across various countries.
Limitations
Our study has several limitations. First, like all economic models, ours presents a somewhat simplified view of clinical practice, such as limiting to a maximum of two the incidence of PSC during 1 year, including a maximum of one PSC during an ‘early’ (i.e., 12-week) period and a maximum of one PSC during a ‘late’ (i.e., 40-week) period. The degree to which these assumptions adequately capture actual patient experience is not known. On a related matter, in the absence of data, we arbitrarily – and somewhat conservatively – set risk of a second PSC. The model also does not differ between ostomy types (e.g., ileostomy, colostomy) in terms of PSC risk, use of skin barriers, and/or use of accessories.
The economic and clinical impacts of CIB are based on findings from ADVOCATE, including but not limited to the incidence of PSCs (55% of SoC patients vs. 41% of CIB patients), and the distribution of patients by ostomy type (about one-third had an ileostomy; about one-half had a colostomy; and all other patients had a urostomy). Further study is needed to better understand the impact of CIB in different populations, both in terms of distribution by ostomy type as well as with different demographic and/or comorbidity profiles than subjects enrolled in ADVOCATE.
We also assumed that publicly available country-specific unit costs for various items used in stoma-related care were adequate representations of what is spent on care of ostomy patients by payers in each country. However, the degree to which this assumption is true for the US – which has many different types of payers (e.g., private commercial insurance, Medicare) and, within some payer types, equal if not more heterogeneity across insurers in terms of reimbursement policies – and other countries of interest in unknown.
Furthermore, while ADVOCATE was limited to the use of two-piece systems, we assumed the use of both one- and two-piece systems, and that benefits of CIB would be consistent across both types of systems. We also assumed that PSC were of fixed duration. However, other studies have reported resolution times varying between 7 weeks to over 3 months4,5,25; consequently, our analyses may have underestimated the economic consequence of PSC. We note, however, that to the degree this occurred, estimated budget impact associated with the use of CIB in lieu of other skin barriers is likely conservative, i.e., the ‘true’ magnitude of savings resulting from the use of CIB may be greater than what is estimated herein.
Conclusions
The use of CIB results in expected cost reductions to payers in the US, UK, Sweden, Australia, Italy and Norway, with the magnitude of expected reductions directly related to percentages of patients assumed to use CIB in lieu of SoC. While our findings are consistent with those of ADVOCATE and previous cost-effectiveness modelling, further research is needed to better understand the economic consequences of the use of CIB (versus other skin barriers) in clinical practice.
Conflict of Interest
Gary W Inglese and George Skountrianos are employees of Hollister Incorporated. Ariel Berger and Mustafa Oguz are employees of Evidera Inc. which provides consulting and other research services to pharmaceutical, device, government and non-government organisations. Evidera Inc. received funding from Hollister Incorporated in connection with conducting this study and with developing this manuscript. Davide Croce is an employee of the Università Carlo Cattaneo and did not receive any funding for the conduct of this study or for the development of this manuscript.
Funding
Funding for this research was provided by Hollister Incorporated.
Impacto presupuestario de las barreras cutáneas con infusión de ceramida frente a las barreras cutáneas de cuidados estándar para nuevos ostomizados: un análisis de seis países
Ariel Berger, Gary Inglese, George Skountrianos, Davide Croce and Mustafa Oguz
DOI: https://doi.org/10.33235/wcet.41.2.22-31
Resumen
Introducción En un estudio controlado aleatorio, el uso de barreras cutáneas con infusión de ceramida (CIB) dio lugar a menores costes de atención durante 12 semanas frente al uso de una barrera cutánea de cuidado estándar (SoC). Sin embargo, no se ha examinado el grado en que esta información puede influir en los patrones de prescripción de productos de ostomía, ni su correspondiente impacto en los presupuestos de los pagadores.
Objetivo Examinar el impacto presupuestario previsto de CIB entre los ostomizados recientes en los Estados Unidos (EE.UU) , el Reino Unido (RU), Suecia, Australia, Italia y Noruega.
Diseñar un modelo de impacto presupuestario para la toma de decisiones.
Métodos Se predijeron los costes totales relacionados con la ostomía (es decir, barreras cutáneas, accesorios de ostomía, cuidado de las complicaciones cutáneas periestómicas [PSC]) durante 1 año para cohortes hipotéticas de ostomizados recientes en cada país de interés. Los costes se evaluaron en dos escenarios alternativos: uno en el que se suponía que todos los pacientes utilizaban barreras distintas de CIB (el escenario SoC), y otro en el que se suponía que el 20% de los pacientes utilizaban CIB en lugar de SoC (el escenario CIB). El impacto presupuestario se supuso igual a la diferencia de estos dos escenarios.
Conclusiones El uso de CIB se tradujo en un ahorro anual de 6,6 millones de dólares en Estados Unidos, 0,4 millones de libras en el Reino Unido, 1,8 millones de coronas suecas, 0,4 millones de dólares australianos, 0,2 millones de euros en Italia y 1,5 millones de coronas noruegas. Los resultados fueron consistentes en los análisis de sensibilidad.
Conclusiones El uso de CIB frente a otras barreras da lugar a unos costes previsiblemente menores para los pagadores en cada país evaluado. Es necesario seguir investigando para comprender mejor los beneficios clínicos y económicos completos asociados al uso de CIB.
Introduccionn
La cirugía de ostomía fecal se realiza para tratar afecciones agudas (por ejemplo, traumatismos) y crónicas (por ejemplo, cáncer colorrectal, enfermedad de Crohn, colitis ulcerosa). Aunque es eficaz para el problema o los problemas subyacentes, una ostomía también tiene su propio riesgo de complicaciones, incluidas las complicaciones cutáneas periestómicas (PSC) como: mecánicas, por ejemplo, desgarro o abrasión de la piel; dermatitis irritante, típicamente causada por fugas que exponen la piel a la salida de la ileostomía; y dermatitis infecciosa. Las PSC se encuentran entre las complicaciones más frecuentes entre los ostomizados, y pueden ocurrir en cualquier momento tras la creación del estoma1-3. Entre el 33,5% y el 78,7% de los ostomizados declaran padecer PSC4-11; un estudio estimó que el 40% de las consultas a las clínicas de ostomía eran por PSC12,. En 2011, se estimó que los costes medios de atención a la PSC oscilaban por ostomía entre 32,45 euros para los casos leves y 147,17 euros para los casos graves, y la media de los costes totales de atención (incluidos los sistemas de bolsa de ostomía, los accesorios, las visitas a los proveedores de atención sanitaria, la hospitalización y los medicamentos) a lo largo de 7 semanas resultó ser aproximadamente un 22% mayor entre los pacientes que experimentaron PSC frente a los que no lo hicieron5. Las PSC también se asocian a impactos nocivos en la calidad de vida, con una "pérdida" de aproximadamente 11 días de vida ajustados por calidad (DVA) / mes para los pacientes con PSC grave (frente a los que no tienen PSC)13.
CeraPlus™ es una nueva barrera cutánea con tecnología Remois (Alcare Co Ltd, Sumida-ku, Tokio, Japón) comercializada actualmente por Hollister Inc. (Libertyville, Illinois, Estados Unidos). Se trata de una barrera con infusión de ceramida (CIB) diseñada para favorecer la salud de la piel periestomal. Las ceramidas son lípidos naturales que son esenciales para la función de barrera de la piel y la bicapa lipídica del estrato córneo14,15, y desempeñan un papel importante en la prevención de la pérdida de agua transepidérmica (TEWL) al fusionarse con los corneocitos del estrato córneo para ayudar a formar una capa protectora16,17.
En el ensayo ADVOCATE15 (un estudio que determina las variaciones en las afecciones cutáneas de los ostomizados y el impacto económico: NCT02401412), 153 adultos con piel periestomal sana que habían sido sometidos recientemente a una cirugía de ostomía fueron asignados aleatoriamente a utilizar CIB (n=79) o una barrera alternativa (New Image FlexWear o New Image Flextend [Hollister Inc.]) (n=74). A lo largo de un seguimiento máximo de 12 semanas (los pacientes fueron evaluados durante 8 semanas, y los que experimentaron PSC fueron observados durante un "período de resolución" adicional de 4 semanas), los costes medios de la atención entre los pacientes asignados al azar a CIB fueron 36,36 dólares menos que los asignados al azar a la barrera de control (223,73 dólares frente a 260,19 dólares; p=0,017); también fueron nominalmente menos propensos a experimentar PSC durante el seguimiento15. Un posterior análisis de coste-eficacia indicó que se esperaba que el uso de CIB entre una cohorte hipotética de 100 pacientes australianos, a lo largo de 1 año, diera lugar a 16 PSC menos, a 35 QALD adicionales y a una reducción de los costes sanitarios de 13.700 dólares australianos (todo ello frente al cuidado estándar [SoC]); el beneficio monetario neto resultante fue de 17.400 dólares australianos, lo que indica que CIB era una alternativa rentable a SoC18.
Objetivo del estudio/publicación
Aunque tanto en ADVOCATE como en los modelos económicos posteriores se ha comprobado que CIB es rentable frente a otras barreras, los pagadores de la sanidad también deben tener en cuenta el impacto general previsto en los presupuestos (es decir, la asequibilidad) asociado a la adopción de nuevas tecnologías. Los profesionales desempeñan un papel importante en el cuidado de los nuevos ostomizados, y a menudo se les pide que equilibren las necesidades de los pacientes con las presiones de contención de costes que les imponen los pagadores. En consecuencia, los resultados que aquí se presentan son probablemente de gran interés para los enfermeros clínicos y otros proveedores de cuidados para esta población vulnerable, ya que utiliza información publicada sobre la eficacia a nivel de paciente y sobre la seguridad de CIB para estimar su valor esperado para los pagadores.
Para examinar ésta y otras cuestiones relacionadas, desarrollamos un modelo de análisis de decisiones que pudiera estimar el impacto presupuestario asociado al uso de CIB en lugar de otras barreras cutáneas. Este modelo se ha calculado para los Estados Unidos , el Reino Unido , Suecia, Australia, Italia y Noruega, basándose en la información de ADVOCATE y completándose con otras fuentes cuando se consideró oportuno.
Métodos y Procedimientos
Resumen del modelo
Se asumió que todos los pacientes comenzaban el modelo dentro de las 12 semanas siguientes a la cirugía de estoma fecal fuera del entorno hospitalario utilizando un sistema de bolsa CIB o un sistema SoC. Se asumió que la distribución de los pacientes por tipo de ostomía era consistente con la reportada por ADVOCATE y que era similar entre los pacientes que usarían CIB frente a SoC- 39%, 52% y 9% de los sujetos aleatorizados a CIB en ADVOCATE habían sido sometidos a ileostomía, colostomía y urostomía, respectivamente; los valores correspondientes para los sujetos aleatorizados a SoC fueron 36%, 54% y 10%, respectivamente; p=0,9715. No se diferenció el tipo de ostomía ya que no hubo diferencias estadísticamente significativas en la distribución del tipo de ostomía al inicio del ensayo ADVOCATE.
El modelo calculó los costes médicos totales esperados durante un año relacionados con la ostomía en dos escenarios alternativos: uno en el que se suponía que todos los pacientes utilizaban barreras distintas de CIB (el escenario SoC), y otro en el que se suponía que un porcentaje de pacientes utilizaba CIB en lugar SoC (el escenario CIB). Asumimos que el escenario SoC representaba cualquier número de barreras de múltiples fabricantes. Los costes relacionados con la ostomía incluyen los sistemas de bolsa de ostomía, los accesorios de ostomía y la gestión de la PSC, como: las visitas de especialistas y enfermeros; los honorarios de las instalaciones (para Estados Unidos y Australia); los esteroides tópicos y los antibióticos; y el uso adicional de barreras, bolsas y accesorios debido a la mayor frecuencia de cambio de barreras. El impacto presupuestario se estimó restando el total de los costes relacionados con la ostomía previstos en el escenario SoC de los del escenario CIB. El horizonte temporal del modelo fue de 1 año (es decir, 12 meses de 30 días). La programación del modelo fue coherente con las recomendaciones sobre los análisis de impacto presupuestario19. En la figura 1 se presenta un esquema del modelo; las principales hipótesis de modelización se presentan en el Tabla 1.

Figura 1. Esquema del modelo
Tabla 1. Supuestos clave de la modelización

Sistemas de bolsas de ostomía y accesorios
El uso de sistemas de bolsas de ostomía se basó en información específica de cada país, al igual que los costes de los servicios sanitarios, incluyendo el baremo de Medicare de 2018 (EE.UU.), el Baremo Nacional de Costes de Referencia 2017-18, NHS Trust y NHS Foundation Trusts (Reino Unido), el Regionala Priser Och Ersattningar for Sodra Sjukvardsregionen de 2018 (Suecia), el 2019 (junio) Stoma Appliance Scheme Schedule (Australia)20, el Sistema Socio Sanitario - Regione Lombardia (ATS Milano Città Metropolitana) (Italia), y el 2019 (enero) Produkt- og Prisliste Refusjonsberettiget etter §5-14 Medisinsk Forbruksmateriell ved Stomi (Noruega). Excepto en el Reino Unido, los costes de los sistemas de bolsa CIB se consideraron equivalentes a los de los sistemas SoC. Los valores de todos los parámetros pertinentes figuran en el Apéndice A.
El uso de accesorios de ostomía (por ejemplo, anillos planos, cinturones de ostomía, spray quita adhesivos) se basó en la información de ADVOCATE, a menos que se dispusiera de datos más relevantes específicos de cada país (Tabla 2). El uso de accesorios se calculó mediante un "perfil de uso medio de accesorios" basado en los porcentajes de pacientes que se supone que utilizan cada accesorio, y el correspondiente número de unidades y coste. Se supuso que el uso de accesorios dependía de la frecuencia semanal de cambio del sistema de bolsas.
Tabla 2. Uso accesorio, por país
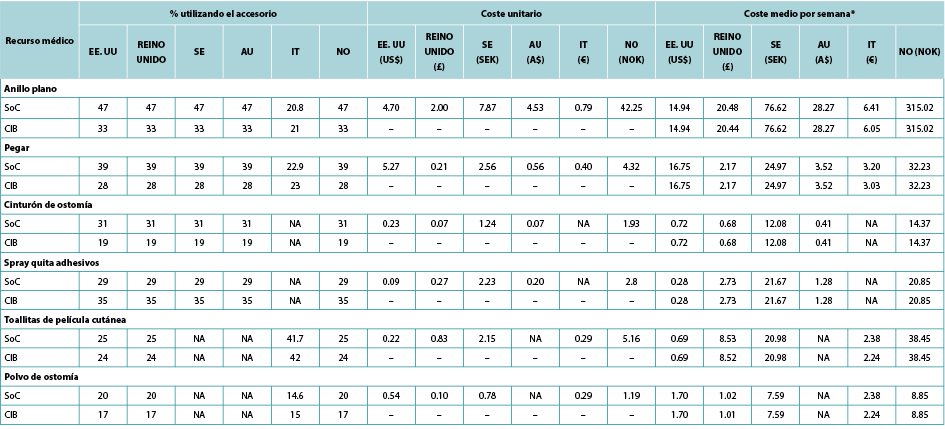
* Calculado utilizando la media del número de cambios de sistemas de ostomía por semana, ponderado por las proporciones que reciben sistemas de una y dos piezas respectivamente.
Incidencia de la PSC
En consonancia con ADVOCATE, asumimos que el 55% de los pacientes con SoC y el 41% de los pacientes con CIB experimentarían PSC; las distribuciones de gravedad de PSC se tomaron de ADVOCATE (Figura 2). Dado su seguimiento relativamente corto, ADVOCATE no se utilizó para estimar la probabilidad de una segunda PSC. En consecuencia, asumimos arbitrariamente que el 10% de los pacientes con CIB experimentarían una segunda PSC, que la diferencia de riesgo del 5% observada en ADVOCATE era constante, y por lo tanto que el 15% de los pacientes con SoC experimentarían una segunda PSC. También asumimos que la adición de accesorios tras la PSC inicial reduciría el riesgo de PSC posterior en un 50% (es decir, 7,5% para SoC; 5% para CIB). La gravedad de la segunda PSC dependía de la de la primera (Tabla 3).

Figura 2. Distribución de la gravedad de la PSC según la barrera recibida
Tabla 3. Distribución de la gravedad de la segunda PSC en función de la gravedad de la primera PSC
Según ADVOCATE, se asumió que el tiempo hasta la resolución del PSC era de 18 días para los casos leves (definidos en ADVOCATE como una puntuación de Decoloración, Erosión, Sobrecrecimiento de Tejido [DET] <4), y de 33 días para los casos moderados (4≤ DET <7) y los casos graves (DET≥7). El tiempo de resolución se supuso invariable a la elección de la barrera. Los patrones de uso de varios servicios sanitarios durante la PSC se basaron en la información de ADVOCATE; aunque no se evaluaron los sistemas de bolsa de una pieza, asumimos que estas barreras tendrían un comportamiento similar a sus homólogas de dos piezas. Según ADVOCATE, asumimos que el uso de suministros de bolsa entre los pacientes con CIB aumentaría en un 29% en el caso de la PSC leve, en un 83% en el caso de la PSC moderada y en un 83% en el caso de la PSC grave; los aumentos correspondientes entre los pacientes con SoC fueron del 64%, el 49% y el 49%, respectivamente. También asumimos que la gestión de la PSC era similar en cada país (Tabla 4).
Tabla 4. Uso y coste de los servicios sanitarios durante la PSC, por gravedad de la PSC, barrera recibida y país
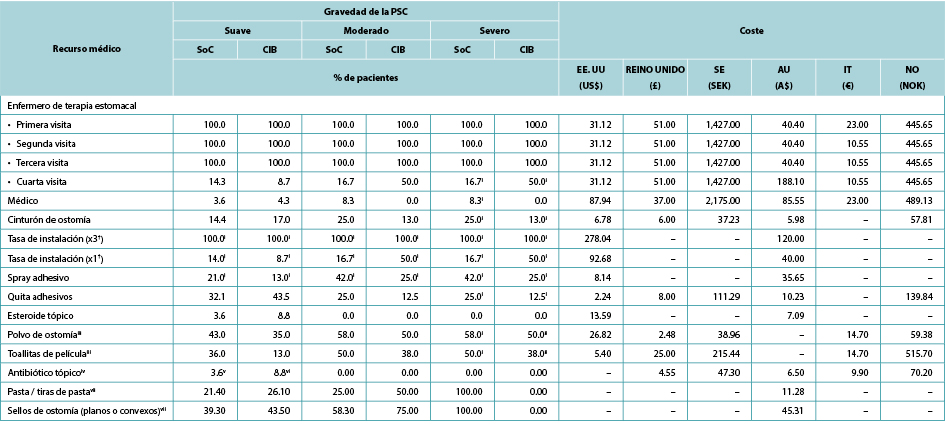
† Tasa de instalación (×3) es la tasa de instalación asociada a las tres primeras visitas de STN. La tasa del centro (×1) es la tasa del centro asociada a la cuarta visita STN.
i 0% para el Reino Unido, Suecia, Noruega e Italia
ii 100% para el Reino Unido, Suecia, Noruega e Italia
iii 0% en Australia
iv 0% en EE. UU.; los valores de la tabla corresponden al Reino Unido, Suecia, Noruega e Italia
v 7.1 en Australia
vi 8.7 en Australia
vii Sólo Australia
Suponemos que habrá 149.000 ostomizados en Estados Unidos, 29.000 en el Reino Unido, 6.900 en Suecia, 9.000 en Australia, 17.000 en Italia y 3.700 en Noruega. En el caso de EE. UU., se asumió que las personas ostomizadas estaban inscritas en un plan de salud compuesto por 58.400.000 miembros; las estimaciones del tamaño del plan se limitaron a EE. UU. ya que los pagadores en EE. UU. tienden a ver las estimaciones del impacto presupuestario en términos de costes por miembro y por mes (PMPM), que se estima dividiendo el coste esperado por el número total de miembros del plan y luego dividiendo el cociente resultante por 12. En el cuadro 5 se presentan las estimaciones específicas de cada país de los cambios en el tamaño de la población (tanto de los miembros del plan como del número de ostomizados), así como la tasa de inflación anual supuesta para los costes médicos.
Análisis de Datos
El modelo generó las cifras totales esperadas de PSC en ambos escenarios y los correspondientes costes esperados relacionados con la ostomía, es decir, la atención relacionada con la PSC más la atención relacionada con la ostomía. El impacto presupuestario de un año se estimó restando los costes totales previstos en el escenario CIB de los del escenario SoC. Hemos calculado las estimaciones del impacto presupuestario de forma alternativa, suponiendo que la adopción de CIB sea del 5%, 10%, 15%, 20% y 25% (todo ello frente al 0% del escenario SoC) (Tabla 6).
Examinamos el impacto presupuestario previsto a 5 años de la CIB, teniendo en cuenta la inflación de los costes y los cambios anuales en el tamaño de la cohorte de ostomía; además, para los EE. UU., estimamos el cambio anual en la inscripción en el plan (Tabla 5). También variamos la adopción de la CIB a lo largo del tiempo, suponiendo que el 5% utilizaría estas barreras en el año 1 del escenario CIB, el 7,5% en el año 2, el 10,0% en el año 3, el 10,0% en el año 4 y el 10,0% en el año 5 (todo ello frente al 0% de SoC) (Tabla 7).
Tabla 5. Estimaciones específicas para cada país de los cambios en el tamaño de la población (tanto los miembros del plan como el número de ostomizados) y la tasa de inflación anual supuesta para los costes médicos: hipótesis para un análisis de 5 años
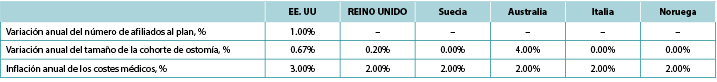
Tabla 6. Resultados del impacto presupuestario a un año bajo diferentes escenarios de CIB
* Basado en un plan con 58.400.000 afiliados.
Nota: Los valores negativos denotan el ahorro previsto.
Realizamos un análisis de sensibilidad en el que los costes de la PSC se modificaron con respecto a los comunicados en un estudio retrospectivo de ostomizados identificados en un sistema sanitario integrado de EE.UU. por Taneja y sus colegas21; los resultados de su estudio indicaron que los pacientes que experimentaron PSC tuvieron una media de 8.031 dólares más en costes de atención médica por todas las causas durante 120 días que los que no lo hicieron (58.329 dólares frente a 50.298 dólares; p=0,251)21. Para este análisis, utilizamos el modelo para estimar la incidencia de PSC en las cohortes de SoC y CIB, y utilizamos estas proporciones para calcular los costes medios de un paciente que se supone que utiliza SoC y CIB, respectivamente. A continuación, multiplicamos estos costes por las correspondientes cuotas de mercado de SoC y CIB, respectivamente, para calcular el impacto presupuestario previsto de CIB. Debido a la fuente de las estimaciones de costes y utilización, este análisis se limitó a los Estados Unidos.
También realizamos análisis de sensibilidad determinista (DSA) para examinar la sensibilidad de los resultados del modelo a la variación de los valores de los parámetros. En estos análisis, cada parámetro del modelo se varió hasta su valor inferior y superior del intervalo de confianza (IC) del 95%, respectivamente.
Resultados
Modelo de 1 año
A lo largo de un año, los costes totales previstos relacionados con el estoma para el escenario SoC fueron de 403,2 millones de dólares estadounidenses, 70,5 millones de libras esterlinas en el Reino Unido, 139,9 millones de coronas suecas, 25,6 millones de dólares australianos, 33,8 millones de euros en Italia y 97,3 millones de coronas noruegas en Noruega; los valores correspondientes al escenario CIB (se supone que el 20% de los pacientes de cada país utiliza CIB en lugar de SoC; el 80% utiliza SoC) fueron de 396,6 millones de dólares, 70,1 millones de libras, 138,0 millones de coronas suecas, 25,2 millones de dólares australianos, 33,6 millones de euros y 95,7 millones de coronas noruegas, respectivamente. El ahorro presupuestario resultante asociado a CIB fue de 6,7 millones de dólares en Estados Unidos, 0,4 millones de libras en el Reino Unido, 1,8 millones de coronas suecas, 0,4 millones de dólares australianos, 0,2 millones de euros en Italia y 1,5 millones de coronas noruegas. Dado que se esperaba que el uso de CIB supusiera un ahorro de costes, también se esperaba que el impacto correspondiente en PMPM en EE. UU. fuera un ahorro de costes, aunque relativamente pequeño debido al gran número de miembros del plan asumido (Tabla 6).
Modelo de 5 año
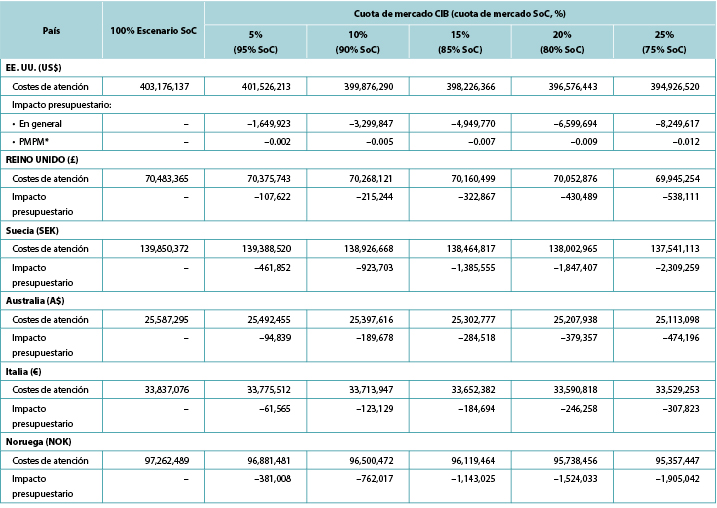
Los análisis quinquenales arrojaron un ahorro de costes que va de 1,7 millones de dólares en el año 1 a 4,0 millones de dólares en el año 5 en EE.UU., de 0,1 millones de libras en el año 1 a 0,2 millones de libras en el año 5 en el Reino Unido, de 0,5 millones de coronas suecas en el año 1 a 1,2 millones en el año 5 en Suecia, de 0,09 millones de dólares australianos en el año 1 a 0,3 millones en el año 5 en Australia, de 0,06 millones de euros en el año 1 a 0,3 millones en el año 5 en Italia, y de 0,4 millones de coronas noruegas en el año 1 a 1,0 millones en el año 5 en Noruega (Tabla 7). Durante el período más largo, el uso de CIB en una población relativamente limitada (es decir, un máximo del 10% de todos los ostomizados elegibles en un año determinado) dio lugar a un ahorro de costes previsto en los cuidados relacionados con el estoma de 15.620.684 dólares estadounidenses, 965.616 libras esterlinas en el Reino Unido, 4.613.414 coronas suecas, 1.042.678 dólares australianos, 560.695 euros en Italia y 3.805.873 coronas noruegas.
Tabla 7. Impacto presupuestario anual previsto de CIB en 5 años
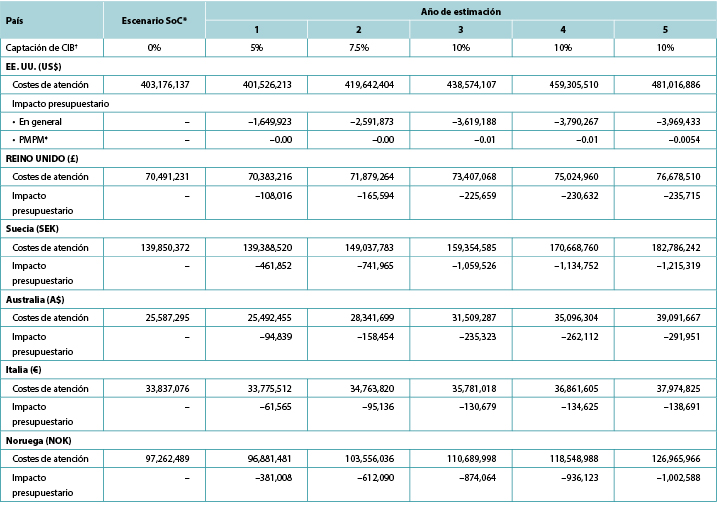
* Los costes de atención en el escenario SoC aumentan anualmente debido a la inflación y a las hipótesis sobre el tamaño de la cohorte.
† En cada año de interés, se supuso que todos los pacientes que no usaban CIB utilizaban barreras SoC.
‡ Basado en un plan con 58.400.000 afiliados.
Nota: Los valores negativos denotan el ahorro previsto.
Análisis de sensibilidad determinista
Las 20 variables para las que los resultados del impacto presupuestario son más sensibles se presentan para cada país en las figuras B1-B6 del Apéndice B, es decir, una figura por país. Independientemente del país, las variables con mayor efecto sobre el impacto presupuestario fueron el porcentaje de pacientes que utilizaban suministros y accesorios de bolsa con costes unitarios relativamente altos, y la probabilidad anual de PSC dado el uso de barreras SoC. En los EE. UU. y Australia, la CIB siguió ahorrando costes en todos los análisis de sensibilidad realizados; en los demás países se esperaba que ahorrara costes en todos los análisis de sensibilidad, excepto en un escenario "extremo": el porcentaje de pacientes que utilizaban suministros o accesorios de bolsa más costosos se fijó en el valor del límite inferior del CI del 95% de los costes semanales para SoC y en el valor del límite superior del CI del 95% para CIB. En este escenario extremo, los incrementos presupuestarios esperados fueron <1% de los costes anuales de atención esperados en el escenario SoC (207.042 libras en el Reino Unido, 116.916 coronas suecas, 293.897 euros en Italia y 112.709 coronas noruegas). En todos los países evaluados, se esperaba que la CIB ahorrara costes cuando la probabilidad de PSC con SoC se fijaba en su valor de CI del 95% de límite inferior y la estimación correspondiente para la CIB se fijaba en su valor de CI del 95% de límite superior.
Análisis de escenarios
Cuando sustituimos los costes derivados de ADVOCATE por los estimados a partir de datos reales de EE. UU. durante el periodo de 120 días posterior a la cirugía de ostomía, las estimaciones resultantes de ahorro presupuestario asociadas a un mayor uso de CIB fueron mayores que las obtenidas en el caso base (Tabla 8).
Tabla 8. Impacto presupuestario esperado en un año asociado al uso de CIB y a los costes sanitarios en el mundo real en pacientes estadounidenses
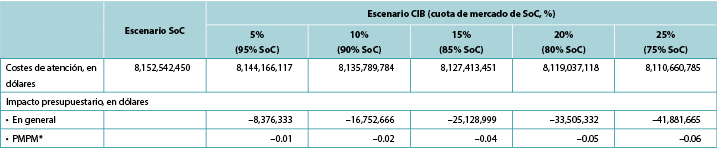
* Basado en un plan con 58.400.000 afiliados.
Discusion
Los resultados de nuestro estudio sugieren que se espera que el uso de CIB en lugar de otras barreras cutáneas suponga un ahorro para los pagadores en el plazo de un año. La magnitud del ahorro previsto depende del porcentaje de ostomizados que utilizarían CIB en lugar de otras barreras cutáneas. Las estimaciones de impacto fueron mayores para Estados Unidos (de 1,7 millones de dólares al 5% de CIB a 8,3 millones de dólares al 25% de CIB), y menores para Noruega (de 381.008 coronas noruegas [43.321 dólares] al 5% de CIB a 1.905.042 coronas noruegas [216.603 dólares] al 25% de CIB)22. Las estimaciones para EE. UU. fueron sustancialmente mayores que las esperadas para otros países de interés, probablemente debido a sus costes relativamente altos de atención médica (incluidos los accesorios) en comparación con los otros países incluidos en esta evaluación. Se esperaba que CIB diera lugar a una reducción de los costes de la atención (es decir, a un ahorro) en los seis países evaluados.
Los resultados fueron bastante sólidos en los análisis de sensibilidad. Las proyecciones de impacto presupuestario a 5 años estaban más influenciadas por los supuestos de la cuota de mercado de la CIB, aunque se proyectaron ahorros adicionales para los pagadores simplemente aumentando el número de ostomizados y/o los costes de la atención médica, respectivamente. Del mismo modo, los resultados del análisis de escenarios que utilizaron los costes reales en EE. UU. del PSC frente a los de ADVOCATE (es decir, aproximadamente 8.000 dólares frente a 36,46 dólares durante un periodo de 12 semanas) también proyectaron un mayor ahorro en todos los escenarios (frente a SoC) en relación con el caso base, independientemente de la adopción supuesta de CIB. Sin embargo, este escenario incluía todos los costes sanitarios, no sólo los específicos del cuidado de la ostomía. Como era de esperar, CIB resultó ser un ahorro de costes en casi todos los escenarios de la DSA, siendo el modelo más sensible a los porcentajes de pacientes que utilizan suministros y accesorios de bolsa relativamente caros y a la incidencia de la PSC. En el único caso "extremo" en el que se esperaba que el uso de CIB aumentara los costes totales, el impacto presupuestario resultante representó un aumento muy modesto de los costes anuales de atención. Los resultados fueron coherentes en todos los países evaluados.
Mientras que el valor económico de los productos farmacéuticos (en términos de coste-eficacia e impacto presupuestario) se ha evaluado durante décadas, comparativamente se hace menos en el caso de los productos sanitarios. Esto es algo contraintuitivo, ya que el número de dispositivos que salen al mercado supera ampliamente al de los productos farmacéuticos. En 2012, se presentaron en Europa más de 10.000 solicitudes de patentes de productos sanitarios, lo que supuso aproximadamente el doble que en el caso de los productos farmacéuticos23. A diferencia de los análisis de rentabilidad, que se centran en los beneficios de la tecnología evaluada a nivel del paciente, los análisis de impacto presupuestario examinan la asequibilidad para el pagador. En nuestra opinión, esta cuestión de la asequibilidad tiene la misma importancia. De hecho, las evaluaciones del impacto presupuestario son una parte "esencial" de la evaluación económica global de la tecnología médica24.
Esta cuestión es quizás aún más importante en campos como el de la ostomía, en el que los enfermeros clínicos y otros proveedores tienen a menudo la doble tarea, a menudo competitiva, de proporcionar una atención de calidad y, al mismo tiempo, contener los costes. En consecuencia, el uso de modelos económicos basados en pruebas obtenidas de ensayos aleatorios y otros estudios bien realizados es un medio importante para que los profesionales sanitarios, los pagadores y otras partes interesadas puedan estimar el valor de un determinado producto en función de su eficacia y seguridad. Los resultados de estos modelos pueden utilizarse para ayudar a alinear a estas partes en una atención al paciente rentable y de alta calidad.
Aplicamos los principios de buenas prácticas para los análisis de impacto presupuestario, según lo establecido por la Sociedad Internacional de Farmacoeconomía e Investigación de Resultados (ISPOR)19, incluyendo nuestra dependencia de ADVOCATE, un ensayo clínico aleatorio, para la mayoría de los valores de entrada utilizados en el modelo, así como la inclusión de análisis de sensibilidad para comprender mejor el grado en que los resultados del modelo dependían de las entradas y los supuestos. Los resultados de nuestros análisis son coherentes con los de ADVOCATE15 y el modelo de coste-eficacia publicado18, y proporcionan pruebas de que el valor de CIB del que disfrutan los pacientes también se manifiesta como un ahorro de costes para los pagadores en varios países.
Limitaciones
Nuestro estudio tiene varias limitaciones. En primer lugar, como todos los modelos económicos, el nuestro presenta una visión algo simplificada de la práctica clínica, como la de limitar a un máximo de dos la incidencia de la PSC durante 1 año, incluyendo un máximo de una PSC durante un periodo "temprano" (es decir, de 12 semanas) y un máximo de una PSC durante un periodo "tardío" (es decir, de 40 semanas). No se sabe hasta qué punto estos supuestos reflejan adecuadamente la experiencia real de los pacientes. En una cuestión relacionada, a falta de datos, fijamos arbitrariamente -y de forma algo conservadora- el riesgo de una segunda PSC. El modelo tampoco difiere entre los tipos de ostomía (por ejemplo, ileostomía, colostomía) en términos de riesgo de PSC, uso de barreras cutáneas y/o uso de accesorios.
Las repercusiones económicas y clínicas de CIB se basan en los hallazgos de ADVOCATE, que incluyen, entre otras cosas, la incidencia de las PSC (55% de los pacientes con SoC frente al 41% de los pacientes con CIB), y la distribución de los pacientes por tipo de ostomía (aproximadamente un tercio tenía una ileostomía; aproximadamente la mitad tenía una colostomía; y todos los demás pacientes tenían una urostomía). Se necesitan más estudios para comprender mejor el impacto de CIB en diferentes poblaciones, tanto en términos de distribución por tipo de ostomía como con diferentes perfiles demográficos y/o de comorbilidad que los sujetos inscritos en ADVOCATE.
También se asumió que los costes unitarios específicos de cada país, disponibles públicamente, para varios artículos utilizados en la atención relacionada con el estoma, eran representaciones adecuadas de lo que se gasta en la atención de los pacientes con ostomía por parte de los pagadores en cada país. Sin embargo, se desconoce hasta qué punto esta suposición es cierta para los EE. UU. -que tiene muchos tipos diferentes de pagadores (por ejemplo, seguros comerciales privados, Medicare) y, dentro de algunos tipos de pagadores, una heterogeneidad igual o mayor entre las aseguradoras en términos de políticas de reembolso- y otros países de interés.
Además, mientras que ADVOCATE se limitaba al uso de sistemas de dos piezas, nosotros asumimos el uso de sistemas de una y dos piezas, y que los beneficios de CIB serían consistentes en ambos tipos de sistemas. También asumimos que las PSC eran de duración fija. Sin embargo, otros estudios han informado de tiempos de resolución que varían entre 7 semanas y más de 3 meses4,5,25; en consecuencia, nuestros análisis pueden haber subestimado la consecuencia económica de la PSC. No obstante, observamos que, en la medida en que esto ha ocurrido, el impacto presupuestario estimado asociado al uso de CIB en lugar de otras barreras cutáneas es probablemente conservador, es decir, la "verdadera" magnitud del ahorro resultante del uso de CIB puede ser mayor que la estimada aquí.
Conclusiones
El uso de CIB da lugar a reducciones de costes previstas para los pagadores en los Estados Unidos, el Reino Unido, Suecia, Australia, Italia y Noruega, y la magnitud de las reducciones previstas está directamente relacionada con los porcentajes de pacientes que se supone que utilizan CIB en lugar de SoC. Aunque nuestros resultados son coherentes con los de ADVOCATE y con los de anteriores modelos de rentabilidad, es necesario seguir investigando para comprender mejor las consecuencias económicas del uso de CIB (frente a otras barreras cutáneas) en la práctica clínica.
Conflicto de Intereses
Gary W Inglese y George Skountrianos son empleados de Hollister Incorporated. Ariel Berger y Mustafa Oguz son empleados de Evidera Inc., que presta servicios de consultoría y otros servicios de investigación a organizaciones farmacéuticas, de dispositivos, gubernamentales y no gubernamentales. Evidera Inc. recibió financiación de Hollister Incorporated en relación con la realización de este estudio y con la elaboración de este manuscrito. Davide Croce es un empleado de la Universidad Carlo Cattaneo y no ha recibido ninguna financiación para la realización de este estudio ni para la elaboración de este manuscrito.
Financiación
Esta investigación ha sido financiada por Hollister Incorporated.
Author(s)
Ariel Berger* MPH
Executive Director, Integrated Solutions – RWE
Evidera, 500 Totten Pond Road, 5th Floor, Waltham, MA 02451, USA
Email ariel.berger@evidera.com
Gary Inglese RN, MBA
Senior Director, Market Access
Hollister Incorporated, Libertyville, IL, USA
George Skountrianos MS
Statistician, Global Clinical Affairs
Hollister Incorporated, Libertyville, IL, USA
Davide Croce MBA
Aggregate Professor
Research Center in Health Economics, Social and Healthcare Management, Università Carlo Cattaneo–LIUC, Castellanza (Va), Italy
Mustafa Oguz PhD
Senior Research Associate, Data Analytics
Evidera Inc., Hammersmith, London, UK
* Corresponding author
References
- Alvey B, Beck DE. Peristomal dermatology. Clin Colon Rectal Surg 2008;21(1):41–44.
- Doctor K, Colibaseanu DT. Peristomal skin complications: causes, effects, and treatments. Chronic Wound Care Manag Res 2017;2017(4):1–6.
- Rolstad BS, Erwin-Toth PL. Peristomal skin complications: prevention and management. Ostomy Wound Manage 2004;50(9):68–77.
- Herlufsen P, Olsen AG, Carlsen B, et al. Study of peristomal skin disorders in patients with permanent stomas. Br J Nurs 2006;15(16):854–862.
- Meisner S, Lehur PA, Moran B, Martins L, Jemec GB. Peristomal skin complications are common, expensive, and difficult to manage: a population based cost modeling study. PLoS One 2012;7(5):e37813.
- Richbourg L, Thorpe JM, Rapp CG. Difficulties experienced by the ostomate after hospital discharge. J Wound Ostomy Continence Nurs 2007;34(1):70–79.
- Salvadalena GD. The incidence of stoma and peristomal complications during the first 3 months after ostomy creation. J Wound Ostomy Continence Nurs 2013;40(4):400–406.
- Taneja C, Netsch D, Rolstad BS, Inglese G, Lamerato L, Oster G. Clinical and economic burden of peristomal skin complications in patients with recent ostomies. J Wound Ostomy Continence Nurs 2017;44(4):350–357.
- Maeda S, Ouchi A, Komori K, et al. Risk factors for peristomal skin disorders associated with temporary ileostomy construction. Surg Today 2021.
- Shiraishi T, Nishizawa Y, Nakajima M, et al. Risk factors for the incidence and severity of peristomal skin disorders defined using two scoring systems. Surg Today 2020;50(3):284–291.
- Voegeli D, Karlsmark T, Eddes EH, et al. Factors influencing the incidence of peristomal skin complications: evidence from a multinational survey on living with a stoma. Gastrointest Nurs 2020;18(Sup4):S31–S38.
- Jemec GB, Nybaek H. Peristomal skin problems account for more than one in three visits to ostomy nurses. Br J Dermatol 2008;159(5):1211–1212.
- Nichols TR, Inglese GW. The burden of peristomal skin complications on an ostomy population as assessed by health utility and the physical component summary of the SF-36v2®. Value Hlth 2018;21(1):89–94.
- Coderch L, Lopez O, de la Maza A, Parra JL. Ceramides and skin function. Am J Clin Dermatol 2003;4(2):107–129.
- Colwell JC, Pittman J, Raizman R, Salvadalena G. A randomized controlled trial determining variances in ostomy skin conditions and the economic impact (ADVOCATE trial). J Wound Ostomy Continence Nurs 2018;45(1):37–42.
- Hollister Inc. The CeraPlus skin barrier product evaluation: clinicians’ feedback; 2017 [cited 2017 Nov 8]. Available from: https://www.hollister.no/-/media/files/pdfs-for-download/ostomy-clinical-evaluations-and-case-studies-pdfs/ceraplus-product-evaluation-113015.ashx.
- Hollister Inc. CeraPlus skin barrier; 2017 [cited 2020 Apr 21]. Available from: https://www.hollister.com/en/ceraplus.
- Berger A, Inglese G, Skountrianos G, Karlsmark T, Oguz M. Cost-effectiveness of a ceramide-infused skin barrier versus a standard barrier: findings from a long-term cost-effectiveness analysis. J Wound Ostomy Continence Nurs 2018;45(2):146–155.
- Mauskopf JA, Sullivan SD, Annemans L, et al. Principles of good practice for budget impact analysis: report of the ISPOR Task Force on good research practices – budget impact analysis. Value Hlth 2007;10(5):336–347.
- Australian Department of Health. Stoma Appliance Scheme – schedule; 2017 [cited 2017 Nov 8]. Available from: http://www.health.gov.au/internet/main/publishing.nsf/Content/AB1C0973EEA98E14CA257BF0001E01C4/$File/sas-schedule-1-july-2017-full.pdf.
- Taneja C, Netsch D, Rolstad BS, Inglese G, Eaves D, Oster G. Risk and economic burden of peristomal skin complications following ostomy surgery. J Wound Ostomy Continence Nurs 2019;46(2):143–149.
- ExchangeRates.org.uk. Euro to US dollar spot exchange rates for 2019; 2019 [cited 2020 Apr 21]. Available from: https://www.exchangerates.org.uk/EUR-USD-spot-exchange-rates-history-2019.html.
- Craig JA, Carr L, Hutton J, Glanville J, Iglesias CP, Sims AJ. A review of the economic tools for assessing new medical devices. Appl Health Econ Health Policy 2015;13(1):15–27.
- Neumann PJ. Budget impact analyses get some respect. Value Hlth 2007;10(5):324–325.
- Persson E, Berndtsson I, Carlsson E, Hallen AM, Lindholm E. Stoma-related complications and stoma size – a 2-year follow up. Colorectal Dis 2010;12(10):971–976.
Appendix A. Pouching Supply Use
With the exception of the UK, the costs of CIB pouching systems were assumed equivalent to those of SoC systems. In the UK, the per package cost of one-piece flat closed, convex closed, flat drainable, and convex drainable systems were £87.75, £98.70, £97.95 and £135.75 for SoC; and £88.68, £99.90, £106.42 and £144.31 for CIB, respectively. The baseplate and pouch package cost for two-piece systems were £20.00 and £1.69, respectively, for both SoC flat and convex systems, £22.24 and £1.69 for CIB flat systems, and £22.72 and £1.69 for CIB convex systems. Pouching supply use parameters are provided in Tables A1 to A6 below.
Table A1. Pouching supply use: US
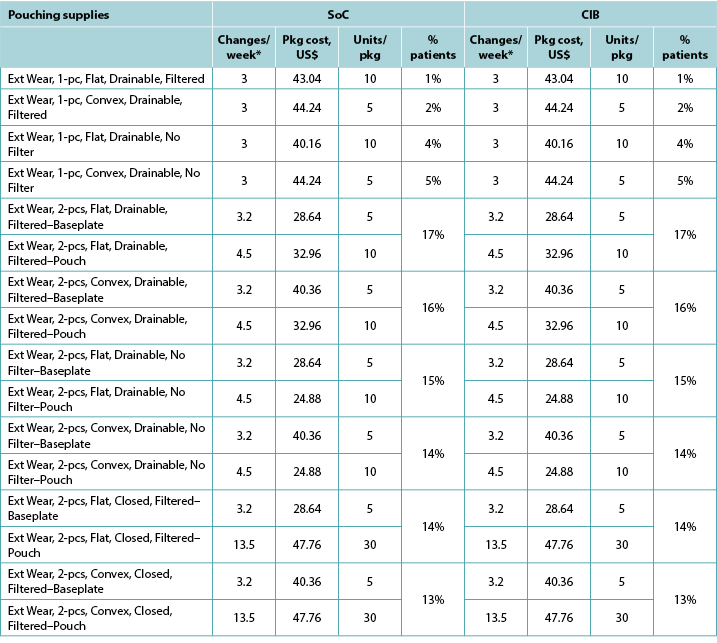
Table A2. Pouching supply use: UK
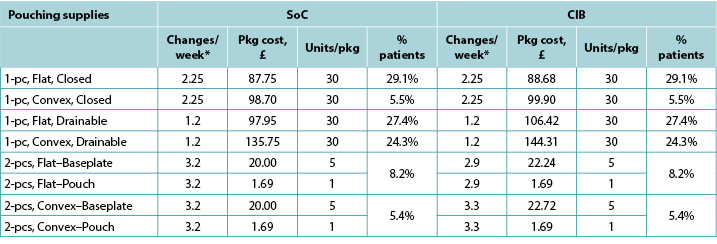
Table A3. Pouching supply use: Sweden
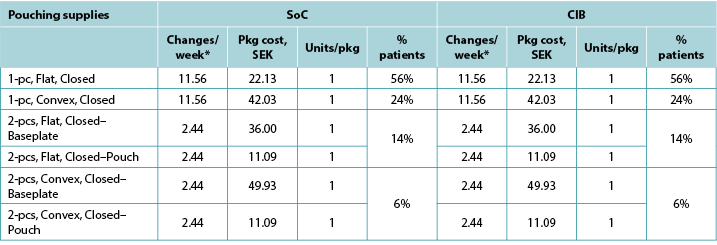
Table A4. Pouching supply use: Australia
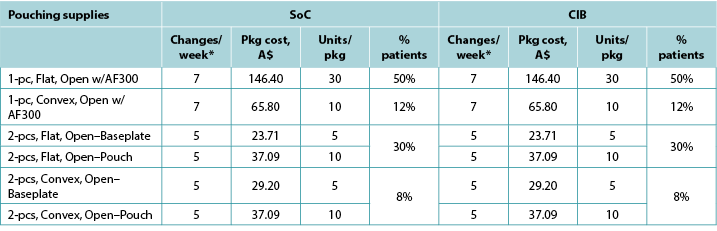
Table A5. Pouching supply use: Italy
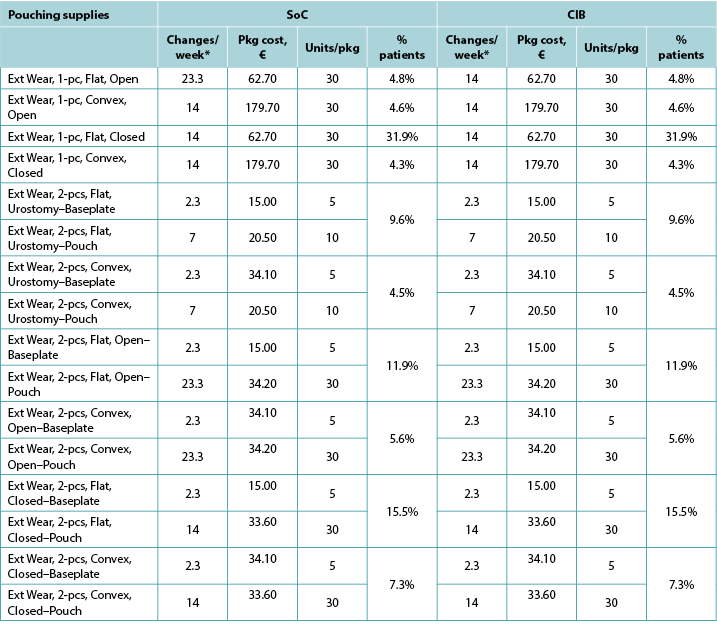
Table A6. Pouching supply use: Norway
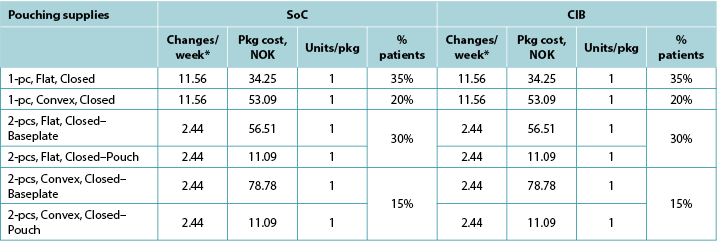
Appendix B. DSA of Expected Budget Impact, by Country
Expected budget impact associated with the use of a CIB versus SoC among patients within 12 weeks of faecal ostomy surgery in Australia, Italy, Norway, Sweden, the UK and the US.
Please note: Figure B1. DSA of expected budget impact: US, was not available at time of publishing
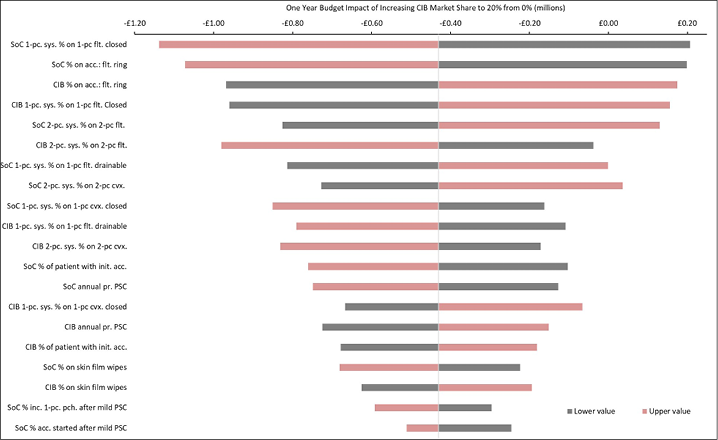
Figure B2. DSA of expected budget impact: UK
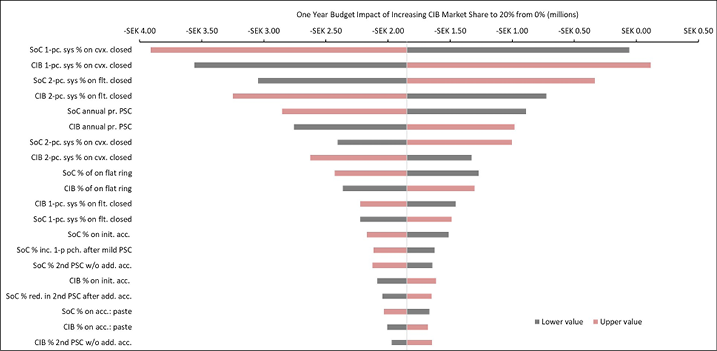
Figure B3. DSA of expected budget impact: Sweden
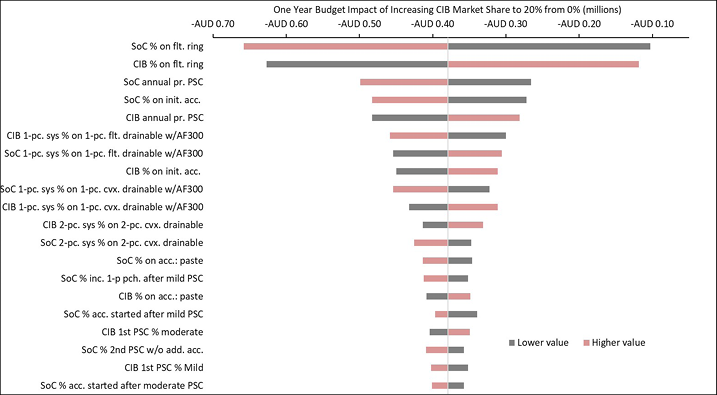
Figure B4. DSA of expected budget impact: Australia
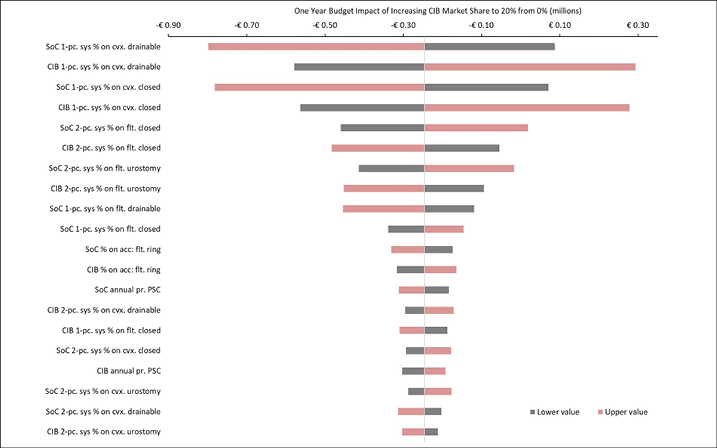
Figure B5. DSA of expected budget impact: Italy
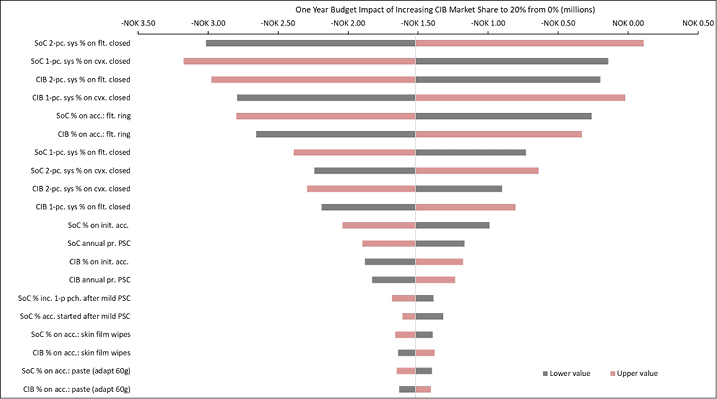
Figure B6. DSA of expected budget impact: Norway



