Volume 42 Number 3
WHAM evidence summary: turmeric for treating radiation dermatitis
Emily Haesler
Keywords radiation dermatitis, turmeric, curcumin, curcuma longa, radiodermatitis
For referencing Haesler E. WHAM evidence summary: turmeric for treating radiation dermatitis. WCET® Journal 2022;42(3):34-37
DOI https://doi.org/10.33235/wcet.42.3.34-37
Clinical question
What is the best available evidence for turmeric products for treating radiation dermatitis?
Summary
Turmeric (Curcuma longa) is a spice harvested in India and other Asian countries that has traditionally been used to treat many ailments, including skin conditions. It is recognised as having anti-inflammatory, antioxidant and antiseptic effects that could play a role in reducing radiation dermatitis, which frequently occurs during radiotherapy because of morphological skin changes. Level 1 evidence1 suggested oral turmeric taken throughout the course of radiotherapy is associated with a delay in onset and severity of radiation dermatitis. Level 1 evidence2–4 reporting on topical turmeric preparations was mixed. Two small studies2,3 found that topical turmeric reduces onset and severity of radiation dermatitis, while a third, larger study4 found no difference in effect compared to other topical preparations. More research on the potential benefits from application of a turmeric-based product during radiotherapy is required.
Clinical practice recommendations
All recommendations should be applied with consideration to the wound, the person, the health professional and the clinical context.
|
Oral turmeric could be considered as an adjunct therapy to reduce the severity of radiation dermatitis in selected people receiving radiation therapy (Grade B). There is insufficient evidence to make a graded recommendation on the use of topical turmeric preparations to reduce the severity of radiation dermatitis |
Sources of evidence: search and appraisal
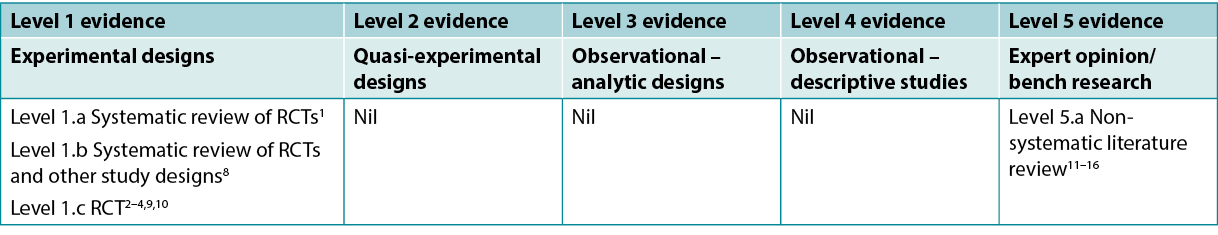
This summary was conducted using methods published by the Joanna Briggs Institute5–7. The summary is based on a systematic literature search combining search terms related to turmeric/curcumin/curcuma longa and radiation dermatitis. Studies reporting turmeric for management of other wounds or skin conditions (e.g., psoriasis) were excluded. Searches were conducted in the CINAHL, PubMed® and Hinari databases and in the Cochrane Library for evidence conducted in humans published up to April 2022 in English. Levels of evidence for intervention studies are reported in Table 1.
Table 1. Levels of evidence for clinical studies
Background
Turmeric (C. longa) is a spice prepared from a rhizome that is used as a traditional medicine in India and other Asian countries. Curcumin, which is the active chemical substance in turmeric17,18, is described as having anti-inflammatory, antioxidant, antiseptic and anti-cancer effects15,18–20.
Radiation dermatitis is a common side effect that affects up to 95% of people receiving radiotherapy for the management of breast cancer4,14,16. Radiotherapy can damage epithelial cells, decreasing the thickness of the epidermis and leading to increasing severity of signs and symptoms as radiotherapy continues, including warmth, pruritus, erythema, oedema, exudate, burning and pain21. It is theorised that curcumin may be effective in reducing the morphological changes that occur to the skin during radiation therapy by decreasing expression of inflammatory cytokines, growth factors and tumour necrosis factor2,12,14,15. Essentially, the anti-inflammatory and antioxidant properties of curcumin are considered advantageous in protecting against the processes that lead to radiation dermatitis14.
Clinical evidence
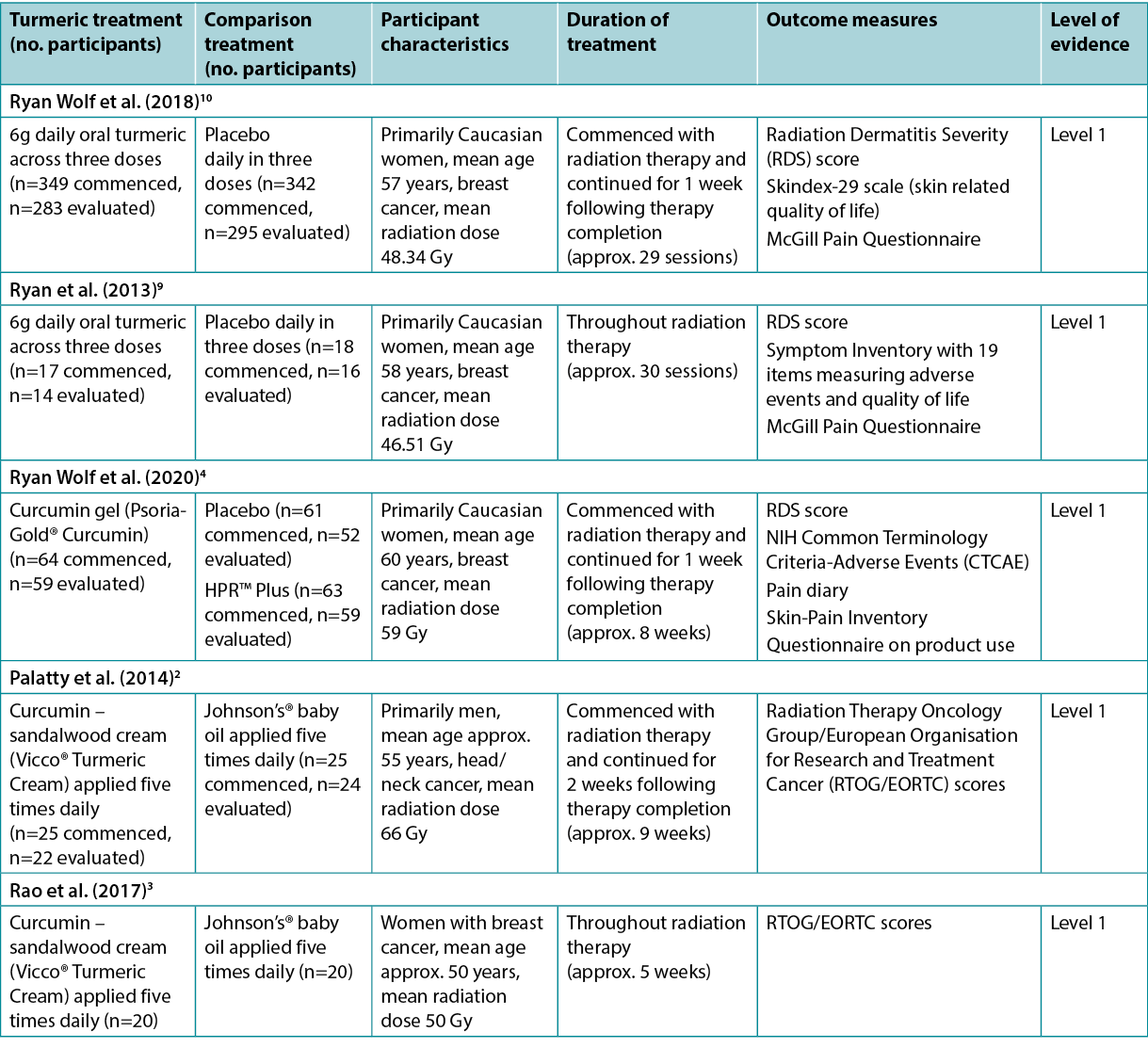
The evidence on turmeric products used to treat radiation dermatitis is summarised in Table 2.
Table 2. Summary of the evidence
Oral turmeric to treat radiation dermatitis
A meta-analysis1 at low risk of bias reported the use of oral curcumin for people receiving radiotherapy. This meta-analysis was conducted to inform an evidence-based clinical guideline22 and included two randomised clinical trials (RCTs)9,10 (n=716). In both the RCTs, people with breast cancer received either 6g curcumin daily (across three doses) or placebo, commencing at the start of radiotherapy and concluding 1 week after radiotherapy finished. There was a reduced risk of experiencing Grade 2 or higher radiation dermatitis associated with oral curcumin (risk ratio [RR]=0.64, 95% confidence interval [CI]=0.42 to 0.96, absolute risk reduction [ARR]=48 fewer cases per 1,000), but the mean difference in Radiation Dermatitis Severity (RDS) score was low (0.8 lower)1 and the RDS score was not statistically significantly different between groups at the end of treatment (p=0.55)22. The evidence was of low certainty and the withdrawal rate was high (curcumin group 18% versus control group 14%)22. The guideline developers made no recommendation on curcumin primarily due to potential interaction with medications, lack of cost-effectiveness data, and small anticipated desirable effects22 (Level 1).These studies were also reported in other reviews8,12–16 that were at higher risk of bias but that reached similar conclusions that oral curcumin was associated with some positive outcomes (Level 1 and 5).
Topical turmeric to treat radiation dermatitis
An RCT4 (n=191) at low risk of bias compared curcumin gel (4% concentration) to HPR™ Plus (described as a white lotion, FDA-approved medical device) to a placebo gel for reducing the severity of radiation dermatitis in people with breast cancer. The topical preparations were applied three times daily from the base of the neck to underneath the breast fold, including the side of the breast and under the arm, commencing with the start of radiotherapy and continuing until 1 week after therapy ceased. There were no statistically significant differences in mean RDS scores (curcumin 2.68 versus HPR™ Plus 2.64 versus placebo 2.63, p=0.929) or rate of moist desquamation (curcumin 25.42% versus HPR™ Plus 20.34% versus placebo 22.64%, p=0.805)4. This study had overall low rates of radiation dermatitis, and some potential benefits of turmeric therapy were reported in sub-analyses, but the study was not designed to measure these effects (Level 1).
An RCT2 (n=50) at moderate risk of bias compared the effect of a topical turmeric–sandalwood cream (16% turmeric extract) to a control (baby oil) for treating radiation dermatitis in people with head and neck cancer. The treatment for both groups was applied five times daily, from the first day of radiotherapy until 2 weeks after therapy concluded (approximately 9 weeks). After 2 weeks, no participants had experienced radiation dermatitis. From week 3 to week 7 the incidence of radiation dermatitis increased in both groups, with statistically significantly lower rates in the turmeric-based cream group in week 3 (12% versus 41.67%, p<0.045) and week 4 (37.5% versus 75%, p<0.028). Severity of radiation dermatitis evaluated using the Radiation Therapy Oncology Group/European Organisation for Research and Treatment Cancer (RTOG/EORTC) score was statistically significantly lower for the turmeric-based cream group from week 3 until conclusion of the study (p<0.05 for all). Grade 3 radiation dermatitis occurred less often in the turmeric-based cream group (9.5% versus 37.5%, p<0.01) and no participants in the study experienced Grade 4 radiation dermatitis2 (Level 1).
A more recent RCT3 (n=50) at moderate risk of bias conducted by the same research team2 explored topical turmeric–sandalwood cream (16% turmeric extract) for women with breast cancer undergoing radiotherapy. The comparator was baby oil, and the treatment regimen was the same as in the study above2. At the end of the second week of radiotherapy, the turmeric-based cream group had a statistically significantly lower rate of radiation dermatitis (32% versus 75%, p=0.0025). In both groups, rates of radiation dermatitis increased throughout the trial, but were statistically significantly lower in the turmeric-based cream group at every weekly measurement (p<0.05 for all)3 (Level 1).
Considerations for use
- Patient-reported outcomes, including pain and skin-related quality of life, were not statistically significantly different compared to a placebo for people taking oral curcumin10 or for people using topical curcumin4.
- Few adverse events have been reported in the literature8–10,12,13. Some evidence indicates curcumin can increase oxalate levels in the kidneys, contributing to development of kidney stones11. Potential to exacerbate gallstone symptoms has also been reported8.
- Curcumin has low bioavailability, which means it is poorly absorbed and used by the body8,10,12,13 and excreted rapidly8,16. Ongoing research is attempting to develop delivery mechanisms (e.g., encapsulation within nanoparticle carriers and developing water-soluble formulations) that will increase its clinical utility10,16.
Conflicts of interest
The author declares no conflicts of interest in accordance with International Committee of Medical Journal Editors (ICMJE) standards.
About wham collaborative evidence summaries
The WHAM Collaborative evidence summaries are consistent with methodology published in Munn, Lockwood and Moola23.
Methods are outlined in resources published by the Joanna Briggs Institute5–7 and on the WHAM Collaborative website: http://WHAMwounds.com. WHAM evidence summaries undergo peer review by an international, multidisciplinary Expert Reference Group. WHAM evidence summaries provide a summary of the best available evidence on specific topics and make suggestions that can be used to inform clinical practice. Evidence contained within this summary should be evaluated by appropriately trained professionals with expertise in wound prevention and management, and the evidence should be considered in the context of the individual, the professional, the clinical setting and other relevant clinical information.
Copyright ©2021 Wound Healing and Management Collaboration, Curtin Health Innovations Research Institute, Curtin University, WA, Australia.
Resumen de evidencias de la WHAM: cúrcuma para el tratamiento de la dermatitis por radiación
Emily Haesler
DOI: https://doi.org/10.33235/wcet.42.3.34-37
Pregunta clinica
¿Cuál es la mejor evidencia disponible de los productos de cúrcuma para el tratamiento de la dermatitis por radiación?
Resumen
La cúrcuma (Curcuma longa) es una especia cosechada en la India y otros países asiáticos que se ha utilizado tradicionalmente para tratar muchas dolencias, incluidas las de la piel. Se le reconocen efectos antiinflamatorios, antioxidantes y antisépticos que podrían desempeñar un papel en la reducción de la dermatitis por radiación, que se produce con frecuencia durante la radioterapia debido a los cambios morfológicos de la piel. Las evidencias de nivel 11, sugieren que la cúrcuma oral tomada durante el curso de la radioterapia se asocia con un retraso en la aparición y la gravedad de la dermatitis por radiación. Las evidencias de nivel 12-4, que informan sobre los preparados tópicos de cúrcuma fueron mixtas. Dos pequeños estudios2,3 descubrieron que la cúrcuma tópica reduce la aparición y la gravedad de la dermatitis por radiación, mientras que un tercer estudio más amplio4 no encontró diferencias en el efecto en comparación con otros preparados tópicos. Es necesario investigar más sobre los posibles beneficios de la aplicación de un producto a base de cúrcuma durante la radioterapia.
Recomendaciones para la practica clinica
Todas las recomendaciones deben aplicarse teniendo en cuenta la herida, la persona, el profesional sanitario y el contexto clínico.
|
La cúrcuma por vía oral podría considerarse un tratamiento complementario para reducir la gravedad de la dermatitis por radiación en personas seleccionadas que reciben radioterapia (Grado B). No hay evidencias suficientes para hacer una recomendación graduada sobre el uso de preparados tópicos de cúrcuma para reducir la gravedad de la dermatitis por radiación. |
Fuentes de evidencias: busqueda y evaluacion
Este resumen se realizó utilizando los métodos publicados por el Instituto Joanna Briggs5–7. El resumen se basa en una búsqueda bibliográfica sistemática que combina términos de búsqueda relacionados con la cúrcuma/curcumina/curcuma longa y la dermatitis por radiación. Se excluyeron los estudios que informaban sobre la cúrcuma para el tratamiento de otras heridas o afecciones cutáneas (por ejemplo, psoriasis). Se realizaron búsquedas en las bases de datos CINAHL, PubMed® e Hinari y en la Biblioteca Cochrane de evidencias realizadas en humanos publicadas hasta abril de 2022 en inglés. Los niveles de evidencia para los estudios de intervención se reportan en la Tabla 1.

Tabla 1. Niveles de evidencia de los estudios clínicos
Antecedentes
La cúrcuma (C. longa) es una especia preparada a partir de un rizoma que se utiliza como medicina tradicional en la India y otros países asiáticos. A la curcumina, que es la sustancia química activa de la cúrcuma17,18, se le atribuyen efectos antiinflamatorios, antioxidantes, antisépticos y anticancerígenos15,18–20.
La dermatitis por radiación es un efecto secundario común que afecta hasta al 95% de las personas que reciben radioterapia para el tratamiento del cáncer de mama4,14,16. La radioterapia puede dañar las células epiteliales, disminuyendo el grosor de la epidermis y provocando un aumento de la gravedad de los signos y síntomas a medida que la radioterapia continúa, incluyendo calor, prurito, eritema, edema, exudado, ardor y dolor21. Se cree que la curcumina puede ser eficaz para reducir los cambios morfológicos que se producen en la piel durante la radioterapia al disminuir la expresión de citoquinas inflamatorias, factores de crecimiento y el factor de necrosis tumoral2,12,14,15. Esencialmente, las propiedades antiinflamatorias y antioxidantes de la curcumina se consideran ventajosas para proteger contra los procesos que conducen a la dermatitis por radiación14.
Evidencia clinica
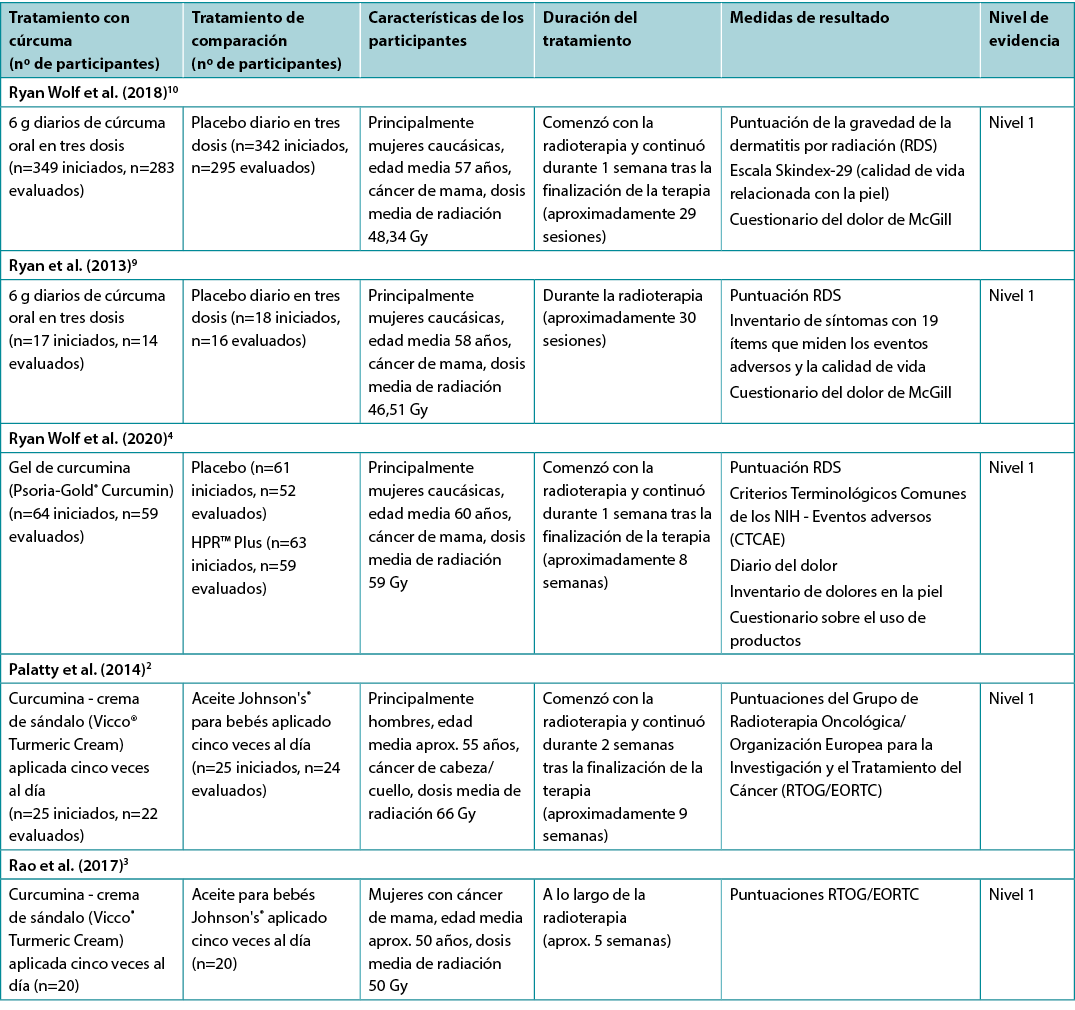
La evidencia sobre los productos de cúrcuma utilizados para tratar la dermatitis por radiación se resume en la Tabla 2.
Tabla 2. Resumen de las evidencias
Cúrcuma oral para tratar la dermatitis por radiación
Un metanálisis1 con bajo riesgo de sesgo informó del uso de curcumina oral para personas que reciben radioterapia. Este metanálisis se realizó para informar una guía clínica basada en la evidencia22 e incluyó dos ensayos clínicos aleatorios (RCT)9,10 (n=716). En ambos RCT, las personas con cáncer de mama recibieron 6 g de curcumina al día (en tres dosis) o un placebo, comenzando al inicio de la radioterapia y concluyendo una semana después de terminada ésta. Hubo una reducción del riesgo de experimentar dermatitis por radiación de Grado 2 o superior asociada a la curcumina oral (cociente de riesgo [RR]=0,64, intervalo de confianza [CI] del 95% =0,42 a 0,96, reducción del riesgo absoluto [ARR]=48 casos menos por cada 1.000), pero la diferencia media en la puntuación de la gravedad de la dermatitis por radiación (RDS) fue baja (0,8 menos)1 y la puntuación de la RDS no fue estadísticamente significativa entre los grupos al final del tratamiento (p=0,55)22. La evidencia era de baja certeza y la tasa de retirada era alta (grupo de curcumina 18% frente al grupo de control 14%)22. Los desarrolladores de las directrices no hicieron ninguna recomendación sobre la curcumina, principalmente debido a la posible interacción con los medicamentos, la falta de datos sobre la relación coste-eficacia y los pequeños efectos deseables previstos22(Nivel 1). Estos estudios también se informaron en otras revisiones8,12–16 que tenían un mayor riesgo de sesgo, pero que llegaron a conclusiones similares de que la curcumina oral se asociaba con algunos resultados positivos (Nivel 1 y 5).
Cúrcuma tópica para tratar la dermatitis por radiación
Un RCT4 (n=191) con bajo riesgo de sesgo comparó el gel de curcumina (concentración del 4%) con HPR™ Plus (descrito como una loción blanca, dispositivo médico aprobado por la FDA) con un gel de placebo para reducir la gravedad de la dermatitis por radiación en personas con cáncer de mama. Los preparados tópicos se aplicaron tres veces al día desde la base del cuello hasta debajo del pliegue mamario, incluyendo el lateral de la mama y la axila, comenzando con el inicio de la radioterapia y continuando hasta una semana después del cese de la terapia. No hubo diferencias estadísticamente significativas en las puntuaciones medias de RDS (curcumina 2,68 frente a HPR™ Plus 2,64 frente a placebo 2,63, p=0,929) ni en la tasa de descamación húmeda (curcumina 25,42% frente a HPR™ Plus 20,34% frente a placebo 22,64%, p=0,805)4. Este estudio tuvo tasas generales bajas de dermatitis por radiación, y en los subanálisis se informaron algunos beneficios potenciales de la terapia con cúrcuma, pero el estudio no fue diseñado para medir estos efectos (Nivel 1).
Un RCT2 (n=50) con riesgo moderado de sesgo comparó el efecto de una crema tópica de cúrcuma y sándalo (16% de extracto de cúrcuma) con un control (aceite para bebés) para el tratamiento de la dermatitis por radiación en personas con cáncer de cabeza y cuello. El tratamiento para ambos grupos se aplicó cinco veces al día, desde el primer día de la radioterapia hasta dos semanas después de concluida la terapia (aproximadamente 9 semanas). Después de 2 semanas, ningún participante había experimentado dermatitis por radiación. De la semana 3 a la 7, la incidencia de la dermatitis por radiación aumentó en ambos grupos, con tasas estadísticamente significativas menores en el grupo de la crema a base de cúrcuma en la semana 3 (12% frente a 41,67%, p<0,045) y en la semana 4 (37,5% frente a 75%, p<0,028). La gravedad de la dermatitis por radiación evaluada mediante la puntuación del Grupo de Radioterapia Oncológica/Organización Europea para la Investigación y el Tratamiento del Cáncer (RTOG/EORTC) fue significativamente menor desde la semana 3 hasta la conclusión del estudio para el grupo de la crema a base de cúrcuma (p<0,05 para todos). La dermatitis por radiación de grado 3 se produjo con menos frecuencia en el grupo de la crema a base de cúrcuma (9,5% frente a 37,5%, p<0,01) y ningún participante del estudio experimentó dermatitis por radiación de Grado 42, (nivel 1).
Un RCT más reciente3 (n=50) con riesgo moderado de sesgo realizado por el mismo equipo de investigación2 exploró la crema tópica de cúrcuma y sándalo (16% de extracto de cúrcuma) para mujeres con cáncer de mama sometidas a radioterapia. El comparador fue el aceite de bebé, y el régimen de tratamiento fue el mismo que en el estudio anterior2. Al final de la segunda semana de radioterapia, el grupo de la crema a base de cúrcuma tenía una tasa estadísticamente significativa menor de dermatitis por radiación (32% frente al 75%, p=0,0025). En ambos grupos, las tasas de dermatitis por radiación aumentaron a lo largo del ensayo, pero fueron significativamente inferiores desde el punto de vista estadístico en el grupo de la crema a base de cúrcuma en cada medición semanal (p<0,05 para todos)3 (Nivel 1).
Consideraciones de uso
- Los resultados comunicados por los pacientes, incluidos el dolor y la calidad de vida relacionada con la piel, no fueron significativamente diferentes desde el punto de vista estadístico en comparación con un placebo para las personas que tomaban curcumina oral10 o para las que utilizaban curcumina tópica4.
- En la literatura se han reportado pocos eventos adversos8–10,12,13. Algunas evidencias indican que la curcumina puede aumentar los niveles de oxalato en los riñones, contribuyendo al desarrollo de cálculos renales11. También se ha informado de la posibilidad de exacerbar los síntomas de los cálculos biliares8.
- La curcumina tiene una baja biodisponibilidad, lo que significa que el cuerpo la absorbe y utiliza poco8,10,12,13 y la excreta rápidamente8,16. Las investigaciones en curso intentan desarrollar mecanismos de administración (por ejemplo, la encapsulación en portadores de nanopartículas y el desarrollo de formulaciones hidrosolubles) que aumenten su utilidad clínica10,16.
Conflictos de intereses
Los autores declaran no tener conflictos de intereses de acuerdo con las normas del Comité Internacional de Editores de Revistas Médicas (ICMJE).
Sobre los resumenes de evidencias en colaboracion de WHAM
Los resúmenes de evidencia en Colaboración WHAM son consistentes con la metodología publicada en Munn, Lockwood y Moola23.
Los métodos se describen en los recursos publicados por el Instituto Joanna Briggs5–7 y en el sitio web de la Colaboración WHAM: http://WHAMwounds.com. Los resúmenes de evidencia de la WHAM son revisados por un Grupo de Referencia de Expertos internacional y multidisciplinar. Los resúmenes de evidencia de la WHAM proporcionan un resumen de la mejor evidencia disponible sobre temas específicos y hacen sugerencias que pueden ser utilizadas para informar la práctica clínica. La evidencia contenida en este resumen debe ser evaluada por profesionales debidamente formados y con experiencia en la prevención y el tratamiento de heridas, y la evidencia debe considerarse en el contexto del individuo, el profesional, el entorno clínico y otra información clínica relevante.
Copyright ©2021 Wound Healing and Management Collaboration, Instituto de Investigación de Innovación Sanitaria de Curtin, Universidad de Curtin, WA Australia.
Author(s)
Emily Haesler
PhD Post Grad Dip Adv Nurs (Gerontics) BNurs Fellow Wounds Australia
Adjunct Professor Wound Healing and Management Collaborative, Curtin Health Innovation Research Institute, Curtin University, WA
References
- Ginex PK, Backler C, Croson E, Horrell LN, Moriarty KA, Maloney C, Vrabel M, Morgan RL. Radiodermatitis in patients with cancer: systematic review and meta-analysis. Oncol Nurs Forum 2020;47(6):E225-E36.
- Palatty PL, Azmidah A, Rao S, Jayachander D, Thilakchand KR, Rai MP, Haniadka R, Simon P, Ravi R, Jimmy R, D’Souza P F, Fayad R, Baliga MS. Topical application of a sandal wood oil and turmeric based cream prevents radiodermatitis in head and neck cancer patients undergoing external beam radiotherapy: a pilot study. Br J Radiol 2014;87(1038):20130490.
- Rao S, Hegde SK, Baliga-Rao MP, Lobo J, Palatty PL, George T, Baliga MS. Sandalwood oil and turmeric-based cream prevents ionizing radiation-induced dermatitis in breast cancer patients: clinical study. Medicines (Basel) 2017;4(3).
- Ryan Wolf J, Gewandter JS, Bautista J, Heckler CE, Strasser J, Dyk P, Anderson T, Gross H, Speer T, Dolohanty L, Bylund K, Pentland AP, Morrow GR. Utility of topical agents for radiation dermatitis and pain: a randomized clinical trial. Supp Care Cancer 2020;28(7):3303–11.
- Aromataris E, Munn Z, editors. Joanna Briggs Institute reviewer’s manual; 2017. Available from: https://reviewersmanual.joannabriggs.org/The Joanna Briggs Institute.
- Joanna Briggs Institute Levels of Evidence and Grades of Recommendation Working Party. New JBI grades of recommendation. Adelaide: Joanna Briggs Institute; 2013.
- The Joanna Briggs Institute Levels of Evidence and Grades of Recommendation Working Party. Supporting document for the Joanna Briggs Institute levels of evidence and grades of recommendation. The Joanna Briggs Institute; 2014. Available from:www.joannabriggs.org
- Vaughn AR, Branum A, Sivamani RK. Effects of turmeric (Curcuma longa) on skin health: a systematic review of the clinical evidence. Phytother Res 2016;30(8):1243–64.
- Ryan JL, Heckler CE, Ling M, Katz A, Williams JP, Pentland AP, Morrow GR. Curcumin for radiation dermatitis: a randomized, double-blind, placebo-controlled clinical trial of thirty breast cancer patients. Radiat Res 2013;180(1):34–43.
- Ryan Wolf J, Heckler CE, Guido JJ, Peoples AR, Gewandter JS, Ling M, Vinciguerra VP, Anderson T, Evans L, Wade J, Pentland AP, Morrow GR. Oral curcumin for radiation dermatitis: a URCC NCORP study of 686 breast cancer patients. Supp Care Cancer 2018;26(12):1543–52.
- Watts R. Evidence summary: turmeric (curcumin) in wound management limited resources communities. Wound Pract Res 2017;25(3):158–9.
- Akbari S, Kariznavi E, Jannati M, Elyasi S, Tayarani-Najaran Z. Curcumin as a preventive or therapeutic measure for chemotherapy and radiotherapy induced adverse reaction: a comprehensive review. Food Chem Toxicol 2020;145:111699.
- Karaboga Arslan AK, Uzunhisarcıklı E, Yerer MB, Bishayee A. The golden spice curcumin in cancer: a perspective on finalized clinical trials during the last 10 years. J Cancer Res Ther 2022;18(1):19–26.
- Farhood B, Mortezaee K, Goradel NH, Khanlarkhani N, Salehi E, Nashtaei MS, Najafi M, Sahebkar A. Curcumin as an anti-inflammatory agent: implications to radiotherapy and chemotherapy. J Cell Physiol 2019;234(5):5728–40.
- Verma V. Relationship and interactions of curcumin with radiation therapy. World J Clin Oncol 2016;7(3):275–83.
- Zoi V, Galani V, Tsekeris P, Kyritsis AP, Alexiou GA. Radiosensitization and radioprotection by curcumin in glioblastoma and other cancers. Biomed 2022;10(2):312.
- Akbik D, Ghadiri M, Chrzanowski W, Rohanizadeh R. Curcumin as a wound healing agent. Life Sci (1973) 2014;116(1):1–7.
- Mohanty C, Sahoo SK. Curcumin and its topical formulations for wound healing applications. Drug Discov Today 2017;22(10):1582–92.
- Maheshwari RK, Singh AK, Gaddipati J, Srimal RC. Multiple biological activities of curcumin: a short review. Life Sci (1973) 2006;78(18):2081–7.
- Ahangari N, Kargozar S, Ghayour-Mobarhan M, Baino F, Pasdar A, Sahebkar A, Ferns GAA, Kim HW, Mozafari M. Curcumin in tissue engineering: a traditional remedy for modern medicine. Biofactor 2019;45(2):135–51.
- Haesler, E. Wound dressings for treating of radiation dermatitis: a WHAM evidence summary. Wound Pract Res 2021;29(3):176–9.
- Gosselin T, Ginex PK, Backler C, Bruce SD, Hutton A, Marquez CM, Shaftic AM, Suarez LV, Moriarty KA, Maloney C, Vrabel M, Morgan RL. ONS guidelines™ for cancer treatment-related radiodermatitis. Oncol Nurs Forum 2020;47(6):654–70.
- Munn Z, Lockwood C, Moola S. The development and use of evidence summaries for point of care information systems: a streamlined rapid review approach. Worldview Evid Based Nurs 2015;12(3):131–8.




