Volume 43 Number 4
Examining the association of immunosuppressants and wound healing: a narrative review
Aria Appoo, Brandon L Christensen, Ranjani Somayaji
Keywords wound healing, Calcineurin inhibitors, glucocorticoids, immunosuppressants, monoclonal antibodies, mTOR inhibitors
For referencing Appoo A, Christensen BL and Somayaji R . Examining the association of immunosuppressants and wound healing: a narrative review. WCET® Journal 2023;43(4):32-39.
DOI
10.33235/wcet.43.4.32-39
Submitted 1 February 2023
Accepted 23 May 2023
Abstract
Objective A review of recent literature to provide clinicians with an understanding of how different classes of immunosuppressants affect wound healing.
Data sources A literature search was conducted in PubMed, Google Scholar, and the University of Calgary Health Sciences Library.
Study Selection Studies chosen for inclusion were screened initially based on title using key words including “immunosuppressive medication, wound healing, and immunosuppression.” If the title and/or abstract contained these key words and addressed wound healing related to immunosuppressant medications and had been published after 2000, they were included in the review. When human data was not available for an immunosuppressant (class), animal studies were included.
Data Extraction Selected papers underwent full text review and summarisation.
Data Synthesis Data were synthesised in a descriptive manner. Corticosteroids and mechanistic target of rapamycin (mTOR) inhibitors most consistently demonstrate detrimental effects on wound healing. For other classes of immunosuppressants, evidence is limited with varying effects on wound healing described.
Conclusions Larger high-quality studies are required to better understand the effects of immunosuppressants particularly with development of new classes of these drugs on wound healing in order to identify those at highest risk of impairing wound healing.
Introduction
Immunosuppressants are medications with a variety of indications including in solid organ and hematopoietic transplants along with autoimmune diseases. They function by suppressing the activity of various components of the adaptive immune system thus diminishing the cascade of inflammatory response to normal host tissue or modulating the natural rejection response to transplanted materials.1 The main classes of immunosuppressants are corticosteroids/glucocorticoids,2,3 calcineurin inhibitors,2,4,5 mechanistic target of rapamycin (mTOR) inhibitors,2,4 polyclonal antibodies,2,4 monoclonal antibodies,2,4 and antiproliferative agents.2 For the purpose of this review, wounds are defined as an opening in the skin as a result of surgery, trauma, or disease that is susceptible to infection.
The immune system plays an important role in the prevention of infection but also the healing process of wounds, with the inflammatory effects leading to cellular proliferation and secretion of important intra and extracellular components.6 With immunosuppressants, the immune system is modulated, thus potentially affecting a wound’s healing time and susceptibility to infection.7 With a growing number of patients on immunosuppressing medications, particularly post-surgical transplant patients, the effect of immunosuppressants on wound healing is an important issue to be considered. This review article aims to provide clinicians with an understanding of how different classes of immunosuppressants affect wound healing.
Materials/methods
A literature search between 2000 through 2021 was conducted using the generic names of a number of commonly used immunosuppressants (glucocorticoids/corticosteroids, mTOR inhibitors, methotrexate, monoclonal antibodies, polyclonal antibodies, calcineurin inhibitors, mycophenolate, azathioprine) as well as the terms “wound healing” and “immunosuppression”. The primary database searched was PubMed. This was supplemented by Google Scholar and the University of Calgary Health Science Library database. When possible, the search was in the following format “immunosuppressant name [MeSH Terms] AND “wound healing [MeSH Terms].” If the immunosuppressant name was not available as a MeSH term, then the term was searched with no restriction applied. Article titles were then screened for relevance to the review based on whether wound healing was described in relation to the immunosuppressive medication/class. The abstract was screened similarly and included in the review accordingly. If the article compared various immunosuppressants, discussed their effects on wound healing, measured wound healing or deleterious effects on wounds it was considered relevant. If search terms did not identify human subject studies, then studies that used animals to evaluate immunosuppressive effects on wound healing were included. When no data was available from 2000 onwards, a historic search was conducted for the relevant immunosuppressive medications.
All included studies were summarised descriptively including immunosuppressive mechanism of action, study subjects, and evidence of effects on wound healing.
Results
The studies screened relevant to this review were used to inform the various categories outlined below. A total of 200 article titles and abstracts were initially screened and 61 articles were included for review. Summary tables highlighting the results of clinical and animal studies are summarised in Table 1. The specific indications for various immunosuppressants including their possible impacts on wounds are outlined in Table 2.
Table 1. Studies Comparing the Effects of Different Immunosuppressants on Wounds
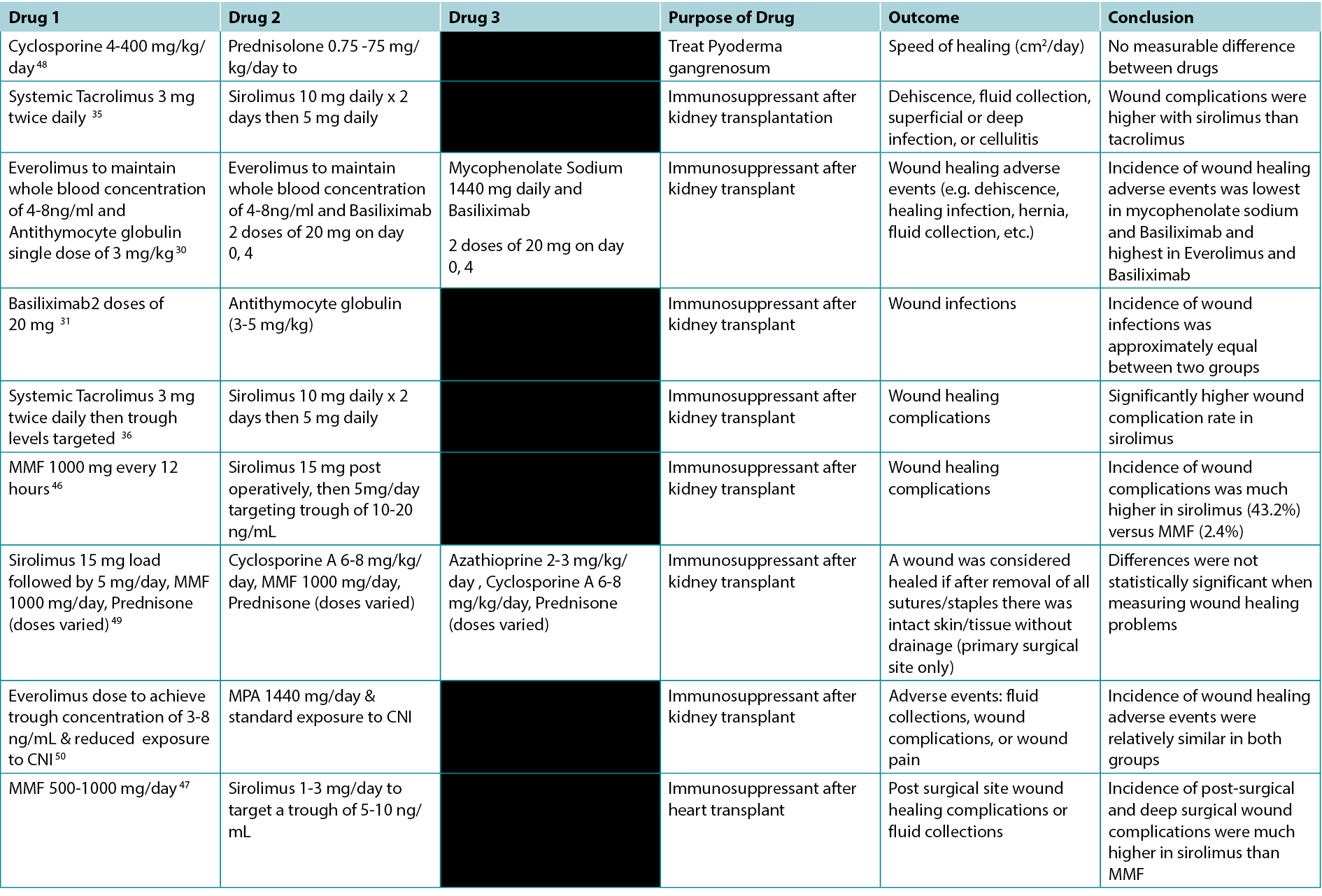
Table 2. Overview of Indications and Wound Effects of Various Immunosuppressants
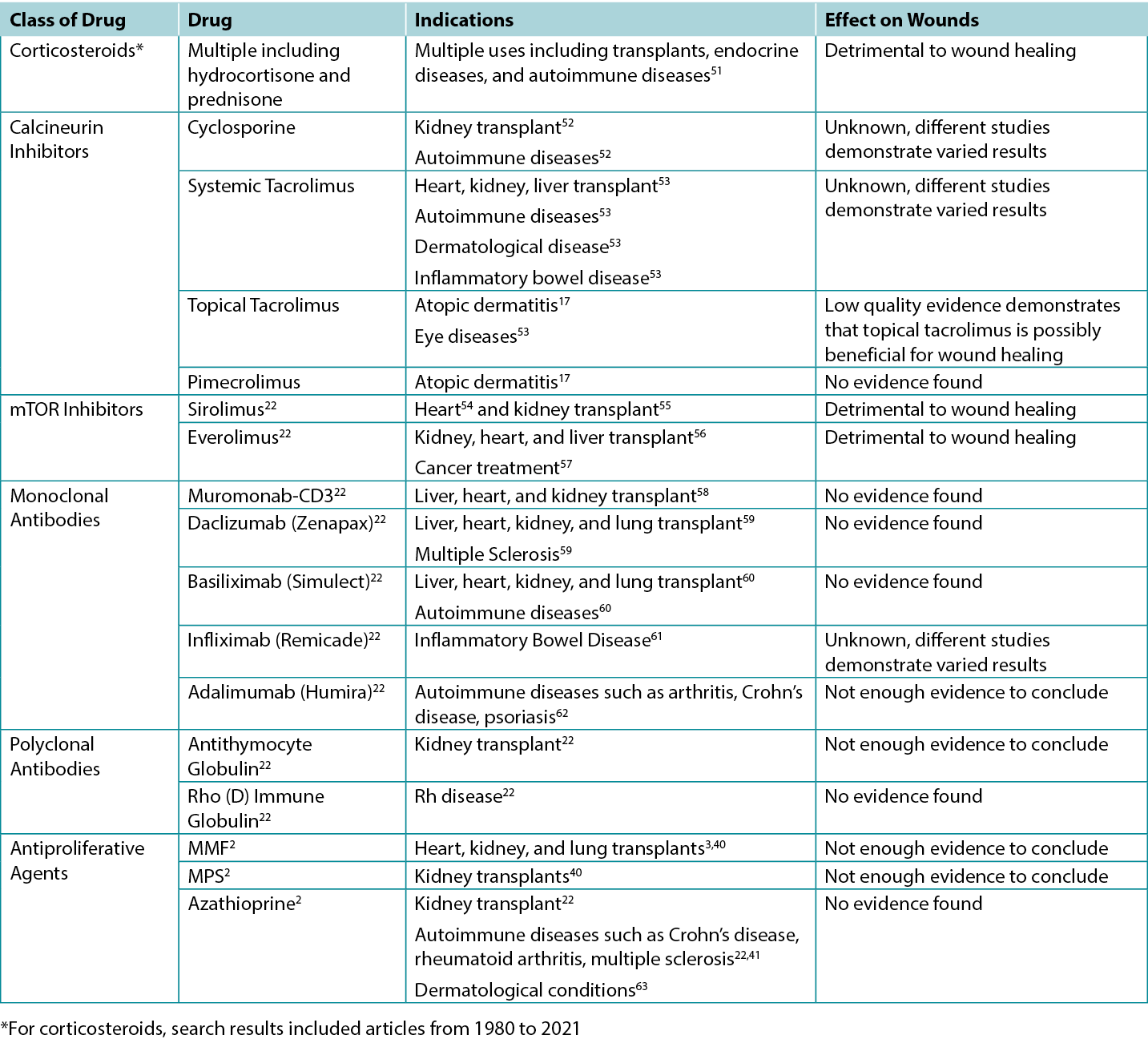
Calcineurin Inhibitors
Calcineurin inhibitors (CNI) are used as immunosuppressants for a variety of different autoimmune diseases, organ transplants, dermatological conditions, and in chronic wounds.8 There are three main types of CNI’s: cyclosporine (systemic), tacrolimus (systemic and topical), pimecrolimus (topical).9 CNI’s work by binding to part of the calcineurin molecule found in human cells, thus stopping the release of certain cytokines that are responsible for activating T cells.8 Therefore, CNI’s disable one of the main arms of the body’s adaptive immune response.
Systemic
There are a lack of studies directly focusing on the effects of CNI’s on wound healing in humans; however, many basic science studies on animals have been performed. Two such studies using rats compared the effect of various doses of systemic tacrolimus versus a control, testing the breaking strengths of the wounds created through surgery. One of the rat studies concluded that tacrolimus does not affect wound healing10 while the other study concluded that tacrolimus is detrimental to wound healing.11 At the same time, case reports using systemic tacrolimus as a treatment for ulcers in a person with lichen planus and pyoderma gangrenosum demonstrated treatment success with this therapy.12
No recent human studies were found regarding the effect of cyclosporine and wound healing. Two other studies using rats also yielded contradictory results. These rat studies focused on the effects of cyclosporine on different markers in the body that signify effective wound healing. One study comparing cyclosporine to methylprednisone demonstrated that cyclosporine had no suppressive effect on the various inflammatory and biochemical markers compared to the glucocorticoid therapy13 whereas the other study showed that cyclosporine had a negative effect on the markers.14 In a different study, after receiving a lung transplant, dogs were assigned to a specific immunosuppressant drug or no immunosuppressant drug and, similar to control, Cyclosporine A was shown to have no significant effect on the healing of the surgical wound as measured by breaking strength in comparison to glucocorticoid and azathioprine immunosuppression.15 Overall, the literature on systemic calcineurin inhibitors and wound healing is dated with a heterogeneity of comparators and mixed results on wound healing.
Topical
Calcineurin inhibitors (tacrolimus and pimecrolimus) are used as topical ointments most commonly for dermatological conditions such as atopic dermatitis but also for chronic dermatologic conditions such as pyoderma gangrenosum.16–18 Some case studies have shown tacrolimus effective at healing complex leg ulcers in the context of venous insufficiency or necrobiosis lipoidica, when regular treatment strategies have been ineffective.19,20 Furthermore, a rat-based study with acute cutaneous injury demonstrated that wounds treated with topical tacrolimus healed equally as quickly as the control (petrolatum).21
Monoclonal Antibodies:
A variety of different monoclonal antibodies (mAb) therapies exist with indications in transplants and autoimmune disorders such as rheumatoid arthritis and psoriasis.22 In general, mAb work by binding to different receptors and antigens to inhibit the effect of cytokines and other signal pathways that activate the immune system.22 A small prospective cohort study among patients with rheumatoid arthritis undergoing orthopedic surgery demonstrated that there was no increased risk of surgical wound infections or healing complications in patients on infliximab compared to conventional therapy.23 Furthermore, a case report claims that topical infliximab was helpful in healing leg ulcers that were resistant to standard treatment suggesting that inhibiting tumor necrosis factor alpha is helpful to wound healing.24 Similar findings were concluded in a case report for treatment of pyoderma gangrenosum with infliximab resulting in improvement of the ulcer.25 Inhibiting tumor necrosis factor alpha was shown to be further associated with wound healing in venous leg ulcers through the use of Adalimumab systemically.26 However, another study used infliximab on rat abdominal wounds and demonstrated that the tensile strength was significantly lower in the wounds of rats who had been given infliximab compared to those who were the control.27 Overall, the limited literature on the subject to date suggests clinical outcomes thus far are favorable in terms of wound healing.
Polyclonal Antibodies
Polyclonal antibodies (pAb’s) are very similar to mAb’s in function, with slightly varied mechanism of action.28,29 Unlike mAb’s, a group of polyclonal antibodies are created from many different lines of B cells and within the group different pAb’s bind to different epitopes of an antigen. In contrast, mAb’s come from a single line of B cells and can bind to only one antigen.28,29 There are two main pAb’s: Antithymocyte Globulin and Rho (D) Immune Globulin.22 Antithymocyte Globulin also known as Antihuman Thymocyte Globulin is most commonly used as an immunosuppressant after kidney transplantation and works by binding to a variety of lymphocytes and depleting the number of T cells in the body.22 Rho (D) Immune Globulin is used in pregnancies where the mother is Rh- and the fetus is Rh+ and essentially stops the formation of anti Rh+ antibodies in the mother.22
Few studies looking at the effects of pAb’s on wound healing were found. Two studies outlined the effects of antithymocyte globulin and Basiliximab. The first study in patients with renal transplants, where both drugs were combined with everolimus, showed higher rates of adverse effects of wound healing in Basiliximab. 30 The second study demonstrating that the incidence of wound infections was equal in patients taking Basiliximab versus antithymocyte globulin post renal transplant.31 Since white blood cells play a key role in wound healing through secreting necessary cytokines and preventing infection,32 it would be reasonable to hypothesise that antithymocyte globulin will affect wound healing since it reduces the number of white blood cells as well as their regulatory mechanisms.
mTOR Inhibitors
Mechanistic target of rapamycin (mTOR) inhibitors are immunosuppressive drugs that works by interacting with proteins in complex signalling pathways to prevent cells moving into the S phase of the cell cycle and therefore suppressing proliferation.3,22 mTOR predominantly targets T cells, but can also affect B cells.3 Interestingly, mTOR can cause an increase of production of certain inflammatory cytokines such as interleukin-6 and decrease production of interleukin-10, an anti-inflammatory cytokine.3 There are two main mTOR inhibitors: sirolimus and everolimus.3,22 In general, mTOR inhibitors have a variety of applications including cancer therapy.3,22 As an immunosuppressant, they are used after transplants.3,22 Everolimus has been shown to inhibit the proliferation of fibroblast in in vitro models33 suggesting that everolimus could have negative consequences for wound healing since fibroblasts are essential for creating an extracellular matrix and creating a frame for other cells.34 In a study comparing sirolimus and systemic tacrolimus, sirolimus had a wound complication rate of 47% compared to tacrolimus with only 8%.35 This is consistent with another study by Larson et al demonstrating higher wound complications with sirolimus compared to tacrolimus.36 Interestingly, obese patients on sirolimus had very high rates of wound complications leading to the study excluding all patients with obesity.36 In line with previous findings, a study on rats showed that increased sirolimus doses decreases wound strength, which the authors hypothesising this effect may be due to lower levels of VEGF and nitric oxide in rats receiving higher doses of sirolimus.37 In one review authors concluded that mTOR inhibitors are harmful to wound healing in high doses, but seem to have a neutral effect in low does.38 Given early concerns with mTOR inhibitors and wound healing, regimens using these immunosuppressive agents have evolved with lower doses of the mTOR inhibitors and combination therapy. In the large TRANSFORM randomised control trial investigators compared everolimus plus reduced dose CNI to mycophenolic acid plus standard dose CNI (standard care) in patients with renal transplants and showed wound related adverse events were not statistically different (20.6% vs 17.3%; RR 1.19 95%CI 0.99 to 1.43).39 One limitation of this study was close monitor of everolimus concentrations and difficulties achieving the targeted plasma concentrations C0 between 3 and 8 ng/mL.39 Overall, review of the current literature is suggestive that mTOR inhibitors have a detrimental effect on wound healing, especially at higher doses, and that improved dosing regimens may lessen or mitigate this risk.
Antiproliferative Agents
There are three regularly used antiproliferative agents: Mycophenolate mofetil (MMF) and Mycophenolate sodium (MPS) (both inosine monophosphate dehydrogenase (IMPDH) inhibitors) and azathioprine.2,40 IMPDH inhibitors have a similar effect to mTOR inhibitors in terms of their mechanism of immunosuppression. In the body, MMF and MPS are converted into mycophenolic acid which blocks a portion of a pathway that is crucial for DNA synthesis, to decrease proliferation of T cells and B cells.2,5,40 MMF is used for its immunosuppressive effect in heart, kidney, and lung transplants.3,40 MPS is used for kidney transplants.40 Azathioprine is used as an immunosuppressive drug for kidney transplants and autoimmune diseases including rheumatoid arthritis, Crohn’s disease, and multiple sclerosis.22,41 In the body, azathioprine reacts with glutathione and is converted into 6-mercaptupurine after which additional metabolites are generated ultimately blocking purine synthesis and stimulation of T-cells.3,22
When a study compared two different doses of MMF in kidney transplant recipients, incidence of wounds requiring surgical intervention were not significantly different, similarly for wounds treated with local wound care.42 Based on review of article titles as part of our search, no studies regarding the sole effect of azathioprine on external wound healing in humans were found. When azathioprine was compared to a placebo in a rat study, the wounds of the rats who were on azathioprine took longer to heal than those on the placebo suggesting that azathioprine can have detrimental effects on wound healing, but the extent that it would affect humans is unclear.43
Anti-metabolite
Methotrexate is a commonly used folate antagonist immunosuppressive agent, with indications in many rheumatologic disorders. It also has antineoplastic activity in higher doses. Upon absorption, it enters the cell and is converted to methotrexate polyglutamates where it competes for dihydrofolate reductase thus preventing the transformation of folic acid for its use in the building of nucleic acids.6 Like other agents described, there is experimental animal studies with in vitro studies suggesting impairment in wound healing but these effects have not been borne out in clinical studies, particularly in post-surgical wounds.6 Thus, it is recommended this drug be continued postoperatively.
Corticosteroids/Glucocorticoids
Glucocorticoids prevent the formation of inflammatory chemicals like cytokines, cell adhesion molecules, and complement factors.3 By inhibiting interleukin-2 formation, glucocorticoids also prevent T cell proliferation and activation.22 They also impair monocytes and B cells.3,22 Glucocorticoids were the first antirejection drug created, but as time has passed, there has been a movement to phase them out due to their serious side effects.3,22 There is consensus that glucocorticoids are highly detrimental to wound healing since they interfere with many key stages of wound healing such as collagen deposition and synthesis, angiogenesis, fibroblast proliferation, growth factors, and phagocytosis among others.2,3,44,45
Practical considerations for health care providers
Persons with compromised immune systems (due to medications, co-morbidities or age extremes) require additional considerations for chronic wound management. Specific to immunosuppressive medications, health care providers should take a careful history not only of the medications and dosing (including changes in dosing), but also of the underlying conditions requiring these medications (e.g. autoimmune disorders, organ transplantation). As many immunosuppressive medications can impair wound healing, it is crucial for health care providers to assess healing potential early on to set and manage patient expectations. Early referral to medical or surgical specialists to assist with wound care and a team-based approach will be essential given the increased complexity of these individuals. In some cases where wounds are not healing, alternate goals of care for the wound may need to be set (e.g. maintenance or non-healable) if immunosuppressive doses cannot be reduced (assuming it is contributing to poor healing) and should be done in consultation with their primary or specialist care providers. As individuals and populations with comorbidities live longer, taking care of persons with chronic wounds on immunosuppressive medications will become increasingly common and must be recognised early by the wound care clinicians.
Discussion
With the ongoing advances in medicine, the need for immunosuppression in the context of transplant, autoimmune disease and malignancy has increased. In our review, we highlight the poverty of robust studies in this field and highlighted the mixed effects of various immunosuppression on wound healing. High quality evidence exists with respect to the deleterious effects of glucocorticoid therapy as well as mTOR therapy, particularly sirolimus on wound healing. Furthermore, when 4 studies compared sirolimus to either MMF or systemic tacrolimus, all the studies demonstrated sirolimus to be associated with an increased incidence of wound complications.35,36,46,47
The literature on agents such as systemic CNIs is mixed with some suggesting adverse effects on wounds and others suggesting benefit, necessitating additional study focusing directly on this question. Newer topical CNIs have shown little impact on delayed wound healing and in some cases benefit, but additional investigation is warranted for their use in chronic wounds directly. Reassuringly, antiproliferative agents, antimetabolite, and newer monoclonal antibiotics have not shown signal toward diminished healing. However, additional study is needed given the poverty of evidence on wound healing in mAB therapy. Overall, our review found the evidence in this area is dated with variable conclusions surrounding the effects of the immunosuppressant on wound healing. In addition, we found little evidence using human subjects. In general, when immunosuppressives are prescribed after transplants to prevent rejection, patients take more than one drug to effectively prevent rejection. Therefore, challenges exist in performing human studies evaluating the effects of individual drugs in isolation.
As we did not conduct a systematic review, certain articles may have been excluded. We did identify a few key reviews before conducting the search and ensured they were present in the search as one form of validation. As well, given the paucity of literature in this area particularly as it relates to the wound care field, a narrative review adds value to educate and increase awareness when working with individuals on these medications.
With the growing need for immunosuppression, additional study in this field is critical. Future directions include conducting more studies in animal subjects with newer classes of immunosuppressants to identify potential pathways to delayed wound healing and potential ways to mitigate such effects. In addition, more high-quality studies are required to evaluate both individual and combination immunotherapies to better understand the risks and how different immunosuppressants may impact wound healing. In order to explore immunosuppressants as a potential treatment for chronic or complex wounds, it is important for future studies to be conducted on a larger scale, control for confounding clinical factors, such as through randomised control trials.
Conclusions
In conclusion, immunosuppressants range from possibly beneficial to floridly deleterious in wound healing. While there is little conclusive evidence in this field, the effects of immunosuppressants on wound healing is worth exploring to better tailor immunosuppression to patients at risk for or experiencing chronic non-healing wounds. Reassuringly, our findings suggest not all immunosuppressants are harmful with some potentially offering benefit to wound treatment when conventional therapies has failed, opening up the possibility of a new treatment option for wounds.
Acknowledgements
University of Alberta Highschool Youth Researcher Summer Program.
Conflict of Interest
The authors declare no conflicts of interest.
Funding
The authors received no funding for this study.
Examen de la asociación entre inmunosupresores y cicatrización de heridas: una revisión narrativa
Aria Appoo, Brandon L Christensen, Ranjani Somayaji
DOI: 10.33235/wcet.43.4.32-39
Resumen
Objetivo Una revisión de la literatura reciente para proporcionar a los clínicos una comprensión de cómo las diferentes clases de inmunosupresores afectan a la cicatrización de heridas.
Fuentes de datos Se realizó una búsqueda bibliográfica en PubMed, Google Scholar y la Biblioteca de Ciencias de la Salud de la Universidad de Calgary.
Selección de estudios Los estudios elegidos para su inclusión se cribaron inicialmente a partir del título utilizando palabras clave como "medicación inmunosupresora, cicatrización de heridas e inmunosupresión". Si el título y/o el resumen contenían estas palabras clave y abordaban la cicatrización de heridas relacionada con la medicación inmunosupresora y se habían publicado después del 2000, se incluyeron en la revisión. Cuando no se disponía de datos en humanos para un inmunosupresor (clase), se incluyeron estudios en animales.
Extracción de datos Los artículos seleccionados se sometieron a revisión y resumen del texto completo.
Síntesis de los datos Los datos se sintetizaron de forma descriptiva. Los corticosteroides y los inhibidores del blanco faramacodinámico de la rapamicina (mTOR) son los que demuestran de forma más sistemática efectos perjudiciales sobre la cicatrización de heridas. Para otras clases de inmunosupresores, la evidencia es limitada y se han descrito efectos variables sobre la cicatrización de heridas.
Conclusiones Se necesitan estudios más amplios y de mayor calidad para comprender mejor los efectos de los inmunosupresores, especialmente con el desarrollo de nuevas clases de estos fármacos sobre la cicatrización de heridas, con el fin de identificar aquellos con mayor riesgo de perjudicar la cicatrización de heridas.
Introducción
Los inmunosupresores son medicamentos con diversas indicaciones, como los trasplantes de órganos sólidos y hematopoyéticos y las enfermedades autoinmunes. Funcionan suprimiendo la actividad de diversos componentes del sistema inmunitario adaptativo, disminuyendo así la cascada de respuesta inflamatoria al tejido normal del huésped o modulando la respuesta natural de rechazo a los materiales trasplantados.1 Las principales clases de inmunosupresores son los corticosteroides/glucocorticoides,2,3 los inhibidores de la calcineurina,2,4,5 los inhibidores del blanco faramacodinámico de la rapamicina (mTOR),2,4 los anticuerpos policlonales,2,4 los anticuerpos monoclonales,2,4 y los agentes antiproliferativos.2 A efectos de esta revisión, las heridas se definen como una abertura en la piel como consecuencia de una intervención quirúrgica, un traumatismo o una enfermedad susceptible de infección.
El sistema inmunitario desempeña un papel importante en la prevención de infecciones, pero también en el proceso de cicatrización de las heridas, ya que los efectos inflamatorios conducen a la proliferación celular y a la secreción de importantes componentes intra y extracelulares.6 Con los inmunosupresores, el sistema inmunitario se modula, lo que puede afectar al tiempo de cicatrización de una herida y a la susceptibilidad a la infección.7 Con un número creciente de pacientes que reciben medicación inmunosupresora, en particular pacientes posquirúrgicos trasplantados, el efecto de los inmunosupresores sobre la cicatrización de las heridas es una cuestión importante que debe tenerse en cuenta. El objetivo de este artículo de revisión es proporcionar a los médicos un conocimiento de cómo afectan las distintas clases de inmunosupresores a la cicatrización de heridas.
Materiales/metodos
Se realizó una búsqueda bibliográfica entre 2000 y 2021 utilizando los nombres genéricos de una serie de inmunosupresores de uso común (glucocorticoides/corticosteroides, inhibidores de mTOR, metotrexato, anticuerpos monoclonales, anticuerpos policlonales, inhibidores de la calcineurina, micofenolato, azatioprina), así como los términos "cicatrización de heridas" e "inmunosupresión". La principal base de datos consultada fue PubMed. Esto se complementó con Google Scholar y la base de datos de la Biblioteca de Ciencias de la Salud de la Universidad de Calgary. Cuando fue posible, la búsqueda se realizó con el siguiente formato "nombre del inmunosupresor [Términos MeSH]" AND "cicatrización de heridas [Términos MeSH]" Si el nombre del inmunosupresor no estaba disponible como término MeSH, se buscó el término sin aplicar ninguna restricción. A continuación, se examinaron los títulos de los artículos para determinar su pertinencia para la revisión en función de si la cicatrización de heridas se describía en relación con la medicación inmunosupresora/clase. El resumen se examinó de forma similar y se incluyó en la revisión en consecuencia. Si el artículo comparaba varios inmunosupresores, discutía sus efectos sobre la cicatrización de heridas, medía la cicatrización de heridas o los efectos deletéreos sobre las heridas, se consideraba relevante. Si los términos de búsqueda no identificaban estudios con sujetos humanos, se incluían los estudios que utilizaban animales para evaluar los efectos inmunosupresores sobre la cicatrización de heridas. Cuando no se dispuso de datos a partir del 2000, se realizó una búsqueda histórica de los medicamentos inmunosupresores pertinentes.
Todos los estudios incluidos se resumieron de forma descriptiva, incluyendo el mecanismo de acción inmunosupresor, los sujetos de estudio y las pruebas de los efectos sobre la cicatrización de heridas.
Resultados
Los estudios seleccionados pertinentes para esta revisión se utilizaron para establecer las diversas categorías que se describen a continuación. Se examinaron inicialmente 200 títulos y resúmenes de artículos y se incluyeron 61 artículos para su revisión. En la Tabla 1 se resumen los resultados de los estudios clínicos y con animales. Las indicaciones específicas de los distintos inmunosupresores, incluidos sus posibles efectos sobre las heridas, se describen en la Tabla 2.
Tabla 1. Estudios que comparan los efectos de distintos inmunosupresores en las heridas
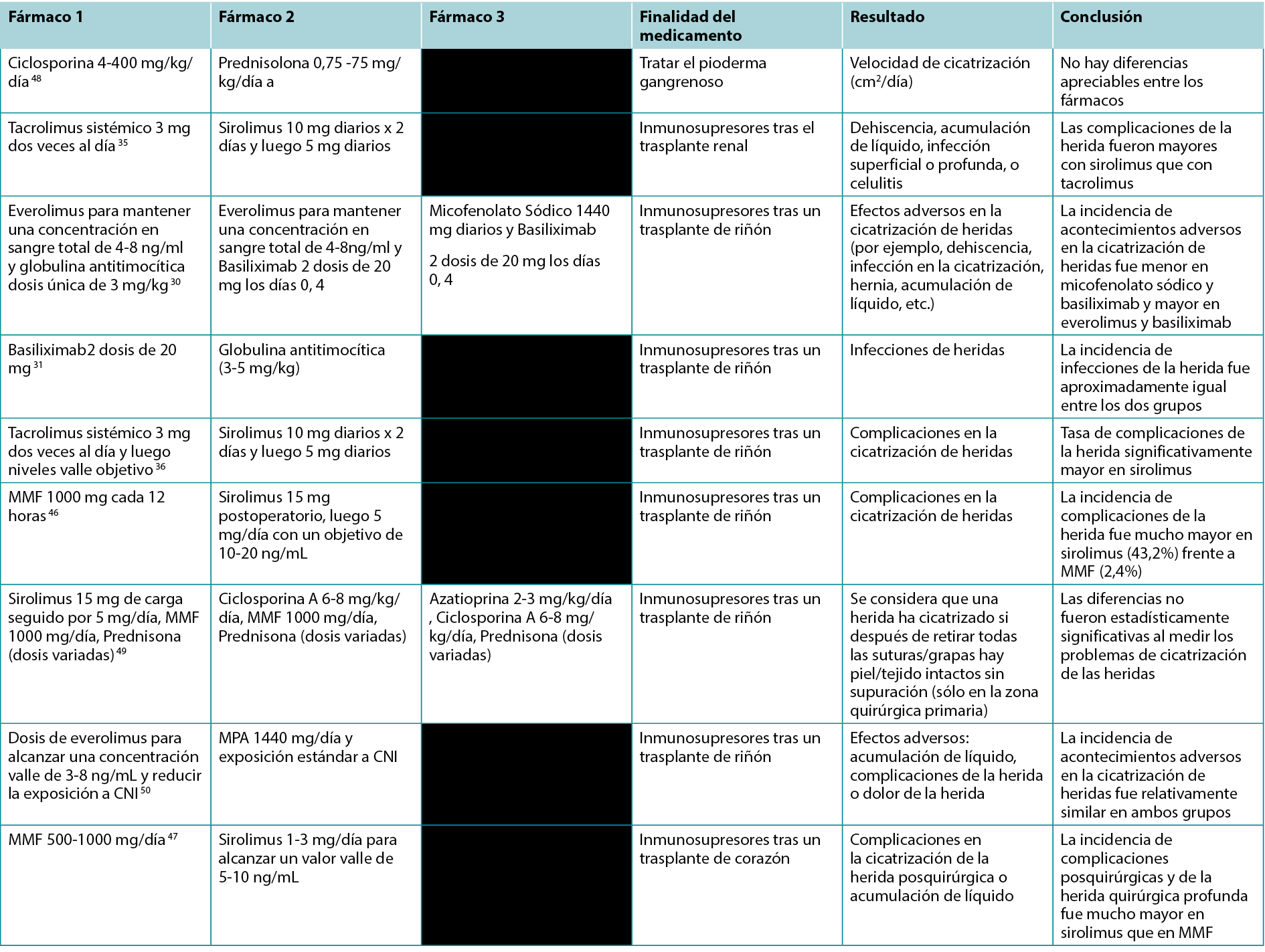
Tabla 2. Visión general de las indicaciones y los efectos sobre las heridas de diversos inmunosupresores
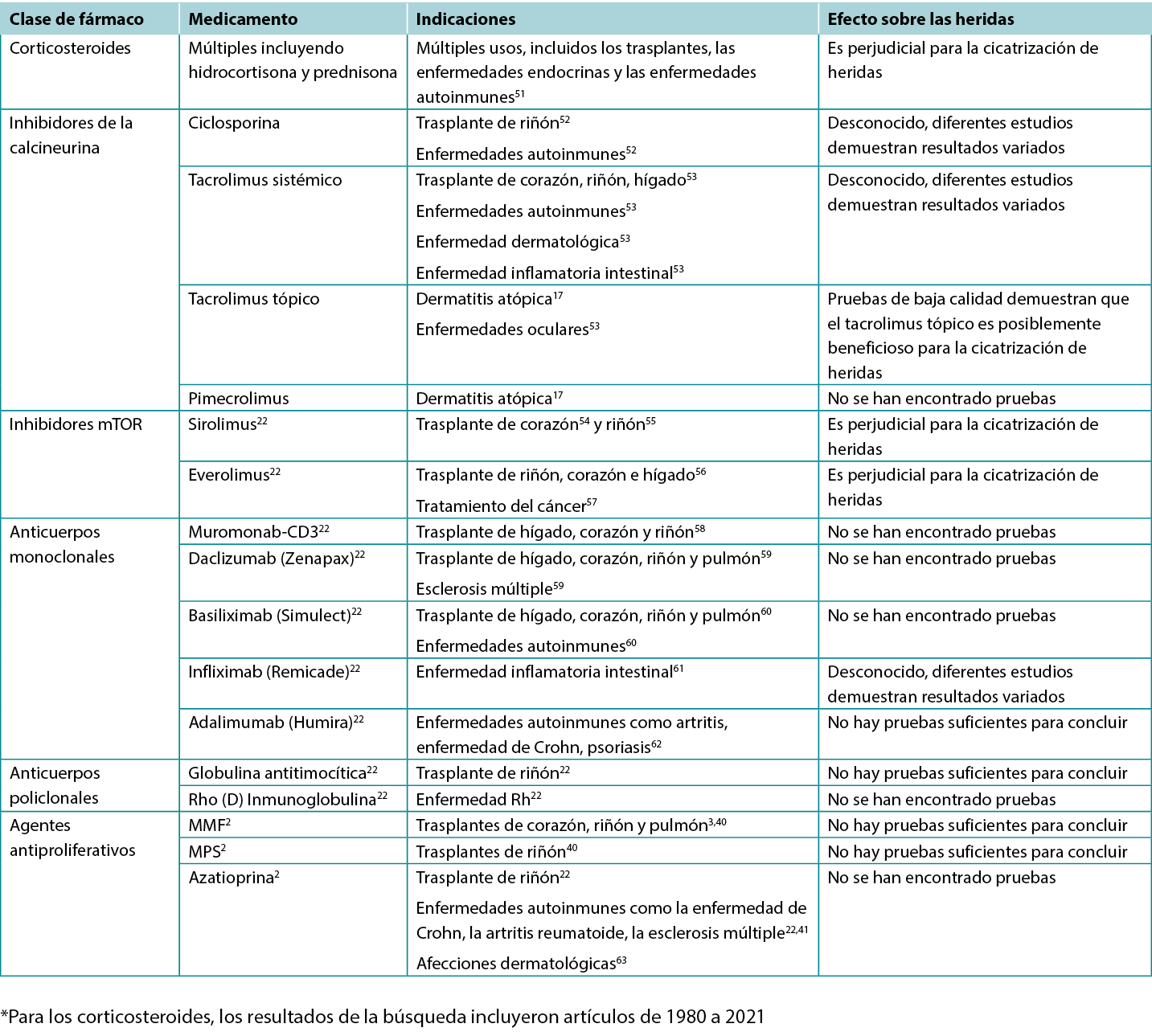
Inhibidores de la calcineurina
Los inhibidores de la calcineurina (CNI) se utilizan como inmunosupresores en diversas enfermedades autoinmunes, trasplantes de órganos, afecciones dermatológicas y heridas crónicas8 Existen tres tipos principales de CNI: ciclosporina (sistémico), tacrolimus (sistémico y tópico) y pimecrolimus (tópico).9 Los CNI actúan uniéndose a una parte de la molécula de calcineurina que se encuentra en las células humanas, deteniendo así la liberación de determinadas citoquinas responsables de la activación de las células T.8 Por lo tanto, los CNI desactivan una de las principales ramas de la respuesta inmunitaria adaptativa del organismo.
Sistémico
Faltan estudios centrados directamente en los efectos de los CNI sobre la cicatrización de heridas en humanos; sin embargo, se han realizado muchos estudios de ciencia básica en animales. Dos de estos estudios con ratas compararon el efecto de varias dosis de tacrolimus sistémico frente a un control, comprobando la resistencia a la rotura de las heridas creadas mediante cirugía. Uno de los estudios con ratas concluyó que el tacrolimus no afecta a la cicatrización de las heridas10, mientras que el otro estudio concluyó que el tacrolimus es perjudicial para la cicatrización de las heridas.11 Al mismo tiempo, los informes de casos en los que se utilizó tacrolimus sistémico como tratamiento de las úlceras en una persona con liquen plano y pioderma gangrenoso demostraron el éxito del tratamiento con esta terapia.12
No se han encontrado estudios recientes en humanos sobre el efecto de la ciclosporina y la cicatrización de heridas. Otros dos estudios realizados con ratas también arrojaron resultados contradictorios. Estos estudios con ratas se centraron en los efectos de la ciclosporina sobre diferentes marcadores del organismo que significan una cicatrización eficaz de las heridas. Un estudio que comparaba la ciclosporina con la metilprednisona demostró que la ciclosporina no tenía ningún efecto supresor sobre los diversos marcadores inflamatorios y bioquímicos en comparación con el tratamiento con glucocorticoides13, mientras que el otro estudio demostró que la ciclosporina tenía un efecto negativo sobre los marcadores.14 En un estudio diferente, tras recibir un trasplante de pulmón, se asignó a los perros un fármaco inmunosupresor específico o ningún fármaco inmunosupresor y, de forma similar al control, se demostró que la ciclosporina A no tenía un efecto significativo sobre la cicatrización de la herida quirúrgica medida por la resistencia a la rotura en comparación con la inmunosupresión con glucocorticoides y azatioprina.15 En general, la bibliografía sobre los inhibidores sistémicos de la calcineurina y la cicatrización de heridas es anticuada, con una heterogeneidad de comparadores y resultados dispares sobre la cicatrización de heridas.
Tópico
Los inhibidores de la calcineurina (tacrolimus y pimecrolimus) se utilizan como pomadas tópicas sobre todo para afecciones dermatológicas como la dermatitis atópica, pero también para afecciones dermatológicas crónicas como el pioderma gangrenoso16-18 Algunos estudios de casos han demostrado que el tacrolimus es eficaz para curar úlceras complejas de las piernas en el contexto de la insuficiencia venosa o la necrobiosis lipoídica, cuando las estrategias de tratamiento habituales han sido ineficaces.19,20 Además, un estudio realizado en ratas con lesiones cutáneas agudas demostró que las heridas tratadas con tacrolimus tópico cicatrizaban igual de rápido que el control (vaselina).21
Anticuerpos monoclonales:
Existen diversos tratamientos con anticuerpos monoclonales (mAb) indicados en trasplantes y trastornos autoinmunitarios como la artritis reumatoide y la psoriasis. 22 En general, los mAb actúan uniéndose a distintos receptores y antígenos para inhibir el efecto de las citocinas y otras vías de señalización que activan el sistema inmunitario.22 Un pequeño estudio prospectivo de cohortes entre pacientes con artritis reumatoide sometidos a cirugía ortopédica demostró que no había un mayor riesgo de infecciones de la herida quirúrgica ni de complicaciones de la cicatrización en los pacientes que recibían infliximab en comparación con el tratamiento convencional.23 Además, un caso clínico afirma que el infliximab tópico fue útil para cicatrizar úlceras de la pierna resistentes al tratamiento estándar, lo que sugiere que la inhibición del factor de necrosis tumoral alfa es útil para la cicatrización de heridas.24 Se llegó a conclusiones similares en un caso clínico de tratamiento del pioderma gangrenoso con infliximab, que produjo una mejoría de la úlcera.25 Se demostró que la inhibición del factor de necrosis tumoral alfa estaba asociada a la cicatrización de heridas en úlceras venosas de la pierna mediante el uso de adalimumab por vía sistémica.26 Sin embargo, en otro estudio se utilizó infliximab en heridas abdominales de ratas y se demostró que la resistencia a la tracción era significativamente inferior en las heridas de las ratas a las que se había administrado infliximab en comparación con las de control.27 En general, la escasa bibliografía sobre el tema hasta la fecha sugiere que los resultados clínicos hasta el momento son favorables en cuanto a la cicatrización de las heridas.
Anticuerpos policlonales
Los anticuerpos policlonales (pAb) son muy similares a los mAb en cuanto a su función, con un mecanismo de acción ligeramente distinto.28,29 A diferencia de los mAb, un grupo de anticuerpos policlonales se crea a partir de muchas líneas diferentes de células B y, dentro del grupo, diferentes pAb se unen a diferentes epítopos de un antígeno. Por el contrario, los mAb proceden de una única línea de células B y sólo pueden unirse a un antígeno.28,29 Existen dos pAb principales: La globulina antitimocítica y la inmunoglobulina Rho (D).22 La globulina antitimocítica, también conocida como globulina antitimocítica humana, se utiliza con mayor frecuencia como inmunosupresor tras el trasplante de riñón y actúa uniéndose a diversos linfocitos y reduciendo el número de linfocitos T del organismo.22 La inmunoglobulina Rho (D) se utiliza en embarazos en los que la madre es Rh- y el feto Rh+ y, básicamente, detiene la formación de anticuerpos anti Rh+ en la madre.22
Se han encontrado pocos estudios que analicen los efectos de los pAb en la cicatrización de heridas. Dos estudios esbozaron los efectos de la globulina antitimocítica y el basiliximab. El primer estudio en pacientes con trasplante renal, en el que se combinaron ambos fármacos con everolimus, mostró tasas más elevadas de efectos adversos en la cicatrización de heridas en Basiliximab. 30 El segundo estudio demostró que la incidencia de infecciones de heridas era igual en pacientes que tomaban basiliximab frente a globulina antitimocítica tras un trasplante renal.31 Dado que los glóbulos blancos desempeñan un papel clave en la cicatrización de heridas mediante la secreción de las citocinas necesarias y la prevención de infecciones,32 sería razonable plantear la hipótesis de que la globulina antitimocítica afectará a la cicatrización de heridas, ya que reduce el número de glóbulos blancos, así como sus mecanismos reguladores.
Inhibidores mTOR
Los inhibidores del blanco faramacodinámico de la rapamicina (mTOR) son fármacos inmunosupresores que actúan interactuando con proteínas en vías de señalización complejas para impedir que las células pasen a la fase S del ciclo celular y, por tanto, suprimiendo la proliferación.3,22 La mTOR se dirige predominantemente a las células T, pero también puede afectar a las células B.3 Curiosamente, la mTOR puede provocar un aumento de la producción de ciertas citocinas inflamatorias, como la interleucina-6, y disminuir la producción de interleucina-10, una citocina antiinflamatoria.3 Existen dos inhibidores principales de mTOR: sirolimus y everolimus.3,22 En general, los inhibidores de mTOR tienen diversas aplicaciones, incluida la terapia contra el cáncer.3,22 Como inmunosupresor, se utilizan después de los trasplantes.3,22 Se ha demostrado que everolimus inhibe la proliferación de fibroblastos enmodelos in vitro33, lo que sugiere que everolimus podría tener consecuencias negativas para la cicatrización de heridas, ya que los fibroblastos son esenciales para crear una matriz extracelular y crear un marco para otras células.34 En un estudio en el que se comparaban el sirolimus y el tacrolimus sistémico, el sirolimus presentaba una tasa de complicaciones de la herida del 47%, mientras que el tacrolimus sólo alcanzaba el 8%.35 Esto concuerda con otro estudio de Larson et al en el que se demostraron mayores complicaciones de la herida con sirolimus que con tacrolimus.36 Curiosamente, los pacientes obesos que recibían sirolimus presentaban tasas muy elevadas de complicaciones de la herida, por lo que el estudio excluyó a todos los pacientes obesos.36 En consonancia con hallazgos anteriores, un estudio en ratas demostró que el aumento de las dosis de sirolimus disminuye la resistencia de la herida, y los autores plantean la hipótesis de que este efecto puede deberse a niveles más bajos de VEGF y óxido nítrico en ratas que reciben dosis más altas de sirolimus.37 En una revisión, los autores llegaron a la conclusión de que los inhibidores de mTOR son perjudiciales para la cicatrización de heridas en dosis altas, pero parecen tener un efecto neutro en dosis bajas.38 Dadas las preocupaciones iniciales sobre los inhibidores de mTOR y la cicatrización de heridas, los regímenes que utilizan estos agentes inmunosupresores han evolucionado con dosis más bajas de inhibidores de mTOR y terapia combinada. En el amplio ensayo de control aleatorizado TRANSFORM, los investigadores compararon everolimus más dosis reducida de CNI con ácido micofenólico más dosis estándar de CNI (tratamiento estándar) en pacientes con trasplante renal y demostraron que los acontecimientos adversos relacionados con las heridas no eran estadísticamente diferentes (20,6% frente a 17,3%; RR 1,19; CI del 95%: 0,99 a 1,43).39 Una limitación de este estudio fue la estrecha monitorización de las concentraciones de everolimus y las dificultades para alcanzar las concentraciones plasmáticas objetivo C0 entre 3 y 8 ng/mL.39 En general, la revisión de la bibliografía actual sugiere que los inhibidores de mTOR tienen un efecto perjudicial sobre la cicatrización de heridas, especialmente a dosis más altas, y que la mejora de los regímenes de dosificación puede disminuir o mitigar este riesgo.
Agentes antiproliferativos
Existen tres agentes antiproliferativos utilizados regularmente: Micofenolato mofetilo (MMF) y Micofenolato sódico (MPS) (ambos inhibidores de la inosina monofosfato deshidrogenasa (IMPDH)) y azatioprina.2,40 Los inhibidores de la IMPDH tienen un efecto similar a los inhibidores de mTOR en cuanto a su mecanismo de inmunosupresión. En el organismo, el MMF y el MPS se convierten en ácido micofenólico, que bloquea una parte de una vía crucial para la síntesis del ADN, con el fin de disminuir la proliferación de linfocitos T y células B.2,5,40 El MMF se utiliza por su efecto inmunosupresor en los trasplantes de corazón, riñón y pulmón.3,40 El MPS se utiliza en los trasplantes de riñón.40 La azatioprina se utiliza como fármaco inmunosupresor en los trasplantes de riñón y las enfermedades autoinmunes, como la artritis reumatoide, la enfermedad de Crohn y la esclerosis múltiple.22,41 En el organismo, la azatioprina reacciona con el glutatión y se convierte en 6-mercaptupurina, tras lo cual se generan metabolitos adicionales que, en última instancia, bloquean la síntesis de purinas y la estimulación de las células T.3,22
Cuando un estudio comparó dos dosis diferentes de MMF en receptores de trasplante de riñón, la incidencia de heridas que requirieron intervención quirúrgica no fue significativamente diferente, de forma similar para las heridas tratadas con cuidados locales.42 Basándonos en la revisión de los títulos de los artículos como parte de nuestra búsqueda, no se encontraron estudios relativos al efecto único de la azatioprina sobre la cicatrización de heridas externas en humanos. Cuando se comparó la azatioprina con un placebo en un estudio con ratas, las heridas de las ratas que tomaban azatioprina tardaron más en cicatrizar que las que tomaban el placebo, lo que sugiere que la azatioprina puede tener efectos perjudiciales sobre la cicatrización de las heridas, pero no está claro hasta qué punto afectaría a los seres humanos.43
Antimetabolitos
El metotrexato es un agente inmunosupresor antagonista del folato de uso común, con indicaciones en muchos trastornos reumatológicos. También tiene actividad antineoplásica en dosis más elevadas. Tras su absorción, entra en la célula y se convierte en poliglutamatos de metotrexato, donde compite por la dihidrofolato reductasa, impidiendo así la transformación del ácido fólico para su uso en la construcción de ácidos nucleicos.6 Al igual que otros agentes descritos, existen estudios experimentales en animales con estudios in vitro que sugieren una alteración en la cicatrización de heridas, pero estos efectos no se han confirmado en estudios clínicos, especialmente en heridas posquirúrgicas.6 Por lo tanto, se recomienda continuar con este fármaco en el postoperatorio.
Corticosteroides/Glucocorticoides
Los glucocorticoides impiden la formación de sustancias químicas inflamatorias como las citocinas, las moléculas de adhesión celular y los factores del complemento.3 Al inhibir la formación de interleucina-2, los glucocorticoides también impiden la proliferación y activación de las células T.22 También perjudican a los monocitos y las células B.3,22 Los glucocorticoides fueron los primeros fármacos antirrechazo que se crearon, pero con el paso del tiempo se ha producido un movimiento para eliminarlos gradualmente debido a sus graves efectos secundarios.3,22 Existe consenso en que los glucocorticoides son muy perjudiciales para la cicatrización de heridas, ya que interfieren en muchas fases clave de la cicatrización de heridas, como la deposición y síntesis de colágeno, la angiogénesis, la proliferación de fibroblastos, los factores de crecimiento y la fagocitosis, entre otras.2,3,44,45
Consideraciones prácticas para los profesionales sanitarios
Las personas con sistemas inmunitarios comprometidos (debido a medicamentos, comorbilidades o edad extrema) requieren consideraciones adicionales para el tratamiento de las heridas crónicas. Por lo que respecta específicamente a los medicamentos inmunosupresores, los profesionales sanitarios deben elaborar un historial minucioso no sólo de los medicamentos y la dosificación (incluidos los cambios de dosificación), sino también de las afecciones subyacentes que requieren estos medicamentos (por ejemplo, trastornos autoinmunitarios, trasplante de órganos). Dado que muchos medicamentos inmunosupresores pueden perjudicar la cicatrización de las heridas, es fundamental que los profesionales sanitarios evalúen el potencial de cicatrización desde el principio para establecer y gestionar las expectativas de los pacientes. La derivación precoz a especialistas médicos o quirúrgicos para ayudar con el cuidado de las heridas y un enfoque basado en el equipo serán esenciales dada la mayor complejidad de estas personas. En algunos casos en los que las heridas no cicatrizan, puede ser necesario establecer objetivos alternativos para el cuidado de la herida (por ejemplo, mantenimiento o no cicatrizable) si no se pueden reducir las dosis de inmunosupresores (suponiendo que esté contribuyendo a una mala cicatrización) y debe hacerse en consulta con sus profesionales de atención primaria o especializada. A medida que las personas y poblaciones con comorbilidades vivan más tiempo, el cuidado de personas con heridas crónicas bajo medicación inmunosupresora será cada vez más frecuente y debe ser reconocido precozmente por los clínicos encargados del cuidado de heridas.
Discusion
Con los continuos avances de la medicina, ha aumentado la necesidad de inmunosupresión en el contexto de los trasplantes, las enfermedades autoinmunes y los tumores malignos. En nuestra revisión, destacamos la pobreza de estudios sólidos en este campo y resaltamos los efectos mixtos de diversas inmunosupresiones sobre la cicatrización de heridas. Existen pruebas de alta calidad con respecto a los efectos nocivos del tratamiento con glucocorticoides, así como del tratamiento con mTOR, en particular sirolimus, sobre la cicatrización de heridas. Además, cuando 4 estudios compararon sirolimus con MMF o tacrolimus sistémico, todos los estudios demostraron que sirolimus se asociaba con una mayor incidencia de complicaciones de la herida.35,36,46,47
La bibliografía sobre agentes como los CNI sistémicos es contradictoria, ya que algunos sugieren efectos adversos sobre las heridas y otros sugieren beneficios, por lo que es necesario realizar estudios adicionales centrados directamente en esta cuestión. Los CNI tópicos más recientes han mostrado escasa repercusión en la cicatrización retardada de las heridas y, en algunos casos, beneficios, pero se justifica una investigación adicional para su uso directo en heridas crónicas. Resulta tranquilizador que los agentes antiproliferativos, los antimetabolitos y los antibióticos monoclonales más recientes no hayan mostrado señales de disminución de la cicatrización. Sin embargo, se necesitan estudios adicionales dada la escasez de pruebas sobre la cicatrización de heridas en la terapia con mAB. En general, nuestra revisión halló que las pruebas en esta área son anticuadas, con conclusiones variables en torno a los efectos del inmunosupresor sobre la cicatrización de heridas. Además, encontramos pocas pruebas en seres humanos. En general, cuando se prescriben inmunosupresores tras un trasplante para prevenir el rechazo, los pacientes toman más de un fármaco para prevenirlo eficazmente. Por lo tanto, la realización de estudios en humanos que evalúen los efectos de fármacos individuales de forma aislada plantea dificultades.
Al no haber realizado una revisión sistemática, es posible que se hayan excluido algunos artículos. Identificamos algunas revisiones clave antes de realizar la búsqueda y nos aseguramos de que estuvieran presentes en la búsqueda como una forma de validación. Además, dada la escasez de bibliografía en este ámbito, especialmente en lo que se refiere al cuidado de heridas, una revisión narrativa añade valor para educar y aumentar la concienciación cuando se trabaja con personas que toman estos medicamentos.
Con la creciente necesidad de inmunosupresión, es fundamental realizar más estudios en este campo. En el futuro habrá que realizar más estudios en animales con nuevas clases de inmunosupresores para identificar posibles vías de retraso en la cicatrización de las heridas y posibles formas de mitigar esos efectos. Además, se necesitan más estudios de alta calidad para evaluar tanto las inmunoterapias individuales como las combinadas, a fin de comprender mejor los riesgos y el modo en que los distintos inmunosupresores pueden influir en la cicatrización de las heridas. Para explorar los inmunosupresores como tratamiento potencial de las heridas crónicas o complejas, es importante que los futuros estudios se realicen a mayor escala y controlen los factores clínicos de confusión, por ejemplo mediante ensayos controlados aleatorizados.
Conclusiones
En conclusión, los inmunosupresores varían de posiblemente beneficiosos a realmente nocivos en la cicatrización de heridas. Aunque hay pocas pruebas concluyentes en este campo, merece la pena explorar los efectos de los inmunosupresores en la cicatrización de heridas para adaptar mejor la inmunosupresión a los pacientes con riesgo de sufrir heridas crónicas que no cicatrizan o que las padecen. Como dato tranquilizador, nuestros hallazgos sugieren que no todos los inmunosupresores son perjudiciales y que algunos pueden ser beneficiosos para el tratamiento de heridas cuando las terapias convencionales han fracasado, lo que abre la posibilidad de una nueva opción terapéutica para las heridas.
Agradecimientos
Programa de verano para jóvenes investigadores de la Universidad de Alberta.
Conflicto de intereses
Los autores declaran no tener conflictos de intereses.
Financiación
Los autores no recibieron financiación por este estudio.
Author(s)
Aria Appoo
Medical Student, University of Oxford, Oxford, UK
Brandon L Christensen
BMSc MD
Resident Physician, University of Calgary, Division of Infectious Diseases, Calgary, Alberta, Canada
Ranjani Somayaji
BScPT MD MPH
Assistant Professor, University of Calgary, Departments of Medicine, Microbiology, Immunology and Infectious Disease and Community Health Sciences, Calgary, Alberta, Canada
References
- Fireman M, DiMartini AF, Armstrong SC, Cozza KL. Immunosuppressants. Psychosomatics. 2004;45(4). doi:10.1176/appi.psy.45.4.354
- Taylor AL, Watson CJE, Bradley JA. Immunosuppressive agents in solid organ transplantation: Mechanisms of action and therapeutic efficacy. Crit Rev Oncol Hematol. 2005;56(1). doi:10.1016/j.critrevonc.2005.03.012
- Weltz A, Scalea J, Popescu M, Xu J, Bromberg JS. Mechanisms of Immunosuppressive Drugs. In: Kidney Transplantation. Springer New York; 2014. doi:10.1007/978-1-4939-0342-9_12
- Subramanian S, Trence DL. Immunosuppressive Agents: Effects on Glucose and Lipid Metabolism. Endocrinol Metab Clin North Am. 2007;36(4). doi:10.1016/j.ecl.2007.07.003
- Mika A, Stepnowski P. Current methods of the analysis of immunosuppressive agents in clinical materials: A review. J Pharm Biomed Anal. 2016;127. doi:10.1016/j.jpba.2016.01.059
- Pountos I, Giannoudis P V. Effect of methotrexate on bone and wound healing. Expert Opin Drug Saf. 2017;16(5):535-545. doi:10.1080/14740338.2017.1310839
- Willems MCM, van der Vliet JA, Lomme RMLM, Hendriks T. Tacrolimus Does Not Affect Early Wound Healing in a Rodent Model of Bowel Anastomoses and Abdominal Wall Closure. PLoS One. 2013;8(9). doi:10.1371/journal.pone.0076348
- Azzi JR, Sayegh MH, Mallat SG. Calcineurin Inhibitors: 40 Years Later, Can’t Live Without …. The Journal of Immunology. 2013;191(12). doi:10.4049/jimmunol.1390055
- Safarani OA, Patel J. Calcineurin Inhibitors. StatPearls Publishing; 2021.
- Willems MCM, van der Vliet JA, Lomme RMLM, Hendriks T. Tacrolimus Does Not Affect Early Wound Healing in a Rodent Model of Bowel Anastomoses and Abdominal Wall Closure. PLoS One. 2013;8(9). doi:10.1371/journal.pone.0076348
- Schäffer MR, Fuchs N, Proksch B, Bongartz M, Beiter T, Becker HD. TACROLIMUS IMPAIRS WOUND HEALING. Transplantation. 1998;65(6). doi:10.1097/00007890-199803270-00008
- The Effect of Tacrolimus on Lower Extremity Ulcers: A Case Study and Review of the Literature. Wound Manag Prev. 2008;54(4).
- Nemlander A, Ahonen J, Wiktorowicz K, et al. Effect of Cyclosporine on Wound Healing An Analysis With Viscous Cellulose Sponges. Transplantation. 1983;36(1):1-5.
- Petri J, Schurk S, Gebauer S, Haustein U. Cyclosporine A delays wound healing and apoptosis and suppresses activin beta-A expression in rats. European Journal of Dermatology. 1998;8(2):104-113.
- Goldberg M, Lima O, Morgan E, et al. A comparison between cyclosporin A and methylprednisolone plus azathioprine on bronchial healing following canine lung autotransplantation. J Thorac Cardiovasc Surg. 1983;85(6). doi:10.1016/S0022-5223(19)37469-0
- Sussman G. The use of topical calcineurin inhibitors in chronic wound management. Wound Practice & Research: Journal of the Australian Wound Management Association. 2000;26(3):140-145.
- Frazier W, Bhardwaj N. Atopic Dermatitis: Diagnosis and Treatment. Am Fam Physician. 2020;101(10):590-598.
- Lyon C, Stapleton M, Smith A, Mendelsohn S, Beck M, Griffiths C. Topical tacrolimus in the management of peristomal pyoderma gangrenosum. Journal of Dermatological Treatment. 2001;12(1). doi:10.1080/095466301750163518
- Ginocchio L, Draghi L, Darvishian F, Ross FL. Refractory Ulcerated Necrobiosis Lipoidica: Closure of a Difficult Wound with Topical Tacrolimus. Adv Skin Wound Care. 2017;30(10). doi:10.1097/01.ASW.0000521867.98577.a5
- Mackelfresh J, Soon S, Arbiser JL. Combination Therapy of Doxycycline and Topical Tacrolimus for Venous Ulcers. JAMA Dermatol. 2005;141(11). doi:10.1001/archderm.141.11.1476
- Namkoong S, Chung J, Yoo J, et al. Topical tacrolimus does not negatively impact acute skin wound healing. Exp Dermatol. 2013;22(5). doi:10.1111/exd.12131
- Khan MM. Immunopharmacology. Springer US; 2008. doi:10.1007/978-0-387-77976-8
- Bibbo C, Goldberg JW. Infectious and Healing Complications after Elective Orthopaedic Foot and Ankle Surgery during Tumor Necrosis Factor-Alpha Inhibition Therapy. Foot Ankle Int. 2004;25(5). doi:10.1177/107110070402500510
- Streit M, Beleznay Z, Braathen LR. Topical application of the tumour necrosis factor-alpha antibody infliximab improves healing of chronic wounds. Int Wound J. 2006;3(3). doi:10.1111/j.1742-481X.2006.00233.x
- Hewitt D, Tait C. Use of infliximab in pyoderma gangrenosum. Australasian Journal of Dermatology. 2007;48(2). doi:10.1111/j.1440-0960.2007.00344.x
- Fox JD, Baquerizo-Nole KL, Keegan BR, et al. Adalimumab treatment leads to reduction of tissue tumor necrosis factor-alpha correlated with venous leg ulcer improvement: a pilot study. Int Wound J. 2016;13(5). doi:10.1111/iwj.12497
- Lopes JV, Freitas LAM de, Marques RD, Bocca AL, Sousa JB de, Oliveira PG de. Analysis of the tensile strength on the healing of the abdominal wall of rats treated with infliximab. Acta Cir Bras. 2008;23(5). doi:10.1590/S0102-86502008000500009
- Larrañaga MD, Lewis S, Richard J, Robert A, eds. Polyclonal Antibodies. In: Hawley’s Condensed Chemical Dictionary. 16th ed. Wiley; 2016.
- Johnson M. Monoclonal Antibodies. In: Longe JL, ed. Gale Encyclopedia of Nursing and Allied Health. 4th ed. Credo Reference; 2018.
- Ueno P, Felipe C, Ferreira A, et al. Wound Healing Complications in Kidney Transplant Recipients Receiving Everolimus. Transplantation. 2017;101(4). doi:10.1097/TP.0000000000001392
- Patel S, Pankewycz O, Kohli R, et al. Obesity in Renal Transplantation: The Role of Induction Therapy on Long-Term Outcomes. Transplant Proc. 2011;43(2). doi:10.1016/j.transproceed.2011.01.040
- Kordestani SS. Atlas of Wound Healing. (Abyaneh S, Fayyazbakhsh, eds.). Elsevier; 2019.
- Azzola A, Havryk A, Chhajed P, et al. Everolimus and mycophenolate mofetil are potent inhibitors of fibroblast proliferation after lung transplantation1. Transplantation. 2004;77(2). doi:10.1097/01.TP.0000101822.50960.AB
- P. B. Wound healing and the role of fibroblasts. J Wound Care. 2013;22(8). doi:10.12968/jowc.2013.22.8.407
- Dean PG, Lund WJ, Larson TS, et al. Wound-Healing Complications After Kidney Transplantation: A Prospective, Randomized Comparison Of Sirolimus And Tacrolimus1. Transplantation. 2004;77(10). doi:10.1097/01.TP.0000123082.31092.53
- Larson TS, Dean PG, Stegall MD, et al. Complete Avoidance of Calcineurin Inhibitors in Renal Transplantation: A Randomized Trial Comparing Sirolimus and Tacrolimus. American Journal of Transplantation. 2006;6(3). doi:10.1111/j.1600-6143.2005.01177.x
- Schäffer M, Schier R, Napirei M, Michalski S, Traska T, Viebahn R. Sirolimus impairs wound healing. Langenbecks Arch Surg. 2007;392(3). doi:10.1007/s00423-007-0174-5
- Nashan B, Citterio F. Wound Healing Complications and the Use of Mammalian Target of Rapamycin Inhibitors in Kidney Transplantation. Transplantation. 2012;94(6). doi:10.1097/TP.0b013e3182551021
- Citterio F, Henry M, Kim DY, et al. Wound healing adverse events in kidney transplant recipients receiving everolimus with reduced calcineurin inhibitor exposure or current standard-of-care: Insights from the 24 month TRANSFORM study. Expert Opin Drug Saf. Published online 2020:1339-1348. doi:10.1080/14740338.2020.1792441
- Staatz CE, Tett SE. Clinical Pharmacokinetics and Pharmacodynamics of Mycophenolate in Solid Organ Transplant Recipients. Clin Pharmacokinet. 2007;46(1). doi:10.2165/00003088-200746010-00002
- Casetta I, Iuliano G, Filippini G. Azathioprine for multiple sclerosis. Cochrane Database of Systematic Reviews. Published online October 17, 2007. doi:10.1002/14651858.CD003982.pub2
- Flechner SM, Feng J, Mastroianni B, et al. The Effect of 2-Gram Versus 1-Gram Concentration Controlled Mycophenolate Mofetil on Renal Transplant Outcomes Using Sirolimus-Based Calcineurin Inhibitor Drug-Free Immunosuppression. Transplantation. 2005;79(8). doi:10.1097/01.TP.0000155430.52845.51
- Ginestal R, Pérez-Köhler B, Pérez-López P, et al. Comparing the influence of two immunosuppressants (fingolimod, azathioprine) on wound healing in a rat model of primary and secondary intention wound closure. Wound Repair and Regeneration. 2019;27(1). doi:10.1111/wrr.12685
- Wicke C. Effects of Steroids and Retinoids on Wound Healing. Archives of Surgery. 2000;135(11). doi:10.1001/archsurg.135.11.1265
- Anstead G. Steroids, retinoids, and wound healing. Adv Wound Care (New Rochelle). 1998;11(6):277-285.
- Valente JF, Hricik D, Weigel K, et al. Comparison of Sirolimus vs. Mycophenolate Mofetil on Surgical Complications and Wound Healing in Adult Kidney Transplantation. American Journal of Transplantation. 2003;3(9). doi:10.1034/j.1600-6143.2003.00185.x
- Kuppahally S, Al-Khaldi A, Weisshaar D, et al. Wound Healing Complications with De Novo Sirolimus Versus Mycophenolate Mofetil-Based Regimen in Cardiac Transplant Recipients. American Journal of Transplantation. 2006;6(5p1). doi:10.1111/j.1600-6143.2006.01282.x
- Ormerod AD, Thomas KS, Craig FE, et al. Comparison of the two most commonly used treatments for pyoderma gangrenosum: results of the STOP GAP randomised controlled trial. BMJ. 2015;350(jun12 3). doi:10.1136/bmj.h2958
- Flechner SM, Zhou L, Derweesh I, et al. The impact of sirolimus, mycophenolate mofetil, cyclosporine, azathioprine, and steroids on wound healing in 513 kidney-transplant recipients. Transplantation. 2003;76(12). doi:10.1097/01.TP.0000093502.26208.42
- Citterio F, Henry M, Kim DY, et al. Wound healing adverse events in kidney transplant recipients receiving everolimus with reduced calcineurin inhibitor exposure or current standard-of-care: insights from the 24-month TRANSFORM study. Expert Opin Drug Saf. 2020;19(10). doi:10.1080/14740338.2020.1792441
- Kapugi M, Cunningham K. Corticosteroids. Orthopaedic Nursing. 2019;38(5):336-339. doi:10.1097/NOR.0000000000000595
- Ponticelli C. Cyclosporine: From Renal Transplantation to Autoimmune Diseases. Ann N Y Acad Sci. 2005;1051(1):551-558. doi:10.1196/annals.1361.099
- Akar Y, Yucel G, Durukan AH, Yucel I, Arici G. Laboratory Science. Systemic toxicity of tacrolimus given by various routes and the response to dose reduction. Clin Exp Ophthalmol. 2005;33(1):53-59. doi:10.1111/j.1442-9071.2005.00942.x
- Kurian K, Addisu A. Sirolimus: A Novel Immunosuppressive Drug in Heart Transplantation. Recent Pat Cardiovasc Drug Discov. 2009;4(3):187-191. doi:10.2174/157489009789152294
- Sehgal SN. Sirolimus: its discovery, biological properties, and mechanism of action. Transplant Proc. 2003;35(3):S7-S14. doi:10.1016/S0041-1345(03)00211-2
- van Gelder T, Fischer L, Shihab F, Shipkova M. Optimizing everolimus exposure when combined with calcineurin inhibitors in solid organ transplantation. Transplant Rev. 2017;31(3):151-157. doi:10.1016/j.trre.2017.02.007
- Falkowski S, Woillard JB. Therapeutic Drug Monitoring of Everolimus in Oncology: Evidences and Perspectives. Ther Drug Monit. 2019;41(5):568-574. doi:10.1097/FTD.0000000000000628
- Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases. LiverTox: Clinical and Research Information on Drug-Induced Liver Injury.; 2020.
- Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases. LiverTox: Clinical and Research Information on Drug-Induced Liver Injury.; 2017. Accessed February 10, 2022. https://www-ncbi-nlm-nih-gov.ezproxy.lib.ucalgary.ca/books/NBK548018/
- Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases. LiverTox: Clinical and Research Information on Drug-Induced Liver Injury.; 2017. Accessed February 10, 2022. https://www-ncbi-nlm-nih-gov.ezproxy.lib.ucalgary.ca/books/NBK548587/
- Lichtenstein L, Ron Y, Kivity S, et al. Infliximab-Related Infusion Reactions: Systematic Review. J Crohns Colitis. 2015;9(9):806-815. doi:10.1093/ecco-jcc/jjv096
- Tracey D, Klareskog L, Sasso EH, Salfeld JG, Tak PP. Tumor necrosis factor antagonist mechanisms of action: A comprehensive review. Pharmacol Ther. 2008;117(2):244-279. doi:10.1016/j.pharmthera.2007.10.001
- Chavez-Alvarez S, Herz-Ruelas M, Villarreal-Martinez A, Ocampo-Candiani J, Garza-Garza R, Gomez-Flores M. Azathioprine: its uses in dermatology. An Bras Dermatol. 2020;95(6):731-736. doi:10.1016/j.abd.2020.05.003



