Volume 42 Number 3
WHAM evidence summary: turmeric for treating radiation dermatitis
Emily Haesler
Keywords radiation dermatitis, turmeric, curcumin, curcuma longa, radiodermatitis
For referencing Haesler E. WHAM evidence summary: turmeric for treating radiation dermatitis. WCET® Journal 2022;42(3):34-37
DOI https://doi.org/10.33235/wcet.42.3.34-37
Clinical question
What is the best available evidence for turmeric products for treating radiation dermatitis?
Summary
Turmeric (Curcuma longa) is a spice harvested in India and other Asian countries that has traditionally been used to treat many ailments, including skin conditions. It is recognised as having anti-inflammatory, antioxidant and antiseptic effects that could play a role in reducing radiation dermatitis, which frequently occurs during radiotherapy because of morphological skin changes. Level 1 evidence1 suggested oral turmeric taken throughout the course of radiotherapy is associated with a delay in onset and severity of radiation dermatitis. Level 1 evidence2–4 reporting on topical turmeric preparations was mixed. Two small studies2,3 found that topical turmeric reduces onset and severity of radiation dermatitis, while a third, larger study4 found no difference in effect compared to other topical preparations. More research on the potential benefits from application of a turmeric-based product during radiotherapy is required.
Clinical practice recommendations
All recommendations should be applied with consideration to the wound, the person, the health professional and the clinical context.
|
Oral turmeric could be considered as an adjunct therapy to reduce the severity of radiation dermatitis in selected people receiving radiation therapy (Grade B). There is insufficient evidence to make a graded recommendation on the use of topical turmeric preparations to reduce the severity of radiation dermatitis |
Sources of evidence: search and appraisal
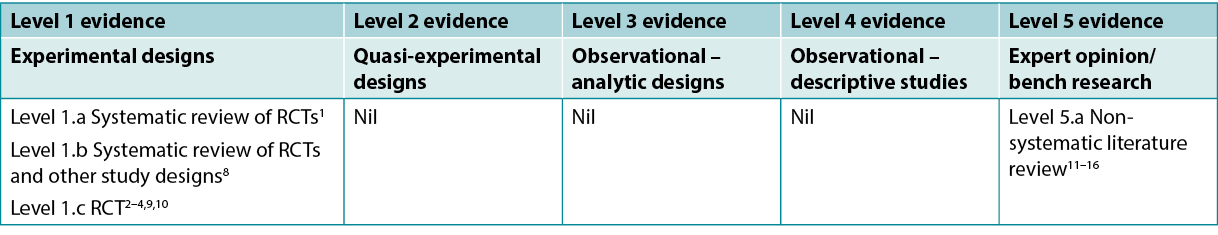
This summary was conducted using methods published by the Joanna Briggs Institute5–7. The summary is based on a systematic literature search combining search terms related to turmeric/curcumin/curcuma longa and radiation dermatitis. Studies reporting turmeric for management of other wounds or skin conditions (e.g., psoriasis) were excluded. Searches were conducted in the CINAHL, PubMed® and Hinari databases and in the Cochrane Library for evidence conducted in humans published up to April 2022 in English. Levels of evidence for intervention studies are reported in Table 1.
Table 1. Levels of evidence for clinical studies
Background
Turmeric (C. longa) is a spice prepared from a rhizome that is used as a traditional medicine in India and other Asian countries. Curcumin, which is the active chemical substance in turmeric17,18, is described as having anti-inflammatory, antioxidant, antiseptic and anti-cancer effects15,18–20.
Radiation dermatitis is a common side effect that affects up to 95% of people receiving radiotherapy for the management of breast cancer4,14,16. Radiotherapy can damage epithelial cells, decreasing the thickness of the epidermis and leading to increasing severity of signs and symptoms as radiotherapy continues, including warmth, pruritus, erythema, oedema, exudate, burning and pain21. It is theorised that curcumin may be effective in reducing the morphological changes that occur to the skin during radiation therapy by decreasing expression of inflammatory cytokines, growth factors and tumour necrosis factor2,12,14,15. Essentially, the anti-inflammatory and antioxidant properties of curcumin are considered advantageous in protecting against the processes that lead to radiation dermatitis14.
Clinical evidence
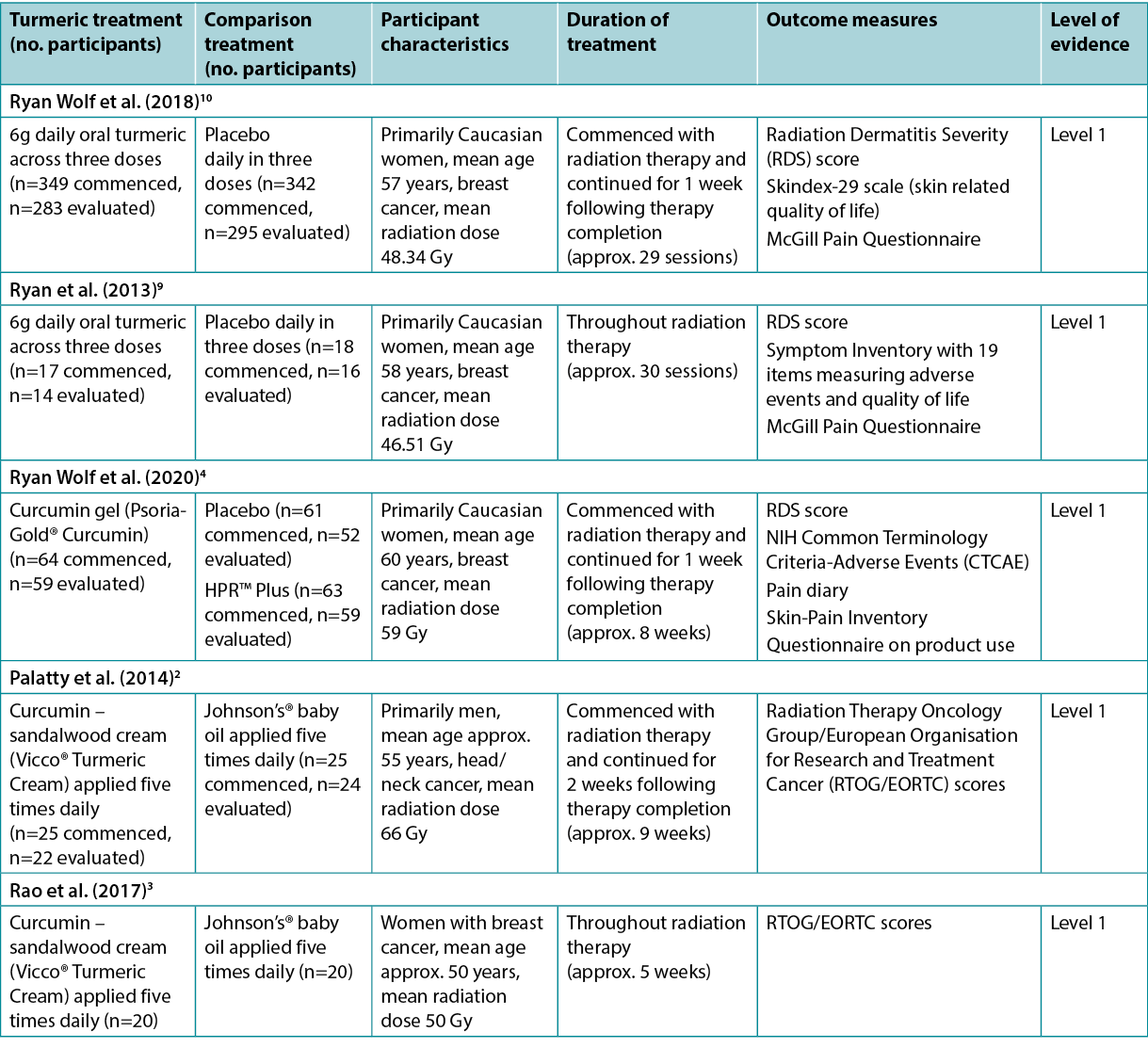
The evidence on turmeric products used to treat radiation dermatitis is summarised in Table 2.
Table 2. Summary of the evidence
Oral turmeric to treat radiation dermatitis
A meta-analysis1 at low risk of bias reported the use of oral curcumin for people receiving radiotherapy. This meta-analysis was conducted to inform an evidence-based clinical guideline22 and included two randomised clinical trials (RCTs)9,10 (n=716). In both the RCTs, people with breast cancer received either 6g curcumin daily (across three doses) or placebo, commencing at the start of radiotherapy and concluding 1 week after radiotherapy finished. There was a reduced risk of experiencing Grade 2 or higher radiation dermatitis associated with oral curcumin (risk ratio [RR]=0.64, 95% confidence interval [CI]=0.42 to 0.96, absolute risk reduction [ARR]=48 fewer cases per 1,000), but the mean difference in Radiation Dermatitis Severity (RDS) score was low (0.8 lower)1 and the RDS score was not statistically significantly different between groups at the end of treatment (p=0.55)22. The evidence was of low certainty and the withdrawal rate was high (curcumin group 18% versus control group 14%)22. The guideline developers made no recommendation on curcumin primarily due to potential interaction with medications, lack of cost-effectiveness data, and small anticipated desirable effects22 (Level 1).These studies were also reported in other reviews8,12–16 that were at higher risk of bias but that reached similar conclusions that oral curcumin was associated with some positive outcomes (Level 1 and 5).
Topical turmeric to treat radiation dermatitis
An RCT4 (n=191) at low risk of bias compared curcumin gel (4% concentration) to HPR™ Plus (described as a white lotion, FDA-approved medical device) to a placebo gel for reducing the severity of radiation dermatitis in people with breast cancer. The topical preparations were applied three times daily from the base of the neck to underneath the breast fold, including the side of the breast and under the arm, commencing with the start of radiotherapy and continuing until 1 week after therapy ceased. There were no statistically significant differences in mean RDS scores (curcumin 2.68 versus HPR™ Plus 2.64 versus placebo 2.63, p=0.929) or rate of moist desquamation (curcumin 25.42% versus HPR™ Plus 20.34% versus placebo 22.64%, p=0.805)4. This study had overall low rates of radiation dermatitis, and some potential benefits of turmeric therapy were reported in sub-analyses, but the study was not designed to measure these effects (Level 1).
An RCT2 (n=50) at moderate risk of bias compared the effect of a topical turmeric–sandalwood cream (16% turmeric extract) to a control (baby oil) for treating radiation dermatitis in people with head and neck cancer. The treatment for both groups was applied five times daily, from the first day of radiotherapy until 2 weeks after therapy concluded (approximately 9 weeks). After 2 weeks, no participants had experienced radiation dermatitis. From week 3 to week 7 the incidence of radiation dermatitis increased in both groups, with statistically significantly lower rates in the turmeric-based cream group in week 3 (12% versus 41.67%, p<0.045) and week 4 (37.5% versus 75%, p<0.028). Severity of radiation dermatitis evaluated using the Radiation Therapy Oncology Group/European Organisation for Research and Treatment Cancer (RTOG/EORTC) score was statistically significantly lower for the turmeric-based cream group from week 3 until conclusion of the study (p<0.05 for all). Grade 3 radiation dermatitis occurred less often in the turmeric-based cream group (9.5% versus 37.5%, p<0.01) and no participants in the study experienced Grade 4 radiation dermatitis2 (Level 1).
A more recent RCT3 (n=50) at moderate risk of bias conducted by the same research team2 explored topical turmeric–sandalwood cream (16% turmeric extract) for women with breast cancer undergoing radiotherapy. The comparator was baby oil, and the treatment regimen was the same as in the study above2. At the end of the second week of radiotherapy, the turmeric-based cream group had a statistically significantly lower rate of radiation dermatitis (32% versus 75%, p=0.0025). In both groups, rates of radiation dermatitis increased throughout the trial, but were statistically significantly lower in the turmeric-based cream group at every weekly measurement (p<0.05 for all)3 (Level 1).
Considerations for use
- Patient-reported outcomes, including pain and skin-related quality of life, were not statistically significantly different compared to a placebo for people taking oral curcumin10 or for people using topical curcumin4.
- Few adverse events have been reported in the literature8–10,12,13. Some evidence indicates curcumin can increase oxalate levels in the kidneys, contributing to development of kidney stones11. Potential to exacerbate gallstone symptoms has also been reported8.
- Curcumin has low bioavailability, which means it is poorly absorbed and used by the body8,10,12,13 and excreted rapidly8,16. Ongoing research is attempting to develop delivery mechanisms (e.g., encapsulation within nanoparticle carriers and developing water-soluble formulations) that will increase its clinical utility10,16.
Conflicts of interest
The author declares no conflicts of interest in accordance with International Committee of Medical Journal Editors (ICMJE) standards.
About wham collaborative evidence summaries
The WHAM Collaborative evidence summaries are consistent with methodology published in Munn, Lockwood and Moola23.
Methods are outlined in resources published by the Joanna Briggs Institute5–7 and on the WHAM Collaborative website: http://WHAMwounds.com. WHAM evidence summaries undergo peer review by an international, multidisciplinary Expert Reference Group. WHAM evidence summaries provide a summary of the best available evidence on specific topics and make suggestions that can be used to inform clinical practice. Evidence contained within this summary should be evaluated by appropriately trained professionals with expertise in wound prevention and management, and the evidence should be considered in the context of the individual, the professional, the clinical setting and other relevant clinical information.
Copyright ©2021 Wound Healing and Management Collaboration, Curtin Health Innovations Research Institute, Curtin University, WA, Australia.
Synthèse de données WHAM : le curcuma dans le traitement de la radiodermite
Emily Haesler
DOI: https://doi.org/10.33235/wcet.42.3.34-37
Question clinique
Quelles sont les meilleures données probantes disponibles concernant les produits à base de curcuma pour le traitement de la radiodermite ?
Synthèse
Le curcuma (Curcuma longa) est une épice récoltée en Inde et dans d'autres pays d'Asie, traditionnellement utilisé pour traiter de nombreux maux, dont les affections cutanées. On lui reconnaît des effets anti-inflammatoires, antioxydants et antiseptiques qui pourraient jouer un rôle dans la réduction des dermatites dues aux radiations, qui surviennent fréquemment pendant la radiothérapie en raison des modifications morphologiques de la peau. Des données de niveau 11 suggèrent que la prise orale de curcuma pendant toute la durée de la radiothérapie est associée à un retard dans l'apparition et la sévérité de la radiodermite. Les données de niveau 12-4 rapportées sur les préparations topiques à base de curcuma étaient mitigées. Deux petites études2,3 ont montré que le curcuma topique réduit l'apparition et la sévérité de la radiodermite, tandis qu'une troisième étude plus importante4 n'a pas trouvé de différence d'effet par rapport à d'autres préparations topiques. Des recherches supplémentaires sur les avantages potentiels de l'application d'un produit à base de curcuma pendant la radiothérapie sont nécessaires.
Recommandations pour la pratique clinique
Toutes les recommandations doivent être appliquées en tenant compte de la plaie, de la personne, du professionnel de santé et du contexte clinique.
|
Le curcuma oral pourrait être considéré comme un traitement d'appoint pour réduire la sévérité de la radiodermite chez certaines personnes recevant une radiothérapie (grade B). Les preuves sont insuffisantes pour formuler une recommandation graduée sur l'utilisation de préparations topiques à base de curcuma pour réduire la sévérité de la radiodermite. |
Sources des données recherche et évaluation
Cette synthèse a été réalisée selon les méthodes publiées par le Joanna Briggs Institute5-7. La synthèse est basée sur une recherche documentaire systématique combinant les termes de recherche associés au curcuma/curcumine/curcuma longa et à la radiodermite. Les études faisant état de l'utilisation du curcuma pour le traitement d'autres plaies ou affections cutanées (par exemple : le psoriasis) ont été exclues. Des recherches ont été effectuées dans les bases de données CINAHL, PubMed® et Hinari ainsi que dans la bibliothèque Cochrane pour les données recherchées chez l'homme publiées jusqu'en avril 2022 en anglais. Les niveaux de données des études d'intervention sont indiqués dans le tableau 1.
Tableau 1. Niveaux des données des études cliniques

Contexte
Le curcuma (C. longa) est une épice préparée à partir d'un rhizome qui est utilisé comme médicament traditionnel en Inde et dans d'autres pays d'Asie. La curcumine, qui est la substance chimique active du curcuma17,18, est décrite comme ayant des effets anti-inflammatoires, antioxydants, antiseptiques et anticancéreux15,18-20.
La radiodermite est un effet secondaire courant qui touche jusqu'à 95 % des personnes recevant une radiothérapie pour le traitement du cancer du sein4,14,16. La radiothérapie peut endommager les cellules épithéliales, diminuant l'épaisseur de l'épiderme et entraînant une sévérité croissante des signes et symptômes au fur et à mesure que la radiothérapie se poursuit, notamment la chaleur, le prurit, l'érythème, l'œdème, l'exsudat, la brûlure et la douleur21. On pense que la curcumine peut être efficace pour réduire les changements morphologiques qui se produisent sur la peau pendant la radiothérapie en diminuant l'expression des cytokines inflammatoires, les facteurs de croissance et le facteur de nécrose tumorale2,12,14,15. Essentiellement, les propriétés anti-inflammatoires et antioxydantes de la curcumine sont considérées comme avantageuses pour la protection contre les processus qui conduisent à la radiodermite14.
Données cliniques
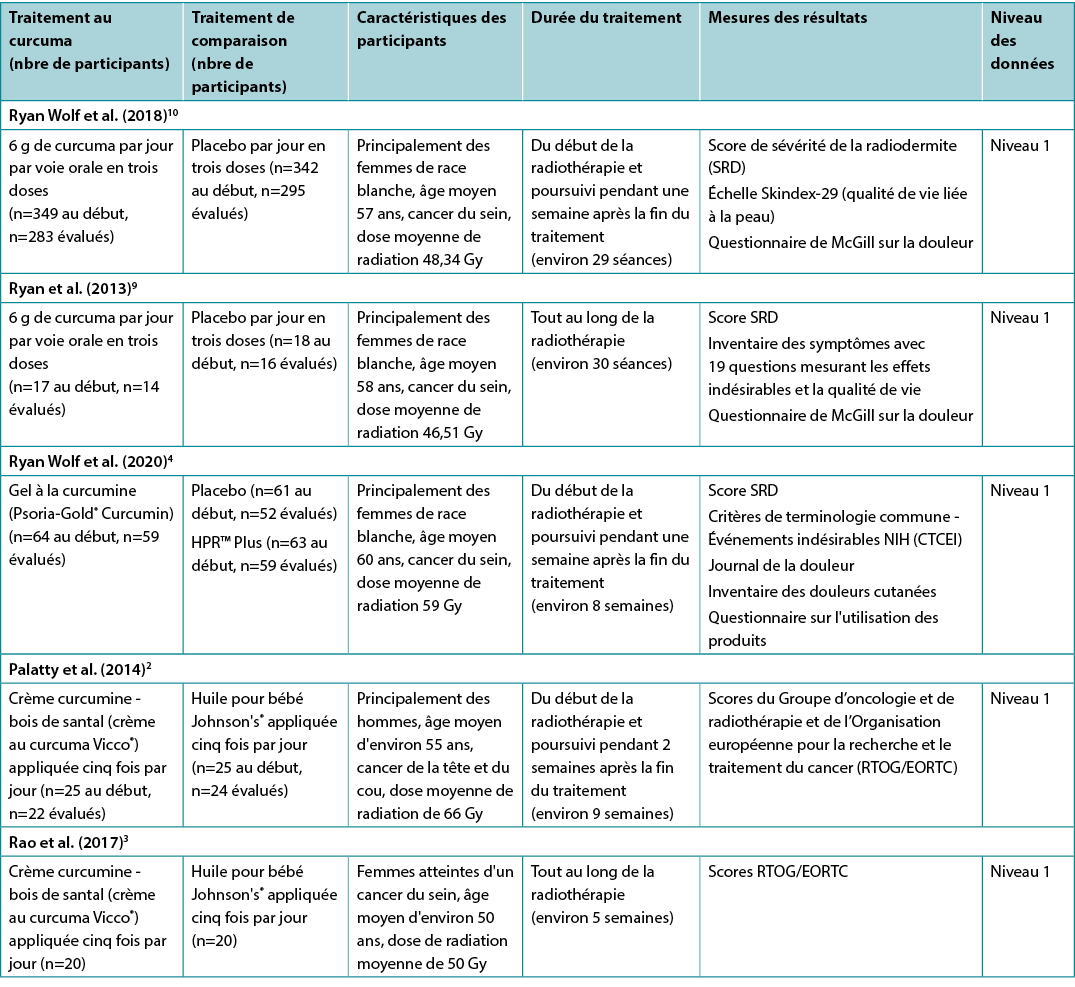
Les données concernant les produits à base de curcuma utilisés pour traiter la radiodermite sont synthétisées dans le tableau 2.
Tableau 2. Synthèse des données
Le curcuma par voie orale pour traiter la radiodermite
Une méta-analyse1 à faible risque de biais a décrit l'utilisation de la curcumine orale pour les personnes recevant une radiothérapie. Cette méta-analyse a été réalisée pour éclairer une directive clinique fondée sur des données probantes22 et comprenait deux essais cliniques randomisés (ECR)9,10 (n=716). Dans les deux ECR, les personnes atteintes d'un cancer du sein ont reçu soit 6 g de curcumine par jour (en trois doses), soit un placebo, en commençant au début de la radiothérapie et en terminant une semaine après la fin de celle-ci. Le risque de souffrir d'une radiodermite de grade 2 ou plus a été réduit avec la curcumine orale (ratio du risque [RR]=0,64, intervalle de confiance à 95 % [IC]=0,42 à 0,96, réduction du risque absolu [RRA]=48 cas de moins pour 1 000), mais la différence moyenne du score de sévérité de la radiodermite (SRD) était faible (0,8 de moins)1 et le score de SRD n'était pas statistiquement différent entre les groupes à la fin du traitement (p=0,55)22. Les données étaient de faible degré de certitude et le taux d'abandon était élevé (groupe curcumine 18 % contre groupe contrôle 14 %)22. Les concepteurs de la directive n'ont formulé aucune recommandation sur la curcumine, principalement en raison de l'interaction potentielle avec les médicaments, de l'absence de données sur le rapport coût-efficacité et de la faiblesse des effets souhaitables anticipés22 (niveau 1).Ces études ont également été rapportées dans d'autres examens8,12-16 qui présentaient un risque plus élevé de biais, mais qui sont parvenus à des conclusions similaires, à savoir que la curcumine orale était associée à certains résultats positifs (niveaux 1 et 5).
Le curcuma topique pour traiter la radiodermite
Un ECR4 (n=191) à faible risque de biais a comparé le gel de curcumine (concentration à 4 %) à l’HPR™ Plus (décrit comme une lotion blanche, dispositif médical approuvé par la FDA) et à un gel placebo pour réduire la sévérité de la radiodermite chez les personnes atteintes d'un cancer du sein. Les préparations topiques ont été appliquées trois fois par jour de la base du cou jusqu'au-dessous du pli du sein, y compris sur le côté du sein et sous le bras, en commençant au début de la radiothérapie et en continuant jusqu'à une semaine après l'arrêt du traitement. Il n'y a pas eu de différences statistiquement significatives dans les scores moyens de SRD (curcumine 2,68 versus HPR™ Plus 2,64 versus placebo 2,63, p=0,929) ou le taux de desquamation humide (curcumine 25,42 % versus HPR™ Plus 20,34 % versus placebo 22,64 %, p=0,805)4. Cette étude présente des taux globalement faibles de radiodermite, et certains avantages potentiels du traitement au curcuma ont été signalés dans des sous-analyses, mais l'étude n'a pas été conçue pour mesurer ces effets (niveau 1).
Un ECR2 (n=50) présentant un risque modéré de biais a comparé l'effet d'une crème topique au curcuma et au bois de santal (16 % d'extrait de curcuma) à un contrôle (huile pour bébé) pour traiter la radiodermite chez des personnes atteintes d'un cancer de la tête et du cou. Le traitement pour les deux groupes a été appliqué cinq fois par jour, depuis le premier jour de la radiothérapie jusqu'à deux semaines après la fin du traitement (environ 9 semaines). Après deux semaines, aucun participant n'avait souffert de radiodermite. De la semaine 3 à la semaine 7, l'incidence de la radiodermite a augmenté dans les deux groupes, avec des taux plus faibles statistiquement significatifs dans le groupe de la crème à base de curcuma à la semaine 3 (12 % contre 41,67 %, p<0,045) et à la semaine 4 (37,5 % contre 75 %, p<0,028). La sévérité de la radiodermite, évaluée à l'aide du score du Groupe d’oncologie et de radiothérapie et de l’Organisation européenne pour la recherche et le traitement du cancer (RTOG/EORTC), était significativement plus faible, d'un point de vue statistique, pour le groupe de la crème à base de curcuma, de la semaine 3 jusqu'à la fin de l'étude (p<0,05 pour tous). Une radiodermite de grade 3 est survenue moins souvent dans le groupe de la crème à base de curcuma (9,5 % contre 37,5 %, p<0,01) et aucun participant de l'étude n'a présenté de radiodermite de grade 42 (niveau 1).
Un ECR plus récent3 (n=50) présentant un risque modéré de biais et mené par la même équipe de recherche2 a exploré la crème topique au curcuma et au bois de santal (16 % d'extrait de curcuma) pour les femmes atteintes d'un cancer du sein et subissant une radiothérapie. Le comparateur était de l'huile pour bébé, et le protocole de soins était le même que dans l'étude ci-dessus2. À la fin de la deuxième semaine de radiothérapie, le groupe de la crème à base de curcuma présentait un taux plus faible statistiquement significatif de radiodermite (32 % contre 75 %, p=0,0025). Dans les deux groupes, les taux de radiodermite ont augmenté tout au long de l'essai, mais les taux statistiquement significatifs étaient plus faibles dans le groupe de la crème à base de curcuma à chaque mesure hebdomadaire (p<0,05 pour tous)3 (niveau 1).
Considérations relatives à l'utilisation
- Les résultats rapportés par les patients, notamment la douleur et la qualité de vie liée à la peau, n'étaient pas statistiquement significativement différents par rapport à un placebo pour les personnes prenant de la curcumine par voie orale10 ou pour les personnes utilisant de la curcumine topique4.
- Peu d'effets indésirables ont été rapportés dans la littérature8–10,12,13. Certaines données indiquent que la curcumine peut augmenter les niveaux d'oxalate dans les reins, contribuant ainsi au développement de calculs rénaux11. Le potentiel d'exacerbation des symptômes de calculs biliaires a également été signalé8.
- La curcumine a une faible biodisponibilité, ce qui signifie qu'elle est mal absorbée et mal utilisée par l'organisme8,10,12,13 et excrétée rapidement8,16. Des recherches en cours tentent de développer des mécanismes d'administration (par exemple, l'encapsulation dans des supports nanoparticulaires et le développement de formulations hydrosolubles) qui augmenteront son utilité clinique10,16.
Conflits d'intérêt
Les auteurs ne déclarent aucun conflit d'intérêt conformément aux normes de Comité international des éditeurs de presse médicale (ICMJE).
À propos des synthèses de données de la collaboration WHAM
Les synthèses de données de la collaboration WHAM sont conformes à la méthodologie publiée par Munn, Lockwood et Moola23.
Les méthodes sont décrites dans les ressources publiées par l'Institut Joanna Briggs5-7 et sur le site internet de la collaboration WHAM : http://WHAMwounds.com. Les synthèses de données WHAM sont soumises à l’examen de pairs membres d’un Groupe de référence international multidisciplinaire d'experts. Les synthèses de données WHAM fournissent une synthèse des meilleures données probantes disponibles sur des sujets spécifiques et font des suggestions qui peuvent être utilisées pour renseigner la pratique clinique. Les données contenues dans cette synthèse doivent être évaluées par des professionnels dûment formés et spécialisés dans la prévention et la prise en charge des plaies, et les données doivent être considérées dans le contexte de l'individu, du professionnel, du cadre clinique et de tout autre information clinique pertinente.
Copyright ©2021 Wound Healing and Management Collaboration, Curtin Health Innovations Research Institute, Université Curtin, WA, Australie.
Author(s)
Emily Haesler
PhD Post Grad Dip Adv Nurs (Gerontics) BNurs Fellow Wounds Australia
Adjunct Professor Wound Healing and Management Collaborative, Curtin Health Innovation Research Institute, Curtin University, WA
References
- Ginex PK, Backler C, Croson E, Horrell LN, Moriarty KA, Maloney C, Vrabel M, Morgan RL. Radiodermatitis in patients with cancer: systematic review and meta-analysis. Oncol Nurs Forum 2020;47(6):E225-E36.
- Palatty PL, Azmidah A, Rao S, Jayachander D, Thilakchand KR, Rai MP, Haniadka R, Simon P, Ravi R, Jimmy R, D’Souza P F, Fayad R, Baliga MS. Topical application of a sandal wood oil and turmeric based cream prevents radiodermatitis in head and neck cancer patients undergoing external beam radiotherapy: a pilot study. Br J Radiol 2014;87(1038):20130490.
- Rao S, Hegde SK, Baliga-Rao MP, Lobo J, Palatty PL, George T, Baliga MS. Sandalwood oil and turmeric-based cream prevents ionizing radiation-induced dermatitis in breast cancer patients: clinical study. Medicines (Basel) 2017;4(3).
- Ryan Wolf J, Gewandter JS, Bautista J, Heckler CE, Strasser J, Dyk P, Anderson T, Gross H, Speer T, Dolohanty L, Bylund K, Pentland AP, Morrow GR. Utility of topical agents for radiation dermatitis and pain: a randomized clinical trial. Supp Care Cancer 2020;28(7):3303–11.
- Aromataris E, Munn Z, editors. Joanna Briggs Institute reviewer’s manual; 2017. Available from: https://reviewersmanual.joannabriggs.org/The Joanna Briggs Institute.
- Joanna Briggs Institute Levels of Evidence and Grades of Recommendation Working Party. New JBI grades of recommendation. Adelaide: Joanna Briggs Institute; 2013.
- The Joanna Briggs Institute Levels of Evidence and Grades of Recommendation Working Party. Supporting document for the Joanna Briggs Institute levels of evidence and grades of recommendation. The Joanna Briggs Institute; 2014. Available from:www.joannabriggs.org
- Vaughn AR, Branum A, Sivamani RK. Effects of turmeric (Curcuma longa) on skin health: a systematic review of the clinical evidence. Phytother Res 2016;30(8):1243–64.
- Ryan JL, Heckler CE, Ling M, Katz A, Williams JP, Pentland AP, Morrow GR. Curcumin for radiation dermatitis: a randomized, double-blind, placebo-controlled clinical trial of thirty breast cancer patients. Radiat Res 2013;180(1):34–43.
- Ryan Wolf J, Heckler CE, Guido JJ, Peoples AR, Gewandter JS, Ling M, Vinciguerra VP, Anderson T, Evans L, Wade J, Pentland AP, Morrow GR. Oral curcumin for radiation dermatitis: a URCC NCORP study of 686 breast cancer patients. Supp Care Cancer 2018;26(12):1543–52.
- Watts R. Evidence summary: turmeric (curcumin) in wound management limited resources communities. Wound Pract Res 2017;25(3):158–9.
- Akbari S, Kariznavi E, Jannati M, Elyasi S, Tayarani-Najaran Z. Curcumin as a preventive or therapeutic measure for chemotherapy and radiotherapy induced adverse reaction: a comprehensive review. Food Chem Toxicol 2020;145:111699.
- Karaboga Arslan AK, Uzunhisarcıklı E, Yerer MB, Bishayee A. The golden spice curcumin in cancer: a perspective on finalized clinical trials during the last 10 years. J Cancer Res Ther 2022;18(1):19–26.
- Farhood B, Mortezaee K, Goradel NH, Khanlarkhani N, Salehi E, Nashtaei MS, Najafi M, Sahebkar A. Curcumin as an anti-inflammatory agent: implications to radiotherapy and chemotherapy. J Cell Physiol 2019;234(5):5728–40.
- Verma V. Relationship and interactions of curcumin with radiation therapy. World J Clin Oncol 2016;7(3):275–83.
- Zoi V, Galani V, Tsekeris P, Kyritsis AP, Alexiou GA. Radiosensitization and radioprotection by curcumin in glioblastoma and other cancers. Biomed 2022;10(2):312.
- Akbik D, Ghadiri M, Chrzanowski W, Rohanizadeh R. Curcumin as a wound healing agent. Life Sci (1973) 2014;116(1):1–7.
- Mohanty C, Sahoo SK. Curcumin and its topical formulations for wound healing applications. Drug Discov Today 2017;22(10):1582–92.
- Maheshwari RK, Singh AK, Gaddipati J, Srimal RC. Multiple biological activities of curcumin: a short review. Life Sci (1973) 2006;78(18):2081–7.
- Ahangari N, Kargozar S, Ghayour-Mobarhan M, Baino F, Pasdar A, Sahebkar A, Ferns GAA, Kim HW, Mozafari M. Curcumin in tissue engineering: a traditional remedy for modern medicine. Biofactor 2019;45(2):135–51.
- Haesler, E. Wound dressings for treating of radiation dermatitis: a WHAM evidence summary. Wound Pract Res 2021;29(3):176–9.
- Gosselin T, Ginex PK, Backler C, Bruce SD, Hutton A, Marquez CM, Shaftic AM, Suarez LV, Moriarty KA, Maloney C, Vrabel M, Morgan RL. ONS guidelines™ for cancer treatment-related radiodermatitis. Oncol Nurs Forum 2020;47(6):654–70.
- Munn Z, Lockwood C, Moola S. The development and use of evidence summaries for point of care information systems: a streamlined rapid review approach. Worldview Evid Based Nurs 2015;12(3):131–8.

