Volume 39 Number 3
Effect of tamsulosin on lower urinary tract symptoms related to double-J ureteral stent: a randomised, double-blinded, placebo controlled trial
Fateme Guitynavard, Shahram Gooran, Parvin Kasiri, Farshad Gholipour and Seyed Mohammad Kazem Aghamir
Keywords urethral stent, stent-related symptoms, lower urinary tract symptoms, tamsulosin, double-J
For referencing Guitynavard F et al. Effect of tamsulosin on lower urinary tract symptoms related to double-J ureteral stent: a randomised, double-blinded, placebo controlled trial. WCET® Journal 2019; 39(3):26-31
DOI https://doi.org/10.33235/wcet.39.3.26-31
Abstract
Objective To evaluate the effect of tamsulosin on stent-related symptoms in patients undergoing double-J ureteral stenting.
Methods and materials Seventy patients (47 men and 23 women; mean age 42.5 years) who underwent double-J stent placement in adjunct to urological surgery were prospectively randomised into two groups. Group 1 included 35 patients who received 0.4 mg of tamsulosin once daily for 4 weeks; group 2 included 35 patients who received a placebo for the same protocol. All patients were interviewed by the same physician about the frequency of stent-related symptoms at 4 weeks after stent insertion.
Results Patients in group 1 showed a lower score for suprapubic pain during the filling phase and lower pain during sexual activity than group 2, although the overall pain score was not significantly different between two groups. The mean urinary urgency score was less in group 1 in comparison to the placebo group (p=0.030). No statistically significant differences were found between two groups concerning haematuria, urinary incontinence, frequency nor dysuria.
Conclusion Tamsulosin improves symptoms associated with double-J ureteral stents, especially body pain during sexual activity.
Introduction
Indwelling ureteral stents are a commonly used tool in urologic practices. Zimskind et al.1 described ureteral stent placement for the first time in 1967. However, despite the documented benefits of double-J stents in preventing ureteral obstruction after urologic procedures2, patients may experience stent-related symptoms and some morbidities, including urinary symptoms, stent-related body pain and sexual difficulties which, together, can severely influence the patients’ quality of life and general health substantially3-8.
Authors have hypothesised several aetiologies responsible for stent-related complications such as bladder trigone irritation and renal reflux7,9. Through the years, manufacturers have made innovations in stent design and materials in order to improve stent-caused problems10,11, yet have failed to design an ideal stent which can significantly reduce adverse effects11,12.
Given the effect of α-blockers in alleviating lower urinary tract symptoms associated with overactive bladder and benign prostate hyperplasia13, several studies investigated the role of these agents on stent-related symptoms using the Ureteral Stent Symptom Questionnaire (USSQ)13-17, the International Prostate Symptom Score (IPSS)17-24, the Visual Analog Pain Score (VAPS)19-21,24, or evaluation of clinical symptoms by interviewing the patients25.
Tamsulosin selectively blocks α-1a/1d adrenergic receptors in smooth muscles of distal ureter, bladder trigone, bladder neck and prostate26. Smooth muscle relaxation is believed to reduce bladder, neck and urethral resistance, which can improve stent-related lower urinary tract symptoms17,18. The purpose of this clinical trial was therefore to evaluate the effectiveness of tamsulosin in reducing double-J stent-related symptoms in patients undergoing ureteral stenting.
Methods and Materials
After ethics committee approval, this prospective double-blinded and placebo controlled randomised clinical trial was carried out between June 2014 and July 2015 in Sina Hospital, Tehran, Iran. The current trial was registered at www.clinicaltrials.gov as IRCT2015042221886N2.
Study population and design
Patients who underwent a double-J ureteral stenting by a single surgeon were assessed for eligibility. Stents were routinely placed before extracorporeal shock wave lithotripsy (ESWL) or following percutaneous nephrolithotomy (PCNL), ureterorenoscopy (URS), endoscopic endopyelotomy, or transureteral ureterolithotomy (TUL) for 4 weeks. Patients with at least 18 years of age and with an unilateral double-J ureteral stent were enrolled into the study after obtaining informed consent about random allocation of treatment and potential side effects of tamsulosin. The exclusion criteria included patients younger than 18 years, pregnant women, patients with bilateral stents, forgotten ureteral stent, long-standing ureteral stent placement, benign prostatic hyperplasia, previous prostatic resection, prostatitis, prostate cancer, bladder neoplasms, recent or recurrent urinary tract infection, history of chronic flank pain, patients previously treated with selective α-blockers, patients with severe cardiovascular disease, and patients affected by risk factors for erectile dysfunction.
Study procedure
Out of 110 patients who were assessed for eligibility, a total of 76 patients (47 men and 29 women, aged 20–74 years) who gave consent were enrolled in the study. Patients were randomly allocated into two groups using a computer randomisation program. In group A, the case group, 38 patients (25 men and 13 women) received a daily 0.4 mg dose of tamsulosin (Maxulosin®, Exir Pharmaceutical Co., Borujerd, Iran). In group B, the control group, 38 patients (25 men and 13 women) received a placebo once a day for 4 weeks. The patients were given numbered containers enclosing unnamed pills. Both participants and physicians were kept blinded to the medication being prescribed.
Before the scheduled operative procedure, routine laboratory tests and imaging were performed. In all patients, an identical flexible double-J ureteral stent was used, although the length and size of stents were individualised for each patient. Stent placement was done under regional or general anaesthesia. The coiled distal end of the stent was the only part of the stent presented in the bladder. Plain abdominal X-ray film was used to assure correct stent positioning. To standardise analgesic consumption, acetaminophen 500 mg was prescribed for pain control. No procedure-related complication occurred. All study procedures were in accordance with the ethical standards of the ethics committee of Tehran University of Medical Sciences on human experimentation and with the Helsinki Declaration of 1975, as revised in 2009.
Patient assessment and outcome measurements
Four weeks after stent placement, patients were interviewed by the same physician about stent-related symptoms including suprapubic pain (filling and voiding phase), haematuria, urinary incontinence, urinary frequency, dysuria, urinary urgency, nocturia, flank pain (filling and voiding phase), genitalia pain, and flank, suprapubic or genitalia pain during sexual activity. Patients were asked to answer the questions regarding the frequency of each symptom in a five-level Likert scale – ‘never’, ‘rarely’, ‘sometimes’, ‘often’, and ‘very often’.
Statistical analysis
Statistical analysis was performed using SPSS ver. 20.0 (SPSS Inc., Chicago, IL, USA). Descriptive statistics were obtained for each study variable. Chi-square, and student’s t-test were used for comparison between the two groups as appropriate; values of p less than 0.05 were considered statistically significant.
Results
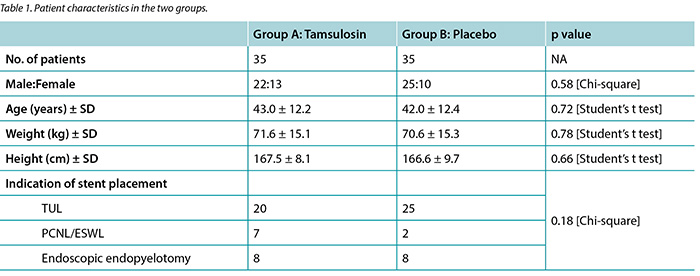
Out of 76 enrolled patients, 70 (92.1%) completed the study. Therapies were well tolerated and no patients had to terminate medication owing to adverse effects, and none underwent stent removal prior to the due date. Characteristics of the study population are presented in Table 1. Group A (35 patients) consisted of 22 men and 13 women (mean age 43.0 ± 12.2 years), and group B consisted of 25 men and 10 women (mean age 42.0 ± 12.4 years). A total of 45 patients (64.2%) underwent transurethral lithotripsy, nine patients (12.8%) underwent percutaneous nephrolithotripsy or ESWL, while endopyelotomy for ureteropelvic junction stricture was performed in 16 patients (22.8%). No statistically significant differences were found regarding gender, age, weight, height, nor indication of stent placement between the case and control groups.
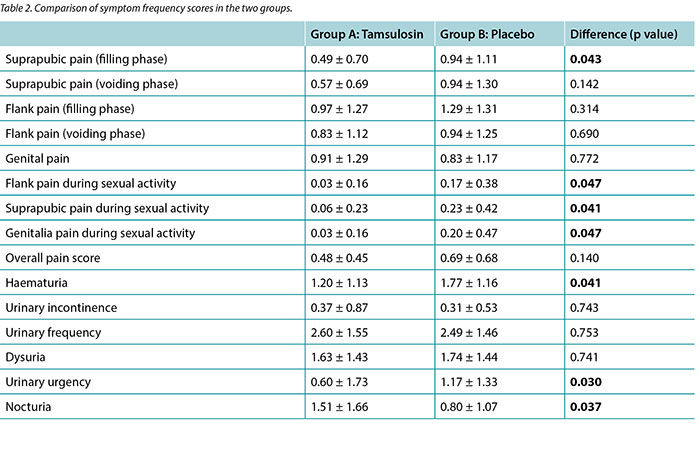
Scores 0 to 4 were attributed respectively to the frequency of scale of symptoms stated by patients, with 0 representing ‘never’ and 4 representing ‘very often’. Table 2 summarises the overall results of our study. Student’s t-test was used to examine the differences of means between groups. As shown in the table, patients receiving tamsulosin expressed higher scores (1.51 ± 1.66) for nocturia than patients in the control group (0.80 ± 1.07) (p=0.037). The mean score for pain in the flank, suprapubic and genital areas during sexual activity was lower in patients receiving tamsulosin in comparison to patients receiving the placebo (p values=0.047, 0.041 and 0.047, respectively). Patients treated with tamsulosin showed lower suprapubic pain in filling phase scores (0.49 ± 0.70) than the control group (0.94 ± 1.11) (p=0.043). The mean urinary urgency score was 0.6 in group 1 and 1.1 in the placebo group (p=0.030). No statistically significant differences were found between the two groups concerning haematuria, urinary incontinence, frequency, dysuria, nor overall pain score (p values >0.05).
Discussion
The results of this double-blind, randomised, placebo-controlled study showed that tamsulosin is effective in relieving stent-related symptoms specially in alleviating pain during sexual activity.
Current indications for ureteral stents in urgent conditions include unbearable acute renal colic, obstructive pyelonephritis and renal failure secondary to ureteral obstruction3. Endoscopic procedures can be followed by stent placement as a safety measure27 in several situations, including ureteral oedema, ureteral perforation, solitary kidney, transplant kidney and history of renal failure. There are also relative indications for indwelling ureteral stents such as passive dilation of ureteral orifice and ureter, before ESWL in stones larger than 2 cm, long-lasting impacted stone, endoscopic procedures lasting over 45 minutes, and pregnancy2,7.
However, despite widespread use of indwelling ureteral stents, there is considerable controversy over the necessity of stent placement after uncomplicated ureteroscopic lithotripsy28. Even after choosing the correct stent size and proper placement, indwelling ureteral stents are associated with inevitable morbidities in over 80% of patients29, including urinary symptoms, haematuria, pain and sexual difficulties which all lead to reduced health-related quality of life6. Some researchers report that the position and completeness of the stent’s lower loop and proper attention to detail throughout stent placement have an effect on symptom severity30,31. For example, an ureteral stent was better tolerated after periureteral injection of botulinum toxin type A after stent placement by significantly decreasing pain and narcotic requirement32.
However, the exact pathophysiology of stent-related symptoms is not fully understood. It is assumed that lower ureteral smooth muscle spasms, involuntary bladder contraction triggered by neuronal-rich trigone irritation, and urine reflux to the kidneys due to increased bladder outlet resistance are responsible factors11,14,15,21,33. α-blockers are recommended as expulsive therapy for ureteral stones and to decrease recurrent colic episodes. They are believed to relieve stent-related morbidity by different ways34-36. Blocking α-adrenergic receptors reduces muscle tone of prostatic urethra, bladder trigone and ureter which leads to decreased bladder outlet resistance, voiding pressure, and urinary reflux17. However, the effectiveness of these medications and proper therapeutic protocols for alleviation of stent-related symptoms are yet to be discovered by further investigations. Results of the current study showed that tamsulosin (a selective α1A antagonist) can control several stent-related morbidities.
The effectiveness of α-blockers in relieving stent-related symptoms has been investigated by several studies, including patients receiving either alfuzosin 10 mg13,14,16,25,37, tamsulosin 0.4 mg15,17,22,23,17, tamsulosin 0.2 mg19,20, terazosin 4 mg21,38, terazosin 2 mg21, or a placebo for 1–6 weeks’ treatment. Damiano et al.15 released the first report of the benefits of a daily dose of tamsulosin 0.4 mg in a prospective study comparing tamsulosin to placebo in 75 patients using the USSQ. Although this study was not double-blinded nor placebo-controlled, the authors found that patients receiving tamsulosin had their general health better preserved. In another study performed by Wang et al.17 on 154 patients using the same measurement tool, those receiving tamsulosin showed lower stent-related symptoms and better quality of life than patients receiving a placebo.
Using both IPSS and VAPS, the effect of lower dose of tamsulosin (0.2 mg once a day) alone and in combination with tolterodin or solifenacin on stent-related symptoms was investigated by Lee et al.19 and Lim et al.20, respectively. Lee et al. found that only the storage symptom scores were significantly lower in patients receiving either mono- or combination therapy than patients treated with no medication. The author stated that correct placement of the stent is therefore more important than medication in reducing stent-related storage symptoms19. Conversely, Lim showed that combination therapy with tamsulosin and solifenacin can better improve both irritative and obstructive symptoms than tamsulosin alone or compared to receiving no medication20; the results were later confirmed by Shalaby et al.23. Further, improvement of stent-related symptoms by α-blockers was found to be independent to the type of α-blocker, as showed by Dellis et al.37 comparing tamsulosin and alfuzosin. To the best of our knowledge, there is only one study18 on α-blocker (doxazosin) ineffectiveness in reducing stent-related symptoms.
In a recent meta-analysis performed by Lamb et al.35 including 461 patients from five studies, all studies showed a reduction in the USSQ urinary symptom score and body pain scores in patients receiving either tamsulosin or alfuzosin. However, general health and sexual matters improvement were not statistically significant. Results of a further 12 studies including a total number of 946 patients’ data were meta-analysed by Yakoubi et al.36. Analyses showed a significant reduction in urinary symptoms and pain scores as well as general health improvement in patients receiving α-blockers.
In our study, the reduction in pain scores in patients treated with tamsulosin was more evident when compared to during sexual activity in all three areas – flank, genital and suprapubic. Ureteral stents were showed to impair the quality of sexual life in both men and women8. Erectile dysfunction was indicated as the main source of sexual distress in men, probably related to lower urinary tract symptoms and stent permanence. In women, sexuality can be severely impaired as a result of stent-related psychological distresses8.
We also found tamsulosin effective in reducing haematuria and urinary urgency, although, patients treated with tamsulosin had increased rate of nocturia than patients receiving placebo. Nocturia has not reported as an adverse effect of tamsulosin previously, so this finding should be investigated by larger-scale studies. Koseoglu et al.39 found tamsulosin ineffective in reducing nocturia in patients being treated for benign prostatic hyperplasia. In another study, combination of α-blockers with zolpidem was shown to better reduce nocturia than α-blockers alone40.
Our study had several limitations. First, our sample size was statistically small in order to detect small differences between two groups. Second, some patients did not complete the study. Third, we utilised clinical interviews with the patients to evaluate urinary symptoms, whereas Joshi et al.6 has developed a specific tool for assessing stent-related symptoms called the USSQ. Fourth, the quantity of the analgesics used by patients was not reliably reported. Finally, we did not investigate any adverse effects made by α-blocker use, although therapies were well tolerated and no patients had to discontinue medication owing to side effects. Therefore, further large-scale, randomised, prospective studies are needed to obtain more accurate information.
Conclusion
The use of tamsulosin 0.4 mg once daily in patients with unilateral ureteral stenting significantly improved stent-related urinary symptoms, especially the body pain during sexual activity. Therefore, tamsulosin should be considered for patients who complain of stent-related symptoms. In the future, large-scale, prospective and randomised studies will be needed.
Ethics approval and consent to participate
Patient consent was undertaken before surgery based on the ethical code of the Tehran University of Medical Sciences Ethics Committee. This trial was registered at www.clinicaltrials.gov as IRCT2015042221886N2. The information is published without the name of the patients. Information, data and photos can be provided if requested.
Competing interests
All authors claim that there is not any potential competing or conflict of interest.
Funding
None.
Acknowledgements
Special thanks to the Urology Research Center, Tehran University of Medical Sciences.
Efecto de la tamsulosina en síntomas de las vías urinarias inferiores relacionados con la endoprótesis ureteral doble J: ensayo aleatorizado, doble ciego y controlado por placebo
Fateme Guitynavard, Shahram Gooran, Parvin Kasiri, Farshad Gholipour and Seyed Mohammad Kazem Aghamir
DOI: https://doi.org/10.33235/wcet.39.3.26-31
Resumen
Objetivo Evaluar el efecto de la tamsulosina en síntomas relacionados con la endoprótesis en pacientes que se someten a la colocación de endoprótesis ureterales doble J.
Métodos y materiales Se estudió en dos grupos y de manera aleatoria a setenta pacientes (47 hombres y 23 mujeres, de una media de edad de 42,5 años) que se sometieron a la colocación de endoprótesis doble J junto con cirugía urológica. El grupo 1 incluía a 35 pacientes que recibieron 0,4 mg de tamsulosina, una vez por día durante 4 semanas; el grupo 2 incluía 35 pacientes que recibieron placebo para el mismo protocolo. El mismo médico conversó con todos los pacientes sobre la frecuencia de los síntomas relacionados con la endoprótesis cuatro semanas después de la colocación de la endoprótesis.
Resultados Los pacientes del grupo 1 mostraron un puntaje inferior para el dolor suprapúbico durante la fase de llenado y un dolor menor durante la actividad sexual en comparación con el grupo 2, si bien el puntaje del dolor a nivel general no era tan diferente entre los dos grupos. El puntaje medio de tenesmo vesical fue inferior en el grupo 1 en comparación con el grupo placebo (p=0,030). No se encontraron diferencias importantes desde el punto de vista estadístico entre los dos grupos con respecto a hematuria, incontinencia urinaria, polaquiuria ni disuria.
Conclusión La tamsulosina mejora los síntomas asociados con la endoprótesis ureteral doble J, especialmente en cuanto al dolor corporal durante la actividad sexual.
Introducción
Las endoprótesis ureterales permanentes son una herramienta de uso común en las prácticas urológicas. Zimskind y cols.1 describieron la colocación de endoprótesis ureterales por primera vez en 1967. Sin embargo, a pesar de los beneficios documentados de las endoprótesis doble J para prevenir obstrucciones ureterales después de procedimientos urológicos2, los pacientes pueden experimentar síntomas relacionados con la endoprótesis y algunas morbilidades, que incluyen síntomas urinarios, dolor corporal relacionado con la endoprótesis y dificultades sexuales lo que, en conjunto, puede influir gravemente en la calidad de vida de los pacientes y, esencialmente, en la salud general3-8.
Los autores han presentado la hipótesis de varias etiologías responsables de las complicaciones relacionadas con la endoprótesis, tales como irritación del triángulo vesical y reflujo renal7,9. A través de los años, los fabricantes han hecho innovaciones en el diseño y en los materiales de las endoprótesis a fin de mejorar los problemas causados por las mismas10,11, aun así, han fracasado en el diseño de una endoprótesis ideal que pueda reducir de manera significativa los efectos adversos11,12.
Dados los efectos de los bloqueantes α para aliviar los síntomas de las vías urinarias inferiores asociados con una vejiga hiperactiva y con la hiperplasia benigna de la próstata13, varios estudios investigaron el papel que desempeñan los agentes en los síntomas relacionados con la endoprótesis utilizando el Cuestionario de Síntomas de Endoprótesis Ureteral (USSQ, por sus siglas en inglés)13-17, la Puntuación Internacional de los Síntomas Prostáticos (IPSS, por sus siglas en inglés)17-24, el Puntaje Visual Analógico del Dolor (VAPS, por sus siglas en inglés)19-21,24, o evaluando los síntomas clínicos en una entrevista con los pacientes 25.
La tamsulosina bloquea selectivamente los receptores adrenérgicos α-1a/1d de los músculos lisos del uréter distal, del triángulo vesical, del cuello de la vejiga y de la próstata26. Se cree que la relajación del músculo liso reduce la resistencia de la vejiga, del cuello y de la uretra, lo que puede mejorar los síntomas de las vías urinarias inferiores relacionados con la endoprótesis17,18. Por consiguiente, el objetivo de este estudio clínico fue evaluar la eficacia de la tamsulosina para reducir los síntomas relacionados con la endoprótesis doble J en los pacientes que se someten a una cirugía de endoprótesis ureteral.
Métodos y materiales
Después de la aprobación del comité de ética, este estudio clínico prospectivo y aleatorio controlado por placebo y doble ciego se llevó a cabo entre junio de 2014 y julio de 2015 en el Hospital Sina, Teherán, Irán. El estudio actual fue registrado en www.clinicaltrials.gov como IRCT2015042221886N2.
Población de estudio y diseño
Se evaluó la elegibilidad de los pacientes que se sometieron a una endopróteis ureteral doble J realizada por un solo médico. Se colocaron las endoprótesis de rutina antes de la litotricia extracorporeal por ondas de choque (LEOC) o después de la nefrolitotomía percutánea (NLPC), ureterorrenoscopia (URS), endopielotomía endoscópica o ureterolitotomía transureteral (ULT) durante 4 semanas. Los pacientes mayores de 18 años como mínimo y con una endoprótesis ureteral doble J unilateral se inscribieron para el estudio después de obtener su consentimiento informado acerca de la asignación aleatoria del tratamiento y de los efectos secundarios posibles de la tamsulosina. El criterio de exclusión incluía a pacientes menores de 18 años, mujeres embarazadas, pacientes con endoprótesis bilaterales, endoprótesis ureterales olvidadas, colocación de endoprótesis ureterales de larga data, hiperplasia benigna de la próstata, resección prostática anterior, prostatitis, cáncer de próstata, neoplasia de vejiga, infección de las vías urinarias reciente o recurrente, antecedentes de dolor lumbar crónico, pacientes tratados previamente con bloqueantes α selectivos, pacientes con enfermedad cardiovascular grave y pacientes afectados por factores de riesgo para disfunción eréctil.
Procedimientos del estudio
De los 110 pacientes evaluados para ser elegidos, un total de 76 pacientes (47 hombres y 29 mujeres, de entre 20 y 74 años) dieron su consentimiento para participar en el estudio. Los pacientes se dividieron aleatoriamente en dos grupos, usando un programa de aleatorización por ordenador. En el grupo A, el grupo de caso, 38 pacientes (25 hombres y 13 mujeres) recibieron una dosis diaria de 0,4 mg de tamsulosina (Maxulosin®, Exir Pharmaceutical Co., Borujerd, Irán). En el grupo B, el grupo de control, 38 pacientes (25 hombres y 13 mujeres) recibieron un placebo una vez por día durante 4 semanas. A los pacientes se les entregaron envases numerados que contenían comprimidos sin nombre. Tanto a los participantes como a los médicos se les ocultó la medicación prescrita.
Antes del procedimiento operativo programado, se realizaron análisis de laboratorio de rutina e imágenes. En todos los pacientes, se utilizaron idénticas endoprótesis ureterales doble J flexibles, a pesar de que la longitud y el tamaño de las endoprótesis estuvieron adaptadas a cada paciente. La colocación de la endoprótesis se realizó con anestesia regional o general. El extremo distal en espiral de la endoprótesis fue la única parte de la endoprótesis introducida en la vejiga. Se usaron radiografías abdominales simples para garantizar el posicionamiento correcto de las endoprótesis. Para estandarizar el consumo de analgésicos, se recetó acetaminofeno de 500 mg para el control del dolor. No existieron complicaciones relacionadas con el procedimiento. Todos los procedimientos del estudio se realizaron según los estándares éticos del comité de ética de la Universidad de Ciencias Médicas de Teherán correspondientes a la experimentación en humanos y a la Declaración de Helsinki de 1975, según la revisión de 2009.
Evaluación del paciente y medición de resultados
Cuatro semanas después de la colocación de la endoprótesis, el mismo médico conversó con los pacientes sobre los síntomas relacionados con la endoprótesis, que incluyen dolor suprapúbico (fase de llenado y vaciado), hematuria, incontinencia urinaria, polaquiuria, disuria, tenesmo vesical, nicturia, dolor lumbar (fase de llenado y vaciado), dolor genital, lumbar o suprapúbico, o dolor genital durante la actividad sexual. Se les pidió a los pacientes que respondan las preguntas con respecto a la frecuencia de cada síntoma en una escala de Likert de cinco niveles: ‘nunca’, ‘rara vez’, ‘algunas veces’, ‘a menudo’ y ‘muy a menudo’.
Análisis estadísticos
Se realizaron análisis estadísticos usando SPSS ver. 20.0 (SPSS Inc., Chicago, IL, EE. UU.). Se obtuvieron estadísticas descriptivas para cada variable del estudio. Para comparar los dos grupos se utilizaron las pruebas Chi-square y t de Student, según correspondiera; los valores de p inferiores a 0,05 se consideraron importantes desde el punto de vista estadístico.
Resultados
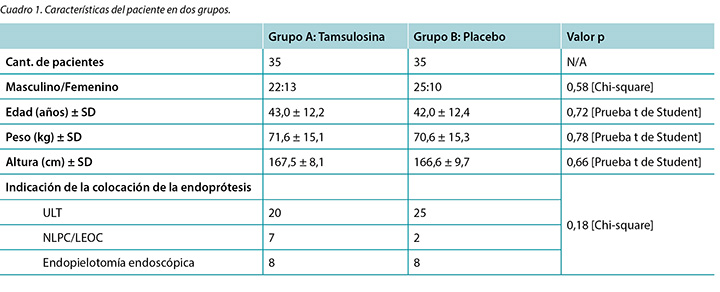
De los 76 pacientes inscritos, 70 (92,1 %) finalizaron el estudio. Los tratamientos fueron bien tolerados y ningún paciente tuvo que suspender la medicación debido a efectos adversos, y ninguno se sometió a una extracción de la endoprótesis antes de la fecha prevista. Las características de la población del estudio están representadas en el Cuadro 1. El grupo A (35 pacientes) consistía en 22 hombres y 13 mujeres (de una media de edad de 43,0 ± 12,2 años), y el grupo B consistía en 25 hombres y 10 mujeres (de una media de edad de 42,0 ± 12,4 años). Un total de 45 pacientes (64,2 %) se sometieron a litotricia transuretral, nueve pacientes (12,8 %) se sometieron a nefrolitotomía percutánea o LEOC, mientras que se les realizó estenosis de la unión ureteropélvica a 16 pacientes (22,8 %). No se encontraron diferencias desde el punto de vista estadístico con respecto a género, edad, altura ni tampoco indicación de colocación de la endoprótesis entre el grupo de caso y el de control.
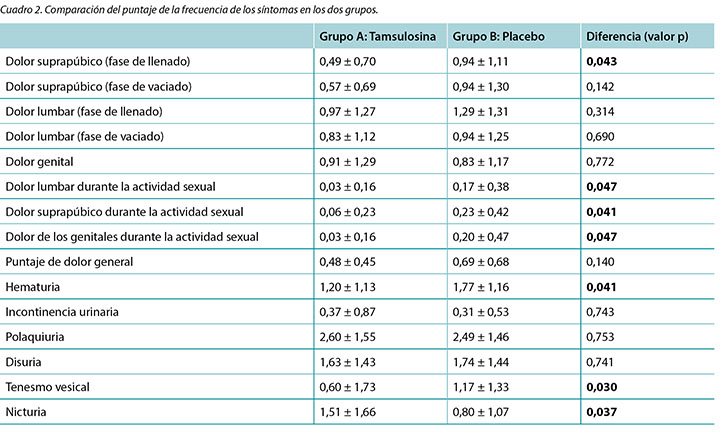
Se atribuyeron puntajes de 0 a 4 respectivamente para la frecuencia de la escala de los síntomas establecidos por los pacientes, en los que el 0 representaba ‘nunca’ y el 4 representaba ‘muy a menudo’. El Cuadro 2 resume los resultados generales de nuestro estudio. Se utilizó la prueba t de Student para analizar las diferencias de las medias entre los grupos. Según lo que se indica en el cuadro, los pacientes que recibieron tamsulosina manifestaron puntajes más altos (1,51 ± 1,66) para nicturia que los pacientes del grupo de control (0,80 ± 1,07) (p=0,037). El puntaje medio para el dolor en las áreas lumbares, suprapúbicas y genitales durante la actividad sexual fue inferior a los pacientes que recibieron tamsulosina en comparación con los pacientes que recibieron el placebo (valores p =0,047, 0,041 y 0,047, respectivamente). Los pacientes tratados con tamsulosina manifestaron menor dolor suprapúbico en los puntajes de la fase de llenado (0,49 ± 0,70) que el grupo de control (0,94 ± 1,11) (p=0,043). El puntaje medio de tenesmo vesical fue 0,6 en el grupo 1 y de 1,1 en el grupo placebo (p=0,030). No se encontraron diferencias importantes desde el punto de vista estadístico entre los dos grupos con respecto a hematuria, incontinencia urinaria, polaquiuria, disuria ni puntaje del dolor en general (valores p >0,05).
Discusión
Los resultados de este ensayo aleatorizado, doble ciego y controlado por placebo demostraron que la tamsulosina es eficaz para aliviar los síntomas relacionados con la endoprótesis, especialmente para aliviar el dolor durante la actividad sexual.
Las indicaciones actuales para las endoprótesis ureterales en condiciones de urgencia incluyen cólicos renales agudos insostenibles, pielonefritis obstructiva e insuficiencia renal secundaria a la obstrucción ureteral3. Después de la colocación de una endoprótesis se pueden realizar en varias situaciones procedimientos endoscópicos como medida de seguridad27, que incluyen edema ureteral, perforación ureteral, riñón único, trasplante de riñón y antecedentes de insuficiencia renal. También hay indicaciones relativas para las endoprótesis ureterales permanentes, tales como dilatación pasiva del orificio ureteral y del uréter, antes del LEOC en cálculos mayores a 2 cm, cálculos impactados de larga duración, procedimientos endoscópicos que duran más de 45 minutos y embarazo2,7.
Sin embargo, a pesar del uso extendido de las endoprótesis ureterales permanentes, existe una controversia considerable con respecto a la necesidad de la colocación de una endoprótesis después de una litroticia ureteroscópica sin complicaciones28. Incluso después de elegir el tamaño correcto de la endoprótesis y de la colocación adecuada, se asocia a las endoprótesis ureterales permanentes con morbilidades inevitables en más de 80 % de los pacientes29, que incluyen síntomas urinarios, hematuria, dolor y dificultades sexuales que llevan a una calidad de vida reducida relacionada con la salud6. Algunos investigadores informan que la posición y la integridad del bucle inferior de la endoprótesis y la atención adecuada y detallada durante toda la colocación de la endoprótesis afecta la gravedad del síntoma30,31. Por ejemplo, se tolera mejor una endoprótesis ureteral después de una inyección periureteral de toxina botulínica de tipo A después de la colocación de una endoprótesis, al reducir significativamente el dolor y la necesidad de narcóticos32.
Sin embargo, no se comprende totalmente la patofisiología exacta de los síntomas relacionados con la endoprótesis. Se supone que los factores responsables son los espasmos de los músculos lisos ureterales inferiores y la contracción involuntaria de la vejiga generada por la irritación del triángulo vesical que posee gran cantidad de neuronas, y el reflujo urinario a los riñones debido a la resistencia aumentada de la salida de la vejiga11,14,15,21,33. Se recomiendan los bloqueantesαcomo tratamientos expulsivos para los cálculos ureterales y para disminuir episodios de cólicos recurrentes. Se cree que alivian la morbilidad relacionada con la endoprótesis de diversas maneras34-36. Los receptores adrenérgicos α bloqueantes reducen la tonicidad muscular de la uretra prostática, del triángulo vesical y del uréter, lo que disminuye la resistencia de la salida de la vejiga, la presión de vaciamiento y el reflujo urinario17. Sin embargo, aún está por descubrirse mediante otras investigaciones la eficacia de estas medicaciones y los protocolos terapéuticos adecuados para aliviar los síntomas relacionados con la endoprótesis. Los resultados del estudio actual mostraron que la tamsulosina (un antagonista α1A selectivo) puede controlar las diferentes morbilidades relacionadas con las endoprótesis.
Diversos estudios han investigado la eficacia de los bloqueantes α para aliviar los síntomas relacionados con la endoprótesis, entre los que se incluyen pacientes que reciben alfuzosina 10 mg13,14,16,25,37, tamsulosina 0,4 mg15,17,22,23,17, tamsulosina 0,2 mg19,20, terazosina 4 mg21,38, terazosina 2 mg21 o un placebo para un tratamiento de 1 a 6 semanas. Damiano y cols.15 publicaron el primer informe de los beneficios de una dosis diaria de tamsulosina de 0,4 mg en un estudio prospectivo que comparaba la tamsulosina con placebo en 75 pacientes usando el USSQ. Si bien este estudio no era controlado ni por placebo ni por doble ciego, los autores encontraron que los pacientes que recibían tamsulosina habían mantenido mejor su salud general. En otro estudio realizado por Wang y cols.17 en 154 pacientes en el que se usó la misma herramienta de medición, los que recibieron tamsulosina manifestaron menos síntomas relacionados con la endoprótesis y una mejor calidad de vida con respecto a los pacientes que recibieron un placebo.
Lee y cols.19 y Lim y cols.20, utilizando tanto la IPSS como el VAPS, respectivamente, investigaron el efecto de una dosis menor de solo tamsulosina (0,2 mg una vez por día) y en combinación con tolterodina o solifenacina para los síntomas relacionados con la endoprótesis. Lee y cols. descubrieron que solo los puntajes de los síntomas de almacenamiento fueron puntajes significativamente más bajos en los pacientes que recibieron un tratamiento único o combinado que los pacientes tratados sin medicación. El autor expresó que la colocación correcta de la endoprótesis es, por consiguiente, más importante que la medicación para reducir los síntomas de almacenamiento relacionados con la endoprótesis19. En cambio, Lim demostró que el tratamiento combinado de tamsulosina y solifenacina puede mejorar más los síntomas tanto irritantes como obstructivos que la tamsulosina sola o comparado con el tratamiento sin medicación20; los resultados fueron confirmados más tarde por Shalaby y cols.23. Además, se encontró que la mejoría de los síntomas relacionados con la endoprótesis tratados con bloqueantes αera independiente del tipo de bloqueante α, según lo demostraron Dellis y cols.37 al comparar tamsulosina y alfuzosina. Según nuestro leal saber y entender, solo hay un estudio18 sobre la ineficacia del bloqueante α (doxazosina) para reducir síntomas relacionados con la endoprótesis.
En un metaanálisis reciente realizado por Lamb y cols.35 que incluía a 461 pacientes de cinco estudios, todos los estudios demostraron una reducción del puntaje del síntoma urinario según el USSQ y de los puntajes de los dolores corporales de los pacientes que recibían tamsulosina o alfuzosina. Sin embargo, la mejoría de los problemas sexuales y de la salud en general no fue significativa desde el punto de vista estadístico. Los resultados de otros 12 estudios que incluían un total de datos de 946 pacientes fueron metaanalizados por Yakoubi y cols.36. Los análisis demostraron una reducción importante en los puntajes de los síntomas urinarios y de dolor, así como también la mejoría de la salud general en los pacientes que recibían bloqueantes α.
En nuestro estudio, la reducción de los puntajes de dolor en pacientes tratados con tamsulosina era más evidente en comparación con el manifestado durante la actividad sexual en las tres áreas: lumbar, genital y suprapúbica. Se demostró que las endoprótesis ureterales afectaban la calidad de la vida sexual tanto en hombres como en mujeres8. Se indicó que la disfunción eréctil era la principal fuente de malestar sexual en los hombres, probablemente relacionado con los síntomas de las vías urinarias inferiores y la permanencia de la endoprótesis. En las mujeres, la sexualidad puede verse gravemente afectada como resultado de los malestares psicológicos relacionados con la endoprótesis8.
También se encontró que la tamsulosina es eficaz para reducir la hematuria y el tenesmo vesical, si bien los pacientes tratados con tamsulosina habían tenido un mayor índice de nicturia que los pacientes que habían recibido un placebo. Anteriormente, no se había informado que la nicturia fuera un efecto adverso de la tamsulosina, de modo que este hallazgo se debe investigar mediante estudios a mayor escala. Koseoglu y cols.39 encontraron que la tamsulosina no era eficaz para reducir la nicturia en los pacientes que se trataban por hiperplasia benigna de la próstata. En otro estudio, se encontró que la combinación de bloqueantes α con zolpidem reducían mejor la nicturia que los bloqueantes α solos40.
Nuestro estudio tenía varias limitaciones. Primero, el tamaño de nuestra muestra era estadísticamente pequeño para detectar pequeñas diferencias entre los dos grupos. Segundo, algunos pacientes no finalizaron el estudio. Tercero, utilizamos entrevistas clínicas con los pacientes para evaluar los síntomas urinarios, mientras que Joshi y cols.6 han desarrollado una herramienta específica para evaluar los síntomas relacionados con la endoprótesis llamado el USSQ. Cuarto, la cantidad de analgésicos utilizados por los pacientes no se informaban de manera confiable. Finalmente, no investigamos ningún efecto adverso provocado por el uso de bloqueantes α, aunque los tratamientos fueron bien tolerados y los pacientes no tuvieron que suspender la medicación debido a efectos colaterales. Por consiguiente, se deben realizar más estudios prospectivos y aleatorios a gran escala para obtener información más exacta.
Conclusión
El uso de tamsulosina de 0,4 mg una vez por día en pacientes con endoprótesis ureteral unilateral mejoró de manera significativa los síntomas urinarios relacionados con la endoprótesis, especialmente el dolor corporal durante la actividad sexual. Por consiguiente, se debe tener en cuenta la tamsulosina para los pacientes que se quejan de síntomas relacionados con la endoprótesis. En el futuro, serán necesarios más estudios prospectivos y aleatorios a gran escala.
Aprobación ética y consentimiento para participar
El consentimiento del paciente fue dado antes de la cirugía, basado en el código ético del Comité de Ética de la Universidad de Ciencias Médicas de Teherán. El estudio fue registrado en www.clinicaltrials.gov como IRCT2015042221886N2. La información se publica sin el nombre de los pacientes. Se puede brindar más información, datos y fotografías si se lo solicita.
Intereses contradictorios
Todos los autores indican que no existe contradicción potencial o conflicto de intereses.
Financiación
Ninguna.
Agradecimientos
Agradecemos especialmente al Centro de Investigación de Urología (Urology Research Center) de la Universidad de Ciencias Médicas de Teherán. (Tehran University of Medical Sciences).
Author(s)
Fateme Guitynavard
Urology Research Center, Tehran University of Medical Sciences, Tehran, Iran
Shahram Gooran
Urology Research Center, Tehran University of Medical Sciences, Tehran, Iran
Parvin Kasiri
Urology Research Center, Tehran University of Medical Sciences, Tehran, Iran
Farshad Gholipour
Urology Research Center, Tehran University of Medical Sciences, Tehran, Iran
Seyed Mohammad Kazem Aghamir*
Urology Research Center, Tehran University of Medical Sciences, Tehran, Iran
Email mkahamir@yahoo.com
* Corresponding author
References
- Zimskind PD, Fetter TR, Wilkerson JL. Clinical use of long-term indwelling silicone rubber ureteral splints inserted cystoscopically. J Urol 1967;97(5):840–844.
- Knudsen BE, Beiko DT, Denstedt JD. Stenting after ureteroscopy: pros and cons. Urol Clin North Am 2004;31(1):173–180.
- Chew BH, Knudsen BE, Denstedt JD. The use of stents in contemporary urology. Curr Opin Urol 2004;14(2):111–115.
- Damiano R, Oliva A, Esposito C, De Sio M, Autorino R, D’Armiento M. Early and late complications of double pigtail ureteral stent. Urologia Int 2002;69(2):136–140.
- Haleblian G, Kijvikai K, de la Rosette J, Preminger G. Ureteral stenting and urinary stone management: a systematic review. J Urol 2008;179(2):424–430.
- Joshi H, Newns N, Stainthorpe A, MacDonagh R, Keeley F, Timoney A. Ureteral stent symptom questionnaire: development and validation of a multidimensional quality of life measure. J Urol 2003;169(3):1060–1064.
- Miyaoka R, Monga M. Ureteral stent discomfort: etiology and management. IJU 2009;25(4):455.
- Sighinolfi M, Micali S, De Stefani S, Mofferdin A, Grande A, Giacometti, M, et al. Indwelling ureteral stents and sexual health: a prospective, multivariate analysis. J Urol 2007;178(1):229–231.
- Ecke TH, Bartel P, Hallmann, S, Ruttloff J. Evaluation of symptoms and patients’ comfort for JJ-ureteral stents with and without antireflux-membrane valve. Urol 2010;75(1):212–216.
- Lingeman JE, Preminger GM, Goldfischer ER, Krambeck AE, Team CS. Assessing the impact of ureteral stent design on patient comfort. J Urol 2009;181(6):2581–2587.
- Thomas R. Indwelling ureteral stents: impact of material and shape on patient comfort. J Endourol 1993;7(2):137–140.
- Candela J, Bellman G. Ureteral stents: impact of diameter and composition on patient symptoms. J Endourol 1997;11(1):45.
- Park SC, Jung SW, Lee JW, Rim JS. The effects of tolterodine extended release and alfuzosin for the treatment of double-J stent-related symptoms. J Endourol 2009;23(11):1913–1917.
- Beddingfield R, Pedro RN, Hinck B, Kreidberg C, Feia K, Monga M. Alfuzosin to relieve ureteral stent discomfort: a prospective, randomized, placebo controlled study. J Urol 2009;181(1):170–176.
- Damiano R, Autorino R, De Sio M, Giacobbe A, Palumbo IM, D’Armiento M. Effect of tamsulosin in preventing ureteral stent-related morbidity: a prospective study. J Endourol 2008;22(4):651–656.
- Deliveliotis C, Chrisofos M, Gougousis E, Papatsoris A, Dellis A, Varkarakis IM. Is there a role for alpha1-blockers in treating double-J stent-related symptoms? Urology 2006;67(1):35–39. doi:10.1016/j.urology.2005.07.038
- Wang C-J, Huang S-W, Chang C-H. Effects of specific α-1A/1D blocker on lower urinary tract symptoms due to double-J stent: a prospectively randomized study. Urol Res 2009;37(3):147–152.
- Kuyumcuoglu U, Eryildirim B, Tuncer M, Faydaci G, Tarhan F, Ozgül A. Effectiveness of medical treatment in overcoming the ureteral double-J stent related symptoms. Can Urol Assoc J 2012;6(6):e234–237.
- Lee SJ, Yoo C, Oh CY, Lee YS, Cho, ST, Lee SH, et al. Stent position is more important than α-blockers or anticholinergics for stent-related lower urinary tract symptoms after ureteroscopic ureterolithotomy: a prospective randomized study. Korean J Urol 2010;51(9):636–641.
- Lim KT, Kim YT, Lee TY, Park SY. Effects of tamsulosin, solifenacin, and combination therapy for the treatment of ureteral stent related discomforts. Korean J Urol 2011;52(7):485–488.
- Mokhtari G, Shakiba M, Ghodsi S, Farzan A, Heidari Nejad S, Esmaeili S. Effect of terazosin on lower urinary tract symptoms and pain due to double-J stent: a double-blind placebo-controlled randomized clinical trial. Urologia Int 2011;87(1):19–22.
- Navanimitkul N, Lojanapiwat B. Efficacy of tamsulosin 0.4 mg/day in relieving double-J stent-related symptoms: a randomized controlled study. J Int Med Res 2010;38(4):1436–1441.
- Shalaby E, Ahmed A.-f, Maarouf A, Yahia I, Ali M, Ghobish A. Randomized controlled trial to compare the safety and efficacy of tamsulosin, solifenacin, and combination of both in treatment of double-j stent-related lower urinary symptoms. Adv Urol 2013.
- Wang C-J, Huang S-W, Chang C-H. Effects of tamsulosin on lower urinary tract symptoms due to double-J stent: a prospective study. Urologia Int 2008;83(1):66–69.
- Nazim SM, Ather MH. Alpha-blockers impact stent-related symptoms: a randomized, double-blind, placebo-controlled trial. J Endourol 2012;26(9):1237–1241.
- Shibasaki M, Sudoh K, Inagaki O, Uchida W, Honda K. Effect of the optical isomers of YM‐12617 on increased intra‐urethral pressure induced by phenylephrine in anaesthetized dogs. J Autonom Pharmacol 1992;12(4):263–268.
- Jeong H, Kwak C, Lee S. Ureteric stenting after ureteroscopy for ureteric stones: a prospective randomized study assessing symptoms and complications. BJU Int 2004;93(7):1032–1034.
- Nabi G, Cook J, N’Dow J, McClinton S. Outcomes of stenting after uncomplicated ureteroscopy: systematic review and meta-analysis. BMJ 2007;334(7593):572.
- Joshi H, Stainthorpe A, MacDonagh R, Keeley F, Timoney A. Indwelling ureteral stents: evaluation of symptoms, quality of life and utility. J Urol 2003;169(3):1065–1069.
- Jeon SS, Choi YS, Hong JH. Determination of ideal stent length for endourologic surgery. J Endourol 2007;21(8):906–910.
- Rane A, Saleemi A, Cahill D, Sriprasad S, Shrotri N, Tiptaft R. Have stent-related symptoms anything to do with placement technique? J Endourol 2001;15(7):741–745.
- Gupta M, Patel T, Xavier K, Maruffo F, Lehman D, Walsh R, Landman J. Prospective randomized evaluation of periureteral botulinum toxin type A injection for ureteral stent pain reduction. J Urol 2010;183(2):598–602.
- Duvdevani M, Chew BH, Denstedt JD. Minimizing symptoms in patients with ureteric stents. Curr Opin Urol 2006;16(2):77–82.
- Dellis A, Joshi HB, Timoney AG, Keeley FX. Relief of stent related symptoms: review of engineering and pharmacological solutions. J Urol 2010;184(4):1267–1272.
- Lamb AD, Vowler SL, Johnston R, Dunn N, Wiseman OJ. Meta‐analysis showing the beneficial effect of α‐blockers on ureteric stent discomfort. BJU Int 2011;108(11):1894–1902.
- Yakoubi R, Lemdani M, Monga M, Villers A, Koenig P. Is there a role for α-blockers in ureteral stent related symptoms? A systematic review and meta-analysis. J Urol 2011;186(3):928–934.
- Dellis AE, Keeley FX, Manolas V, Skolarikos AA. Role of α-blockers in the treatment of stent-related symptoms: a prospective randomized control study. Urol 2014;83(1):56–62.
- Tehranchi A, Rezaei Y, Khalkhali H, Rezaei M. Effects of terazosin and tolterodine on ureteral stent related symptoms: a double-blind placebo-controlled randomized clinical trial. Int Braz J Urol 2013;39(6):832–840.
- Koseoglu H, Aslan G, Ozdemir I, Esen A. Nocturnal polyuria in patients with lower urinary tract symptoms and response to alpha-blocker therapy. Urol 2006;67(6):1188–1192.
- Song YS, Ku JH. Zolpidem pharmacotherapy combined with alpha-blocker therapy for nocturia unresponsive to alpha-blocker monotherapy in men with lower urinary tract symptoms: a preliminary study. Int Urol Nephrol 2007;39(4):1147–1152.



