Volume 39 Number 3
Effect of tamsulosin on lower urinary tract symptoms related to double-J ureteral stent: a randomised, double-blinded, placebo controlled trial
Fateme Guitynavard, Shahram Gooran, Parvin Kasiri, Farshad Gholipour and Seyed Mohammad Kazem Aghamir
Keywords urethral stent, stent-related symptoms, lower urinary tract symptoms, tamsulosin, double-J
For referencing Guitynavard F et al. Effect of tamsulosin on lower urinary tract symptoms related to double-J ureteral stent: a randomised, double-blinded, placebo controlled trial. WCET® Journal 2019; 39(3):26-31
DOI https://doi.org/10.33235/wcet.39.3.26-31
Abstract
Objective To evaluate the effect of tamsulosin on stent-related symptoms in patients undergoing double-J ureteral stenting.
Methods and materials Seventy patients (47 men and 23 women; mean age 42.5 years) who underwent double-J stent placement in adjunct to urological surgery were prospectively randomised into two groups. Group 1 included 35 patients who received 0.4 mg of tamsulosin once daily for 4 weeks; group 2 included 35 patients who received a placebo for the same protocol. All patients were interviewed by the same physician about the frequency of stent-related symptoms at 4 weeks after stent insertion.
Results Patients in group 1 showed a lower score for suprapubic pain during the filling phase and lower pain during sexual activity than group 2, although the overall pain score was not significantly different between two groups. The mean urinary urgency score was less in group 1 in comparison to the placebo group (p=0.030). No statistically significant differences were found between two groups concerning haematuria, urinary incontinence, frequency nor dysuria.
Conclusion Tamsulosin improves symptoms associated with double-J ureteral stents, especially body pain during sexual activity.
Introduction
Indwelling ureteral stents are a commonly used tool in urologic practices. Zimskind et al.1 described ureteral stent placement for the first time in 1967. However, despite the documented benefits of double-J stents in preventing ureteral obstruction after urologic procedures2, patients may experience stent-related symptoms and some morbidities, including urinary symptoms, stent-related body pain and sexual difficulties which, together, can severely influence the patients’ quality of life and general health substantially3-8.
Authors have hypothesised several aetiologies responsible for stent-related complications such as bladder trigone irritation and renal reflux7,9. Through the years, manufacturers have made innovations in stent design and materials in order to improve stent-caused problems10,11, yet have failed to design an ideal stent which can significantly reduce adverse effects11,12.
Given the effect of α-blockers in alleviating lower urinary tract symptoms associated with overactive bladder and benign prostate hyperplasia13, several studies investigated the role of these agents on stent-related symptoms using the Ureteral Stent Symptom Questionnaire (USSQ)13-17, the International Prostate Symptom Score (IPSS)17-24, the Visual Analog Pain Score (VAPS)19-21,24, or evaluation of clinical symptoms by interviewing the patients25.
Tamsulosin selectively blocks α-1a/1d adrenergic receptors in smooth muscles of distal ureter, bladder trigone, bladder neck and prostate26. Smooth muscle relaxation is believed to reduce bladder, neck and urethral resistance, which can improve stent-related lower urinary tract symptoms17,18. The purpose of this clinical trial was therefore to evaluate the effectiveness of tamsulosin in reducing double-J stent-related symptoms in patients undergoing ureteral stenting.
Methods and Materials
After ethics committee approval, this prospective double-blinded and placebo controlled randomised clinical trial was carried out between June 2014 and July 2015 in Sina Hospital, Tehran, Iran. The current trial was registered at www.clinicaltrials.gov as IRCT2015042221886N2.
Study population and design
Patients who underwent a double-J ureteral stenting by a single surgeon were assessed for eligibility. Stents were routinely placed before extracorporeal shock wave lithotripsy (ESWL) or following percutaneous nephrolithotomy (PCNL), ureterorenoscopy (URS), endoscopic endopyelotomy, or transureteral ureterolithotomy (TUL) for 4 weeks. Patients with at least 18 years of age and with an unilateral double-J ureteral stent were enrolled into the study after obtaining informed consent about random allocation of treatment and potential side effects of tamsulosin. The exclusion criteria included patients younger than 18 years, pregnant women, patients with bilateral stents, forgotten ureteral stent, long-standing ureteral stent placement, benign prostatic hyperplasia, previous prostatic resection, prostatitis, prostate cancer, bladder neoplasms, recent or recurrent urinary tract infection, history of chronic flank pain, patients previously treated with selective α-blockers, patients with severe cardiovascular disease, and patients affected by risk factors for erectile dysfunction.
Study procedure
Out of 110 patients who were assessed for eligibility, a total of 76 patients (47 men and 29 women, aged 20–74 years) who gave consent were enrolled in the study. Patients were randomly allocated into two groups using a computer randomisation program. In group A, the case group, 38 patients (25 men and 13 women) received a daily 0.4 mg dose of tamsulosin (Maxulosin®, Exir Pharmaceutical Co., Borujerd, Iran). In group B, the control group, 38 patients (25 men and 13 women) received a placebo once a day for 4 weeks. The patients were given numbered containers enclosing unnamed pills. Both participants and physicians were kept blinded to the medication being prescribed.
Before the scheduled operative procedure, routine laboratory tests and imaging were performed. In all patients, an identical flexible double-J ureteral stent was used, although the length and size of stents were individualised for each patient. Stent placement was done under regional or general anaesthesia. The coiled distal end of the stent was the only part of the stent presented in the bladder. Plain abdominal X-ray film was used to assure correct stent positioning. To standardise analgesic consumption, acetaminophen 500 mg was prescribed for pain control. No procedure-related complication occurred. All study procedures were in accordance with the ethical standards of the ethics committee of Tehran University of Medical Sciences on human experimentation and with the Helsinki Declaration of 1975, as revised in 2009.
Patient assessment and outcome measurements
Four weeks after stent placement, patients were interviewed by the same physician about stent-related symptoms including suprapubic pain (filling and voiding phase), haematuria, urinary incontinence, urinary frequency, dysuria, urinary urgency, nocturia, flank pain (filling and voiding phase), genitalia pain, and flank, suprapubic or genitalia pain during sexual activity. Patients were asked to answer the questions regarding the frequency of each symptom in a five-level Likert scale – ‘never’, ‘rarely’, ‘sometimes’, ‘often’, and ‘very often’.
Statistical analysis
Statistical analysis was performed using SPSS ver. 20.0 (SPSS Inc., Chicago, IL, USA). Descriptive statistics were obtained for each study variable. Chi-square, and student’s t-test were used for comparison between the two groups as appropriate; values of p less than 0.05 were considered statistically significant.
Results
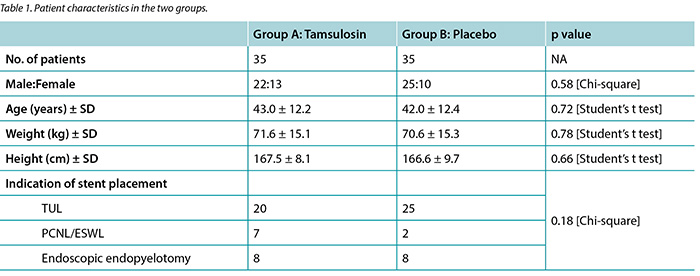
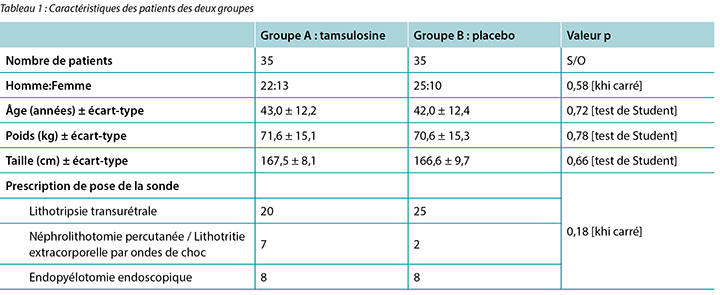
Out of 76 enrolled patients, 70 (92.1%) completed the study. Therapies were well tolerated and no patients had to terminate medication owing to adverse effects, and none underwent stent removal prior to the due date. Characteristics of the study population are presented in Table 1. Group A (35 patients) consisted of 22 men and 13 women (mean age 43.0 ± 12.2 years), and group B consisted of 25 men and 10 women (mean age 42.0 ± 12.4 years). A total of 45 patients (64.2%) underwent transurethral lithotripsy, nine patients (12.8%) underwent percutaneous nephrolithotripsy or ESWL, while endopyelotomy for ureteropelvic junction stricture was performed in 16 patients (22.8%). No statistically significant differences were found regarding gender, age, weight, height, nor indication of stent placement between the case and control groups.
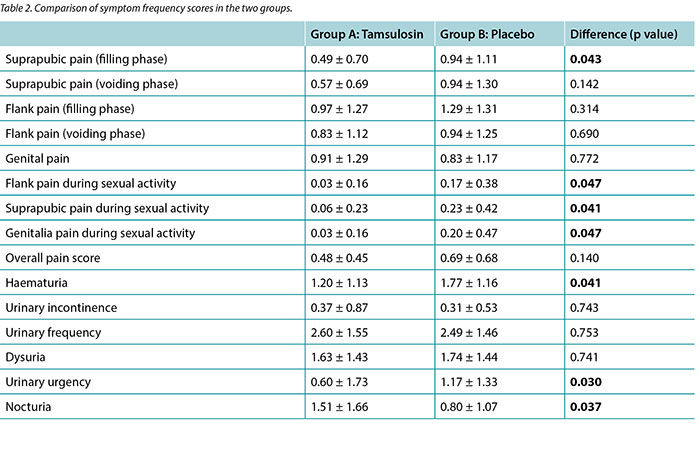
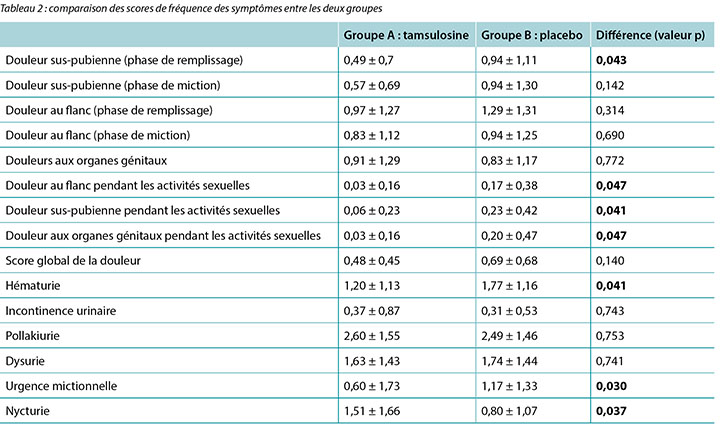
Scores 0 to 4 were attributed respectively to the frequency of scale of symptoms stated by patients, with 0 representing ‘never’ and 4 representing ‘very often’. Table 2 summarises the overall results of our study. Student’s t-test was used to examine the differences of means between groups. As shown in the table, patients receiving tamsulosin expressed higher scores (1.51 ± 1.66) for nocturia than patients in the control group (0.80 ± 1.07) (p=0.037). The mean score for pain in the flank, suprapubic and genital areas during sexual activity was lower in patients receiving tamsulosin in comparison to patients receiving the placebo (p values=0.047, 0.041 and 0.047, respectively). Patients treated with tamsulosin showed lower suprapubic pain in filling phase scores (0.49 ± 0.70) than the control group (0.94 ± 1.11) (p=0.043). The mean urinary urgency score was 0.6 in group 1 and 1.1 in the placebo group (p=0.030). No statistically significant differences were found between the two groups concerning haematuria, urinary incontinence, frequency, dysuria, nor overall pain score (p values >0.05).
Discussion
The results of this double-blind, randomised, placebo-controlled study showed that tamsulosin is effective in relieving stent-related symptoms specially in alleviating pain during sexual activity.
Current indications for ureteral stents in urgent conditions include unbearable acute renal colic, obstructive pyelonephritis and renal failure secondary to ureteral obstruction3. Endoscopic procedures can be followed by stent placement as a safety measure27 in several situations, including ureteral oedema, ureteral perforation, solitary kidney, transplant kidney and history of renal failure. There are also relative indications for indwelling ureteral stents such as passive dilation of ureteral orifice and ureter, before ESWL in stones larger than 2 cm, long-lasting impacted stone, endoscopic procedures lasting over 45 minutes, and pregnancy2,7.
However, despite widespread use of indwelling ureteral stents, there is considerable controversy over the necessity of stent placement after uncomplicated ureteroscopic lithotripsy28. Even after choosing the correct stent size and proper placement, indwelling ureteral stents are associated with inevitable morbidities in over 80% of patients29, including urinary symptoms, haematuria, pain and sexual difficulties which all lead to reduced health-related quality of life6. Some researchers report that the position and completeness of the stent’s lower loop and proper attention to detail throughout stent placement have an effect on symptom severity30,31. For example, an ureteral stent was better tolerated after periureteral injection of botulinum toxin type A after stent placement by significantly decreasing pain and narcotic requirement32.
However, the exact pathophysiology of stent-related symptoms is not fully understood. It is assumed that lower ureteral smooth muscle spasms, involuntary bladder contraction triggered by neuronal-rich trigone irritation, and urine reflux to the kidneys due to increased bladder outlet resistance are responsible factors11,14,15,21,33. α-blockers are recommended as expulsive therapy for ureteral stones and to decrease recurrent colic episodes. They are believed to relieve stent-related morbidity by different ways34-36. Blocking α-adrenergic receptors reduces muscle tone of prostatic urethra, bladder trigone and ureter which leads to decreased bladder outlet resistance, voiding pressure, and urinary reflux17. However, the effectiveness of these medications and proper therapeutic protocols for alleviation of stent-related symptoms are yet to be discovered by further investigations. Results of the current study showed that tamsulosin (a selective α1A antagonist) can control several stent-related morbidities.
The effectiveness of α-blockers in relieving stent-related symptoms has been investigated by several studies, including patients receiving either alfuzosin 10 mg13,14,16,25,37, tamsulosin 0.4 mg15,17,22,23,17, tamsulosin 0.2 mg19,20, terazosin 4 mg21,38, terazosin 2 mg21, or a placebo for 1–6 weeks’ treatment. Damiano et al.15 released the first report of the benefits of a daily dose of tamsulosin 0.4 mg in a prospective study comparing tamsulosin to placebo in 75 patients using the USSQ. Although this study was not double-blinded nor placebo-controlled, the authors found that patients receiving tamsulosin had their general health better preserved. In another study performed by Wang et al.17 on 154 patients using the same measurement tool, those receiving tamsulosin showed lower stent-related symptoms and better quality of life than patients receiving a placebo.
Using both IPSS and VAPS, the effect of lower dose of tamsulosin (0.2 mg once a day) alone and in combination with tolterodin or solifenacin on stent-related symptoms was investigated by Lee et al.19 and Lim et al.20, respectively. Lee et al. found that only the storage symptom scores were significantly lower in patients receiving either mono- or combination therapy than patients treated with no medication. The author stated that correct placement of the stent is therefore more important than medication in reducing stent-related storage symptoms19. Conversely, Lim showed that combination therapy with tamsulosin and solifenacin can better improve both irritative and obstructive symptoms than tamsulosin alone or compared to receiving no medication20; the results were later confirmed by Shalaby et al.23. Further, improvement of stent-related symptoms by α-blockers was found to be independent to the type of α-blocker, as showed by Dellis et al.37 comparing tamsulosin and alfuzosin. To the best of our knowledge, there is only one study18 on α-blocker (doxazosin) ineffectiveness in reducing stent-related symptoms.
In a recent meta-analysis performed by Lamb et al.35 including 461 patients from five studies, all studies showed a reduction in the USSQ urinary symptom score and body pain scores in patients receiving either tamsulosin or alfuzosin. However, general health and sexual matters improvement were not statistically significant. Results of a further 12 studies including a total number of 946 patients’ data were meta-analysed by Yakoubi et al.36. Analyses showed a significant reduction in urinary symptoms and pain scores as well as general health improvement in patients receiving α-blockers.
In our study, the reduction in pain scores in patients treated with tamsulosin was more evident when compared to during sexual activity in all three areas – flank, genital and suprapubic. Ureteral stents were showed to impair the quality of sexual life in both men and women8. Erectile dysfunction was indicated as the main source of sexual distress in men, probably related to lower urinary tract symptoms and stent permanence. In women, sexuality can be severely impaired as a result of stent-related psychological distresses8.
We also found tamsulosin effective in reducing haematuria and urinary urgency, although, patients treated with tamsulosin had increased rate of nocturia than patients receiving placebo. Nocturia has not reported as an adverse effect of tamsulosin previously, so this finding should be investigated by larger-scale studies. Koseoglu et al.39 found tamsulosin ineffective in reducing nocturia in patients being treated for benign prostatic hyperplasia. In another study, combination of α-blockers with zolpidem was shown to better reduce nocturia than α-blockers alone40.
Our study had several limitations. First, our sample size was statistically small in order to detect small differences between two groups. Second, some patients did not complete the study. Third, we utilised clinical interviews with the patients to evaluate urinary symptoms, whereas Joshi et al.6 has developed a specific tool for assessing stent-related symptoms called the USSQ. Fourth, the quantity of the analgesics used by patients was not reliably reported. Finally, we did not investigate any adverse effects made by α-blocker use, although therapies were well tolerated and no patients had to discontinue medication owing to side effects. Therefore, further large-scale, randomised, prospective studies are needed to obtain more accurate information.
Conclusion
The use of tamsulosin 0.4 mg once daily in patients with unilateral ureteral stenting significantly improved stent-related urinary symptoms, especially the body pain during sexual activity. Therefore, tamsulosin should be considered for patients who complain of stent-related symptoms. In the future, large-scale, prospective and randomised studies will be needed.
Ethics approval and consent to participate
Patient consent was undertaken before surgery based on the ethical code of the Tehran University of Medical Sciences Ethics Committee. This trial was registered at www.clinicaltrials.gov as IRCT2015042221886N2. The information is published without the name of the patients. Information, data and photos can be provided if requested.
Competing interests
All authors claim that there is not any potential competing or conflict of interest.
Funding
None.
Acknowledgements
Special thanks to the Urology Research Center, Tehran University of Medical Sciences.
Effet de la tamsulosine sur les symptômes des voies urinaires inférieures découlant d’une sonde urétérale de type double J : essai en double aveugle randomisé contrôlé avec placebo
Fateme Guitynavard, Shahram Gooran, Parvin Kasiri, Farshad Gholipour and Seyed Mohammad Kazem Aghamir
DOI: https://doi.org/10.33235/wcet.39.3.26-31
Résumé
Objectif Évaluer les effets de la tamsulosine sur les symptômes liés aux sondes (endoprothèses) urétérales de type double J.
Méthodes et matériels utilisés Soixante-dix patients (47 hommes et 23 femmes d’une moyenne d’âge de 42,5 ans) ayant subi la pose d’une sonde de type double J en complément d’une intervention urologique ont été prospectivement randomisés en deux cohortes. Le premier groupe comprenait 35 patients ayant pris 0,4 mg de tamsulosine une fois par jour pendant
4 semaines. Le deuxième groupe se composait de 35 patients ayant reçu un placebo dans le cadre du même protocole. Tous les patients ont discuté avec le même médecin de la fréquence des symptômes liés à la sonde 4 semaines après sa mise en place.
Résultats Les scores de douleurs sus-pubiennes pendant la phase de remplissage et pendant les activités sexuelles du groupe 1 étaient inférieurs à ceux du groupe 2, même si le score d'évaluation globale de la douleur entre les deux groupes ne différait pas grandement. Le score moyen d’urgence mictionnelle du groupe 1 était inférieur à celui du groupe placebo (p = 0,030). Aucune différence majeure d’un point de vue statistique n’a été décelée entre les deux groupes en matière d’hématurie, d’incontinence urinaire, de pollakiurie ou de dysurie.
Conclusion La tamsulosine atténue les symptômes liés à une sonde urétérale de type double J, notamment les douleurs corporelles pendant les activités sexuelles.
Introduction
Des sondes urétérales à demeure sont couramment utilisées dans les pratiques urologiques. Zimskind et al.1 ont décrit la toute première pose d’une sonde en 1967. Pourtant, malgré les avantages démontrés des sondes double J dans la prévention des obstructions urétérales après des procédures urologiques,2 les patients peuvent présenter des symptômes et des morbidités (problèmes urinaires, douleurs corporelles et problèmes sexuels provoqués par la sonde) qui, ensemble, peuvent grandement nuire à la qualité de vie du patient et à son état de santé général.3-8
Des auteurs ont émis des hypothèses sur les étiologies des complications liées aux sondes, comme l’irritation du trigone vésical et les reflux rénaux.7, 9 Si au fil des années, les innovations ont été nombreuses dans le domaine des sondes et accessoires afin d’éviter les problèmes,10, 11 la sonde idéale sans réel effet secondaire n’existe toujours pas.11, 12
Étant donné l’effet des alpha-bloquants sur l’atténuation des symptômes des infections des voies urinaires inférieures associés à une vessie hyperactive et à une hyperplasie bénigne de la prostate,13 plusieurs études se sont penchées sur le rôle de ces agents sur les symptômes liés aux sondes. Ont été utilisés à cet égard l’Ureteral Stent Symptom Questionnaire (USSQ)13-17, l’International Prostate Symptom Score (IPSS)17-24, l’échelle visuelle analogue de la douleur (Visual Analog Pain Score, VAPS)19-21, 24 et un examen des symptômes cliniques par des entretiens menés avec des patients.25
La tamsulosine bloque de manière sélective les adréno-récepteurs alpha-1a/1d des muscles lisses de l’urètre distal, du trigone vésical, du col vésical et de la prostate.26 Le relâchement des muscles lisses réduirait la résistance de la vessie, du col vésical et de l’urètre et est susceptible d’atténuer les symptômes des voies urinaires inférieures liés aux sondes.17, 18 L’objectif de cet essai clinique était donc d’évaluer l’efficacité de la tamsulosine à atténuer les symptômes chez les patients porteurs d’une sonde urétérale double J.
Méthodes et matériel utilisés
Après avoir obtenu l’approbation du comité d'éthique, cet essai clinique prospectif en double aveugle randomisée contrôlé avec placebo s’est déroulé de juin 2014 à juillet 2015 à l’hôpital de Sina, à Téhéran, en Iran. Cet essai a été enregistré sur www.clinicaltrials.gov avec comme référence IRCT2015042221886N2.
Population et méthodologie
Des patients porteurs d’une sonde urétérale de type double J posée par un chirurgien ont été évalués pour voir s’ils pouvaient participer à l’essai. Les sondes étaient généralement posées avant une lithotripsie extracorporelle par ondes de choc (ESWL) ou après une néphrolithotomie percutanée (PCNL), une urétérorénoscopie (URS), une endopyélotomie endoscopique ou une urétérolithotomie transurétrale (TUL), pour une durée de 4 semaines. Des patients âgés de plus de 18 ans et porteurs d’une sonde urétérale de type double J unilatérale ont été inscrits pour participer à l’étude après avoir reçu un formulaire de consentement éclairé sur l’attribution aléatoire de traitements et sur les effets secondaires potentiels de la tamsulosine. Les critères d’exclusion étaient les suivants : être âgé de moins de 18 ans, une grossesse, le port d’une sonde bilatérale, une sonde urétérale oubliée, la pose d’une sonde urétérale de longue date, une hyperplasie bénigne de la prostate, une ancienne résection prostatique, une prostatite, un cancer de la prostate, des néoplasmes de la vessie, une infection des voies urinaires récente ou récurrente, des antécédents de douleurs chroniques au flanc, avoir déjà reçu un traitement d’alpha-bloquants sélectifs, souffrir d’une maladie cardiovasculaire grave et présenter des facteurs de risques de dysfonction érectile.
Procédure
Sur 110 patients considérés, un total de 76 (47 hommes et 29 femmes âgés de 20 à 74 ans) ayant donné leur consentement ont été inscrits pour participer à l’étude. Les patients ont été répartis au hasard pour former deux groupes à l’aide d’un programme informatique de répartition aléatoire. Dans le groupe A (groupe expérimental) 38 patients (25 hommes et 13 femmes) ont reçu une dose quotidienne de 0,4 mg de tamsulosine (Maxulosin®, Exir Pharmaceutical Co., Borujerd, Iran). Dans le groupe B (groupe témoin), 38 patients (25 hommes et 13 femmes) ont reçu un placebo une fois par jour pendant quatre semaines. Les patients ont reçu des récipients numérotés contenant des comprimés non identifiés. Les participants tout comme les médecins n’ont pas été informés des médicaments prescrits.
Avant l’intervention chirurgicale prévue, des tests individuels en laboratoire et des examens d’imagerie médicale ont été effectués. Tous les patients ont bénéficié de la même sonde urétérale de type double J, seules la longueur et la taille de la sonde différaient d’un patient à un autre. La pose de la sonde s’est déroulée sous anesthésie locale ou générale. L’extrémité distale en spirale de la sonde est la seule partie de la sonde présente dans la vessie. Des radiographies normales de l’abdomen ont été réalisées pour s’assurer de la bonne mise en place de la sonde. Afin de standardiser la prise d’analgésiques, de l’acétaminophène 500 mg a été prescrit contre les douleurs. Il n’y a eu aucune complication en lien avec la procédure. Toutes les procédures de l’étude se sont déroulées conformément aux normes déontologiques du comité d’éthique de l’université de médecine de Téhéran sur l’expérimentation humaine et de la Déclaration d’Helsinki de 1975, révisée en 2009.
Examen des patients et évaluation des résultats
Quatre semaines après la pose de la sonde, les patients se sont entretenus avec le même docteur pour discuter des symptômes en lien avec la sonde, comme : douleurs sus-pubiennes (phases de remplissage et de miction), hématurie, incontinence urinaire, pollakiurie, dysurie, urgence mictionnelle, nycturie, douleurs au flanc (phases de remplissage et de miction), douleurs aux organes génitaux, et douleurs sus-pubiennes, au flanc ou aux organes génitaux pendant les activités sexuelles. Il a été demandé aux patients de répondre à des questions sur la fréquence de chaque symptôme sur l’échelle de Likert allant de 1 à 5 comme suit : « Jamais », « Rarement », « Parfois », « Souvent » et « Très souvent ».
Analyses statistiques
Des analyses statistiques ont été effectuées à l’aide de la SPSS ver. 20.0 (SPSS Inc., Chicago, IL, États-Unis). Des statistiques descriptives ont été obtenues pour chaque variable de l’étude. Le test de khi carré et le test de Student ont été utilisés pour comparer les deux groupes de manière appropriée. Les valeurs p inférieures à 0,05 ont été considérées comme significatives d’un point de vue statistique.
Résultats
Sur 76 patients inscrits à l’étude, 70 (92,1 %) sont allés jusqu’au bout. Les thérapies ont été bien tolérées et aucun patient n’a dû cesser de prendre les médicaments en raison d’effets secondaires. Aucun n’a dû se faire retirer la sonde avant la date prévue. Les caractéristiques de la population étudiée sont présentées dans le tableau 1. Le groupe A (35 patients) comprenait 22 hommes et 13 femmes (âge moyen 43 ans ± 12,2 ans) et le groupe B, 25 hommes et 10 femmes (âge moyen 42 ans ± 12,4 ans). Un total de 45 patients (64,2 %) ont subi une lithotritie transurétrale, 9 patients (12,8 %) une néphrolithotripsie percutanée ou une lithotripsie extracorporelle par ondes de choc, et 16 patients (22,8 %) une endopyélotomie pour rétrécissement de jonction pyélo-urétérale. Aucune différence statistique significative n’a été décelée en termes de genre, d’âge, de poids, de taille ou de prescription d’emplacement de la sonde entre le groupe expérimental et le groupe témoin.
Des scores compris entre 0 et 4 ont été attribués à la fréquence des symptômes indiqués par les patients, sur une échelle de valeurs où 0 correspond à « Jamais » et 4 à « Très souvent ». Le tableau 2 résume l’ensemble des résultats de notre étude. Le test de Student a servi à examiner les différences de moyennes entre les groupes. Comme l’indique le tableau, les patients ayant reçu de la tamsulosine ont des scores (1,51 ± 1,66) de nycturie plus élevés que les patients du groupe témoin (0,80 ± 1,07) (p = 0,037). Le score moyen des douleurs au flanc, sus-pubiennes et aux organes génitaux pendant les activités sexuelles était plus bas chez les patients ayant reçu de la tamsulosine que chez les patients ayant reçu le placebo (valeurs p respectives de 0,047, 0,041 et 0,047). Les patients ayant reçu de la tamsulosine ont manifesté des douleurs sus-pubiennes en phase de remplissage moins intenses (score de 0,49 ± 0,70) que le groupe témoin (score de 0,94 ± 1,11)
(p = 0,043). Le score moyen d’urgence mictionnelle était de 0,06 pour le groupe 1 et de 1,1 pour le groupe ayant reçu le placebo (p = 0,030). Aucune différence importante d’un point de vue statistique n’a été décelée entre les deux groupes concernant l’hématurie, l’incontinence urinaire, la pollakiurie et la dysurie, ainsi que les scores de douleurs globaux (valeurs p > 0,05).
Discussion
Les résultats de cette étude en double aveugle, randomisée et contrôlée avec placebo démontrent l’efficacité de la tamsulosine pour atténuer les symptômes des sondes, et notamment pour soulager les douleurs pendant les activités sexuelles.
Les prescriptions actuelles de port de sonde urétérale dans des conditions d’urgence sont pour les cas de colique néphrétique aiguë insupportable, de pyélonéphrite obstructive et d’insuffisance rénale due à une obstruction urétérale.3 Des procédures endoscopiques peuvent être suivies d’une pose de sonde par mesure de sécurité27 dans certains cas, notamment d’œdème urétéral, de perforation urétérale, de rein unique, de transplantation de rein ou d’antécédents d’insuffisance rénale. Quant aux sondes urétérales à demeure, elles peuvent être éventuellement prescrites en cas de dilatation passive de l’orifice urétéral et de l’urètre, avant une lithotripsie extracorporelle par ondes de choc pour des calculs d’une taille supérieure à 2 cm, pour les calculs enclavés durables, pour les procédures endoscopiques de plus de 45 minutes et en cas de grossesse.2,7
Néanmoins, malgré une utilisation généralisée de sondes urétérales à demeure, la nécessité d’une pose de sonde après une lithotritie urétéroscopique sans complication reste très controversée.28 Même si la taille et l’emplacement de la sonde sont corrects, les sondes urétérales à demeure sont associées à des morbidités inévitables chez plus de 80 % des patients.29 Il s’agit de symptômes urinaires, d’hématurie, de douleurs et complications pendant les activités sexuelles, tous réduisant la qualité de vie du porteur de la sonde.6 Selon certains chercheurs, le positionnement et l’achèvement de la boucle inférieure de la sonde, ainsi que la minutie de la pose de la sonde influent sur la gravité des symptômes.30, 31 Par exemple, une sonde urétérale est mieux tolérée si une injection péri-urétérale de toxine botulinique de type A est réalisée après la pose, réduisant de manière significative les douleurs et la prise de médicaments.32
Cependant, la physiopathologie exacte de symptômes en lien avec les sondes n’est pas encore bien claire. On suppose que les spasmes des muscles lisses urétéraux inférieurs, la contraction involontaire de la vessie déclenchée par une irritation du trigone neuronal et un reflux urinaire vers les reins dû à une résistance accrue de l’orifice de sortie de la vessie sont des causes.11, 14, 15, 21, 33 Des alpha-bloquants sont recommandés comme thérapie expulsive pour les calculs urétéraux et pour diminuer les épisodes de colique récurrents. Ils semblent pouvoir soulager la morbidité en lien avec les sondes de différentes manières.34-36 Les adréno-récepteurs alpha-bloquants réduisent le tonus musculaire de l’urètre prostatique, du trigone de la vessie et de l’urètre, aboutissant à un recul de la résistance de l’orifice de sortie de la vessie, à une pression de miction et à un reflux urinaire.17 Cependant, l’efficacité de ces médicaments et du recours à des protocoles thérapeutiques adaptés pour soulager les symptômes liés aux sondes reste à prouver et des études complémentaires sont nécessaires. Les résultats de cette étude indiquent que la tamsulosine (un antagoniste sélectif α1A) peut aider à contrôler certaines morbidités des sondes.
L’efficacité des alpha-bloquants à atténuer des symptômes en lien avec les sondes a fait l'objet de recherches dans le cadre de plusieurs études impliquant notamment la prise par des patients d’alfuzosine 10 mg13, 14, 16, 25, 37, de tamsulosine 0,4 mg15, 17, 22, 23, 17, de tamsulosine 0,2 mg19, 20, de térazosine 4 mg21, 38, de térazosine 2 mg21 ou d’un placebo pendant 1 à 6 semaines. Damiano et al.15 ont publié le premier rapport sur les bénéfices d’une prise quotidienne de tamsulosine 0,4 mg dans une étude prospective comparant la tamsulosine au placebo chez 75 patients à l’aide de l’USSQ. Même si cette étude n’était pas en double aveugle ni contrôlée avec placebo, les auteurs ont découvert que les patients ayant reçu de la tamsulosine restaient en meilleure santé. Dans une autre étude réalisée par Wang et al.17 sur 154 patients et recourant au même outil d’évaluation, les personnes ayant pris de la tamsulosine ont manifesté moins de symptômes liés à la sonde et ont témoigné d’une meilleure qualité de vie que les patients ayant reçu un placebo.
À l’aide des IPSS et VAPS, l’effet sur les symptômes liés aux sondes d’une plus faible dose de tamsulosine (0,2 mg une fois par jour) seule et en association avec de la toltérodine et de la solifénacine a été étudié respectivement par Lee et al.19 et Lim et al..20 Lee et al. ont découvert que seuls les scores des symptômes de stockage étaient significativement inférieurs chez les patients recevant soit une thérapie de tamulosine seule ou de tamulosine en association avec un autre médicament que chez les patients n’ayant pris aucun médicament. L’auteur a indiqué qu’un positionnement correct de la sonde est plus important qu’une prise de médicaments pour atténuer les symptômes de stockage en lien avec les sondes.19 Inversement, Lim a indiqué qu’une thérapie combinée de tamsulosine et solifénacine peut davantage atténuer les symptômes d’irritation et d’obstruction qu’une prise de tamsulosine seule ou qu’aucune prise de médicament.20 Ces résultats ont ensuite été confirmés par Shalaby et al..23 En outre, il a été conclu que l’atténuation des symptômes en lien avec les sondes grâce à la prise d’alpha-bloquants ne dépend pas du type d’alpha-bloquant, comme l’ont démontré Dellis et al.37 en comparant tamsulosine et alfuzosine. À notre connaissance, il n’existe qu’une seule étude 18 sur l’inefficacité des alpha-bloquants (doxazosine) dans la réduction des symptômes dus aux sondes.
Dans le cadre d’une méta-analyse récente menée par Lamb et al.35 sur 461 patients de cinq études, toutes les études ont révélé une réduction du score des symptômes urinaires de l’USSQ et des scores de douleurs corporelles chez les patients recevant soit de la tamsulosine, soit de l’alfuzosine. Cependant, les améliorations de santé sexuelle et générale n’ont pas été statistiquement significatives. Les résultats et données de 12 autres études portant sur un total de 946 patients ont fait l’objet d’une méta-analyse par Yakoubi et al.36. Les analyses ont révélé une diminution significative des scores de symptômes urinaires et de douleurs, ainsi qu’une amélioration de l’état de santé général chez les patients ayant pris des alpha-bloquants.
Dans le cadre de notre étude, la réduction des scores de douleurs des patients traités avec de la tamsulosine est plus évidente comparé aux douleurs au flanc, aux organes génitaux et
sus-pubiennes pendant les activités sexuelles. Il a été démontré que les sondes urétérales nuisent à la qualité de la vie sexuelle aussi bien chez les hommes que chez les femmes.8 Il semble que les dysfonctions érectiles sont la principale source de détresse sexuelle chez les hommes, probablement à cause des symptômes des voies urinaires inférieures et de la permanence de la sonde. Les femmes, quant à elles, souffrent d'une détresse psychologique en lien avec la sonde qui nuit gravement à leur sexualité.8
Nous avons également découvert que la tamsulosine permet de réduire l’hématurie et l’urgence mictionnelle, bien que les patients traités avec de la tamsulosine ont un taux de nycturie supérieur à celui des patients ayant reçu un placebo. La nycturie n’avait auparavant jamais été signalée comme effet secondaire de la tamsulosine. Ce résultat doit donc faire l’objet d’études à plus grande échelle. Koseoglu et al.39 ont découvert que la tamsulosine ne permet pas de réduire la nycturie chez les patients traités pour une hyperplasie bénigne de la prostate. Une autre étude a démontré qu’une association d’alpha-bloquants et de zolpidem réduit mieux la nycturie que la prise d’alpha-bloquants uniquement.40
Notre étude présente plusieurs limites. Premièrement, la taille de notre échantillon était statistiquement petite afin de repérer les légères différences entre les deux groupes. Deuxièmement, certains patients n’ont pas achevé l’étude. Troisièmement, nous avons mené des entretiens cliniques avec les patients pour évaluer les symptômes urinaires, tandis que Joshi et al.6 ont développé un outil spécifique d’évaluation des symptômes liés aux sondes appelé l’USSQ. Quatrièmement, aucune donnée fiable sur la quantité d’analgésiques prise par les patients n’a été fournie. Enfin, nous n’avons pas étudié les éventuels effets secondaires des alpha-bloquants, même si les thérapies ont bien été tolérées et aucun patient n’a choisi de cesser la prise de médicaments en raison d’effets secondaires. Par conséquent, d’autres études prospectives à grande échelle randomisées sont nécessaires pour obtenir des informations plus précises.
Conclusion
La prise de tamsulosine 0,4 mg une fois par jour chez les patients porteurs d’une sonde urétérale unilatérale a atténué les symptômes urinaires liés aux sondes, notamment les douleurs corporelles pendant les activités sexuelles. Par conséquent, la tamsulosine peut être envisagée pour les patients souffrant de symptômes liés à une sonde. À l’avenir, des études prospectives randomisées à grande échelle seront nécessaires.
Approbation éthique et consentement à la participation
Le consentement des patients a été obtenu avant l’opération conformément au code de déontologie du comité d'éthique des sciences médicales de l’université de Téhéran. Cet essai est enregistré sur www.clinicaltrials.gov sous la référence IRCT2015042221886N2. Les informations publiées ne permettent pas d’identifier les patients. Des informations, données et photos peuvent être fournies sur demande.
Conflits d’intérêts
Tous les auteurs ont déclaré n’avoir aucun intérêt contradictoire ou conflit d’intérêts.
Financement
Aucun.
Remerciements
Nous souhaitons adresser tous nos remerciements au Centre de recherche sur l’urologie, université de Téhéran des sciences médicales, Téhéran, Iran
Author(s)
Fateme Guitynavard
Urology Research Center, Tehran University of Medical Sciences, Tehran, Iran
Shahram Gooran
Urology Research Center, Tehran University of Medical Sciences, Tehran, Iran
Parvin Kasiri
Urology Research Center, Tehran University of Medical Sciences, Tehran, Iran
Farshad Gholipour
Urology Research Center, Tehran University of Medical Sciences, Tehran, Iran
Seyed Mohammad Kazem Aghamir*
Urology Research Center, Tehran University of Medical Sciences, Tehran, Iran
Email mkahamir@yahoo.com
* Corresponding author
References
- Zimskind PD, Fetter TR, Wilkerson JL. Clinical use of long-term indwelling silicone rubber ureteral splints inserted cystoscopically. J Urol 1967;97(5):840–844.
- Knudsen BE, Beiko DT, Denstedt JD. Stenting after ureteroscopy: pros and cons. Urol Clin North Am 2004;31(1):173–180.
- Chew BH, Knudsen BE, Denstedt JD. The use of stents in contemporary urology. Curr Opin Urol 2004;14(2):111–115.
- Damiano R, Oliva A, Esposito C, De Sio M, Autorino R, D’Armiento M. Early and late complications of double pigtail ureteral stent. Urologia Int 2002;69(2):136–140.
- Haleblian G, Kijvikai K, de la Rosette J, Preminger G. Ureteral stenting and urinary stone management: a systematic review. J Urol 2008;179(2):424–430.
- Joshi H, Newns N, Stainthorpe A, MacDonagh R, Keeley F, Timoney A. Ureteral stent symptom questionnaire: development and validation of a multidimensional quality of life measure. J Urol 2003;169(3):1060–1064.
- Miyaoka R, Monga M. Ureteral stent discomfort: etiology and management. IJU 2009;25(4):455.
- Sighinolfi M, Micali S, De Stefani S, Mofferdin A, Grande A, Giacometti, M, et al. Indwelling ureteral stents and sexual health: a prospective, multivariate analysis. J Urol 2007;178(1):229–231.
- Ecke TH, Bartel P, Hallmann, S, Ruttloff J. Evaluation of symptoms and patients’ comfort for JJ-ureteral stents with and without antireflux-membrane valve. Urol 2010;75(1):212–216.
- Lingeman JE, Preminger GM, Goldfischer ER, Krambeck AE, Team CS. Assessing the impact of ureteral stent design on patient comfort. J Urol 2009;181(6):2581–2587.
- Thomas R. Indwelling ureteral stents: impact of material and shape on patient comfort. J Endourol 1993;7(2):137–140.
- Candela J, Bellman G. Ureteral stents: impact of diameter and composition on patient symptoms. J Endourol 1997;11(1):45.
- Park SC, Jung SW, Lee JW, Rim JS. The effects of tolterodine extended release and alfuzosin for the treatment of double-J stent-related symptoms. J Endourol 2009;23(11):1913–1917.
- Beddingfield R, Pedro RN, Hinck B, Kreidberg C, Feia K, Monga M. Alfuzosin to relieve ureteral stent discomfort: a prospective, randomized, placebo controlled study. J Urol 2009;181(1):170–176.
- Damiano R, Autorino R, De Sio M, Giacobbe A, Palumbo IM, D’Armiento M. Effect of tamsulosin in preventing ureteral stent-related morbidity: a prospective study. J Endourol 2008;22(4):651–656.
- Deliveliotis C, Chrisofos M, Gougousis E, Papatsoris A, Dellis A, Varkarakis IM. Is there a role for alpha1-blockers in treating double-J stent-related symptoms? Urology 2006;67(1):35–39. doi:10.1016/j.urology.2005.07.038
- Wang C-J, Huang S-W, Chang C-H. Effects of specific α-1A/1D blocker on lower urinary tract symptoms due to double-J stent: a prospectively randomized study. Urol Res 2009;37(3):147–152.
- Kuyumcuoglu U, Eryildirim B, Tuncer M, Faydaci G, Tarhan F, Ozgül A. Effectiveness of medical treatment in overcoming the ureteral double-J stent related symptoms. Can Urol Assoc J 2012;6(6):e234–237.
- Lee SJ, Yoo C, Oh CY, Lee YS, Cho, ST, Lee SH, et al. Stent position is more important than α-blockers or anticholinergics for stent-related lower urinary tract symptoms after ureteroscopic ureterolithotomy: a prospective randomized study. Korean J Urol 2010;51(9):636–641.
- Lim KT, Kim YT, Lee TY, Park SY. Effects of tamsulosin, solifenacin, and combination therapy for the treatment of ureteral stent related discomforts. Korean J Urol 2011;52(7):485–488.
- Mokhtari G, Shakiba M, Ghodsi S, Farzan A, Heidari Nejad S, Esmaeili S. Effect of terazosin on lower urinary tract symptoms and pain due to double-J stent: a double-blind placebo-controlled randomized clinical trial. Urologia Int 2011;87(1):19–22.
- Navanimitkul N, Lojanapiwat B. Efficacy of tamsulosin 0.4 mg/day in relieving double-J stent-related symptoms: a randomized controlled study. J Int Med Res 2010;38(4):1436–1441.
- Shalaby E, Ahmed A.-f, Maarouf A, Yahia I, Ali M, Ghobish A. Randomized controlled trial to compare the safety and efficacy of tamsulosin, solifenacin, and combination of both in treatment of double-j stent-related lower urinary symptoms. Adv Urol 2013.
- Wang C-J, Huang S-W, Chang C-H. Effects of tamsulosin on lower urinary tract symptoms due to double-J stent: a prospective study. Urologia Int 2008;83(1):66–69.
- Nazim SM, Ather MH. Alpha-blockers impact stent-related symptoms: a randomized, double-blind, placebo-controlled trial. J Endourol 2012;26(9):1237–1241.
- Shibasaki M, Sudoh K, Inagaki O, Uchida W, Honda K. Effect of the optical isomers of YM‐12617 on increased intra‐urethral pressure induced by phenylephrine in anaesthetized dogs. J Autonom Pharmacol 1992;12(4):263–268.
- Jeong H, Kwak C, Lee S. Ureteric stenting after ureteroscopy for ureteric stones: a prospective randomized study assessing symptoms and complications. BJU Int 2004;93(7):1032–1034.
- Nabi G, Cook J, N’Dow J, McClinton S. Outcomes of stenting after uncomplicated ureteroscopy: systematic review and meta-analysis. BMJ 2007;334(7593):572.
- Joshi H, Stainthorpe A, MacDonagh R, Keeley F, Timoney A. Indwelling ureteral stents: evaluation of symptoms, quality of life and utility. J Urol 2003;169(3):1065–1069.
- Jeon SS, Choi YS, Hong JH. Determination of ideal stent length for endourologic surgery. J Endourol 2007;21(8):906–910.
- Rane A, Saleemi A, Cahill D, Sriprasad S, Shrotri N, Tiptaft R. Have stent-related symptoms anything to do with placement technique? J Endourol 2001;15(7):741–745.
- Gupta M, Patel T, Xavier K, Maruffo F, Lehman D, Walsh R, Landman J. Prospective randomized evaluation of periureteral botulinum toxin type A injection for ureteral stent pain reduction. J Urol 2010;183(2):598–602.
- Duvdevani M, Chew BH, Denstedt JD. Minimizing symptoms in patients with ureteric stents. Curr Opin Urol 2006;16(2):77–82.
- Dellis A, Joshi HB, Timoney AG, Keeley FX. Relief of stent related symptoms: review of engineering and pharmacological solutions. J Urol 2010;184(4):1267–1272.
- Lamb AD, Vowler SL, Johnston R, Dunn N, Wiseman OJ. Meta‐analysis showing the beneficial effect of α‐blockers on ureteric stent discomfort. BJU Int 2011;108(11):1894–1902.
- Yakoubi R, Lemdani M, Monga M, Villers A, Koenig P. Is there a role for α-blockers in ureteral stent related symptoms? A systematic review and meta-analysis. J Urol 2011;186(3):928–934.
- Dellis AE, Keeley FX, Manolas V, Skolarikos AA. Role of α-blockers in the treatment of stent-related symptoms: a prospective randomized control study. Urol 2014;83(1):56–62.
- Tehranchi A, Rezaei Y, Khalkhali H, Rezaei M. Effects of terazosin and tolterodine on ureteral stent related symptoms: a double-blind placebo-controlled randomized clinical trial. Int Braz J Urol 2013;39(6):832–840.
- Koseoglu H, Aslan G, Ozdemir I, Esen A. Nocturnal polyuria in patients with lower urinary tract symptoms and response to alpha-blocker therapy. Urol 2006;67(6):1188–1192.
- Song YS, Ku JH. Zolpidem pharmacotherapy combined with alpha-blocker therapy for nocturia unresponsive to alpha-blocker monotherapy in men with lower urinary tract symptoms: a preliminary study. Int Urol Nephrol 2007;39(4):1147–1152.
